A FMEK LTALNOS JELLEMZSE Elemek esetn EN0 a







- Slides: 13

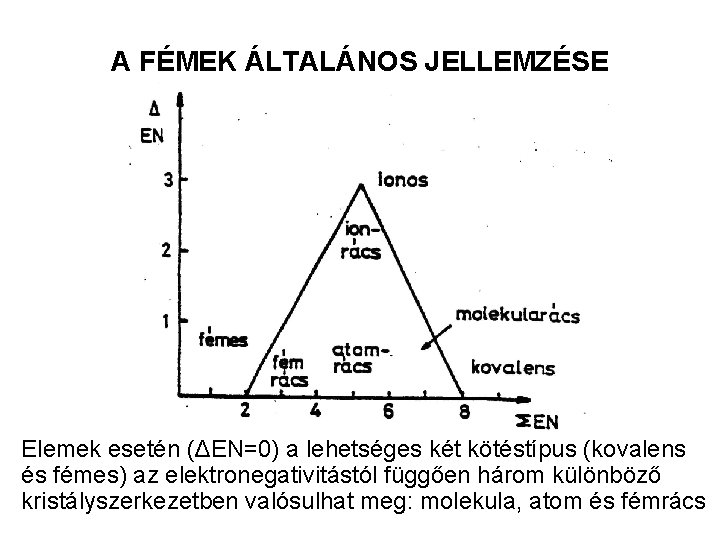
A FÉMEK ÁLTALÁNOS JELLEMZÉSE Elemek esetén (ΔEN=0) a lehetséges két kötéstípus (kovalens és fémes) az elektronegativitástól függően három különböző kristályszerkezetben valósulhat meg: molekula, atom és fémrács

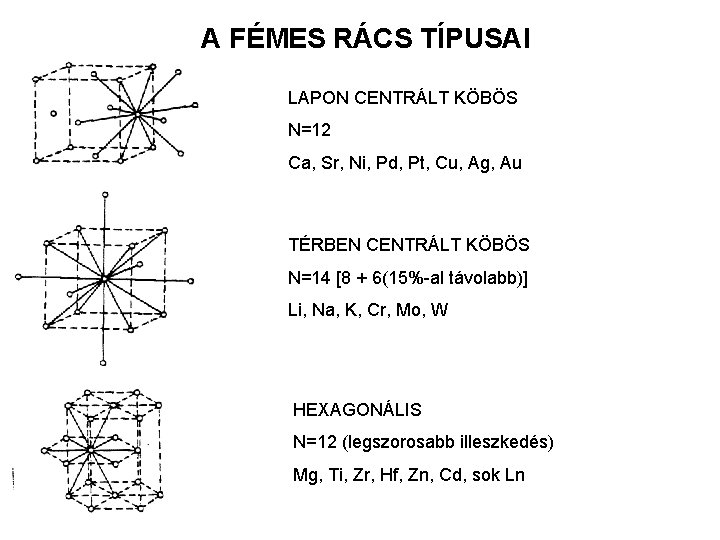
A FÉMES RÁCS TÍPUSAI LAPON CENTRÁLT KÖBÖS N=12 Ca, Sr, Ni, Pd, Pt, Cu, Ag, Au TÉRBEN CENTRÁLT KÖBÖS N=14 [8 + 6(15%-al távolabb)] Li, Na, K, Cr, Mo, W HEXAGONÁLIS N=12 (legszorosabb illeszkedés) Mg, Ti, Zr, Hf, Zn, Cd, sok Ln

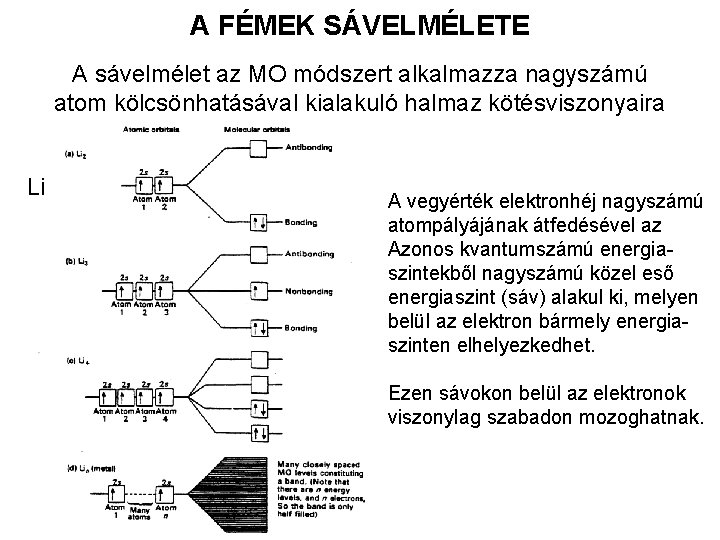
A FÉMEK SÁVELMÉLETE A sávelmélet az MO módszert alkalmazza nagyszámú atom kölcsönhatásával kialakuló halmaz kötésviszonyaira Li A vegyérték elektronhéj nagyszámú atompályájának átfedésével az Azonos kvantumszámú energiaszintekből nagyszámú közel eső energiaszint (sáv) alakul ki, melyen belül az elektron bármely energiaszinten elhelyezkedhet. Ezen sávokon belül az elektronok viszonylag szabadon mozoghatnak.

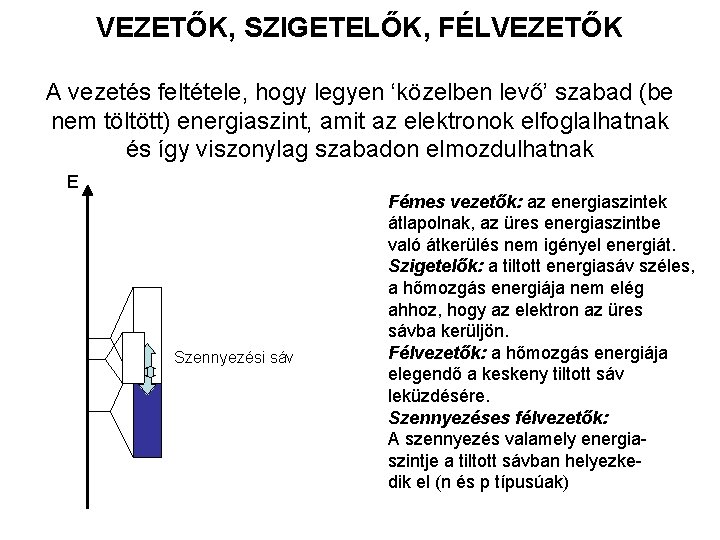
VEZETŐK, SZIGETELŐK, FÉLVEZETŐK A vezetés feltétele, hogy legyen ‘közelben levő’ szabad (be nem töltött) energiaszint, amit az elektronok elfoglalhatnak és így viszonylag szabadon elmozdulhatnak E Szennyezési sáv Fémes vezetők: az energiaszintek átlapolnak, az üres energiaszintbe való átkerülés nem igényel energiát. Szigetelők: a tiltott energiasáv széles, a hőmozgás energiája nem elég ahhoz, hogy az elektron az üres sávba kerüljön. Félvezetők: a hőmozgás energiája elegendő a keskeny tiltott sáv leküzdésére. Szennyezéses félvezetők: A szennyezés valamely energiaszintje a tiltott sávban helyezkedik el (n és p típusúak)

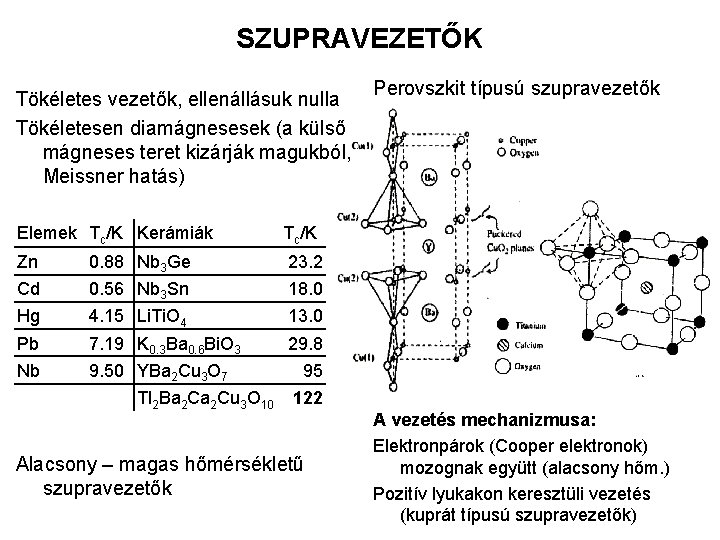
SZUPRAVEZETŐK Tökéletes vezetők, ellenállásuk nulla Tökéletesen diamágnesesek (a külső mágneses teret kizárják magukból, Meissner hatás) Elemek Tc/K Kerámiák Tc/K Zn 0. 88 Nb 3 Ge 23. 2 Cd 0. 56 Nb 3 Sn 18. 0 Hg 4. 15 Li. Ti. O 4 13. 0 Pb 7. 19 K 0. 3 Ba 0. 6 Bi. O 3 29. 8 Nb 9. 50 YBa 2 Cu 3 O 7 Tl 2 Ba 2 Cu 3 O 10 Perovszkit típusú szupravezetők 95 122 Alacsony – magas hőmérsékletű szupravezetők A vezetés mechanizmusa: Elektronpárok (Cooper elektronok) mozognak együtt (alacsony hőm. ) Pozitív lyukakon keresztüli vezetés (kuprát típusú szupravezetők)

A FÉMEK FIZIKAI TULAJDONSÁGAI Jó hő és elektromos vezetőképesség Fémes fény (kis fényáteresztő képesség, nagy fény visszaverő képesség), finom eloszlásban fekete porok (a beeső fényt elnyelik) Jó megmunkálhatóság (nyújthatók, hajlíthatók, rugalmasak): a fém-fém kötés közepes energiájú és nincs kitüntetett iránya Rossz fizikai oldhatóság, jó egymásban való oldhatóság (ötvözetek): helyettesítéses, intersticiális, vegyület Sűrűség: csoportban lefelé nő (Li 0, 53 g/ml, Os 22, 6 g/ml), könnyűfémek < 5 g/ml < nehézfémek Olvadáspont, forráspont: többségüké magas (> 1000 °C) cseppfolyós fémek: Hg, Cs, Ga olvadáspont tartomány: Hg: -38°C, W: 3410 °C

A FÉMEK KÉMIAI TULAJDONSÁGAI Pozitív oxidációs állapot kialakítására való hajlam (ionos vagy kovalens vegyületek egyaránt) Oxidjaik: alacsony oxidációs állapotúak bázikusak, a magasak savasak, a közbensőek amfoterek Reakcióképességük széles határok között változik (alkáli fémektől a platina fémekig) mivel szembeni reakcióképesség: hard-szoft sajátság szemcseméret, védőréteg (Al, Fe)

FÉMEK ELŐFORDULÁSA Elemi állapotban: az oxigénnel szemben kis reakció-képességű szoft nemesfémek: Au, Ag, Pt +1 - +3(+4) oxidációs állapotú rosszul oldódó sóik (karbonátok, foszfátok, szulfátok) vagy oxidok/hidroxidok (HARD), illetve szulfidok, arzidok (SZOFT) formájában Az üledékes kőzetek a fő nyersanyagforrások. A magmás kőzetek fizikai, mechanikai és kémiai mállásának eredményei kémiai mállás (e/r értéktől függően): <4: oldatba megy és oldatban marad (Na, Mg, Ca) <12: oxoanionként (szulfát, foszfát, kromát, molibdát, stb. ) rosszul oldódó vegyületeket képeznek közbülsők: redukáló közegben oldatba mennek, oxidálóban kiválnak (pl. Fe, Mn)

FÉMEK ELŐFORDULÁSA Ércek: a fémek gazdaságos kinyerésére alkalmas ásványok, kőzetek Gazdaságossághoz szükséges min. fémtartalom A használatos ércek átlagos fémtartalma Alumímium 16% 30 -35% Antimon 40% 50 -60% 0, 0002% 0, 001% 3% 10 -30% Higany 0, 5% 1 -3% Mangán 35% 45 -55% Molibdén 0, 25% 0, 1 -1, 8% Nikkel 1% 2, 3% Ólom 4% 6 -10% 0, 0004% 0, 001% Réz 0, 8% 1, 5 -5% Titán 1, 8% 2, 4 -5% Vanádium 0, 8% 1, 7 -4, 5% Vas 30% 40 -60% A fém neve Arany Cink Platina

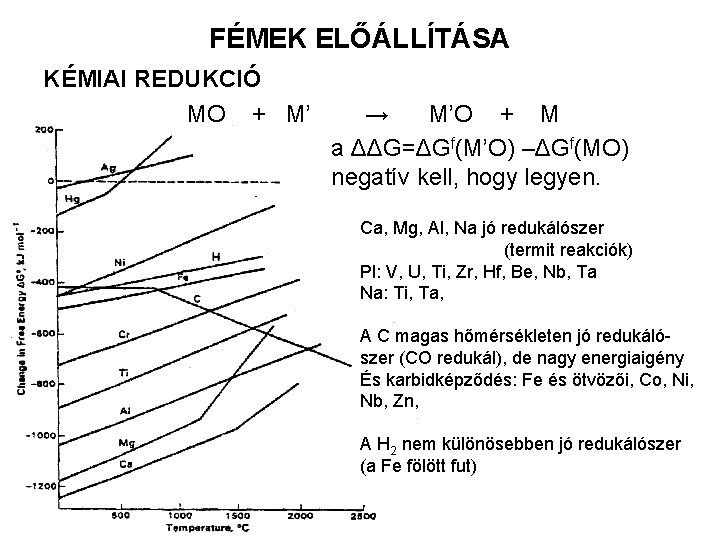
FÉMEK ELŐÁLLÍTÁSA KÉMIAI REDUKCIÓ MO + M’ → M’O + M a ΔΔG=ΔGf(M’O) –ΔGf(MO) negatív kell, hogy legyen. Ca, Mg, Al, Na jó redukálószer (termit reakciók) Pl: V, U, Ti, Zr, Hf, Be, Nb, Ta Na: Ti, Ta, A C magas hőmérsékleten jó redukálószer (CO redukál), de nagy energiaigény És karbidképződés: Fe és ötvözői, Co, Ni, Nb, Zn, A H 2 nem különösebben jó redukálószer (a Fe fölött fut)

FÉMEK ELŐÁLLÍTÁSA Elektrolitikus redukció olvadékból: alkáli és alkáli földfémek kloridjai, Al oxidja oldatból: Cu (réz raffinálás), Co, Ni, Cr, Mn, Ga, Cd, Cementálás nemesebb fémek kiválasztása kevésbé nemes fémekkel (fémhulladékok feldolgozása): In, Tl, Ge, Re, Pt-fémek 2 In 3+ + 3 Fe = 2 In + 3 Fe 2+ Ciánlúgozás (arany- és ezüstércek feldolgozása) érc + 0, 1% Na. CN oldat + levegő 4 Au + 8 Na. CN + 2 H 2 O + O 2 = 4 Na[Au(CN)2] + Na. OH majd Zn-por hozzáadása az oldathoz 4 Na[Au(CN)2] + 2 Zn = 2 Na 2[Zn(CN)4] + 4 Au

FÉMEK ELŐÁLLÍTÁSA TERMIKUS BONTÁS drága eljárások nagy tisztaságú fémek előállítására (jodidok, karbonilok, oxidok, azidok hőbontása) van Arkel-de Boer eljárás: a fémjodid (Ti. I 4, Zr. I 4, Hf. I 4, Th. I 4, Bi. I 3) gőzeit vékony ízzó W szálra kondenzáltatják, ahol termikusan bomlik és a fém a szálra rakódik. Fém-karbonilok bontása (Ni(CO)4, W(CO)6, Mo(CO)6) 50°C 230°C Ni + 4 CO —→ Ni(CO)4 —→ Ni + 4 CO 150°C, 20 bar 1 bar Fémhidridek bontása (Ti, V, Nb, Ta, Zr, ritkaföldfémek) Fémoxidok bontása 2 Hg. O → 2 Hg + O 2 Ag 2 CO 3 → Ag 2 O + CO 2 → 2 Ag + ½ O 2 (Mond eljárás)

FÉMEK FELHASZNÁLÁSA Szerkezeti anyagok megmunkálhatók, könnyűek, kemények, korrózióállóak ötvözetek készíthetők belőlük könnyűfém ötvözetek (Al, Ti, Mg), Fe ötvözetek, nem-Fe ötvözetek, Elektromos vezetők: Cu, Al, W, Kémiai reaktánsok: Na, Ca, Mg, Al, Zn, Katalizátorok: Pt, Pd, Ni, Fe, (és vegyületeik),