ZKLADN KOLA SLOVAN KROM PSPVKOV ORGANIZACE ZEYEROVA 3354










- Slides: 16

ZÁKLADNÍ ŠKOLA SLOVAN, KROMĚŘÍŽ, PŘÍSPĚVKOVÁ ORGANIZACE ZEYEROVA 3354, 767 01 KROMĚŘÍŽ projekt v rámci vzdělávacího programu VZDĚLÁNÍ PRO KONKURENCESCHOPNOST ŠABLONA ČÍSLO: III/2 NÁZEV: INOVACE A ZKVALITNĚNÍ VÝUKY PROSTŘEDNICTVÍM ICT PŘEDMĚT: Chemie ROČNÍK: 9. ročník TÉMA: Soli II. – vzorce solí dvojsytných kyslíkatých kyselin AUTOR: Ing. Pavla Zezulová DATUM VYTVOŘENÍ: 6. 10. 2012 VY_32_INOVACE_33_PZ

Anotace Výukový materiál je určen pro žáky 9. ročníku. Seznamuje žáky s principy tvorby solí dvojsytných kyslíkatých kyselin. Tak jako i v předešlých případech výuky tvorby solí je využívaná analogie s již známými sloučeninami – oxidy. Za základ odvození je opět použito křížové pravidlo. Znovu jsou pro větší názornost použity postupné animace. Pilotáž Materiál byl ověřován ve všech paralelních třídách devátého ročníku. U slabších žáků se vyskytli problémy se psaním závorek ve vzorcích a pletli si sírany a siřičitany.

Soli II VZORCE SOLÍ DVOJSYTNÝCH KYSLÍKATÝCH KYSELIN

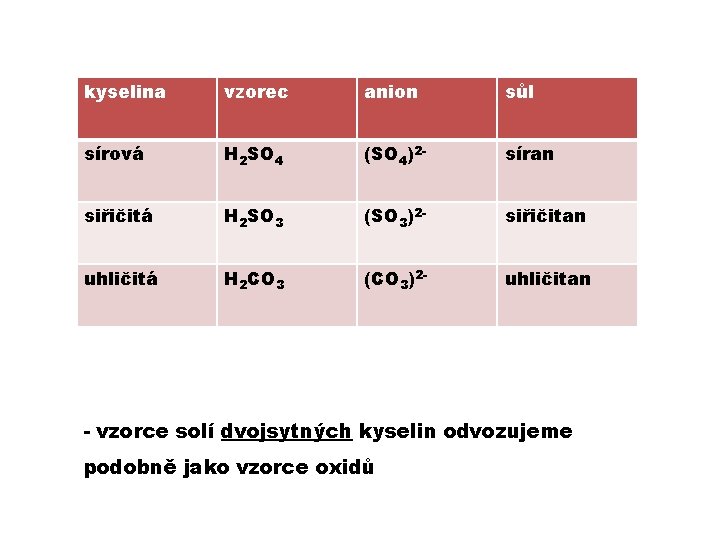
kyselina vzorec anion sůl sírová H 2 SO 4 (SO 4)2 - síran siřičitá H 2 SO 3 (SO 3)2 - siřičitan uhličitá H 2 CO 3 (CO 3)2 - uhličitan - vzorce solí dvojsytných kyselin odvozujeme podobně jako vzorce oxidů

Sírany ox. č. I II IV V VI VIII název soli odvození vzorce vzorec sluč. poměr

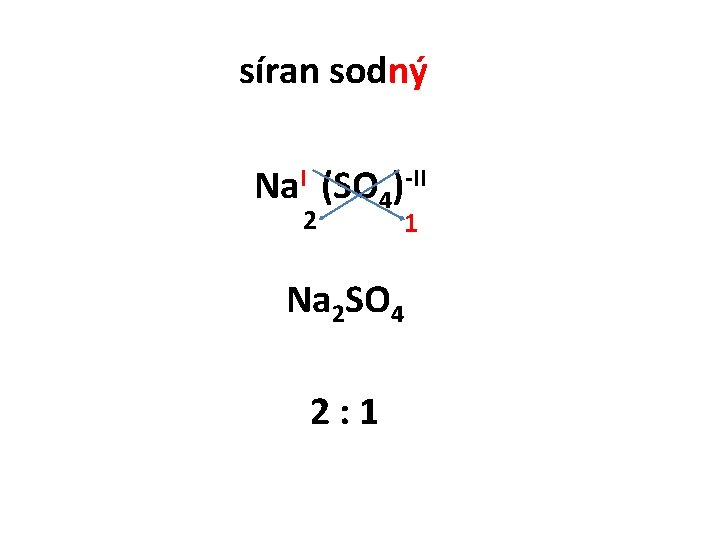
síran sodný Na. I (SO 4)-II 2 1 Na 2 SO 4 2: 1

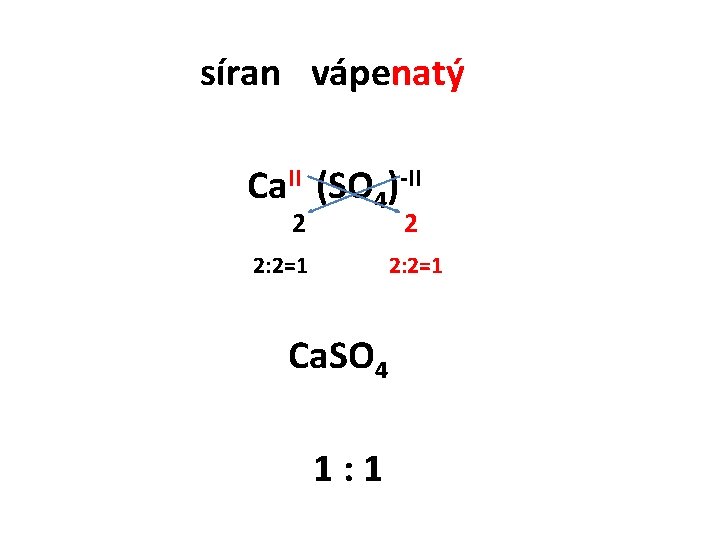
síran vápenatý Ca. II (SO 4)-II 2 2 2: 2=1 Ca. SO 4 1: 1

síran hlinitý Al. III (SO 4)-II 2 Al 2(SO 4)3 2: 3 3

síran olovičitý Pb. IV (SO 4)-II 2 2: 2=1 4 4: 2=2 Pb(SO 4)2 1: 2

síran arseničný As. V (SO 4)-II 2 5 As 2(SO 4)5 2: 5

síran wolframový WVI (SO 4)-II 2 6 2: 2=1 6: 2=3 W(SO 4)3 1: 3

síran manganistý Mn. VII (SO 4)-II 2 7 Mn 2(SO 4)7 2: 7

síran osmičelý Os. VIII (SO 4)-II 2 8 2: 2=1 8: 2=4 Os(SO 4)4 1: 4

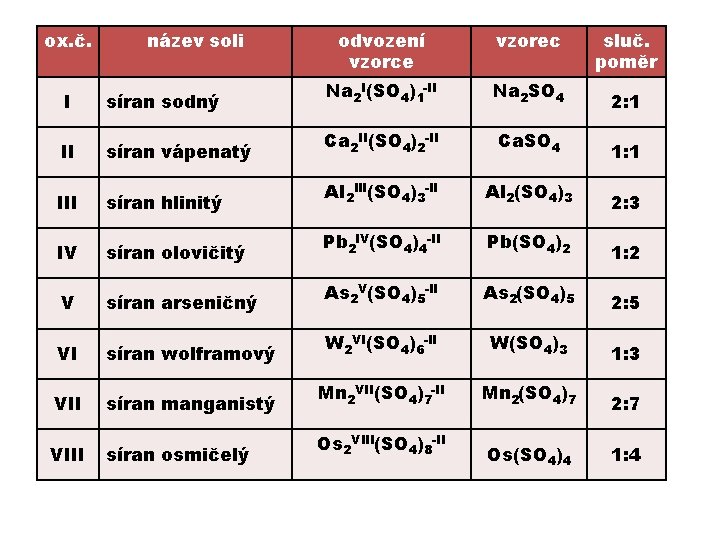
ox. č. I II IV V VI VIII název soli odvození vzorce vzorec sluč. poměr síran sodný Na 2 I(SO 4)1 -II Na 2 SO 4 2: 1 síran vápenatý Ca 2 II(SO 4)2 -II Ca. SO 4 1: 1 síran hlinitý AI 2 IIl(SO 4)3 -II Al 2(SO 4)3 2: 3 síran olovičitý Pb 2 IV(SO 4)4 -II Pb(SO 4)2 1: 2 síran arseničný As 2 V(SO 4)5 -II As 2(SO 4)5 2: 5 síran wolframový W 2 VI(SO 4)6 -II W(SO 4)3 1: 3 síran manganistý Mn 2 VII(SO 4)7 -II Mn 2(SO 4)7 2: 7 síran osmičelý Os 2 VIII(SO 4)8 -II Os(SO 4)4 1: 4

Napiš vzorce následujících sloučenin: síran olovnatý Pb. SO 4 siřičitan draselný K 2 SO 3 uhličitan vanadičný V 2(CO 3)5 síran chromitý Cr 2(SO 4)3 siřičitan cíničitý Sn(SO 3)2 uhličitan hořečnatý Mg. CO 3 síran železnatý Fe. SO 4

Zdroje Vlastní tvorba
 Iç anadolu bölgesi tarım ürünleri
Iç anadolu bölgesi tarım ürünleri Nel in de krom menu
Nel in de krom menu Wat is die intensiewe vorm van lelik
Wat is die intensiewe vorm van lelik Organizace pro hospodářskou spolupráci a rozvoj
Organizace pro hospodářskou spolupráci a rozvoj životní cyklus organizace
životní cyklus organizace Barvy organizace
Barvy organizace Mezinárodní organizace test
Mezinárodní organizace test Organizace sklonovani
Organizace sklonovani Lokacija teretnih kola
Lokacija teretnih kola Prsa sklonovani
Prsa sklonovani Ivi kola
Ivi kola Vzorec obvod trojuholnika
Vzorec obvod trojuholnika Karolina kola
Karolina kola Kola reg
Kola reg Moja kola
Moja kola Sağ kürek kemiğinden kola vuran ağrı
Sağ kürek kemiğinden kola vuran ağrı Lig inguinale
Lig inguinale