Unterrichtsvorbereitung Vom Bildungsplan zum Unterricht Ziel Hilfestellung fr

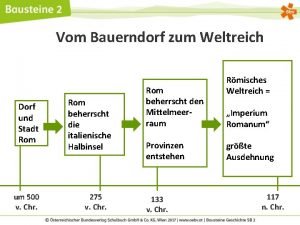
Unterrichtsvorbereitung Vom Bildungsplan zum Unterricht Ziel: Hilfestellung für Unterrichtspraktikanten wie man Chemie-Unterricht vorbereiten kann Beispiel: Polyaddition Chemie Neigungsfach 13_1 Zeit: eine Doppelstunde Unterrichtsform: „Team-teaching“ Lehrer und Praktikant wechseln sich während des Unterrichts ab Methodische und didaktische Hinweise

Bildungsplan: Polyaddition Bei der Behandlung von Kunststoffen lernen die Schülerinnen und Schüler Stoffe mit großer Bedeutung im Alltag und in der Technik kennen. Sie verstehen, wie mit der Kenntnis des Zusammenhangs von Struktur und Eigenschaften gezielt Werkstoffe hergestellt werden können. Die Behandlung eines Reaktionsmechanismus vertieft ihr Verständnis von Reaktionsabläufen. Am Beispiel der Verwertung von Kunststoffabfällen erhalten sie Einblick in die Umweltproblematik und in einen technischen Stoffkreislauf. Prinzip der Polyaddition Herstellung eines Polyurethans Zusammenhang zwischen Struktur und Eigenschaften bei Kunststoffen Thermoplaste, Duroplaste, Elaste Vorteile und Nachteile bei der Verarbeitung und Verwendung von Kunststoffen Vergleich mit anderen Werkstoffen Tipp: in Powerpoint die Themen in Textfelder schreiben, ergänzen, sortieren und einen Unterrichtsgang finden: Wichtig: Motivation & Spannungsbogen
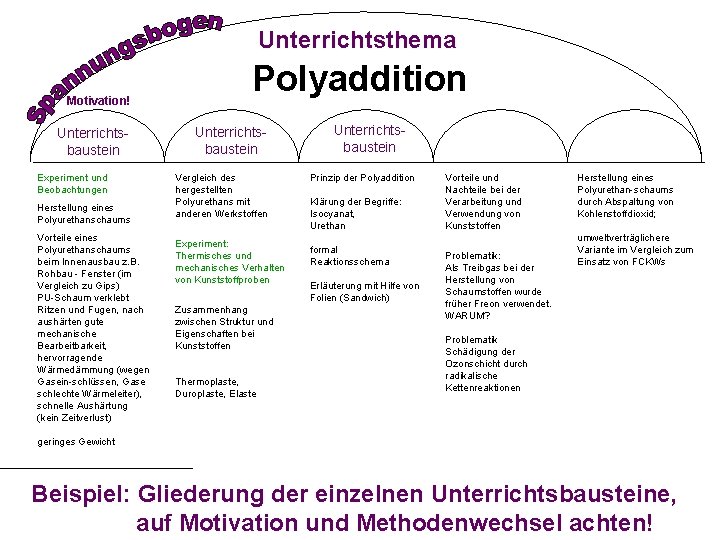
Unterrichtsthema Motivation! Unterrichtsbaustein Experiment und Beobachtungen Herstellung eines Polyurethanschaums Vorteile eines Polyurethanschaums beim Innenausbau z. B. Rohbau - Fenster (im Vergleich zu Gips) PU-Schaum verklebt Ritzen und Fugen, nach aushärten gute mechanische Bearbeitbarkeit, hervorragende Wärmedämmung (wegen Gasein-schlüssen, Gase schlechte Wärmeleiter), schnelle Aushärtung (kein Zeitverlust) Polyaddition Unterrichtsbaustein Vergleich des hergestellten Polyurethans mit anderen Werkstoffen Experiment: Thermisches und mechanisches Verhalten von Kunststoffproben Zusammenhang zwischen Struktur und Eigenschaften bei Kunststoffen Thermoplaste, Duroplaste, Elaste Unterrichtsbaustein Prinzip der Polyaddition Klärung der Begriffe: Isocyanat, Urethan formal Reaktionsschema Erläuterung mit Hilfe von Folien (Sandwich) Vorteile und Nachteile bei der Verarbeitung und Verwendung von Kunststoffen Problematik: Als Treibgas bei der Herstellung von Schaumstoffen wurde früher Freon verwendet. WARUM? Herstellung eines Polyurethan-schaums durch Abspaltung von Kohlenstoffdioxid; umweltverträglichere Variante im Vergleich zum Einsatz von FCKWs Problematik Schädigung der Ozonschicht durch radikalische Kettenreaktionen geringes Gewicht Beispiel: Gliederung der einzelnen Unterrichtsbausteine, auf Motivation und Methodenwechsel achten!
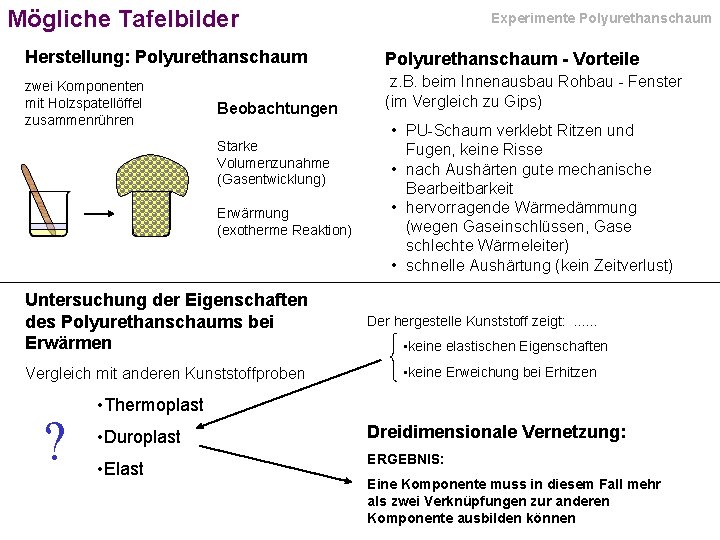
Mögliche Tafelbilder Experimente Polyurethanschaum Herstellung: Polyurethanschaum - Vorteile zwei Komponenten mit Holzspatellöffel zusammenrühren z. B. beim Innenausbau Rohbau - Fenster (im Vergleich zu Gips) Beobachtungen Starke Volumenzunahme (Gasentwicklung) Erwärmung (exotherme Reaktion) • PU-Schaum verklebt Ritzen und Fugen, keine Risse • nach Aushärten gute mechanische Bearbeitbarkeit • hervorragende Wärmedämmung (wegen Gaseinschlüssen, Gase schlechte Wärmeleiter) • schnelle Aushärtung (kein Zeitverlust) Untersuchung der Eigenschaften des Polyurethanschaums bei Erwärmen Der hergestelle Kunststoff zeigt: . . . Vergleich mit anderen Kunststoffproben • keine Erweichung bei Erhitzen ? • keine elastischen Eigenschaften • Thermoplast • Duroplast • Elast Dreidimensionale Vernetzung: ERGEBNIS: Eine Komponente muss in diesem Fall mehr als zwei Verknüpfungen zur anderen Komponente ausbilden können
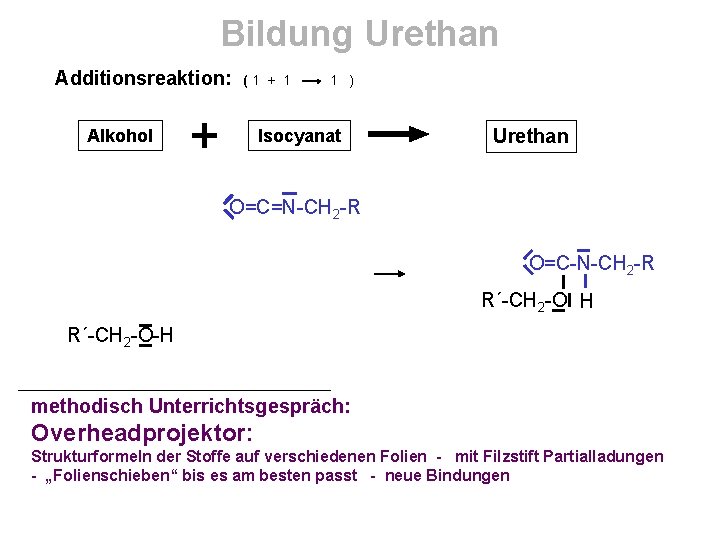
Bildung Urethan Additionsreaktion: (1 + 1 Alkohol 1 ) Isocyanat Urethan O=C=N-CH 2 -R O=C-N-CH 2 -R R´-CH 2 -O H R´-CH 2 -O-H methodisch Unterrichtsgespräch: Overheadprojektor: Strukturformeln der Stoffe auf verschiedenen Folien - mit Filzstift Partialladungen - „Folienschieben“ bis es am besten passt - neue Bindungen
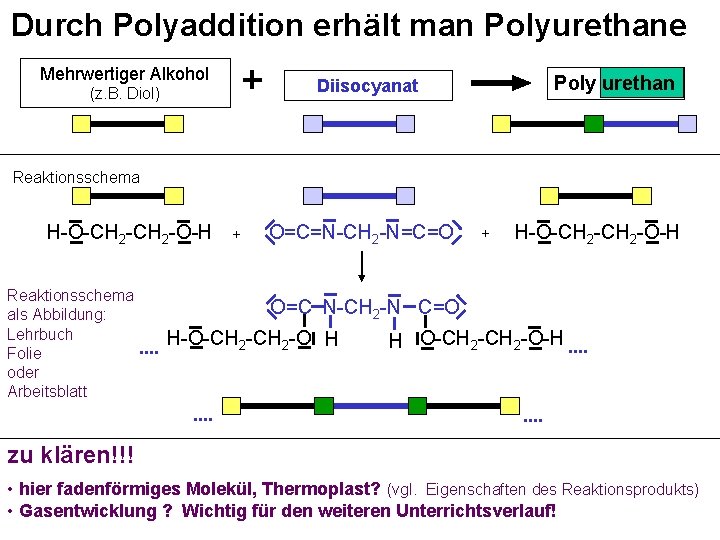
Durch Polyaddition erhält man Polyurethane Mehrwertiger Alkohol Poly urethan Diisocyanat (z. B. Diol) Reaktionsschema H-O-CH 2 -O-H Reaktionsschema als Abbildung: Lehrbuch Folie oder Arbeitsblatt + O=C=N-CH 2 -N=C=O + H-O-CH 2 -O-H O=C N-CH 2 -N C=O. . H-O-CH 2 -O H. . H O-CH 2 -O-H. . . . zu klären!!! • hier fadenförmiges Molekül, Thermoplast? (vgl. Eigenschaften des Reaktionsprodukts) • Gasentwicklung ? Wichtig für den weiteren Unterrichtsverlauf!
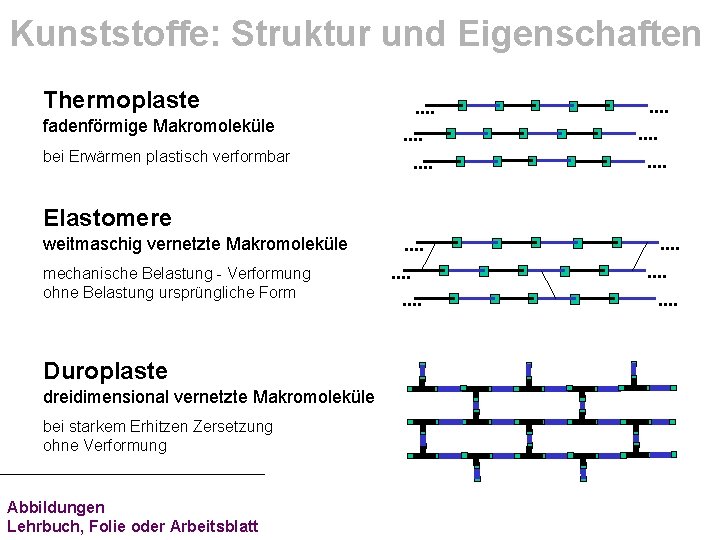
Kunststoffe: Struktur und Eigenschaften Thermoplaste fadenförmige Makromoleküle bei Erwärmen plastisch verformbar . . . Elastomere weitmaschig vernetzte Makromoleküle mechanische Belastung - Verformung ohne Belastung ursprüngliche Form Duroplaste dreidimensional vernetzte Makromoleküle bei starkem Erhitzen Zersetzung ohne Verformung Abbildungen Lehrbuch, Folie oder Arbeitsblatt . . .

Gasentwicklung bei der Polyaddition 1. Vermischen einer Komponente mit leicht flüchtigen Stoffen 60 er Jahre Dichlor-difluor-methan (oder ähnlich aufgebaute FCKWs) Problematik: Schädigung der Ozonschicht durch radikalische Kettenreaktionen, FCKWs katalysieren Ozonabbau Vortrag: Schädigung der Ozonschicht durch radikalische Kettenreaktionen Material: Folie bzw. Skizze: Aufbau der Atmosphäre mit Lage der Ozonschicht (Ziel auch Wiederholung Radikalkettenmechanismus): Start: Fortplanzung 1: Fortplanzung 2: Kettenabbruch: Abspaltung Chlorradikal von Freon; Chlorradikal + Ozon --> O 2 + Cl. O-Radikal; Cl. O-Radikal + Ozon --> 2 O 2 + Chlorradikal Diskussion verschiedener Möglichkeiten
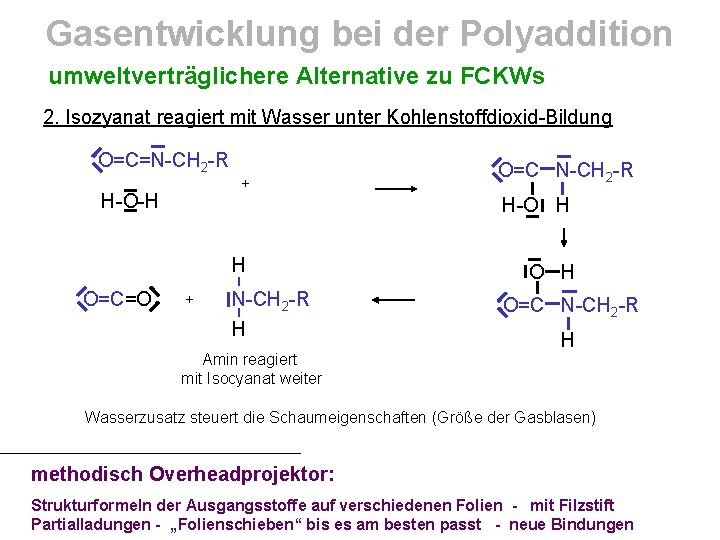
Gasentwicklung bei der Polyaddition umweltverträglichere Alternative zu FCKWs 2. Isozyanat reagiert mit Wasser unter Kohlenstoffdioxid-Bildung O=C=N-CH 2 -R + H-O-H H-O H + N-CH 2 -R H Amin reagiert mit Isocyanat weiter O H O=C=O O=C N-CH 2 -R H Wasserzusatz steuert die Schaumeigenschaften (Größe der Gasblasen) methodisch Overheadprojektor: Strukturformeln der Ausgangsstoffe auf verschiedenen Folien - mit Filzstift Partialladungen - „Folienschieben“ bis es am besten passt - neue Bindungen
- Slides: 9