Teorija ligandnog polja Slobodni atomi i ioni prelaznih
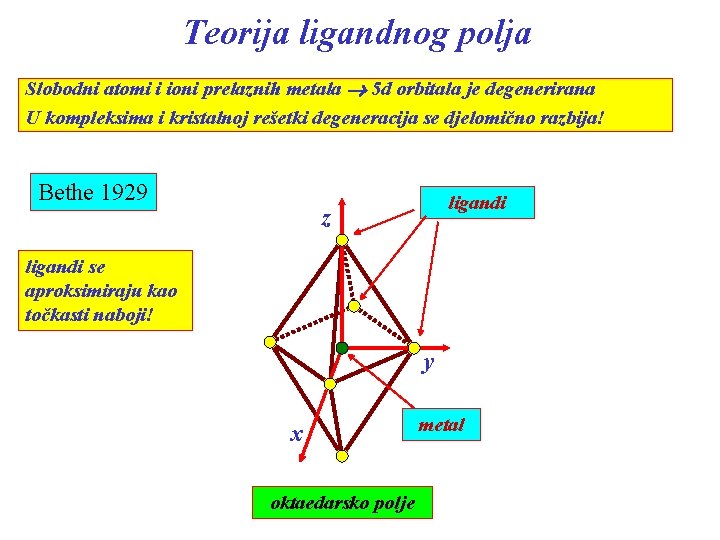
Teorija ligandnog polja Slobodni atomi i ioni prelaznih metala 5 d orbitala je degenerirana U kompleksima i kristalnoj rešetki degeneracija se djelomično razbija! Bethe 1929 ligandi z ligandi se aproksimiraju kao točkasti naboji! y x oktaedarsko polje metal
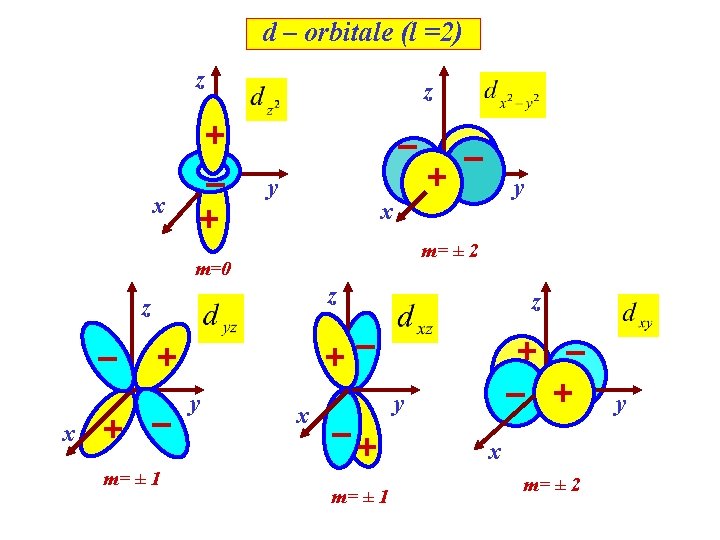
d – orbitale (l =2) z z x y m= ± 2 z z m= ± 1 z y x y x m=0 m= ± 1 x m= ± 2 y
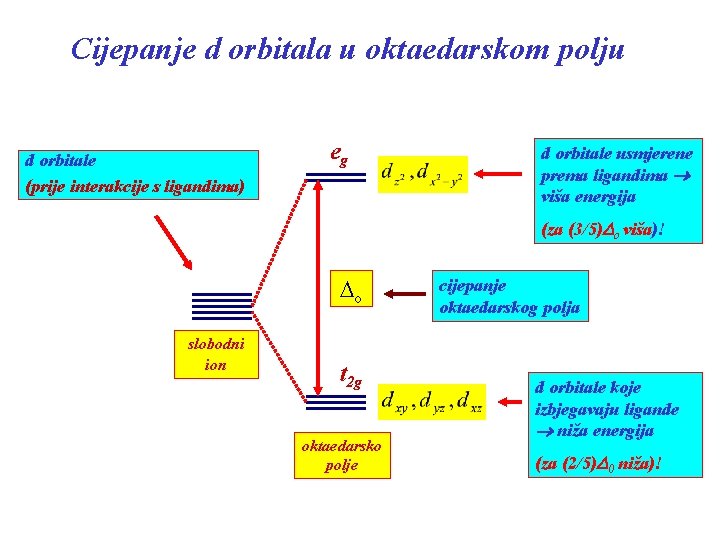
Cijepanje d orbitala u oktaedarskom polju d orbitale (prije interakcije s ligandima) eg d orbitale usmjerene prema ligandima viša energija (za (3/5)Do viša)! o slobodni ion t 2 g oktaedarsko polje cijepanje oktaedarskog polja d orbitale koje izbjegavaju ligande niža energija (za (2/5)D 0 niža)!
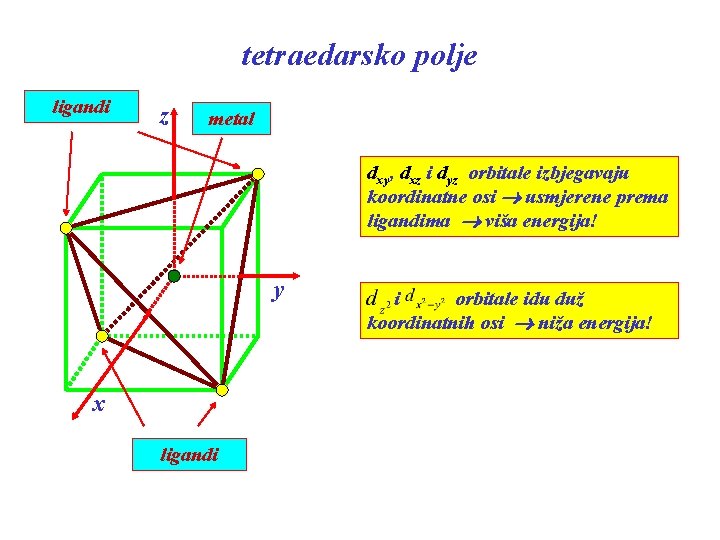
tetraedarsko polje ligandi z metal dxy, dxz i dyz orbitale izbjegavaju koordinatne osi usmjerene prema ligandima viša energija! y x ligandi i orbitale idu duž koordinatnih osi niža energija!
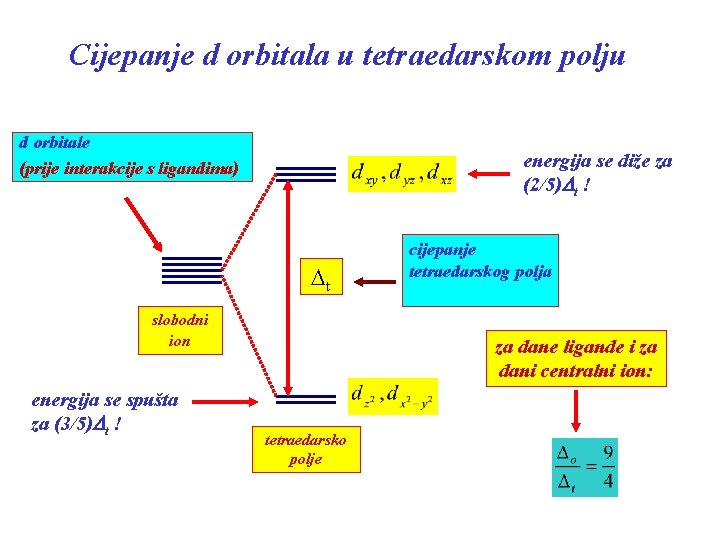
Cijepanje d orbitala u tetraedarskom polju d orbitale (prije interakcije s ligandima) energija se diže za (2/5)Dt ! t slobodni ion energija se spušta za (3/5)Dt ! cijepanje tetraedarskog polja za dane ligande i za dani centralni ion: tetraedarsko polje
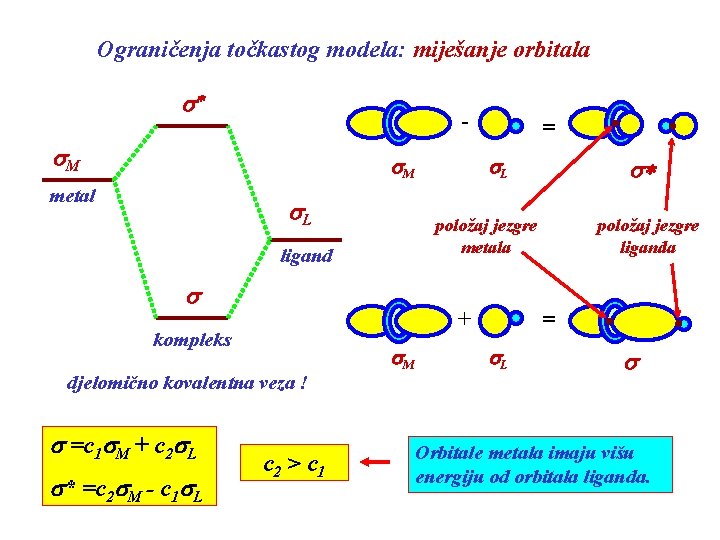
Ograničenja točkastog modela: miješanje orbitala s* - s. M metal s. L s + kompleks djelomično kovalentna veza ! s* =c 2 s. M - c 1 s. L c 2 > c 1 s* s. L položaj jezgre metala ligand s =c 1 s. M + c 2 s. L = s. M položaj jezgre liganda = s. L s Orbitale metala imaju višu energiju od orbitala liganda.
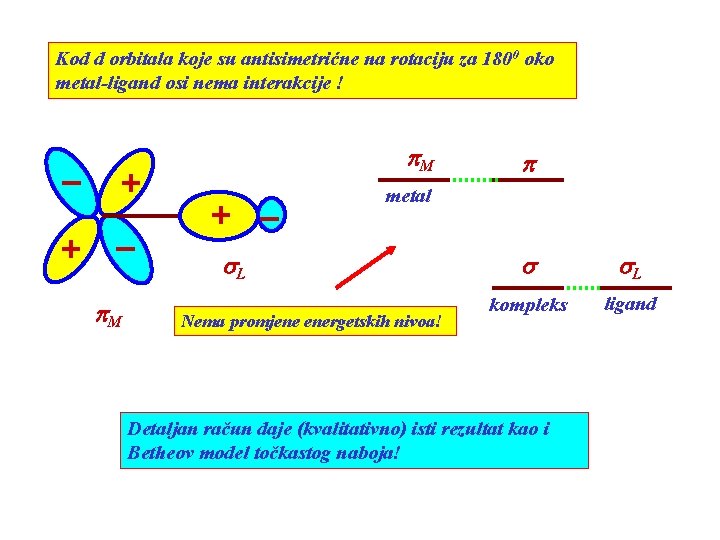
Kod d orbitala koje su antisimetrićne na rotaciju za 1800 oko metal-ligand osi nema interakcije ! p. M p metal s. L Nema promjene energetskih nivoa! s s. L kompleks ligand Detaljan račun daje (kvalitativno) isti rezultat kao i Betheov model točkastog naboja!
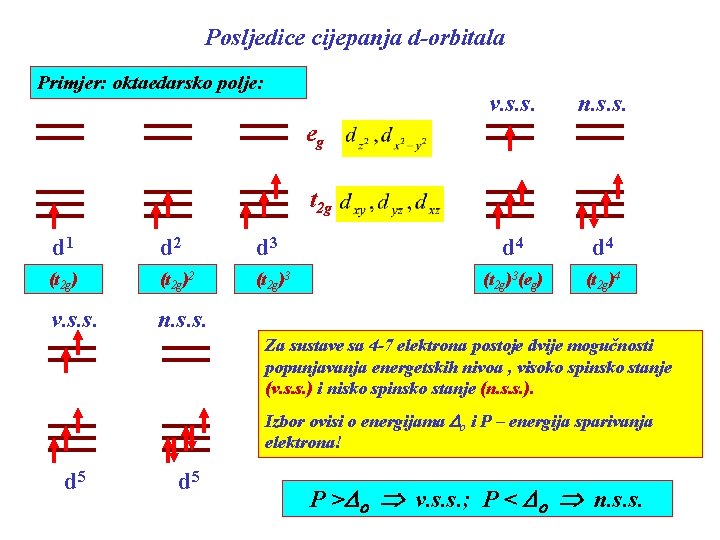
Posljedice cijepanja d-orbitala Primjer: oktaedarsko polje: v. s. s. n. s. s. d 4 (t 2 g)3(eg) (t 2 g)4 eg t 2 g d 1 d 2 d 3 (t 2 g)2 (t 2 g)3 v. s. s. n. s. s. Za sustave sa 4 -7 elektrona postoje dvije mogučnosti popunjavanja energetskih nivoa , visoko spinsko stanje (v. s. s. ) i nisko spinsko stanje (n. s. s. ). Izbor ovisi o energijama Do i P – energija sparivanja elektrona! d 5 P >Do v. s. s. ; P < Do n. s. s.
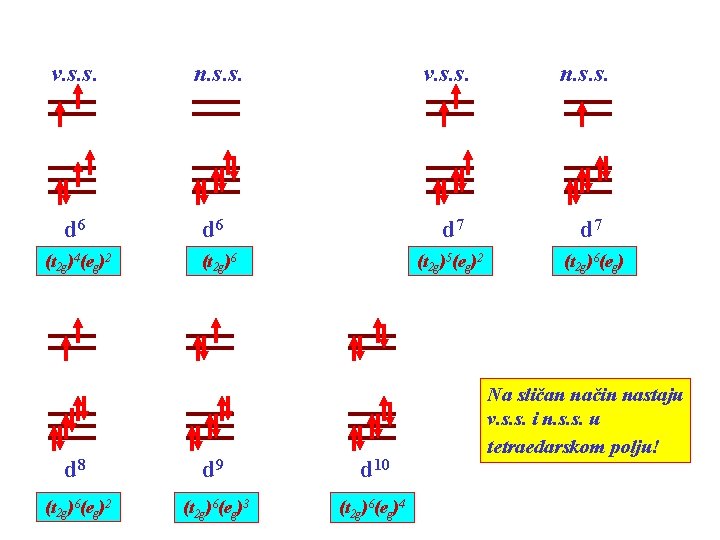
v. s. s. n. s. s. d 6 d 7 (t 2 g)5(eg)2 (t 2 g)6(eg) (t 2 g)4(eg)2 (t 2 g)6 d 8 d 9 d 10 (t 2 g)6(eg)2 (t 2 g)6(eg)3 (t 2 g)6(eg)4 Na sličan način nastaju v. s. s. i n. s. s. u tetraedarskom polju!
Posljedice cijepanja d-orbitala Prelazi t 2 g eg. Apsorpcija zračenja u vidljivom području. Kompleksni spojevi prelaznih metala su često intenzivno obojeni. Iz spektra se može procjeniti D. Ovisi o ligandu: D raste! I- < Br- < Cl- < F- < H 2 O ligandi s O < NH 3 ligandi s N < CNSpektroskopski niz! Magnetske posljedice: ukupni spin određuje magnetska svojstva. (susceptibilnost). Iz mjerenja tih svojstava može se odrediti elektronska struktura spoja!
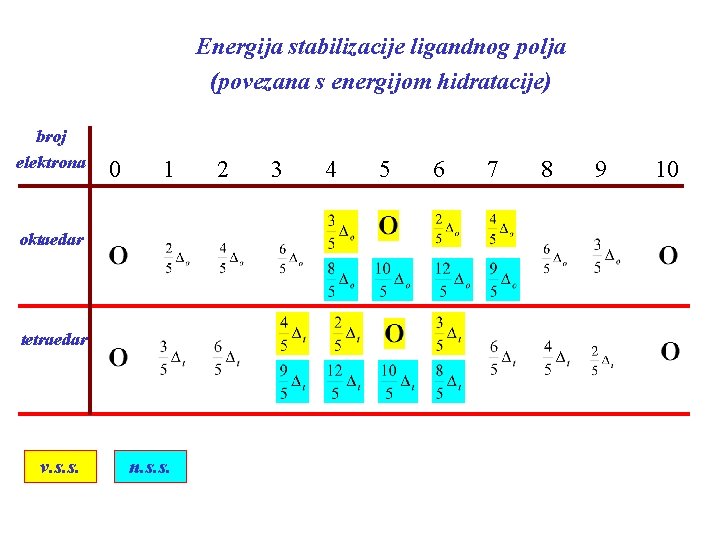
Energija stabilizacije ligandnog polja (povezana s energijom hidratacije) broj elektrona 0 1 oktaedar tetraedar v. s. s. n. s. s. 2 3 4 5 6 7 8 9 10

Pitanja Ligandno polje • Što se dešava sa d-orbitalama u ligandnom polju? Zašto? • Nacrtajte d-orbitale i objasnite u kom odnosu su te orbitale prema koordinatnim osima! • Tko je razvio teoriju ligandnog polja? Što je on predpostavio? • Kako se cijepaju d-orbitale u oktaedarskom polju? Zašto? • Kako se cijepaju d-orbitale u tetraedarskom polju? Zašto? • Za dani ligand i za dani centralni ion koji je odnos cijepanja u oktaedarskom i cijepanja u tetraedarskom polju? • Koji su nedostaci točkastog modela ligandnog polja? Kako se ligandno polje opisuje ako se u razmatranje uključe orbitale liganada? Što daje taj točniji pristup? • Koje su posljedice cijepanja d-orbitala u ligandnom polju? • Što su to visoko spinska a što nisko spinska stanja? Kada nastaje jedno a kada drugo stanje? Objasnite na primjeru oktaedarskog (tetraedarskog) polja! • Što je to spektroskopski niz? Objasnite! • Koji je utjecaj ligandnog polja na magnetska svojstva? • Objasnite energiju stabilizacije ligandnog polja!
- Slides: 12