Stowarzyszenie na Rzecz Dobrej Praktyki Bada Klinicznych w

Stowarzyszenie na Rzecz Dobrej Praktyki Badań Klinicznych w Polsce (Association for Good Clinical Practice in Poland) Badania kliniczne Wojciech Masełbas © GCPpl

Trochę statystyki GCPpl _____________________ • Na świecie co roku rozpoczyna się ok. 17 tys. badań klinicznych • Uczestniczy w nich ponad 1 milion osób (pacjentów lub zdrowych uczestników) • Łączne nakłady na Bi. R w przemyśle farmaceutycznym wynoszą ok. 50 mld USD/rok © GCPpl

Trochę statystyki GCPpl _____________________ • Na terenie Wspólnoty Europejskiej rozpoczyna się 5 -6 000 badań klinicznych rocznie, • uczestniczy w nich 400 -600 tys. osób (pacjentów lub zdrowych ochotników) – 64% badania bezpośrednio finansowane przez przemysł farmaceutyczny – 36% badania akademickie i inne (fundacje, granty 7 PR, IMI, itp. ) • Nakłady na Bi. R w Europie poniesione przez firmy zrzeszone w efpia wyniosły w 2009 r. 26 mld Euro • z tego 47, 8% (12, 4 mld Euro) stanowiły koszty badań klinicznych © GCPpl
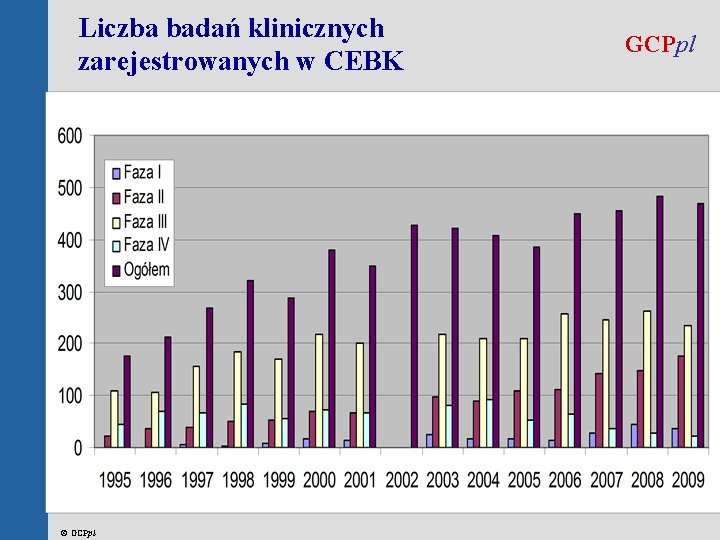
Liczba badań klinicznych zarejestrowanych w CEBK © GCPpl
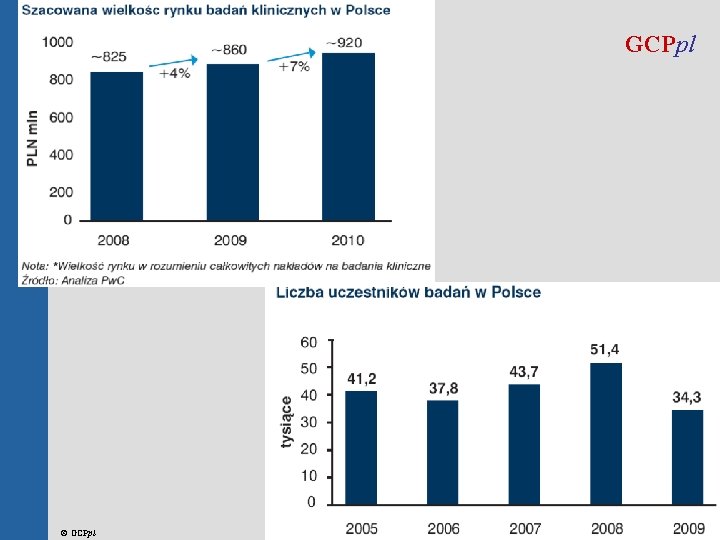
GCPpl © GCPpl
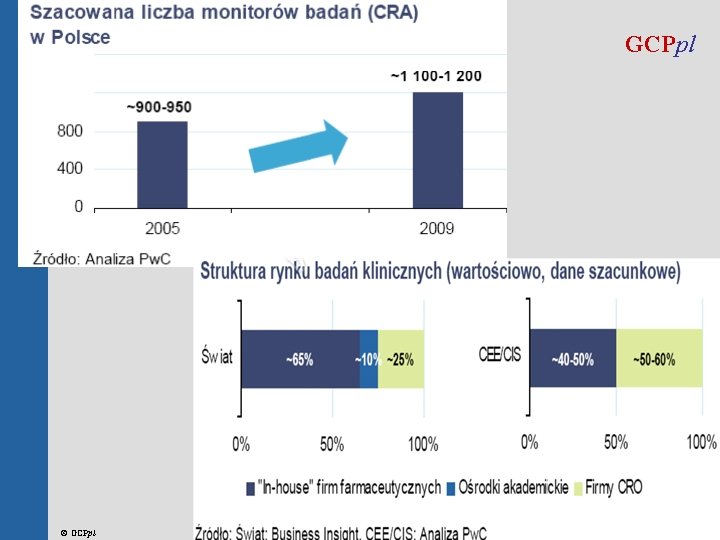
GCPpl © GCPpl
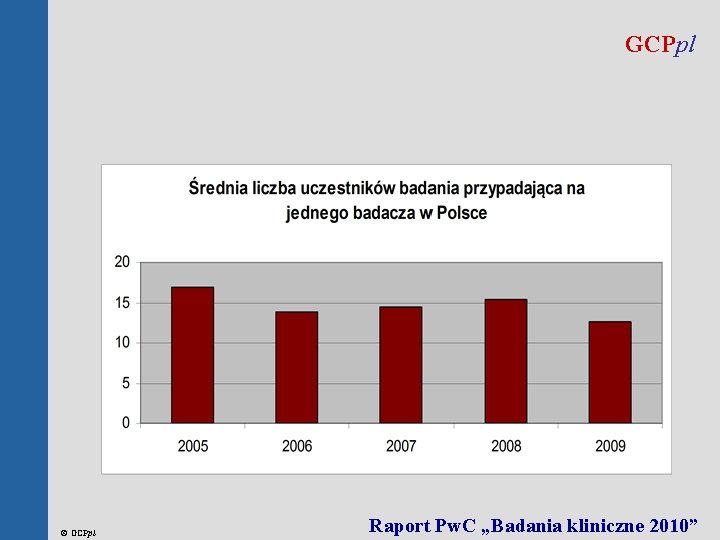
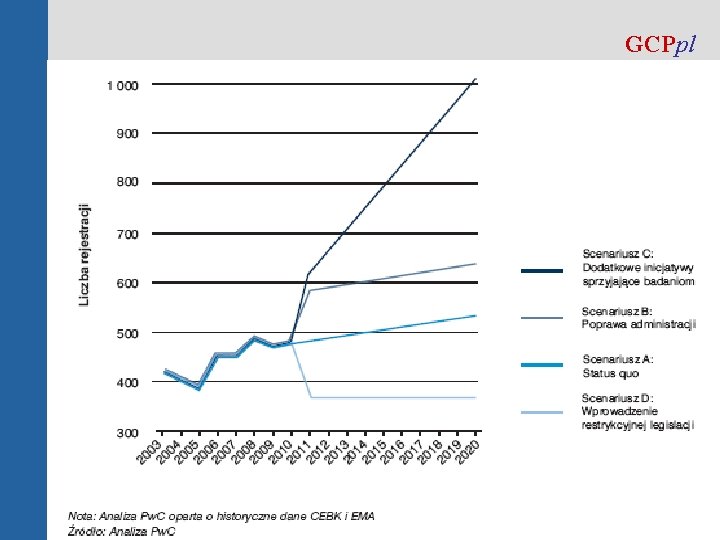
GCPpl © GCPpl Raport Pw. C „Badania kliniczne 2010”
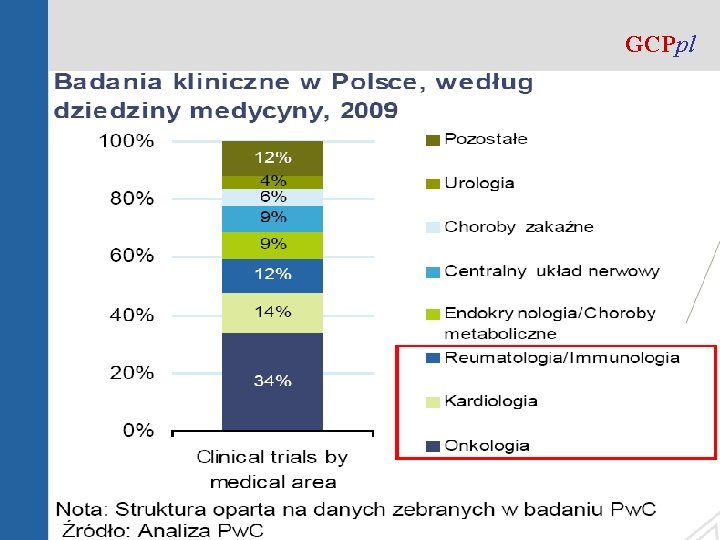
GCPpl © GCPpl
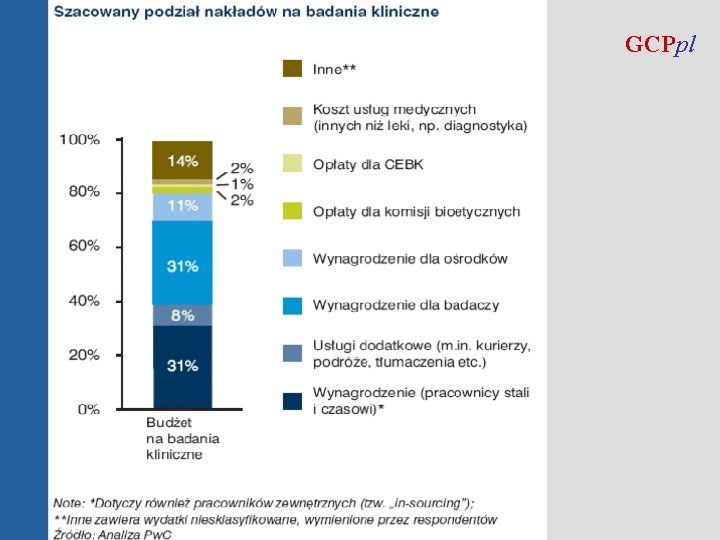
GCPpl © GCPpl
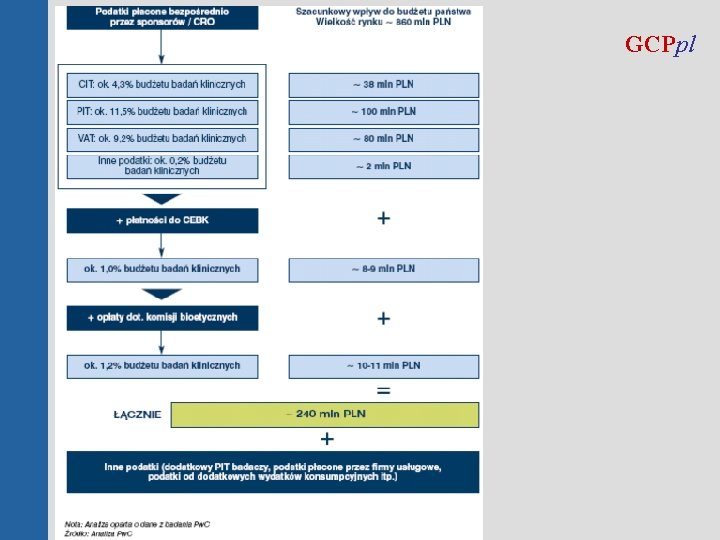
GCPpl © GCPpl

Rynek badań klinicznych – potencjał rozwoju GCPpl _____________________ • Wielka Brytania, Niemcy – około 1500 nowych badań rocznie • Australia – 700 badań na rok • Rosja – ponad 500 badań • Węgry, Czechy – około 300 badań na rok • Ukraina 185 badania kliniczne w 2007 r. • Bułgaria – 150 badań klinicznych w skali roku • Wielka Brytania, Belgia – przychody z tytułu Bi. R produktów leczniczych ok. 7 mld Euro rocznie • Wiele krajów aktywnie zabiega o zwiększenie ilości badań klinicznych prowadzonych na ich terytorium © GCPpl
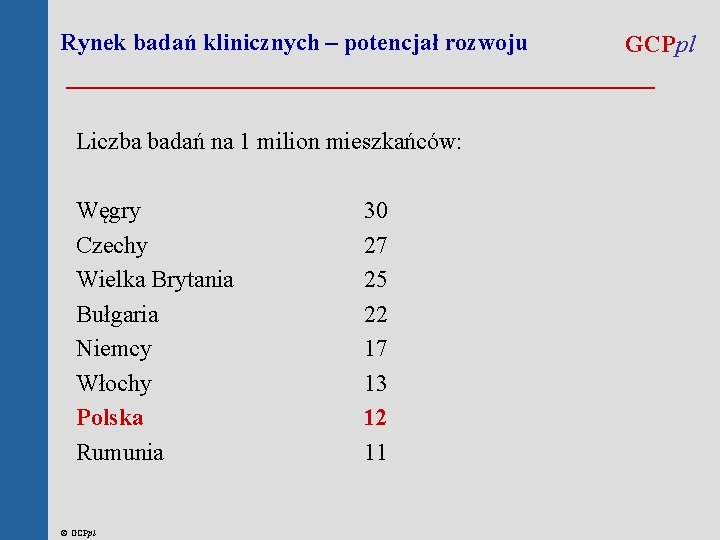
Rynek badań klinicznych – potencjał rozwoju GCPpl _____________________ Liczba badań na 1 milion mieszkańców: Węgry Czechy Wielka Brytania Bułgaria Niemcy Włochy Polska Rumunia © GCPpl 30 27 25 22 17 13 12 11

Bariery rozwoju GCPpl _____________________ • Długi czas uzyskiwania pozwoleń na rozpoczęcie badania • Brak harmonizacji wymagań między komisjami bioetycznymi a URPL • Mnogość i nieprzewidywalność wymagań administracyjnych • Częste zmiany interpretacji przepisów (komunikaty, informacje na stronie internetowej, zalecenia ustne) a jednocześnie… • Zbyt wolne zmiany prawa, które nie nadąża za rozwojem nauki oraz wymaganiami współczesnego świata (Polska do tej pory nie implementowała Dyrektywy 2005/28/EC mimo, że termin jej włączenia do krajowego prawodawstwa minął w styczniu 2006 r. ) © GCPpl
GCPpl © GCPpl
- Slides: 14