SIRDS KANALOPTIJAS PRIMRAS SIRDS ELEKTRISKAS SASLIMANAS Mrti Purenkovs


















- Slides: 54

SIRDS KANALOPĀTIJAS (PRIMĀRAS SIRDS ELEKTRISKAS SASLIMŠANAS). Mārtiņš Purenkovs MF VI kurss

Sirds jonu kanāli. • Kanālus nosauc tā jona vārdā, kuru visvairāk tas laiž cauri; • Nozīmīgākie ir K, Na, Cl kanāli; • Visi kanāli nav selektīvi tikai vienam jonam, tie laiž cauri arī citus jonus, piemēram, Ca jonu atkarīgie kanāliem permeabilitāte(P(K)/P(Ca)) ir 1: 3000 un tie ir necaurlaidīgi anjoniem; • Jonu kustība, virziens passīvi cauri atvērtam jonu kanālam pie jebkura transmembrānas potenciāla tiek kontrolēta ar atgriezenisko šī jona potenciālu un jonu koncentrāciju abpus membrānai, un to virzības ātrums ir lielāks tad, ja tie pārvietojas no augstākas koncentrācijas uz zemāku; • Visi jonu kanāli sastāv no poru formējošām alfa subvienībām un papildus – beta, delta, gamma. Šo molekulu savstarpējās attiecības un uzbūve nodrošina dažādu jonu caurlaidību. Tāpat kā izmaiņas noved pie dažādām sirds saslimšanām un var būt par pamatu aritmiju attīstībai. • Jonu kanāliem nav sliekšņa potenciāla, pie kura tie visi atveras un līdzīgi tāpat aizveras, šis process ir pakāpenisks. Pēc pilnīgas aktivācijas tie atjaunojas un paliek inaktivēti, pēc kuras var atkal aktivizēties pie attiecīgiem potenciāliem. Katram kanālam ir savs atjaunošanās laiks.

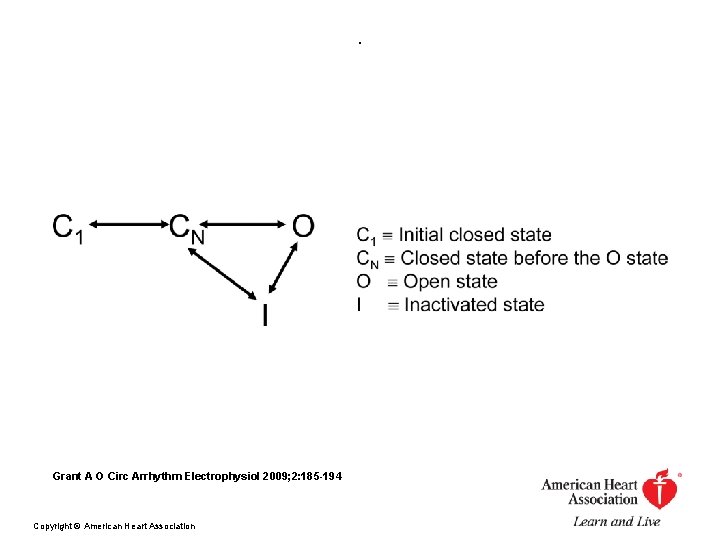
. Grant A O Circ Arrhythm Electrophysiol 2009; 2: 185 -194 Copyright © American Heart Association

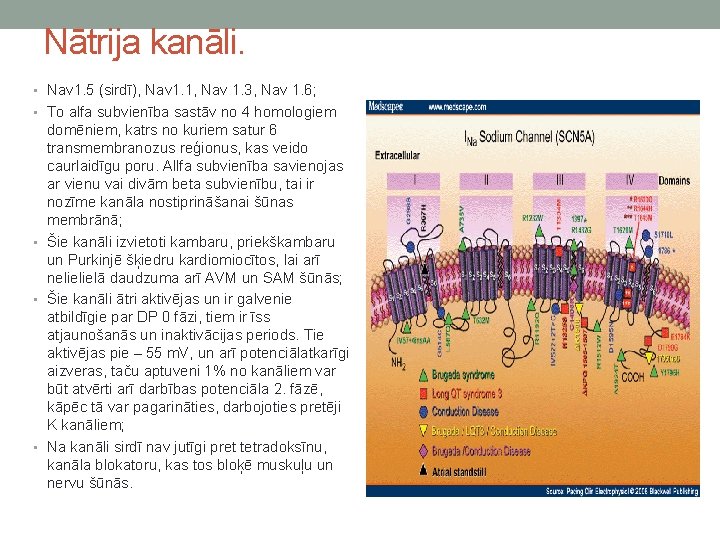
Nātrija kanāli. • Nav 1. 5 (sirdī), Nav 1. 1, Nav 1. 3, Nav 1. 6; • To alfa subvienība sastāv no 4 homologiem domēniem, katrs no kuriem satur 6 transmembranozus reģionus, kas veido caurlaidīgu poru. Allfa subvienība savienojas ar vienu vai divām beta subvienību, tai ir nozīme kanāla nostiprināšanai šūnas membrānā; • Šie kanāli izvietoti kambaru, priekškambaru un Purkinjē šķiedru kardiomiocītos, lai arī nelielielā daudzuma arī AVM un SAM šūnās; • Šie kanāli ātri aktivējas un ir galvenie atbildīgie par DP 0 fāzi, tiem ir īss atjaunošanās un inaktivācijas periods. Tie aktivējas pie – 55 m. V, un arī potenciālatkarīgi aizveras, taču aptuveni 1% no kanāliem var būt atvērti arī darbības potenciāla 2. fāzē, kāpēc tā var pagarināties, darbojoties pretēji K kanāliem; • Na kanāli sirdī nav jutīgi pret tetradoksīnu, kanāla blokatoru, kas tos bloķē muskuļu un nervu šūnās.

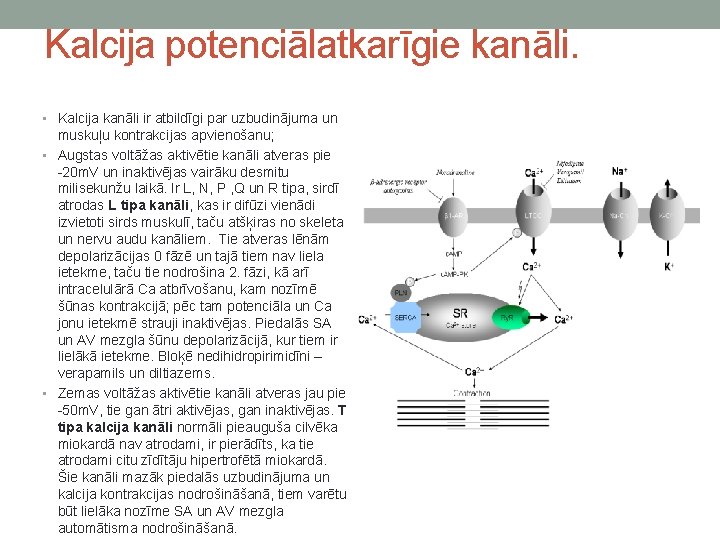
Kalcija potenciālatkarīgie kanāli. • Kalcija kanāli ir atbildīgi par uzbudinājuma un muskuļu kontrakcijas apvienošanu; • Augstas voltāžas aktivētie kanāli atveras pie -20 m. V un inaktivējas vairāku desmitu milisekunžu laikā. Ir L, N, P , Q un R tipa, sirdī atrodas L tipa kanāli, kas ir difūzi vienādi izvietoti sirds muskulī, taču atšķiras no skeleta un nervu audu kanāliem. Tie atveras lēnām depolarizācijas 0 fāzē un tajā tiem nav liela ietekme, taču tie nodrošina 2. fāzi, kā arī intracelulārā Ca atbrīvošanu, kam nozīmē šūnas kontrakcijā; pēc tam potenciāla un Ca jonu ietekmē strauji inaktivējas. Piedalās SA un AV mezgla šūnu depolarizācijā, kur tiem ir lielākā ietekme. Bloķē nedihidropirimidīni – verapamils un diltiazems. • Zemas voltāžas aktivētie kanāli atveras jau pie -50 m. V, tie gan ātri aktivējas, gan inaktivējas. T tipa kalcija kanāli normāli pieauguša cilvēka miokardā nav atrodami, ir pierādīts, ka tie atrodami citu zīdītāju hipertrofētā miokardā. Šie kanāli mazāk piedalās uzbudinājuma un kalcija kontrakcijas nodrošināšanā, tiem varētu būt lielāka nozīme SA un AV mezgla automātisma nodrošināšanā.

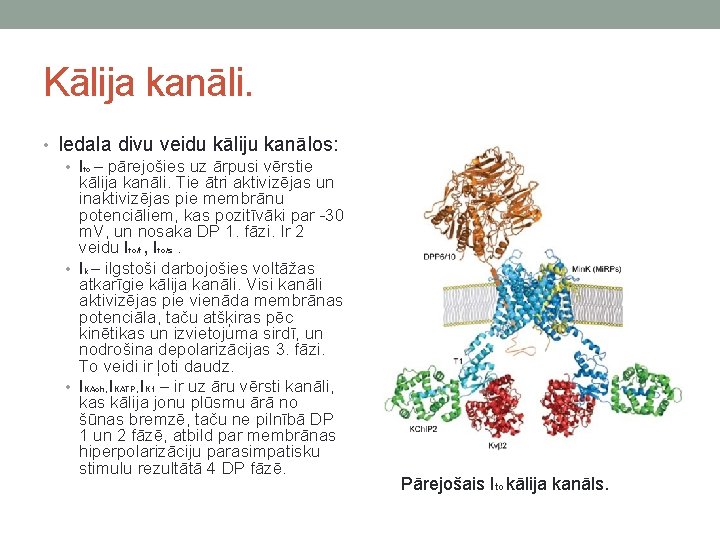
Kālija kanāli. • Iedala divu veidu kāliju kanālos: • Ito – pārejošies uz ārpusi vērstie kālija kanāli. Tie ātri aktivizējas un inaktivizējas pie membrānu potenciāliem, kas pozitīvāki par -30 m. V, un nosaka DP 1. fāzi. Ir 2 veidu Ito/f , Ito/s. • Ik – ilgstoši darbojošies voltāžas atkarīgie kālija kanāli. Visi kanāli aktivizējas pie vienāda membrānas potenciāla, taču atšķiras pēc kinētikas un izvietojuma sirdī, un nodrošina depolarizācijas 3. fāzi. To veidi ir ļoti daudz. • IKAch, IKATP, IK 1 – ir uz āru vērsti kanāli, kas kālija jonu plūsmu ārā no šūnas bremzē, taču ne pilnībā DP 1 un 2 fāzē, atbild par membrānas hiperpolarizāciju parasimpatisku stimulu rezultātā 4 DP fāzē. Pārejošais Ito kālija kanāls.

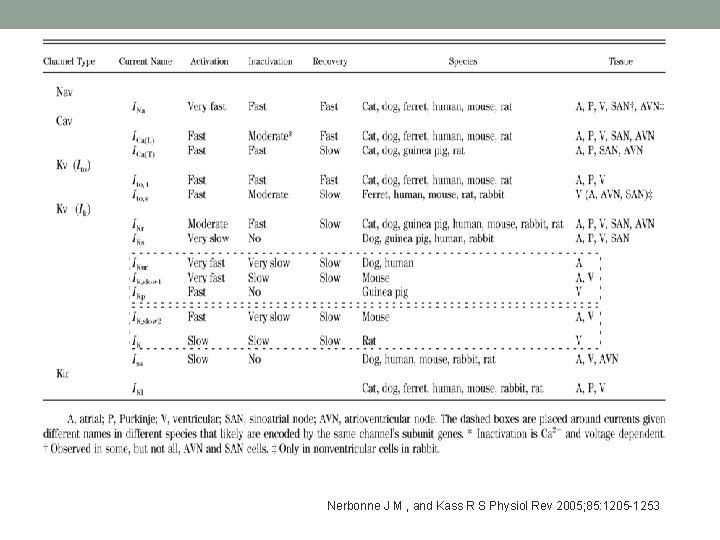
Nerbonne J M , and Kass R S Physiol Rev 2005; 85: 1205 -1253

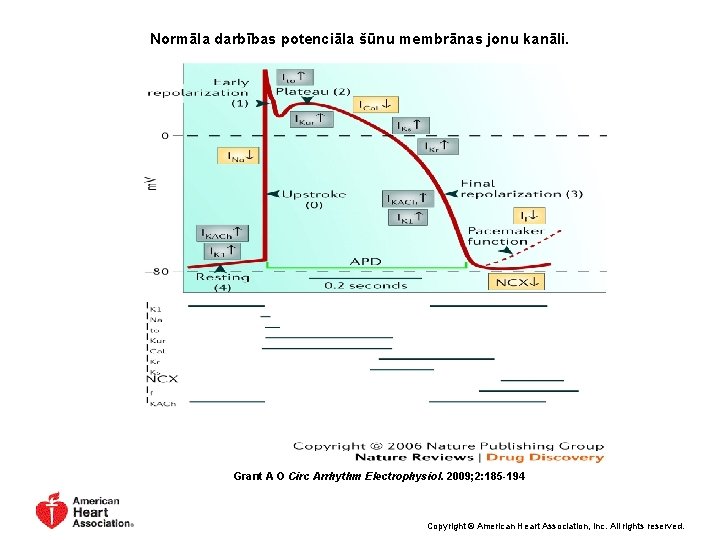
Normāla darbības potenciāla šūnu membrānas jonu kanāli. Grant A O Circ Arrhythm Electrophysiol. 2009; 2: 185 -194 Copyright © American Heart Association, Inc. All rights reserved.

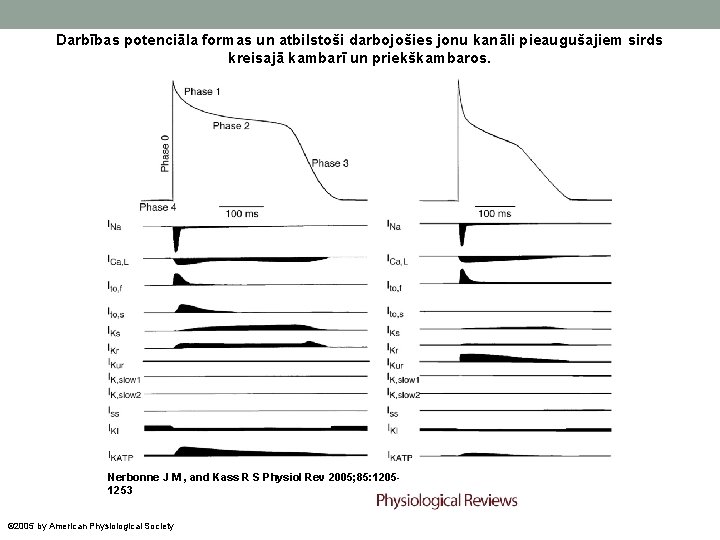
Darbības potenciāla formas un atbilstoši darbojošies jonu kanāli pieaugušajiem sirds kreisajā kambarī un priekškambaros. Nerbonne J M , and Kass R S Physiol Rev 2005; 85: 12051253 © 2005 by American Physiological Society


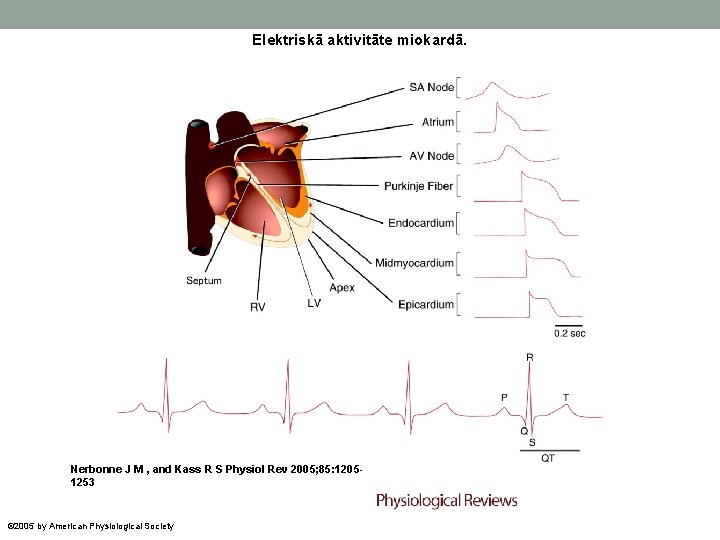
Elektriskā aktivitāte miokardā. Nerbonne J M , and Kass R S Physiol Rev 2005; 85: 12051253 © 2005 by American Physiological Society

Sirds kanalopātijas. • Ģenētiskas sirds saslimšanas, kuras raksturo izmainīta sirds uzbudinātība un nav strukturālas sirds slimības (iedzimtas aritmogēnas sirds slimības, primāras elektriskas slimības). • Pēkšņa kardiāla nāve Austrālijā jaunākiem par 36 gadiem (Doolan et al. 2004).

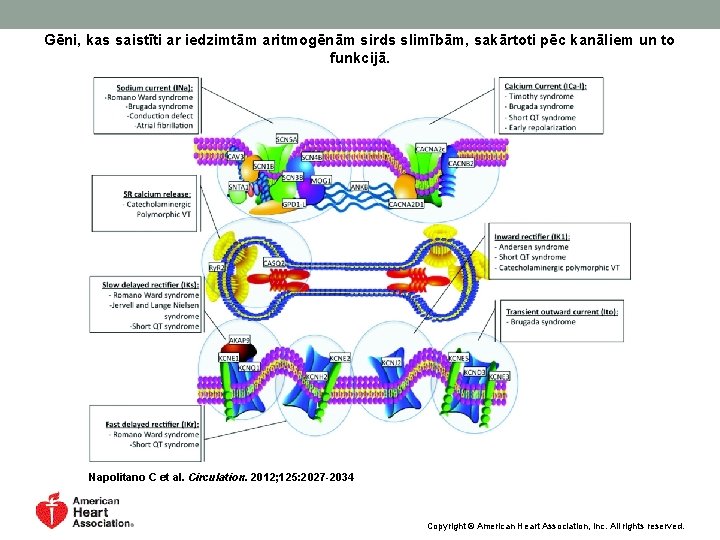
Gēni, kas saistīti ar iedzimtām aritmogēnām sirds slimībām, sakārtoti pēc kanāliem un to funkcijā. Napolitano C et al. Circulation. 2012; 125: 2027 -2034 Copyright © American Heart Association, Inc. All rights reserved.

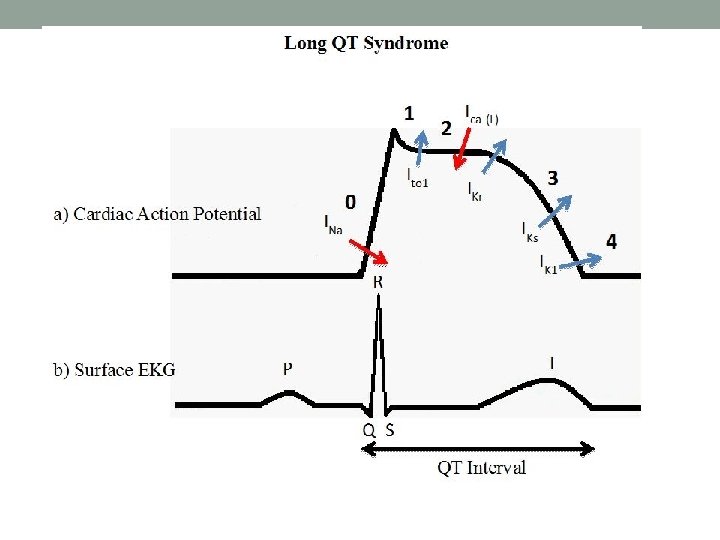
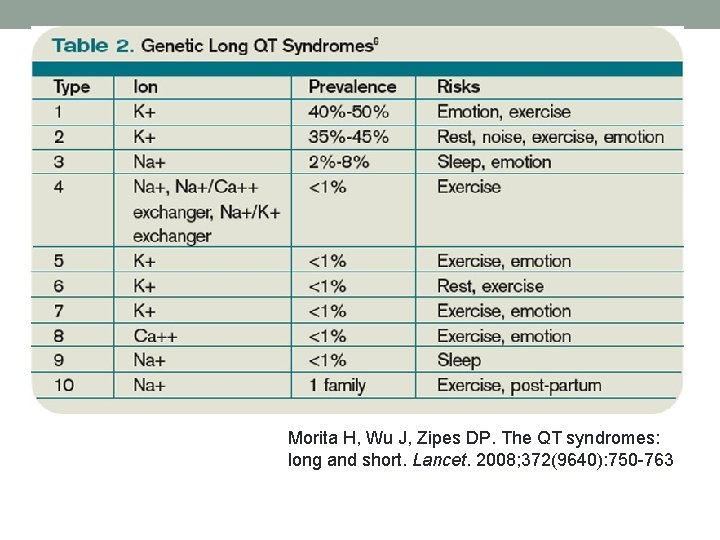
Pagarināta QT sindroms. • Iedzimta slimību grupa, kas raksturojas pagarinātu QT intervālu un izmainītu T vilni elektrokardiogrammā. • 1: 10 000 • QTc: • Bazetta formula = QT / √ (RR interval); • Friderika formula =QT / (RR)0. 33. • QTc > 480 msec, > 440 msec (vīriešiem), > 460 msec (sievietēm). • Pagarinās darbības potenciāls sakarā ar izmainīt jonu kanālu darbību. • 12 pagarināta QT sindromi (LQT 1, 2. . . ). • 75 - 90% gadījumu LQT 1, LQT 2, LQT 3. • 20 – 25 % gadījumu nav atrodama mutācija.



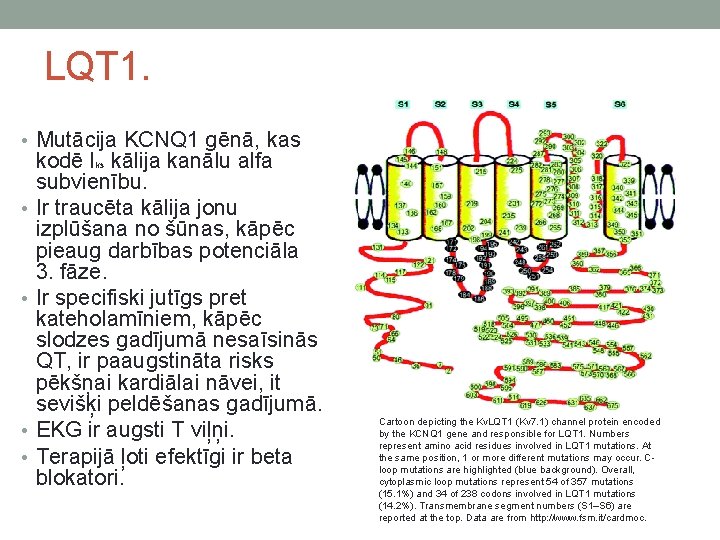
LQT 1. • Mutācija KCNQ 1 gēnā, kas • • kodē Iks kālija kanālu alfa subvienību. Ir traucēta kālija jonu izplūšana no šūnas, kāpēc pieaug darbības potenciāla 3. fāze. Ir specifiski jutīgs pret kateholamīniem, kāpēc slodzes gadījumā nesaīsinās QT, ir paaugstināta risks pēkšņai kardiālai nāvei, it sevišķi peldēšanas gadījumā. EKG ir augsti T viļņi. Terapijā ļoti efektīgi ir beta blokatori. Cartoon depicting the Kv. LQT 1 (Kv 7. 1) channel protein encoded by the KCNQ 1 gene and responsible for LQT 1. Numbers represent amino acid residues involved in LQT 1 mutations. At the same position, 1 or more different mutations may occur. Cloop mutations are highlighted (blue background). Overall, cytoplasmic loop mutations represent 54 of 357 mutations (15. 1%) and 34 of 238 codons involved in LQT 1 mutations (14. 2%). Transmembrane segment numbers (S 1–S 6) are reported at the top. Data are from http: //www. fsm. it/cardmoc.

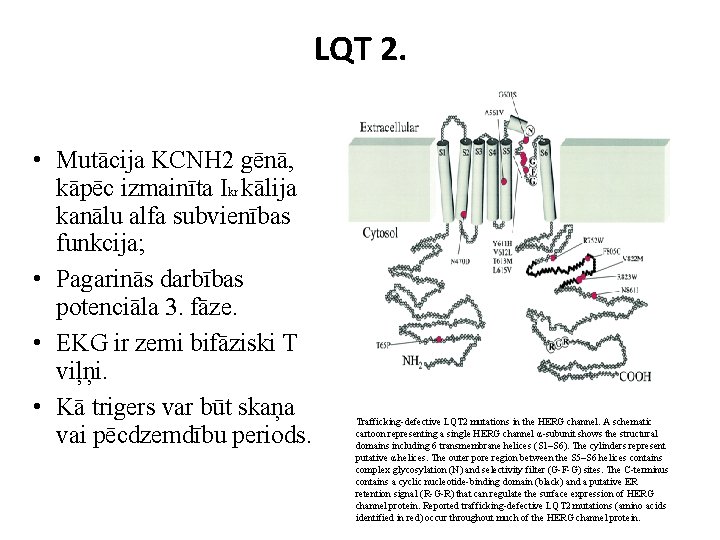
LQT 2. • Mutācija KCNH 2 gēnā, kāpēc izmainīta Ikr kālija kanālu alfa subvienības funkcija; • Pagarinās darbības potenciāla 3. fāze. • EKG ir zemi bifāziski T viļņi. • Kā trigers var būt skaņa vai pēcdzemdību periods. Trafficking-defective LQT 2 mutations in the HERG channel. A schematic cartoon representing a single HERG channel α-subunit shows the structural domains including 6 transmembrane helices (S 1–S 6). The cylinders represent putative α helices. The outer pore region between the S 5–S 6 helices contains complex glycosylation (N) and selectivity filter (G-F-G) sites. The C-terminus contains a cyclic nucleotide-binding domain (black) and a putative ER retention signal (R-G-R) that can regulate the surface expression of HERG channel protein. Reported trafficking-defective LQT 2 mutations (amino acids identified in red) occur throughout much of the HERG channel protein.

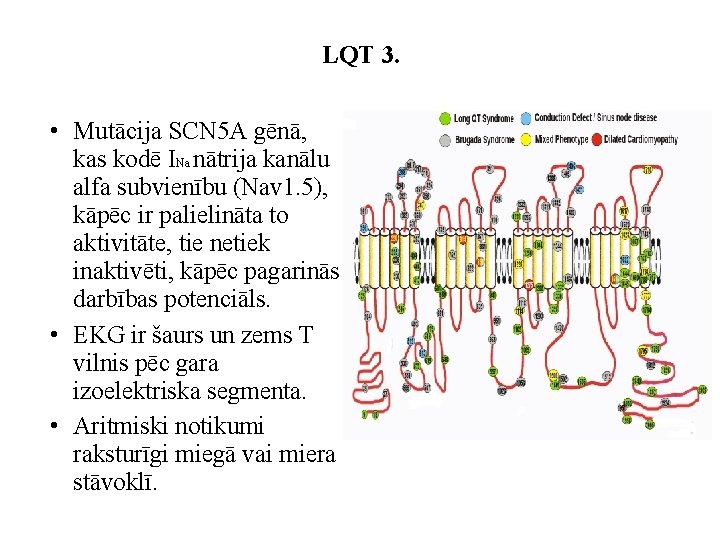
LQT 3. • Mutācija SCN 5 A gēnā, kas kodē INa nātrija kanālu alfa subvienību (Nav 1. 5), kāpēc ir palielināta to aktivitāte, tie netiek inaktivēti, kāpēc pagarinās darbības potenciāls. • EKG ir šaurs un zems T vilnis pēc gara izoelektriska segmenta. • Aritmiski notikumi raksturīgi miegā vai miera stāvoklī.

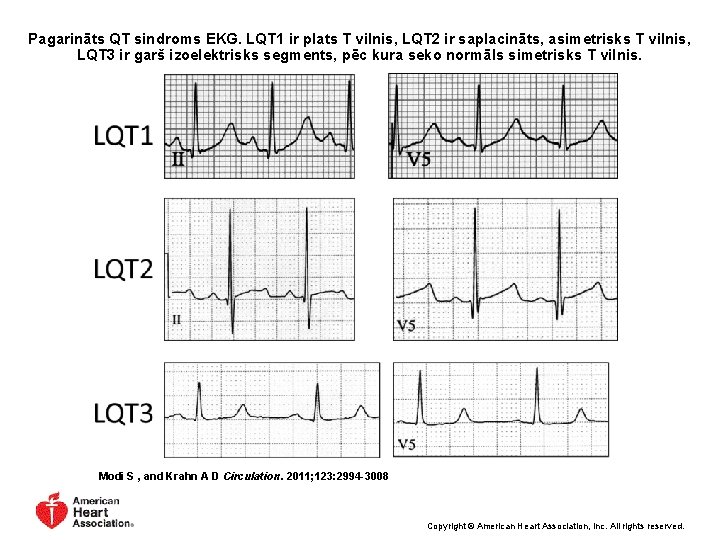
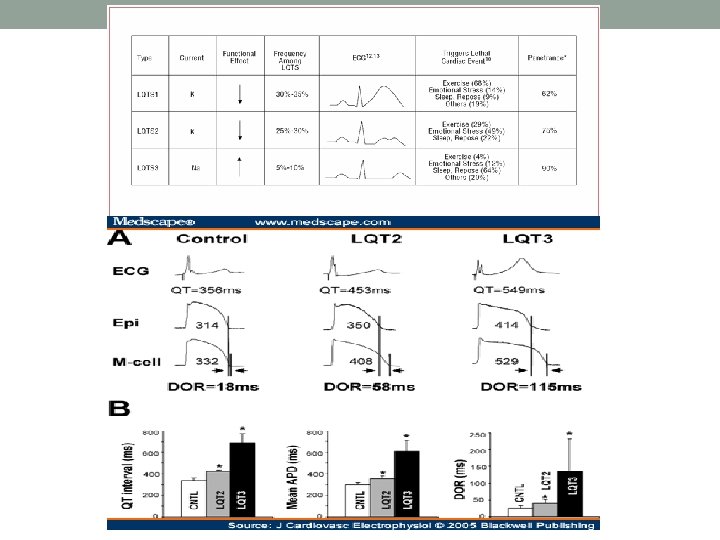
Pagarināts QT sindroms EKG. LQT 1 ir plats T vilnis, LQT 2 ir saplacināts, asimetrisks T vilnis, LQT 3 ir garš izoelektrisks segments, pēc kura seko normāls simetrisks T vilnis. Modi S , and Krahn A D Circulation. 2011; 123: 2994 -3008 Copyright © American Heart Association, Inc. All rights reserved.


Morita H, Wu J, Zipes DP. The QT syndromes: long and short. Lancet. 2008; 372(9640): 750 -763

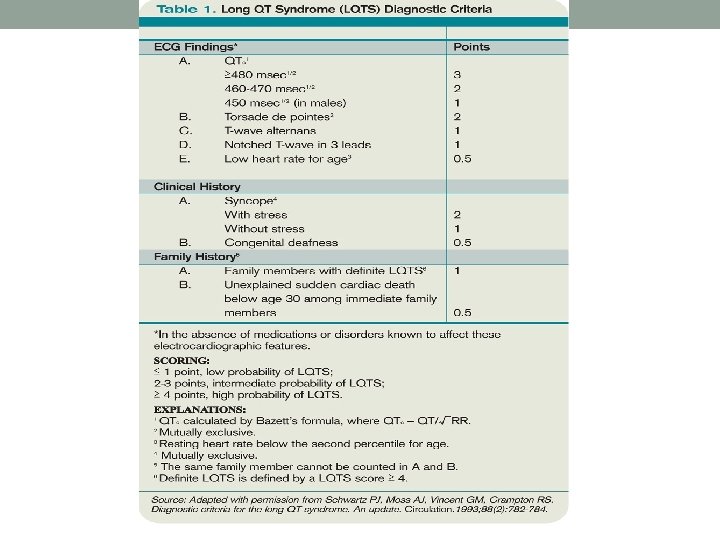
Klīniskā aina. • EKG raksturīgās izmaiņas – pagarināts QT (var būt arī nepilnīga penetrance, kuras gadījumā QTc garums var būt pelēkajā zonā (420 – 460 ms), izmainīts T vilnis). • Sinkope, ko izraisījusi polimorfa vetrikulāra tahikardija (torsades de pointes), kas var pāriet ventrikulārā fibrilācijā un izraisīt pēkšņu nāvi veicinošo faktoru ietekmē atkarībā no sindroma veida. • Vidējais simptomu attīstības vecums 12 gadi. • Prognozi nosaka vecums, QTc garums (>500 ms 5 kārtīgi pieaug kardiālas nāves risks), sieviešu dzimums (pēcdzemdību periods).

Diagnostika. • Jānosaka kālija, magnija līmenis asinīs, vairogdziedzera funkcija, citas repolarizācijas izmaiņas nosakoši faktori, medikamenti. • EKG. • Farmakoloģiski provokācijas testi ar epinefrīnu un izoprotenerolu. • Ģenētiskie testi.


Ārstēšana. • Beta blokatori: nadolols, metoprolols, propranolols, atenolols. Laba efektivitāte LQT 1 gadījumā. • LQT 3 gadījumā mexiletin (nātrija kanālu blokators). • Kardiostimulators un kardioverteris – defibrilators. • Simpātiskā sirds denervācija (kreisās puses cervikotorokāla stellectomija). • Dzīvesveida maiņa, lai mazinātu veicinošos faktorus, kas provocē aritmiju. • Nedrīkst lietot medikamentus, kas pagarina QT inetvālu. Jāizvairās no hipokaliēmiju provocējošiem stāvokļiem (diareja u. c. ).

QT intervālu pagarinošie medikamenti. • Astmas preparāti, adrenalīnu kā lokālo anestētiķi; • Hipokaliēmiju veicinošie medikamenti (indapamīds, diareju un vemšanu veicinoši līdzekļi, epleronons); • Psihotropie līdzekļi (haloperidols u. c. ); • Pretsēnīšu preparāti (ketokanozols, flukanazols, itrakonazols); • Cisaprīds (GERS ārstēšanā); • Antiaritmiķi ( Kvinidīns, Prokaīnamīds, Dizopiramīds, Sotalols, Probukols, Dofetilīds, Ibutilīds). • Antibiotikas (eritromicīns, biseptols); • Antihistamīna preparāti (terfenadīns, astemizols, difenhidramīns).

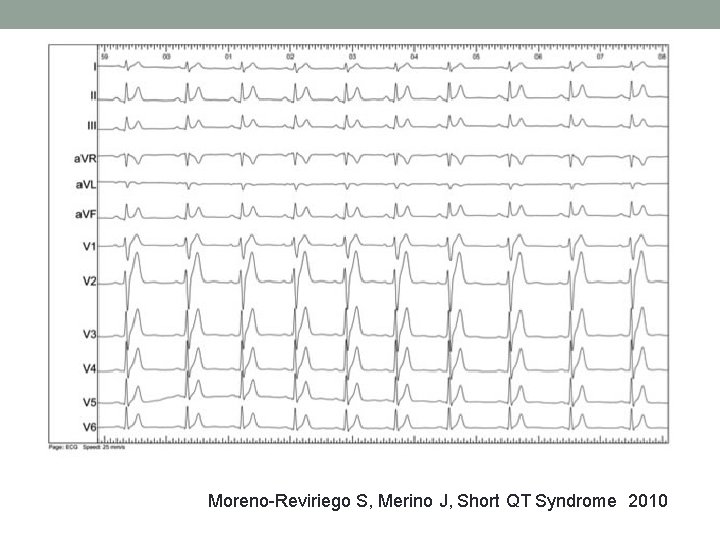
Saīsināta QT sindroms. • Iedzimta sirds jonopātija, kas raksturojas ar saīsinātu QT intervālu un • • • paaugstinātu risku attīstīties ātriju un kambaru fibrilācijai. Diagnoze pamatojas uz simptomu, ģimenes anamnēzes un 12 novadījumu EKG pieraksta datiem. 5 sindroma varianti. Autosomāli dominanta saslimšana. Nezināma prevelence. QTc < 340 ms (QT < 320 ms). Klīniskā aina: • Pēkšņa kardiāla nāve 28 % gadījumu ir pirmā klīniskā pazīme vidēji 30 gadu vecumā; • Sinkope 24 % gadījumos, kuru izraisījusi Ventrikulāra fibrilācija; • Agrīna priekškambaru mirgošana 80% pacientu. • Sekundāri iemesli: hipertermija, hiperkaliēmija, hiperkalcēmija, acidoze. • Diagnostika: ģimenes anamnēze, klīnika, EKG (īss QT intervāls, nav ST segmenta, izmainīts T vilnis), elektrofizioloģiska izmeklēšana (VF ierosināšana), ģenētiska testēšana. • Ārstēšna: • Kardioverteris – defibrilators (ir jābūt uzstādītam, lai nebūtu pastiprināta jutība pret T vilni); • Medikamentoza terpaija (zināma tikai SQT 1) – Kvinidīns, Dizopiramīds, Propafenons (ĀF profilaksei).

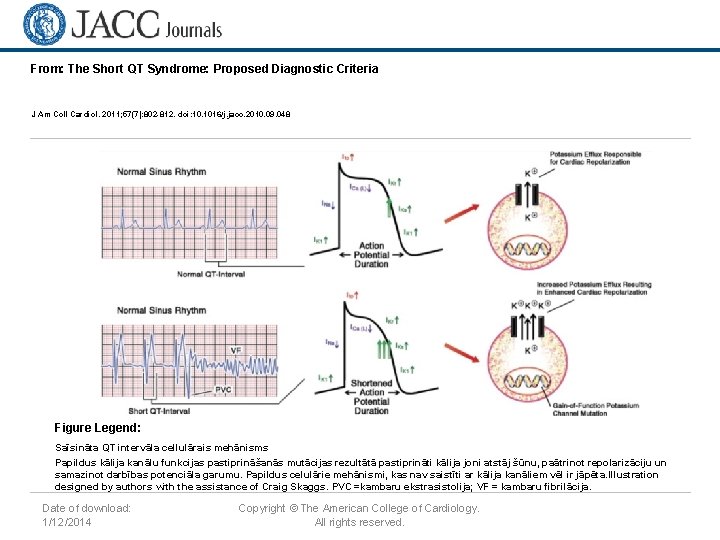
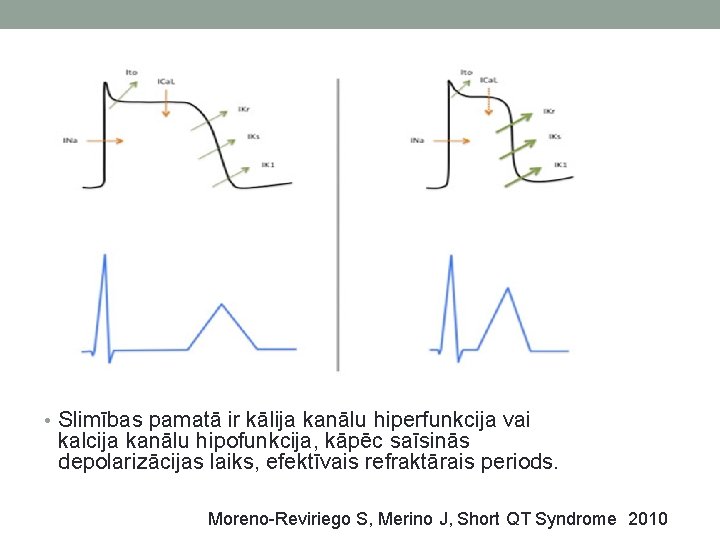
From: The Short QT Syndrome: Proposed Diagnostic Criteria J Am Coll Cardiol. 2011; 57(7): 802 -812. doi: 10. 1016/j. jacc. 2010. 09. 048 Figure Legend: Saīsināta QT intervāla cellulārais mehānisms Papildus kālija kanālu funkcijas pastiprināšanās mutācijas rezultātā pastiprināti kālija joni atstāj šūnu, paātrinot repolarizāciju un samazinot darbības potenciāla garumu. Papildus celulārie mehānismi, kas nav saistīti ar kālija kanāliem vēl ir jāpēta. Illustration designed by authors with the assistance of Craig Skaggs. PVC =kambaru ekstrasistolija; VF = kambaru fibrilācija. Date of download: 1/12/2014 Copyright © The American College of Cardiology. All rights reserved.

• Slimības pamatā ir kālija kanālu hiperfunkcija vai kalcija kanālu hipofunkcija, kāpēc saīsinās depolarizācijas laiks, efektīvais refraktārais periods. Moreno-Reviriego S, Merino J, Short QT Syndrome 2010

Moreno-Reviriego S, Merino J, Short QT Syndrome 2010

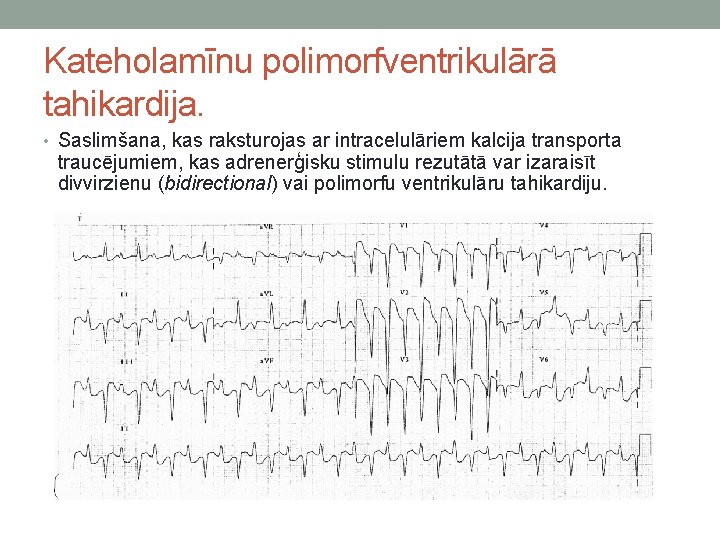
Kateholamīnu polimorfventrikulārā tahikardija. • Saslimšana, kas raksturojas ar intracelulāriem kalcija transporta traucējumiem, kas adrenerģisku stimulu rezutātā var izaraisīt divvirzienu (bidirectional) vai polimorfu ventrikulāru tahikardiju.

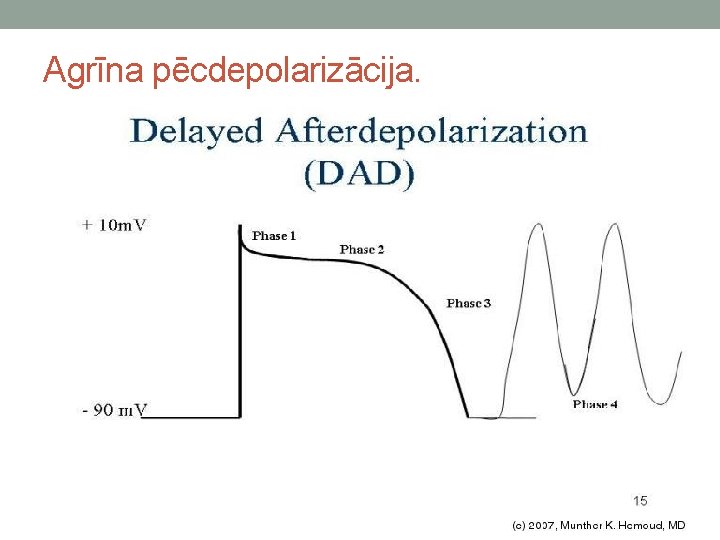
Patoģenēze. • Slimības pamatā ir mutācija Ry. R 2 (95 – 97% gadījumu) vai CASQ 2, • • • atsevišķos gadījumos iespējams KCNJ 2, kas ir saistīts ar LQT 7 (Andersena sindromu) vai mutāciju anikrīna B gēnā. Rianodīns – jonu kanāls sarkoplazmatiskajā tīklā, caur kuru kalcija joni nonāk kardiomiocītu citoplazmā un nosaka to kontrakciju. Kalsekvestrīns – kalcija saistošs proteīns, kas saista kalciju sarkoplazmatiskajā tīklā un nosaka brīvā kalcija daudzumu tajā, kā arī piesaistoties rianodīnam (junktīnu un triadīnu), nosaka kalcija transportu caur to. Mutāciju rezultātā vienā no molekulām izmainās funkcija (-as), kas nosaka pastiprinātu kalcijas atbrīvošanu no sarkplazmatiskā tīkla. Kateholamīnu ietekmē ar proteīnkināzes A, kalmodulīna kināzes starpniecību notiek kalcijas atbrīvošanu nosakošo molekulu funkcijas pastiprināšanās, kāpēc kalcija koncentrācija ir daudz augstāka nekā nepieciešams. Pieaugot potenciālam citoplazmā 2 kalcija joni tiek apmainīti ar 3 nātrija, kāpēc pieaug potenciāls un depolarizējas priekšlaicīgi kardiomiocīts. Beigu rezultātā attīstās - delayed afterdepolarization (DAD), kas izraisa trigera aktivitāti un attīstās ventrikulāra tahikardija.

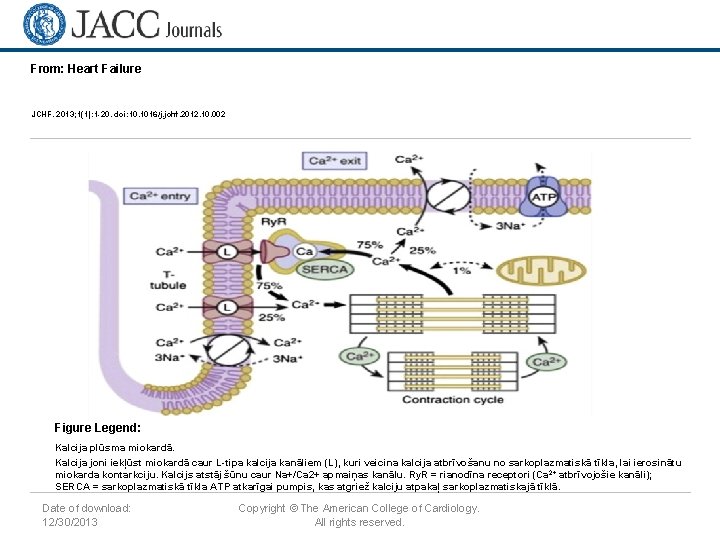
From: Heart Failure JCHF. 2013; 1(1): 1 -20. doi: 10. 1016/j. jchf. 2012. 10. 002 Figure Legend: Kalcija plūsma miokardā. Kalcija joni iekļūst miokardā caur L-tipa kalcija kanāliem (L), kuri veicina kalcija atbrīvošanu no sarkoplazmatiskā tīkla, lai ierosinātu miokarda kontarkciju. Kalcijs atstāj šūnu caur Na+/Ca 2+ apmaiņas kanālu. Ry. R = rianodīna receptori (Ca 2+ atbrīvojošie kanāli); SERCA = sarkoplazmatiskā tīkla ATP atkarīgai pumpis, kas atgriež kalciju atpakaļ sarkoplazmatiskajā tīklā. Date of download: 12/30/2013 Copyright © The American College of Cardiology. All rights reserved.

Agrīna pēcdepolarizācija.

• Klīniskā aina: • Prevelence 1: 10 000. • Vidējais simptomu attīstības vecums ir 12 gadi. • Sinkope, pēkšņa kardiāla nāve. • Simptomu attīstība ir saistīta ar fizisku aktivitāti, un līdzīgi aprakstīti nāves gadījumi peldēšanas laikā neskaidru apstākļu rezultātā kā pie LQT 1. • Simptomātiski līdz 75 – 80% slimnieku līdz 40 gadu vecumam. • Diagnostika: • Elektrokardiogramma miera stāvoklī ir normāla, taču slodzes testu laikā vai pēc kateholamīnu infūzijas attīstās aritmija vidēji pie 90 – 110 reizēm/minūtē kā nepastāvīga VT vai ekstrasistolija, turpinot attiecīgo testu progresē VT, kuras rezultātā var parādīties raksturīgā divvirzienu (bidirectional) kambaru tahikardija.

Ārstēšana. • Beta blokatori (nadolols, propranolols, metoprolols? ) – kontrolējot devas efektu, t. i. , jāsasniedz tāda deva, lai būtu pēc iespējas mazāk aritmisku notikumu, kāpēc regulāri jāveic holtera monitorēšana, slodzes testi terapijas laikā. Lietojami arī akūtu notikumu gadījumā. • Iespējams flekainīds, propafenons, verapamils, amiodorons. • Kreisā sirds puses simpātiska denervācija; • Kardioverteris – defibrilators (rekomendēts arī pie labas medikamentozas terapijas). • Ierobežota fiziskā aktivitāte. • Akūti – jāizvairās no kateholamīniem, indicēti beta blokatori.

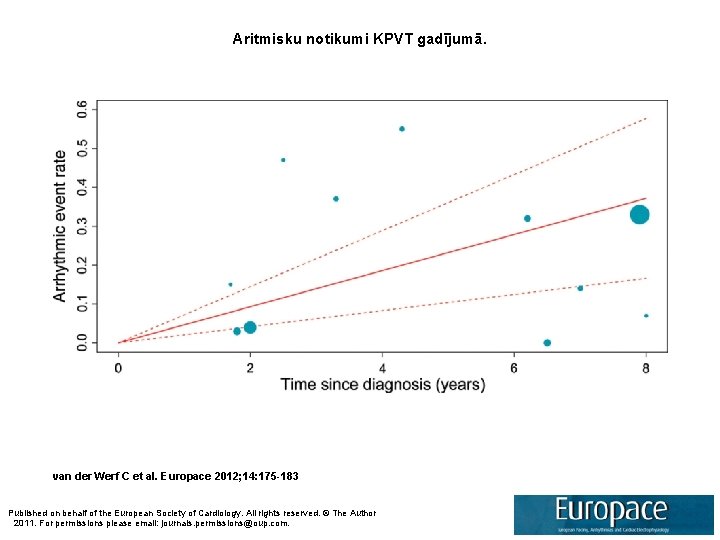
Aritmisku notikumi KPVT gadījumā. van der Werf C et al. Europace 2012; 14: 175 -183 Published on behalf of the European Society of Cardiology. All rights reserved. © The Author 2011. For permissions please email: journals. permissions@oup. com.

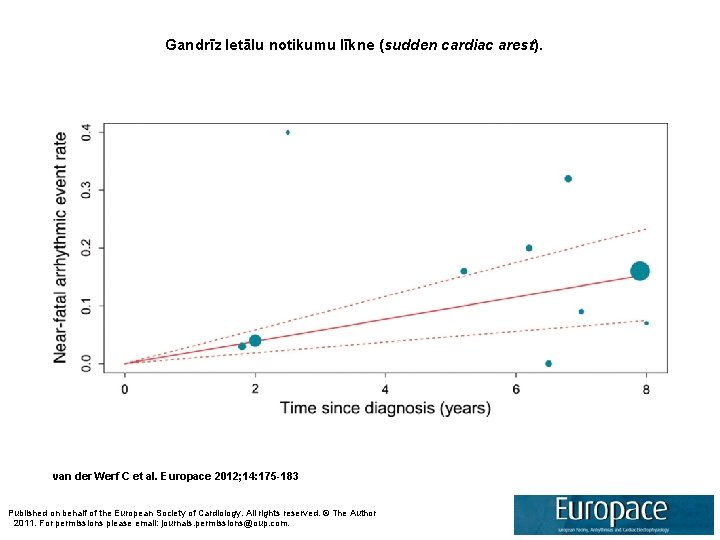
Gandrīz letālu notikumu līkne (sudden cardiac arest). van der Werf C et al. Europace 2012; 14: 175 -183 Published on behalf of the European Society of Cardiology. All rights reserved. © The Author 2011. For permissions please email: journals. permissions@oup. com.

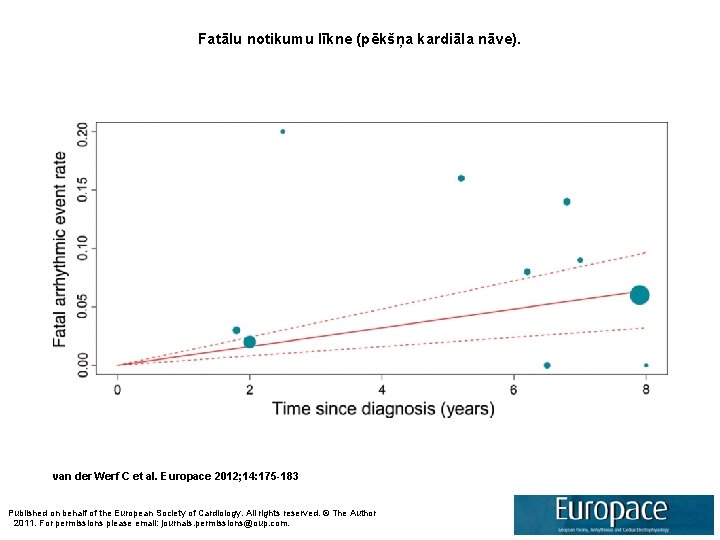
Fatālu notikumu līkne (pēkšņa kardiāla nāve). van der Werf C et al. Europace 2012; 14: 175 -183 Published on behalf of the European Society of Cardiology. All rights reserved. © The Author 2011. For permissions please email: journals. permissions@oup. com.


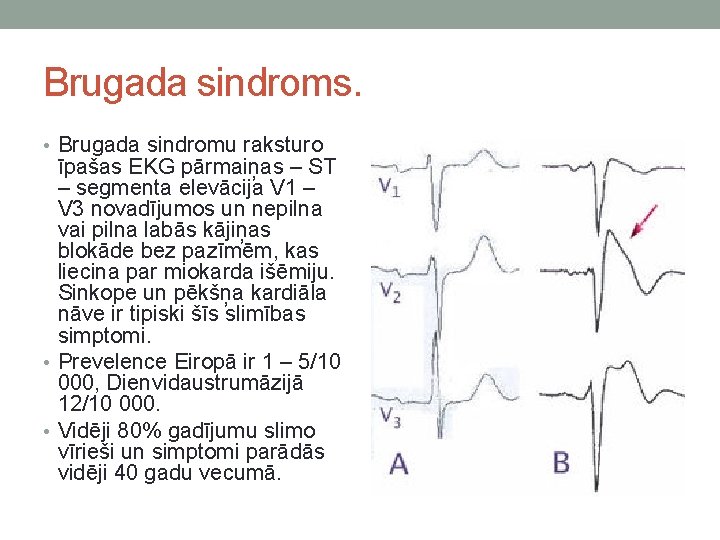
Brugada sindroms. • Brugada sindromu raksturo īpašas EKG pārmaiņas – ST – segmenta elevācija V 1 – V 3 novadījumos un nepilna vai pilna labās kājiņas blokāde bez pazīmēm, kas liecina par miokarda išēmiju. Sinkope un pēkšņa kardiāla nāve ir tipiski šīs slimības simptomi. • Prevelence Eiropā ir 1 – 5/10 000, Dienvidaustrumāzijā 12/10 000. • Vidēji 80% gadījumu slimo vīrieši un simptomi parādās vidēji 40 gadu vecumā.

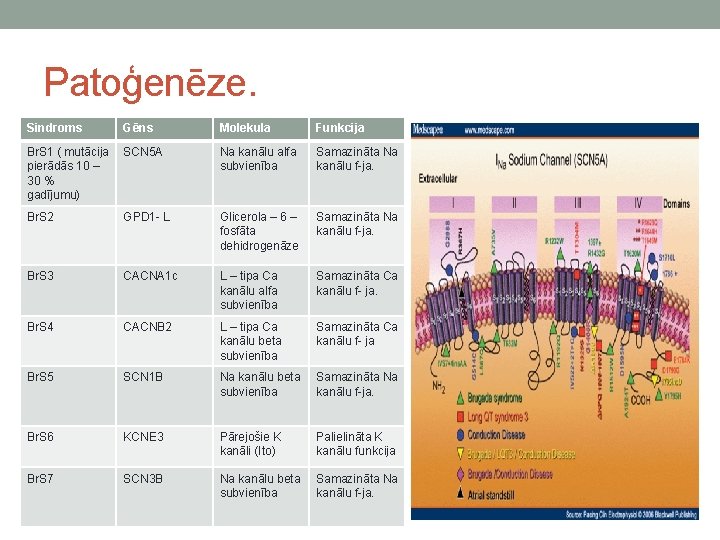
Patoģenēze. Sindroms Gēns Molekula Funkcija Br. S 1 ( mutācija SCN 5 A pierādās 10 – 30 % gadījumu) Na kanālu alfa subvienība Samazināta Na kanālu f-ja. Br. S 2 GPD 1 - L Glicerola – 6 – fosfāta dehidrogenāze Samazināta Na kanālu f-ja. Br. S 3 CACNA 1 c L – tipa Ca kanālu alfa subvienība Samazināta Ca kanālu f- ja. Br. S 4 CACNB 2 L – tipa Ca kanālu beta subvienība Samazināta Ca kanālu f- ja Br. S 5 SCN 1 B Na kanālu beta subvienība Samazināta Na kanālu f-ja. Br. S 6 KCNE 3 Pārejošie K kanāli (Ito) Palielināta K kanālu funkcija Br. S 7 SCN 3 B Na kanālu beta subvienība Samazināta Na kanālu f-ja.

• Na kanālu funkcijas traucējumi samazina tā plūsmu 0 un 1 DP fāzē, un šīs pārmaiņas dažādi skar labā kambara endokardu un epikardu. • Iemesls varētu būt, ka pārejošie kālija kanāli vairāk izvietoti epikardā nekā endokardā, kāpēc Na kanālu funkcijas traucējumu dēļ ir izteiktāks transmurālais gradients, ko var novērot EKG. • EKG pārmaiņas ir atkarīgas no depolarizācijas izmaiņām, kas nosaka to, vai būs normāls T vilnis vai negatīvs attiecīgajos novadījumos, izmainot arī ST segmentu. • Tas nosaka 3 veidu EKG iespējamās pārmaiņas Brugada sindroma gadījumā. • Transmurālā gradienta dēļ var rasties 2. fāzes reentry mehānisma tahikardija, kas ir pametu VT attīstībai.

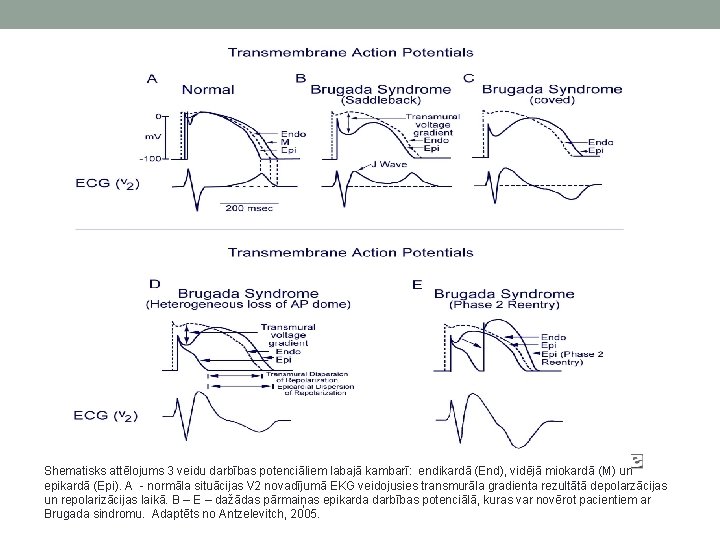
Shematisks attēlojums 3 veidu darbības potenciāliem labajā kambarī: endikardā (End), vidējā miokardā (M) un epikardā (Epi). A - normāla situācijas V 2 novadījumā EKG veidojusies transmurāla gradienta rezultātā depolarzācijas un repolarizācijas laikā. B – E – dažādas pārmaiņas epikarda darbības potenciālā, kuras var novērot pacientiem ar Brugada sindromu. Adaptēts no Antzelevitch, 2005.

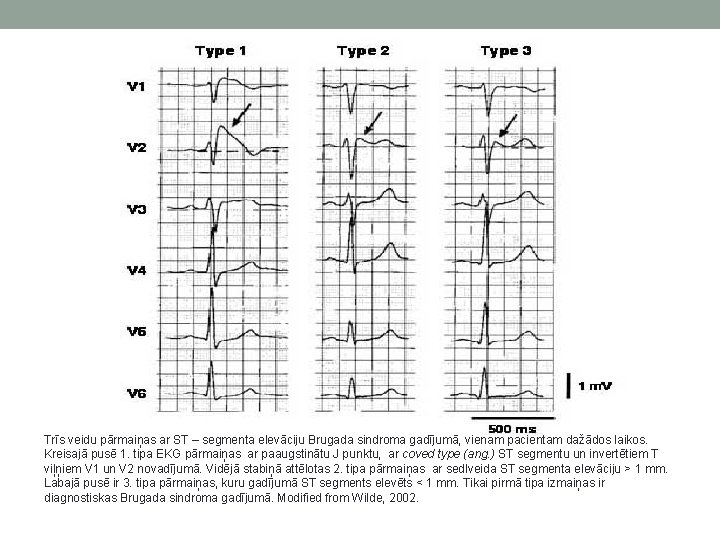
• Klīnika: • Galvenie simptomi ir sinkope un pēkšņa kardiāla nāve. Predisponējošie faktori ir miegs, drudzis un pārmērīga alkohola lietošana, kā arī medikamentu lietošana (lokālais anestētiķis – bupivakaīns, kokaīns, alfa receptoru agonists – metoksamīns, beta blokatori, tricikliskie antidepresanti, opioīdu analgētiķi, propofols). Līdz 60 gadu vecumam simptomi attīstās 20%. • Diagnostika: • EKG 3 iespējamās pārmaiņas: • 1) izteikta, asa ST segmenta elevācija ar J punkta amplitūdu vai ST segmenta elevāciju > 2 mm, sekojot negatīvam T vilnim; • 2) J punkta elevācija > 2 mm, > 1 mm ST segmenta elevācija un sedlveida pārmaiņam, sekojot pozitīvam vai bifāziskam T vilnim; • 3) sedlveida vai asa tipa izmaiņas, bet ar ST segmenta elevāciju < 1 mm. 1. tipa izmaiņas ir vienīgās diagnostiskās, bet 2. un 3. tipa pārmaiņu gadījumā diagnoze ir tikai apsverama.

Trīs veidu pārmaiņas ar ST – segmenta elevāciju Brugada sindroma gadījumā, vienam pacientam dažādos laikos. Kreisajā pusē 1. tipa EKG pārmaiņas ar paaugstinātu J punktu, ar coved type (ang. ) ST segmentu un invertētiem T viļņiem V 1 un V 2 novadījumā. Vidējā stabiņā attēlotas 2. tipa pārmaiņas ar sedlveida ST segmenta elevāciju > 1 mm. Labajā pusē ir 3. tipa pārmaiņas, kuru gadījumā ST segments elevēts < 1 mm. Tikai pirmā tipa izmaiņas ir diagnostiskas Brugada sindroma gadījumā. Modified from Wilde, 2002.

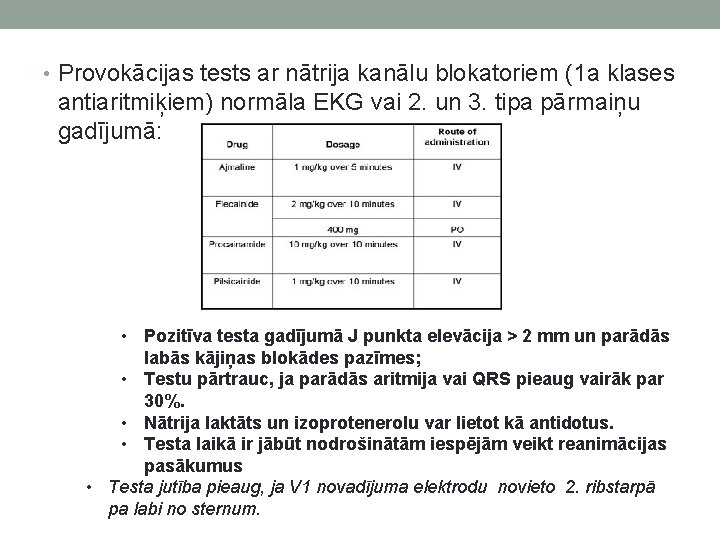
• Provokācijas tests ar nātrija kanālu blokatoriem (1 a klases antiaritmiķiem) normāla EKG vai 2. un 3. tipa pārmaiņu gadījumā: • Pozitīva testa gadījumā J punkta elevācija > 2 mm un parādās labās kājiņas blokādes pazīmes; • Testu pārtrauc, ja parādās aritmija vai QRS pieaug vairāk par 30%. • Nātrija laktāts un izoprotenerolu var lietot kā antidotus. • Testa laikā ir jābūt nodrošinātām iespējām veikt reanimācijas pasākumus • Testa jutība pieaug, ja V 1 novadījuma elektrodu novieto 2. ribstarpā pa labi no sternum.

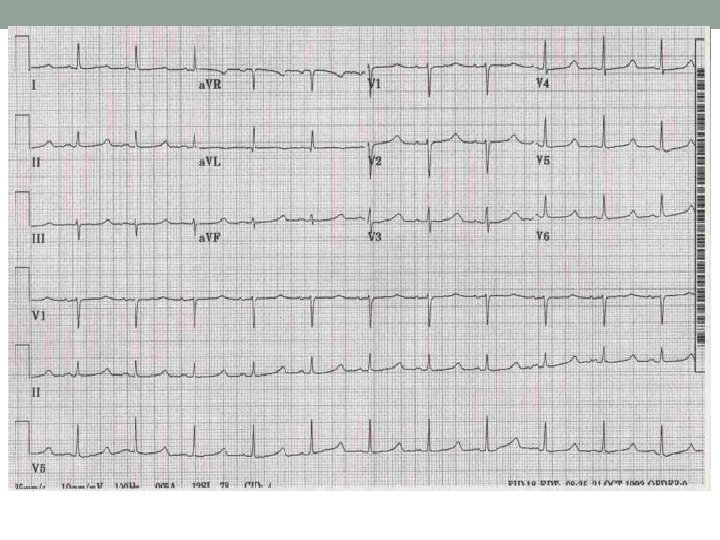
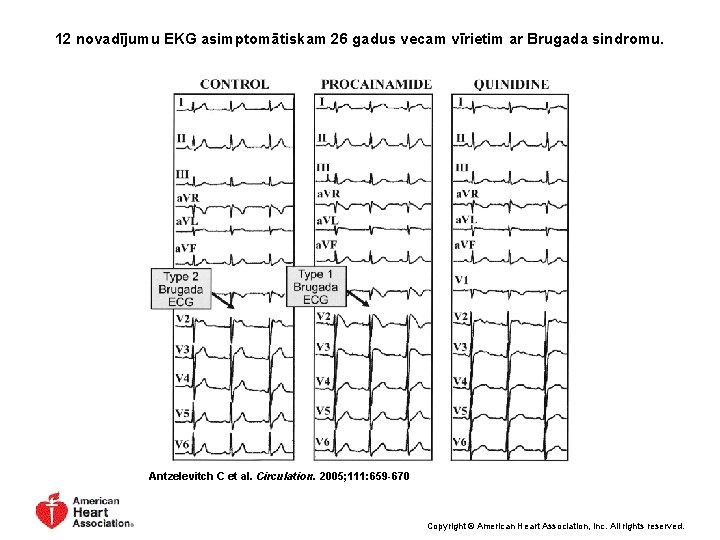
12 novadījumu EKG asimptomātiskam 26 gadus vecam vīrietim ar Brugada sindromu. Antzelevitch C et al. Circulation. 2005; 111: 659 -670 Copyright © American Heart Association, Inc. All rights reserved.

• Jāizslēdz citi iemesli līdzīgām pārmaiņām: • Akūts miokardīts, perikardīts, hemoperikards, labā kambara infarkts, aortas disekcija, PATE, Dišēna muskuļu distrofija, hiperkalciēmija, hiperkaliēmija, mediastīna tumors, pagarināta QT sindroma 3 tips, agrīna repolarizācija, hipotermija, kreisā kambra hipertrofija, kreisās kājiņas blokāde, aritmogēna labā kambara kardiomiopātija. • Elektrofizioloģiska izmeklēšana riska noteikšanai nav izrādījusies lietderīga. • Diagnoze ir droša, ja ir 1. tipa izmaiņas EKG un pozitīva ģimenes anamnēze un/vai aritmijas simptomi un/vai dokumentēta VF vai VT. Ja ir 1. tipa izmaiņas EKG tad ir tikai idiopātiskas Brugada sindromam līdzīgas EKG pārmaiņas.

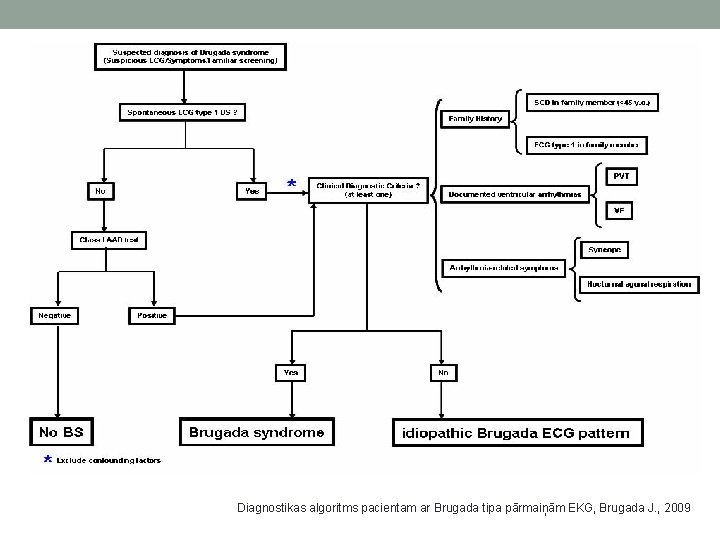
Diagnostikas algoritms pacientam ar Brugada tipa pārmaiņām EKG, Brugada J. , 2009

Ārstēšana. • Kardioverteris defibrilators. • Rekomendēts visiem, kam spontānas 1. tipa izmaiņas EKG vai tiem, kuriem ir bijusi sinkope. • Medikamentoza terapija: • Ito kanālu selektīvs blokators (nav tāda); • Kvinidīns, izoprotenerols, cilostazols, tedisamils (? ); • Predisponējošo faktoru novēršana (miegs, drudzis, alkohols).

Izmantotā literatūra. Literatūra: • Robert O. Bonow et al. , Braunwald’s Heart Diseases, Ninth edition Volume 1, 2012; • Valentin Fuster et al. , Hurst’s The Heart, 13 th edition Volume 1, 2011. Publikācijas interneta resursos: • Antzlevitch et al. Brugada syndrome: report of the second consensus conference: endorsed by the Heart Rhythm Society and the European Heart Rhythm Association. Circulation, 2005, http: //circ. ahajournals. org/content/111/5/659. full. pdf+html • Augustus O. Grant. Cardiac Ion Channels. Circulation: Arrhythmia and Electrophysiolog, 2009, http: //circep. ahajournals. org/content/2/2/185. extract. • Brugada J. Management of patients with a Brugada ECG pattern. 2009, http: //www. escardio. org/communities/councils/ccp/e-journal/volume 7/Pages/management-brugada-ECGpattern. aspx#. Us. Q 9 u. NIW 3 UI. • Christian van der Werf et al. Therapeutic approach for patients with catecholaminergic polymorphic ventricular tachycardia: state of the art and future developments. Europace, 2012, http: //europace. oxfordjournals. org/cgi/pmidlookup? view=long&pmid=21893508 • Delisle Brian P. , Anson Blake D. , Sridharan Rajamani, Craig T. Biology of Cardiac Arrhythmias Ion Channel Protein Trafficking, Circulation Research, 2004, http: //circres. ahajournals. org/content/94/11/1418. figuresonly.

• Dizon Jose M, Brugada Syndrome Treatment & Management. 201 3, http: //emedicine. medscape. com/article/163751 -treatment. • Jeanne M. Nerbonne and Robert S. Kass. Molecular Physiology of Cardiac Repolarization, Physiology reviews, 2005. http: //physrev. physiology. org/content/85/4/1205. long. • Michael H. Gollob The Short QT Syndrome Proposed Diagnostic Criteria. J Am Coll Cardiol. 2011, http: //content. onlinejacc. org/article. aspx? articleid=1144151. • Moreno-Reviriego Merino J. L. Short QT Syndrome. E-Journal of the ESC Council for Cardiology Practice , 2010, http: //www. escardio. org/communities/councils/ccp/ejournal/volume 9/Pages/Short_Qt_Syndrome_Reviriego. aspx#. Us. G 82 t. IW 3 UI • Napolitano Carlo, Priori Silvia G. Diagnosis and treatment of catecholaminergic polymorphic ventricular tachycardia. , Heart Rhythm, 2007. http: //www. ncbi. nlm. nih. gov/books/NBK 1289/. • Shephard Rhian, Semsarian Christopher. Advances in the Prevention of Sudden Cardiac Death in the Young. Ther Adv Cardiovasc Dis, 2009, http: //www. medscape. com/viewarticle/589999_2. • Sovari Ali A. et al. Long QT Syndrome. 2013, http: //emedicine. medscape. com/article/157826 -overview.