POTENSIOMETRI Edi Nasra S Si M Si SEL















![Selektifitas Membran [A]E dan [I]E adalah konsentrasi analit dan pengganggu yang memberikan nilai potensial Selektifitas Membran [A]E dan [I]E adalah konsentrasi analit dan pengganggu yang memberikan nilai potensial](https://slidetodoc.com/presentation_image_h/32efa54eafd0b6a56c9fd8a633301c7b/image-21.jpg)





- Slides: 33

POTENSIOMETRI Edi Nasra, S. Si. , M. Si

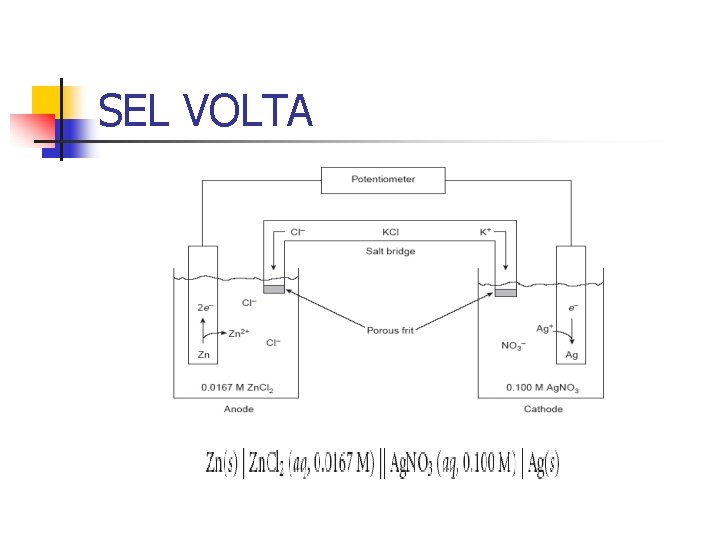
SEL VOLTA

Potensial Sel

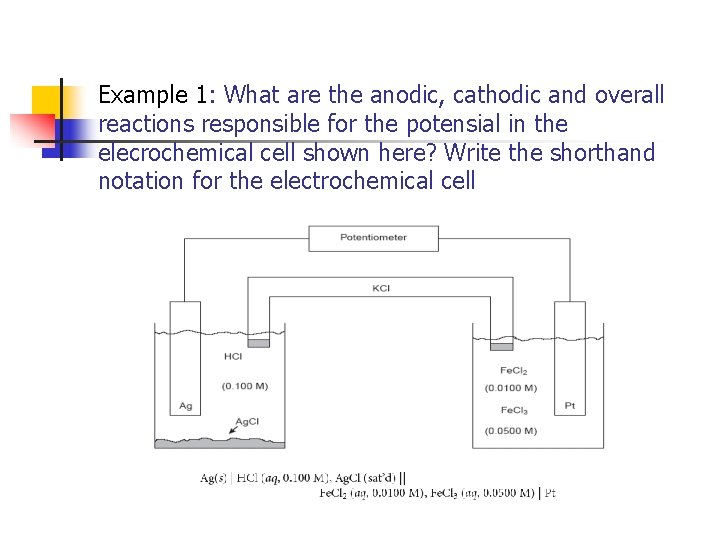
Example 1: What are the anodic, cathodic and overall reactions responsible for the potensial in the elecrochemical cell shown here? Write the shorthand notation for the electrochemical cell

Example 2: what is the potential of the electrochemical cell shown in example 1 (Eo Fe 3+/Fe 2+ = +0. 771 V ; Eo Ag. Cl/Ag = +0. 2223 V

Example 3: what is the concentration of Fe 3+ in an electrochemical cell similar to that shown in example 1 if concentration of HCl in the left-hand cell is 1. 0 M, the concentration of Fe. Cl 2 in the right-hand cell is 0. 0151 M and the measured potential is +0. 546 V

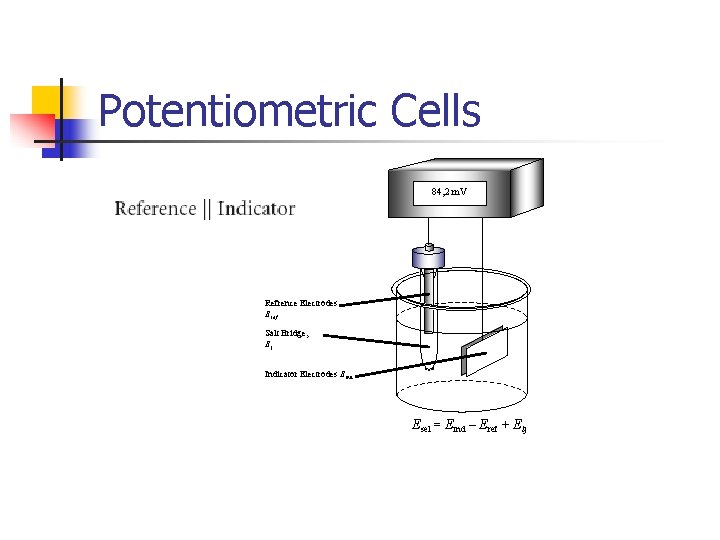
Potentiometric Cells 84, 2 m. V Refrence Electrodes Eref Salt Bridge, Ej Indicator Electrodes Eind Esel = Eind – Eref + Elj

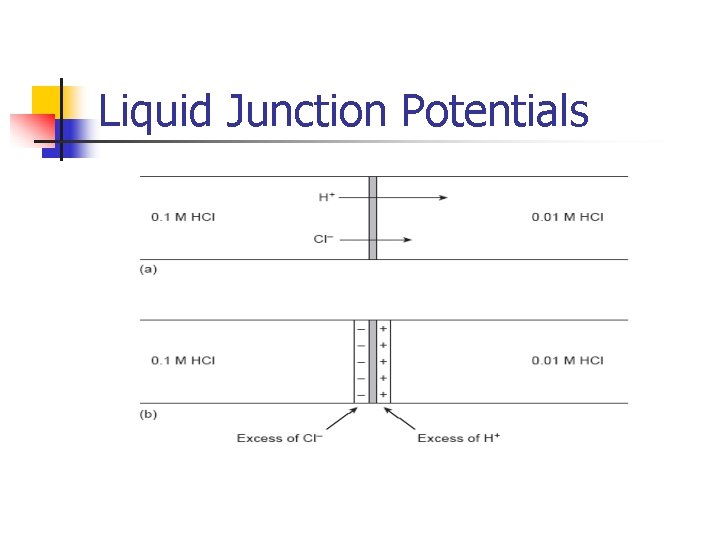
Liquid Junction Potentials

Elektroda Pembanding Elektroda yang mempunyai harga potensial tetap dan konstan dan tidak dipengaruhi konsentrasi analit dalam larutan

Elektroda Hidrogen Standar

Elektroda Kalomel Besarnya potensial sel: • jika digunakan KCl jenuh + 0. 2440 V • jika [KCl] 3. 5 M maka E = +0. 2500 V • jika [KCl] 0. 1 M maka E = +0. 3356 V

Elektroda Ag/Ag. Cl Besarnya potensial: • jika digunakan KCl jenuh E = 0. 199 V • jika digunakan KCl 3. 5 M maka E = 0. 205 V

Elektroda Indikator Elektroda yang potensialnya bergantung pada konsentrasi zat yang sedang diselidiki

Elektroda Kerja Logam n Elektroda Jenis Pertama Logam yang dicelupkan kedalam larutan ionnya Contoh: logam tembaga yang dicelupkan ke dalam larutan ion Cu 2+

Elektroda Jenis Pertama

Elektroda Jenis Kedua Elektroda logam yang dicelupkan ke dalam larutan yang dijenuhkan dengan garam sukar larut dari ion logam tersebut.

Elektroda Jenis Kedua

Example 4: Calculate the formation constant Kf for Ag(CN)2 - if the cell: SCE || Ag(CN)2 - (7. 50 x 10 -3 M, CN- (0. 0250 M)| Ag develops a potential of -0, 625 V

Elektroda Redoks Elektroda logam inert dicelupkan ke dalam larutan yang mengandung ion yang dapat mengalami reaksi reduksi/oksidasi di permukaan elektroda tersebut. Elektroda ini tidak terlibat dalam reaksi tersebut. Contoh: Fe 3+, Fe 2+ Pt

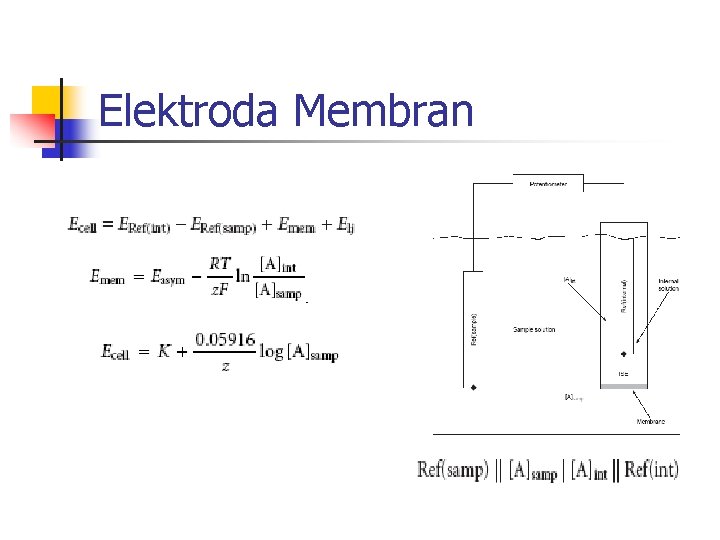
Elektroda Membran
![Selektifitas Membran AE dan IE adalah konsentrasi analit dan pengganggu yang memberikan nilai potensial Selektifitas Membran [A]E dan [I]E adalah konsentrasi analit dan pengganggu yang memberikan nilai potensial](https://slidetodoc.com/presentation_image_h/32efa54eafd0b6a56c9fd8a633301c7b/image-21.jpg)
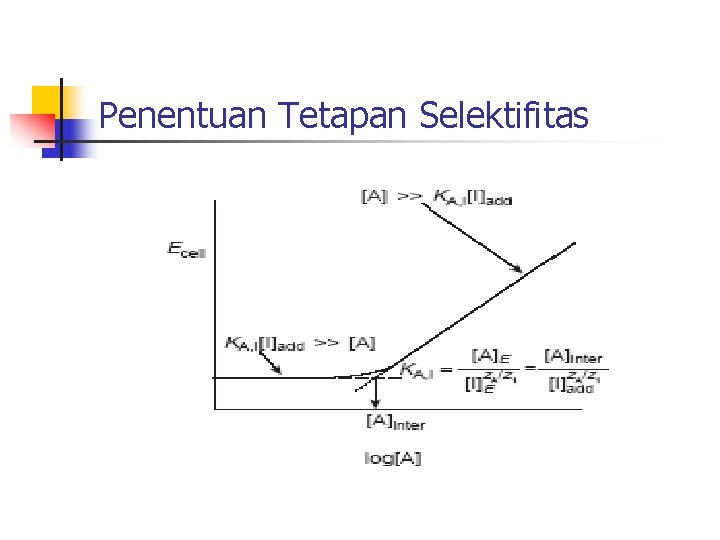
Selektifitas Membran [A]E dan [I]E adalah konsentrasi analit dan pengganggu yang memberikan nilai potensial sel yang sama

Penentuan Tetapan Selektifitas

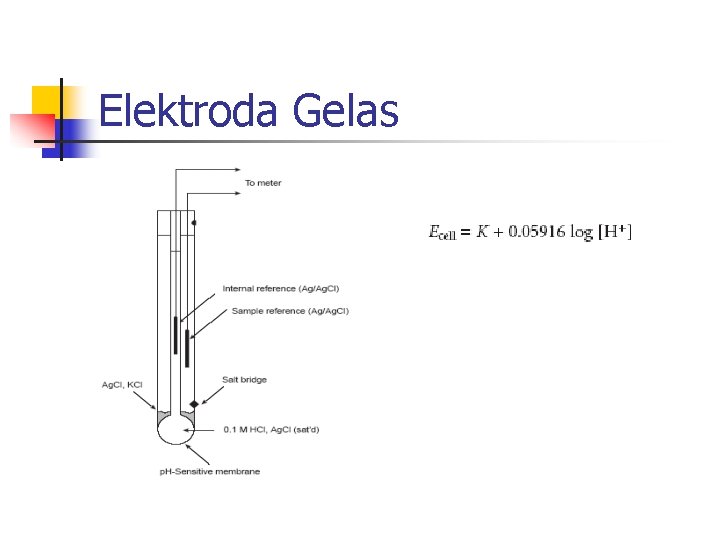
Elektroda Gelas

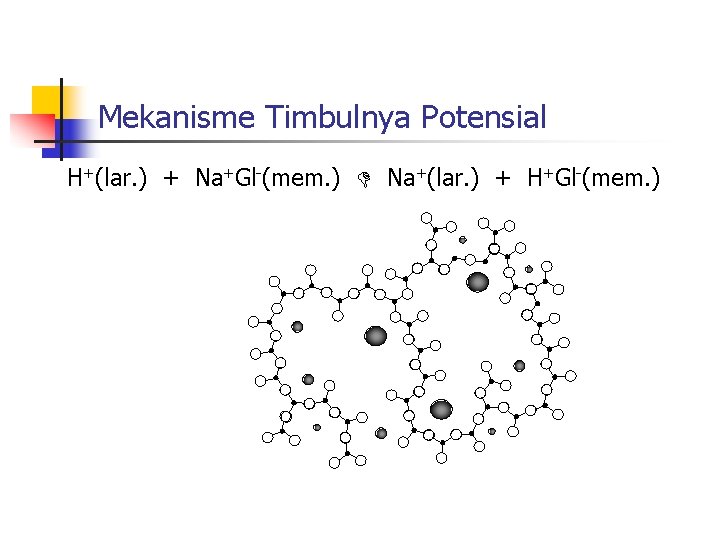
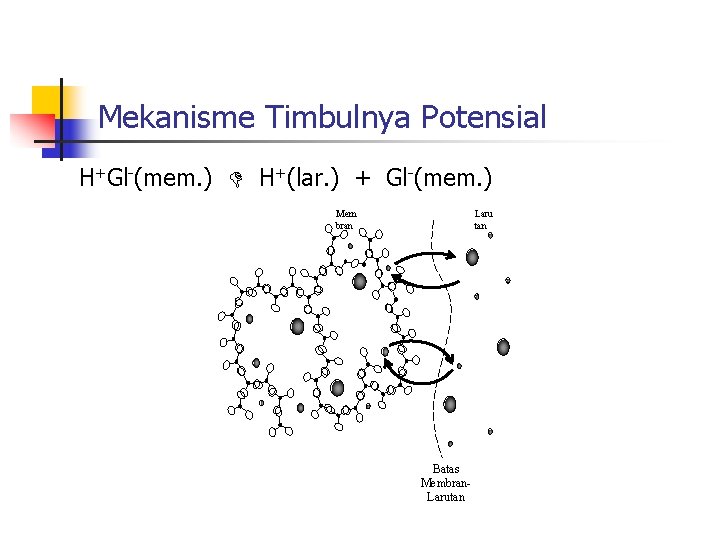
Mekanisme Timbulnya Potensial H+(lar. ) + Na+Gl-(mem. ) Na+(lar. ) + H+Gl-(mem. )

Mekanisme Timbulnya Potensial H+Gl-(mem. ) H+(lar. ) + Gl-(mem. ) Mem bran Laru tan Batas Membran. Larutan

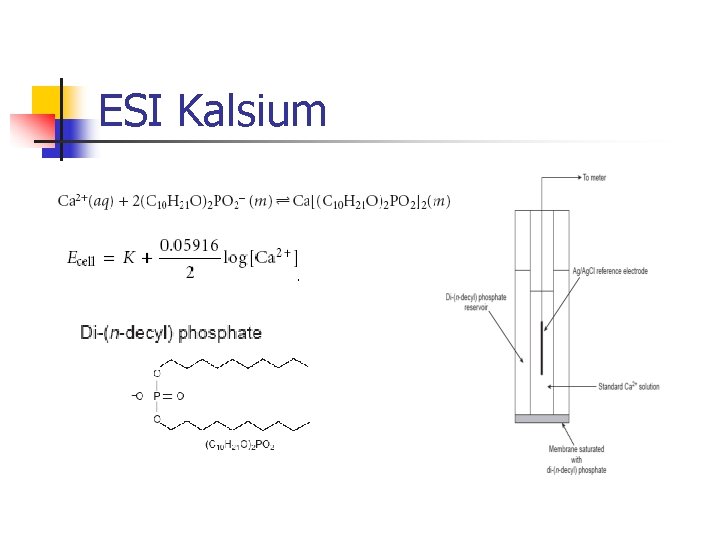
ESI Kalsium

Aktivitas vs Konsentrasi Jika tetap

Ionic Strength Adjuster Kekuatan Ion ( ) Debeye-Huckel =diameter efektif ion

Analisis Kuantitatif n Method of external standards What is the concentration of Ca 2+ in the water sample if its cell potential is found to be -0. 084 V?

Quantitative Analysis n Method of Standard Additions Contoh: The concentration of Ca 2+ in a sample of sea water is determinedusing a Ca ion selective and a one point standard addition. A 10. 00 m. L sample is transferred to a 100 m. L volumetric flask and diluted to volume. A 50. 00 m. L aliquot of sample is placed in a beaker with the Ca ion-selective electrode and a reference electrode, and the potential is measured as -0. 05290 V. A 1. 00 m. L aliquot of a 5. 00 x 10 -2 M standard solution of Ca 2+ is added, and a potential of -0. 04417 V is measured. What is the concentration of Ca in the sample of sea water?

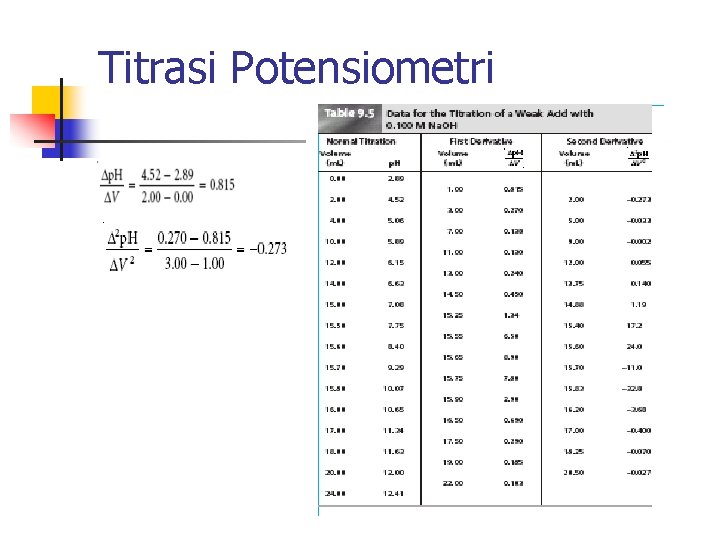
Titrasi Potensiometri n n n Elektroda kerja dan elektroda pembanding dicelupkan ke dalam larutan analit. Potensial sel diamati selama penambahan titran. Titik akhir ditentukan dari kurva titrasi

Titrasi Potensiometri

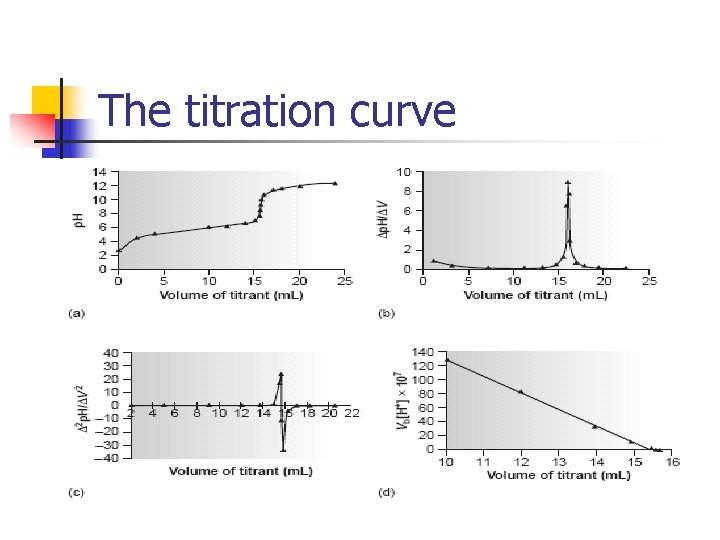
The titration curve