Ostre biaaczki Ostre biaaczki Nowotwory ukadu krwiotwrczego ktrych

Ostre białaczki

Ostre białaczki • Nowotwory układu krwiotwórczego, których istotą jest obecność klonu transformowanych nowotworowo komórek wywodzących się z wczesnych stadiów rozwojowych hematopoezy • Występowanie: 7/100000 populacji • Etiologia: – wirusy – predyspozycja genetyczna – zewnętrzne czynniki środowiskowe „rakotwórcze” • Transformacja nowotworowa – proces wielostopniowy • Podział – Ostre białaczki szpikowe 85 -90% (dorośli) – Ostre białaczki limfoblastyczne 10 -15% (dorośli)

Objawy ostrych białaczek • Laboratoryjne – Anemia – Trombocytopenia – Leukocytoza z blastozą (ale możliwy początek z leukopenią lub prawidłową liczbą leukocytów) • Kliniczne – – – – zakażenia objawy skazy krwotocznej osłabienie bóle kostne powiększenie węzłów chłonnych hepato- i/lub splenomegalia objawy związane z naciekaniem innych narządów i tkanek • OUN, gonady, przewód pokarmowych, skóra
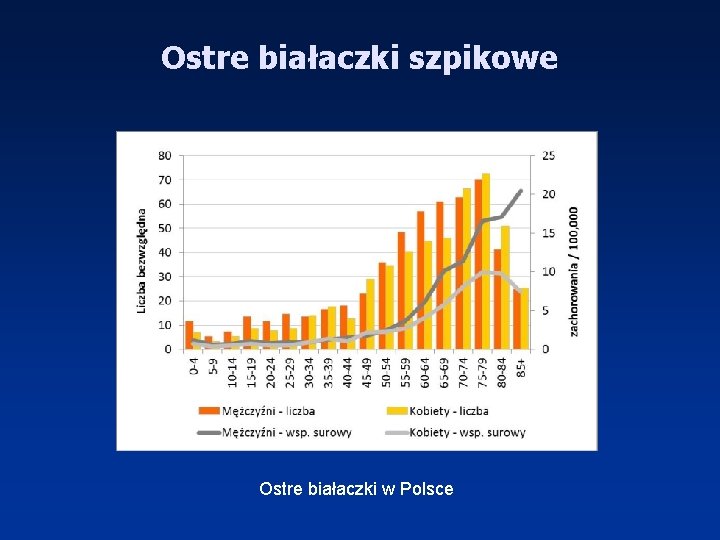
Ostre białaczki szpikowe Ostre białaczki w Polsce

Rozpoznanie i określanie podtypu OBS • Morfologia krwi wraz z rozmazem krwi obwodowej • Ocena morfologiczna szpiku (MGG) – Komórki blastyczne w szpiku ≥ 20% – Zaburzenia genetyczne t(8; 21), inv(16), t(16; 16), t(15; 17) niezależnie od odsetka blastów • Trepanobiopsja • Badania cytochemiczne – aktywność mieloperoksydazy (POX), zawartość glikogenu (PAS), aktywność niespecyficznych esteraz (NE), obecność złogów żelaza • Badanie immunofenotypowe – Markery prekursorowe, , granulocytarne, monocytowe, magakariocytowe, erytroidalne • Badania cytogenetyczne (cytogenetyka klasyczna, FISH) • Badania molekularne
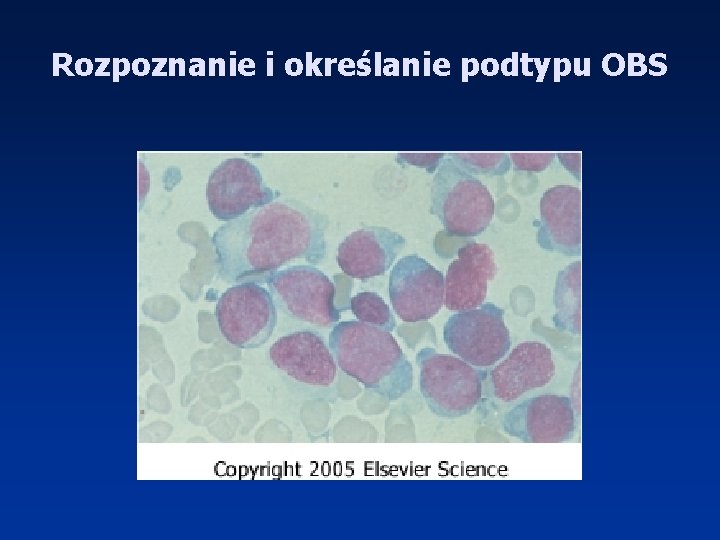
Rozpoznanie i określanie podtypu OBS
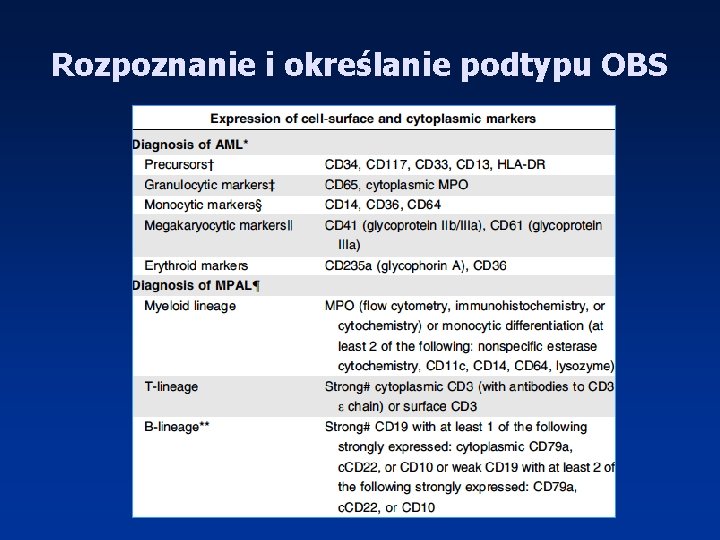
Rozpoznanie i określanie podtypu OBS
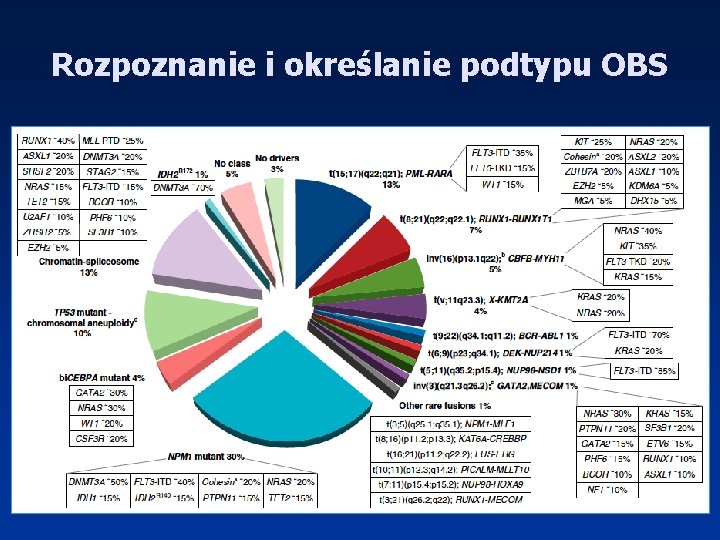
Rozpoznanie i określanie podtypu OBS

Ostre białaczki szpikowe Klasyfikacja WHO

Ostre białaczki szpikowe Klasyfikacja WHO

Ostre białaczki szpikowe • Czynniki prognostyczne – – – Wiek i stan ogólny Schorzenia współistniejące Zaburzenia genetyczne Odpowiedź na leczenie Charakter białaczki • Pierwotne • Wtórne – Poprzedzone chorobą hematologiczną • MDS • NNH • Nowotwory mieloproliferacyjne – Związane z wcześniejszą chemioterapią • Leki alkilujące - delecje długiego ramienia chormosomu 5 lub 7; 35 lat po leczeniu • Inhibitory topoizomerazy II DNA (np. antracykliny) rearanżacja genu MLL w obrębie 11 q 23; 12 -18 miesięcy po leczeniu
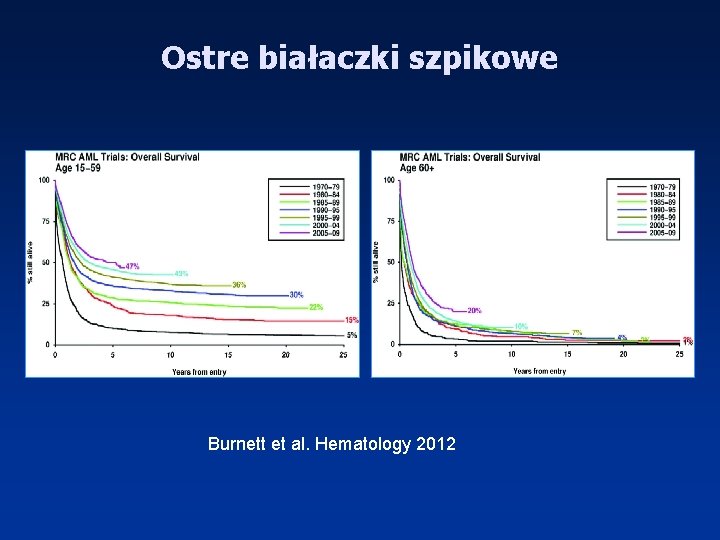
Ostre białaczki szpikowe Burnett et al. Hematology 2012
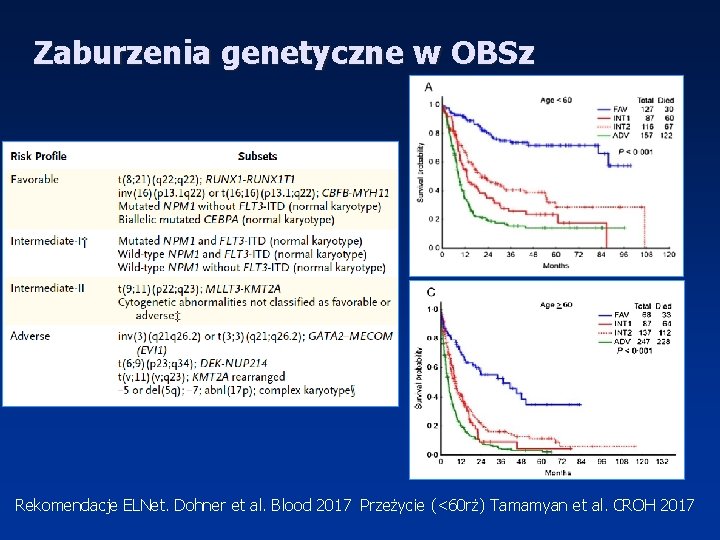
Zaburzenia genetyczne w OBSz Rekomendacje ELNet. Dohner et al. Blood 2017 Przeżycie (<60 rż) Tamamyan et al. CROH 2017

Leczenie ostrych białaczek • Indukcja remisji • Leczenie poremisyjne – Intensyfikacja/konsolidacja – allo. HSCT – auto. HSCT (? ) – Leczenie podtrzymujące: wybrane postacie • Leczenie wznowy i oporności

Pierwotny cel leczenia - remisja całkowita • Odsetek mieloblastów w szpiku < 5%, prawidłowy rozmaz krwi • Liczba płytek >100 G/L • Liczba granulocytów >1 G/L • Choroba resztkowa ujemna

Leczenie ostrych białaczek szpikowych • Chorzy kwalifikujący się do intensywnej chemioterapii: całkowita remisja 75% – Indukcja: daunorubicine + cytarabine (3+7) • warianty – Konsolidacja • Korzsytne rokowanie: 2 -4 cykle HD-Ara. C • Pośrednie ryzyko: HD-Ara. C + allo. SCT (lub 2 -4 cykle HD-Ara. C lub auto. SCT) • Złe rokowanie: HD-Ara. C + allo. SCT • Chorzy nie kwalifikujcy się do intensywnej chemioterapii – – Azacytydyna Decytabina LD-Ara. C Leczenie wspomagające
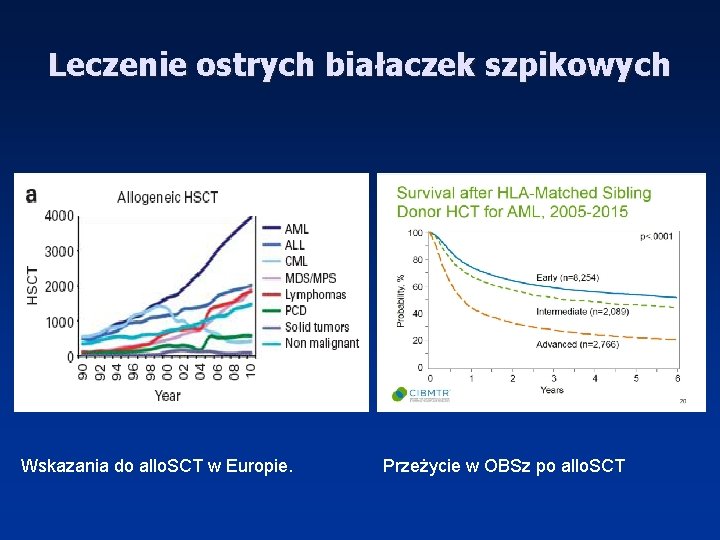
Leczenie ostrych białaczek szpikowych Wskazania do allo. SCT w Europie. Przeżycie w OBSz po allo. SCT

Leczenie ostrej białaczki promielocytowej t(15: 17) gen PML/RAR-alfa • Indukcja remisji, intensyfikacja i leczenie podtrzymujące oparte na kwasie all-trans retynowym (ATRA) podawanym w skojarzeniu • CR >85% • ATRA indukuje dojrzewanie promielocytów, co zapobiega zespołowi wykrzepiania wewnątrznaczyniowego (DIC) • Leczenie nawrotu/oporności: trójtlenek arsenu (Trisenox) • Leczenie za pomocą transplantacji rozważane u chorych z dodatnią chorobą resztkową w badaniu met. FISH lub badaniu molekularnym metodą PCR lub po nawrocie choroby

Leczenie ostrej białaczki promielocytowej t(15: 17) gen PML/RAR-alfa Lo-Cocco et al. NEJM 2013, Abaza et al. Blood 2017

Leczenie ostrych białaczek szpikowych • Nowe leki i metody – Terapia celowana „molekularna” • Inhibitory FLT 3 (midostauryna) • Inhibitory IDH 1/IDH 2 (ensidenib/ivosidenib) • Inhibitory BCL-2 (venetoclax) – Immunoterapia antygenowo-specyficzna • Przeciwciała monoklonalne skoniugowane (gemtuzumab ozogamycin) • Przeciwciała bi-specyficzne • CAR-T (chimeric antigen receptor limfocyte T) – Transplantacja allogenicznych komórek krwiotwórczych • • Kwalifikacja oparta o markery rokownicze (molekularne) Wybór dawcy Kondycjonowanie o zredukowanej toksyczności Leczenie potransplantacyjne - immunoterapia
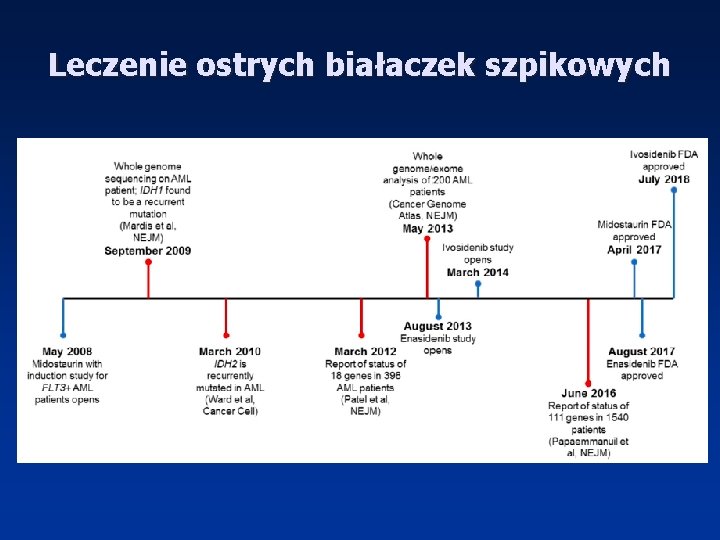
Leczenie ostrych białaczek szpikowych
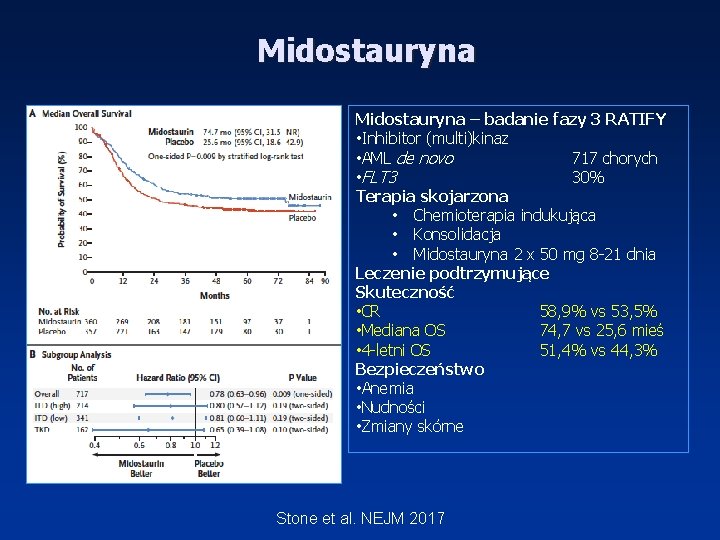
Midostauryna – badanie fazy 3 RATIFY • Inhibitor (multi)kinaz • AML de novo 717 chorych • FLT 3 30% Terapia skojarzona • Chemioterapia indukująca • Konsolidacja • Midostauryna 2 x 50 mg 8 -21 dnia Leczenie podtrzymujące Skuteczność • CR 58, 9% vs 53, 5% • Mediana OS 74, 7 vs 25, 6 mieś • 4 -letni OS 51, 4% vs 44, 3% Bezpieczeństwo • Anemia • Nudności • Zmiany skórne Stone et al. NEJM 2017
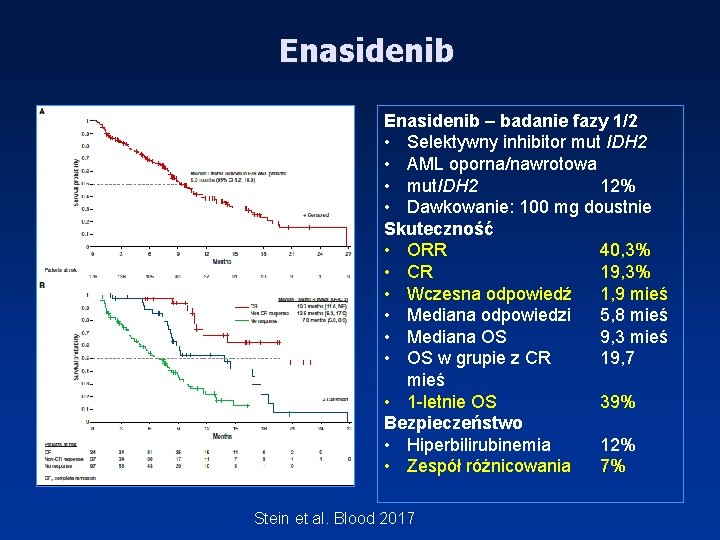
Enasidenib – badanie fazy 1/2 • Selektywny inhibitor mut IDH 2 • AML oporna/nawrotowa • mut. IDH 2 12% • Dawkowanie: 100 mg doustnie Skuteczność • ORR 40, 3% • CR 19, 3% • Wczesna odpowiedź 1, 9 mieś • Mediana odpowiedzi 5, 8 mieś • Mediana OS 9, 3 mieś • OS w grupie z CR 19, 7 mieś • 1 -letnie OS 39% Bezpieczeństwo • Hiperbilirubinemia 12% • Zespół różnicowania 7% Stein et al. Blood 2017
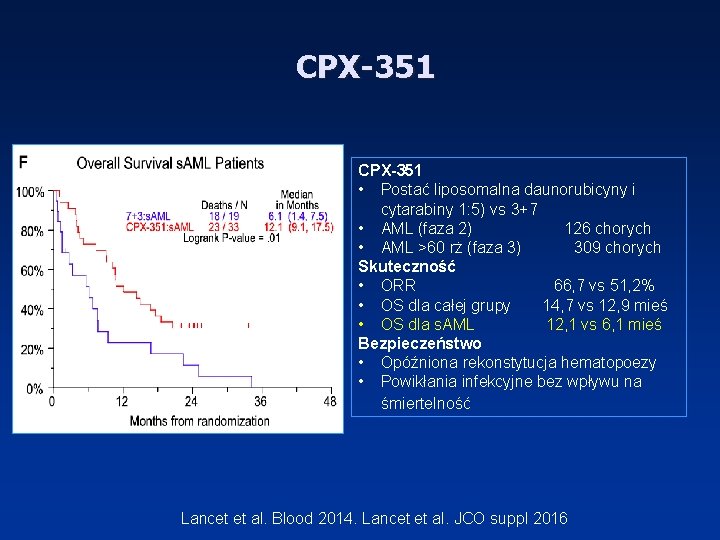
CPX-351 • Postać liposomalna daunorubicyny i cytarabiny 1: 5) vs 3+7 • AML (faza 2) 126 chorych • AML >60 rż (faza 3) 309 chorych Skuteczność • ORR 66, 7 vs 51, 2% • OS dla całej grupy 14, 7 vs 12, 9 mieś • OS dla s. AML 12, 1 vs 6, 1 mieś Bezpieczeństwo • Opóźniona rekonstytucja hematopoezy • Powikłania infekcyjne bez wpływu na śmiertelność Lancet et al. Blood 2014. Lancet et al. JCO suppl 2016
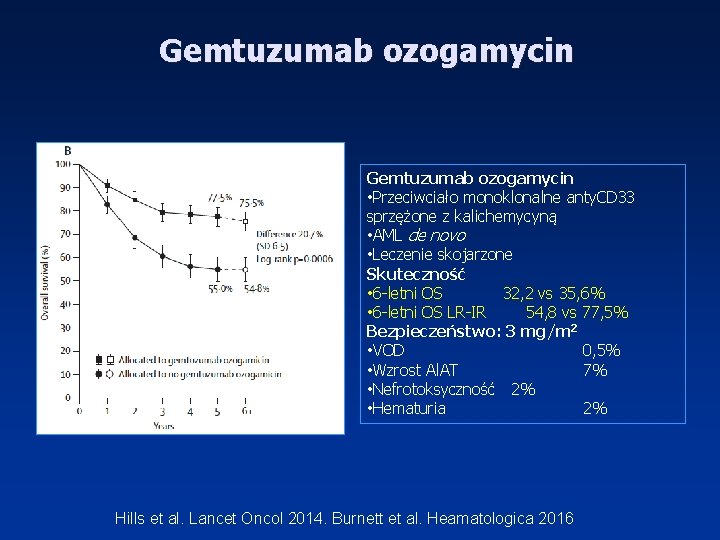
Gemtuzumab ozogamycin • Przeciwciało monoklonalne anty. CD 33 sprzężone z kalichemycyną • AML de novo • Leczenie skojarzone Skuteczność • 6 -letni OS 32, 2 vs 35, 6% • 6 -letni OS LR-IR 54, 8 vs 77, 5% Bezpieczeństwo: 3 mg/m 2 • VOD 0, 5% • Wzrost Al. AT 7% • Nefrotoksyczność 2% • Hematuria 2% Hills et al. Lancet Oncol 2014. Burnett et al. Heamatologica 2016
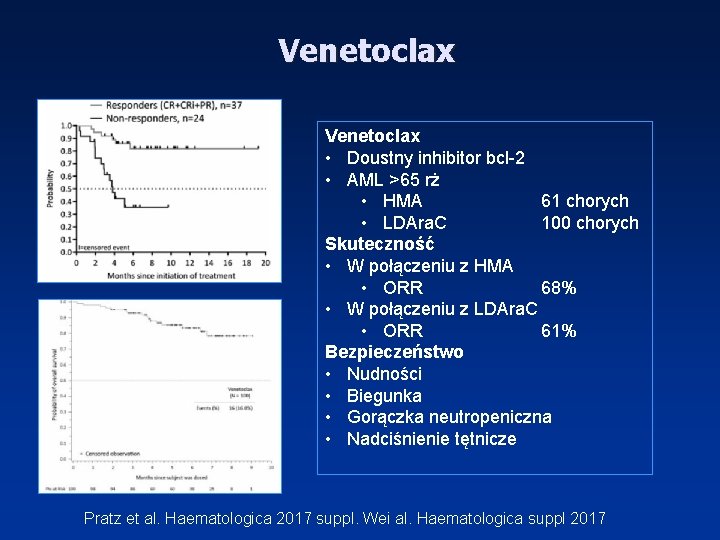
Venetoclax • Doustny inhibitor bcl-2 • AML >65 rż • HMA 61 chorych • LDAra. C 100 chorych Skuteczność • W połączeniu z HMA • ORR 68% • W połączeniu z LDAra. C • ORR 61% Bezpieczeństwo • Nudności • Biegunka • Gorączka neutropeniczna • Nadciśnienie tętnicze Pratz et al. Haematologica 2017 suppl. Wei al. Haematologica suppl 2017

Leczenie ostrych białaczek szpikowych

KLASYFIKACJA OSTRYCH BIAŁACZEK (wg WHO) Ostre białaczki limfoblastyczne (OBL) – OBL i chłoniaki limfoblastyczne z linii B • • OBL pre, pre-B (pro-B) OBL common OBL pre-B OBL B mature – OBL i chłoniaki z prekursorów linii T • • • OBL pre-T (pro-T) OBL pre-T OBL T cortical OBL T mature OBL T /β OBL T /

Klasyfikacja immunologiczna obl B- liniowa (80%) Markery Pro-B Common Pre-B CD 19(+), Tdt(+), CD 10(-), Cy. Ig(-), CD 19(+), Tdt(+), CD 10(+), Cy. Ig(+), Sm. Ig(-) Mature-B CD 19(+), Tdt(+), CD 10(±), Cy. Ig(±), Sm. Ig(+) T-liniowa (20%) Pro-T Pre-T Mature-T cy. CD 3(+), Td. T, CD 7(+), CD 34(+) CD 7(+), CD 2(+), Td. T(+), CD 5(+) CD 7(+), CD 2(+), Tdt(+), CD 4(+) lub CD 8(+)

Podział chorych na grupy ryzyka 1. Grupa ryzyka standardowego 2. Grupa ryzyka wysokiego 3. Grupa ryzyka bardzo wysokiego

Czynniki ryzyka n Czynniki standardowe n n Zmiany cytogenetyczne/molekularne n n Wiek > 35 rż. WBC > 30 G/L w B-ALL; WBC > 100 G/L w T-ALL Podtyp immunologiczny (? ) Chromosom Philadelfia (Ph)/bcr-abl Translokacja (4; 11)/MLL Złożone zmiany cytogenetyczne (≥ 5) Odpowiedź na leczenie n Brak remisji po 4 tygodniach leczenia indukującego n Obecność choroby resztkowej po leczeniu (0, 01% blastów)

Leczenie ostrej białaczki limfoblastycznej • Indukcja remisji • Leczenie poremisyjne – Leczenie konsolidujące – Transplantacja komórek hematopoetycznych – Leczenie podtrzymujące • Profilaktyka / leczenie zmian w OUN • Leczenie wznowy i postaci opornych

Indukcja i intensyfikacja remisji • Schemat podstawowy indukcji (4 -8 tygodni): – prednizon, winkrystyna, antracyklina, L-asparaginaza (postać natywna, postać pegylowana), cyklofosfamid, arabinozyd cytozyny – CR 70 -85% • Intensyfikacja remisji (8 -12 tygodni) – HD Ara-C, Mtx, Cyklofosfamid, L-asparginaza • Modyfikacje – Deksametazon – G-CSF

Leczenie poremisyjne • intensyfikacja / konsolidacja remisji • leczenie podtrzymujące • allo. BMT/PBSCT • auto. BMT/PBSCT ?

Leczenie podtrzymujące • Wskazania – Wszystkie postacie (z wyjątkiem B-ALL) leczone za pomocą Ch. T (lub auto. SCT) • Leki – Metotreksat (1 raz w tygodniu) – 6 -merkaptopuryna – Winkrystyna + prednizon + antracyklina co 6 tygodni

Leczenie ALL bcr/abl+ • Inhibitory kinazy tyrozynowej – imatynib, dazatynib – W okresie indukcji/konsolidacji – W leczeniu podtrzymującym remisję po transplantacji komórek hematopoetycznych CR: 95% Remisje molekularne: 40% - 60% DFS 2 letnie: 50% - 65%

Profilaktyka i leczenie zmian w OUN • Profilaktyka – Metotreksat 12 -15 mg, prednizolon 25 mg, (Ara -C 45 mg) i. t. , łącznie 6 x w okresie indukcji i intensyfikacji – Napromienianie OUN 18 Gy • Leczenie – Metotreksat 15 mg, prednizolon 25 mg, Ara-C 45 mg i. t. , 2 -3 x w tygodniu do ustąpienia zmian, następnie rzadziej – Napromienianie OUN 24 Gy
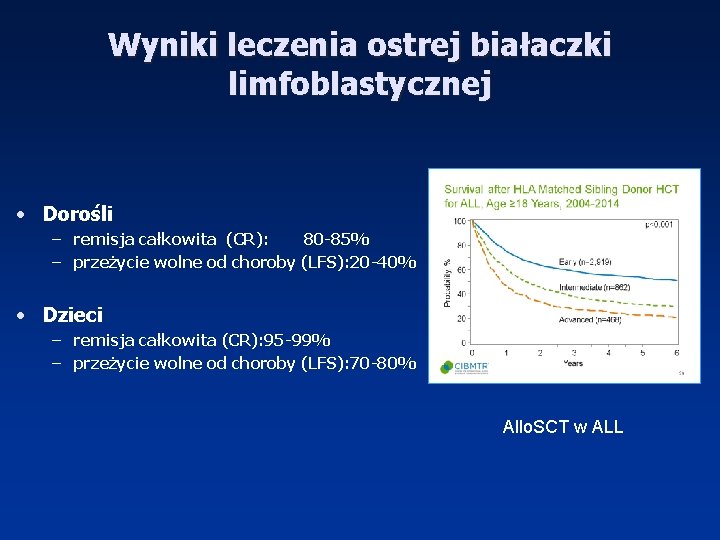
Wyniki leczenia ostrej białaczki limfoblastycznej • Dorośli – remisja całkowita (CR): 80 -85% – przeżycie wolne od choroby (LFS): 20 -40% • Dzieci – remisja całkowita (CR): 95 -99% – przeżycie wolne od choroby (LFS): 70 -80% Allo. SCT w ALL

Nowe leki i metody • Nowe leki – Inhibitor kinazy tyrozynowej (imatinib, dazatynib) – Inhibitor transferazy farnezylowej (FTI) – Przeciwciała monoklonalne (rytuksymab - anty CD 20; inotuzumab – anty. CD 22+kalichemycyna, blinatumomabanty. CD 3/CD 19) – Nowe cytostatyki (nowe analogi puryn-nelarabina, klofarabina) • Nowe metody – Chimeryczne receptory antygenowe (CAR) • Nowe metody w transplantologii – RIC (reduced-intensity conditioning) + allo. SCT – Intensyfikacja Gv. L
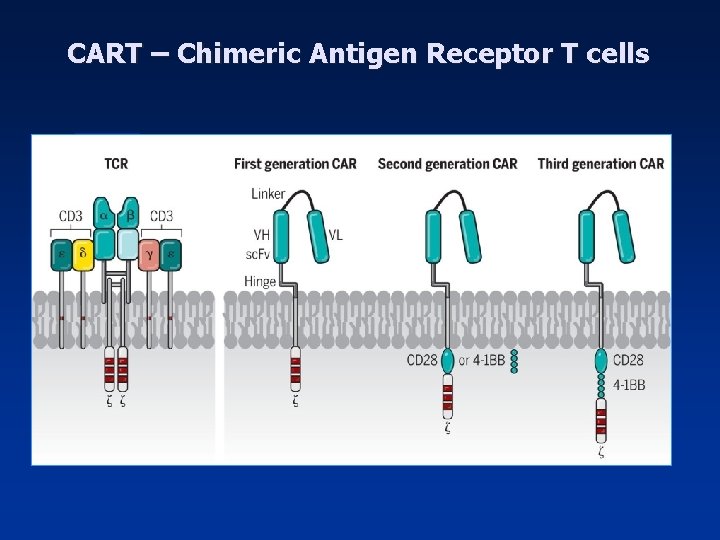
CART – Chimeric Antigen Receptor T cells
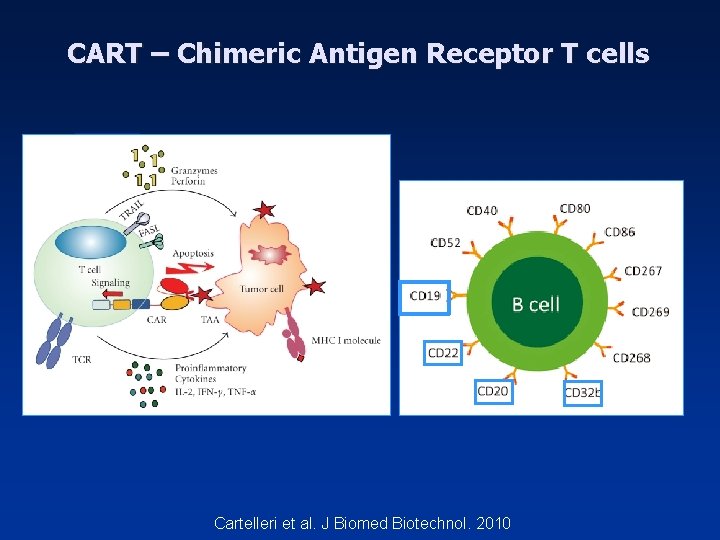
CART – Chimeric Antigen Receptor T cells Cartelleri et al. J Biomed Biotechnol. 2010

CART – Chimeric Antigen Receptor T cells Tisagenlecleucel (Kymriah, Novartis) is approved for use in pediatric and young adult patients (age 3 to 25 years) with B -cell ALL that is refractory or in second or later relapse (August 30, 2017) Axicabtagene ciloleucel (Yescarta, Kite) is approved for use in adult patients with large B-cell lymphoma after at least two other kinds of treatment failed, including DLBCL, primary mediastinal large B-cell lymphoma, high grade Bcell lymphoma and DLBCL arising from follicular lymphoma (October 18, 2017)
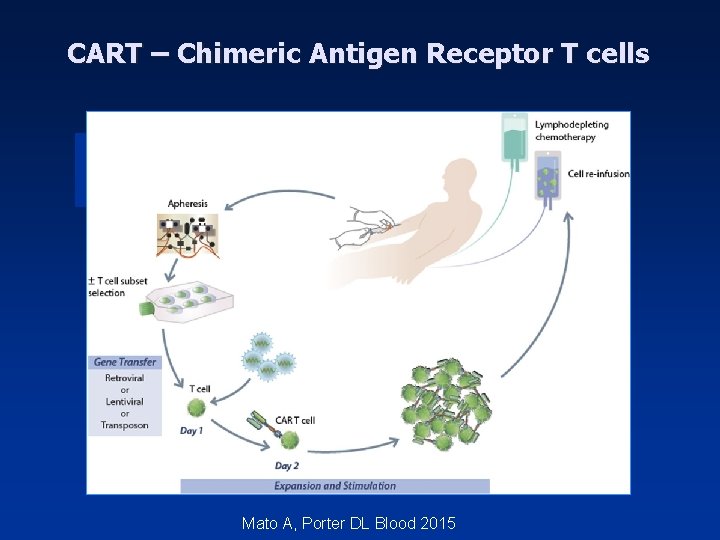
CART – Chimeric Antigen Receptor T cells Mato A, Porter DL Blood 2015
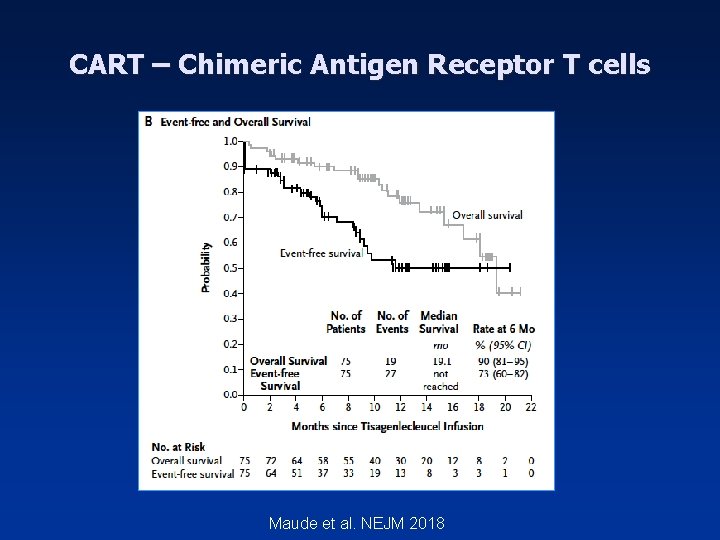
CART – Chimeric Antigen Receptor T cells Maude et al. NEJM 2018

Leczenie ostrych białaczek • • • Profilaktyka infekcji Leczenie zakażeń Preparaty krwiopochodne Żywienie Pomoc psychosocjologiczna

Ostre białaczki
- Slides: 46
























