Organick chemie organick sloueniny vznikaj ivotn innost rostlin





- Slides: 11

Organická chemie – – organické sloučeniny vznikají životní činností rostlin a živočichů – při látkových přeměnách v organismech jsou základní stavební složkou jejich těl (tzv. ústrojné látky) některé z nich se však v přírodě nevyskytují – byly vytvořeny uměle (plasty, syntetická vlákna, …) organické sloučeniny obsahují – C, H, O, N, S, P, halogeny

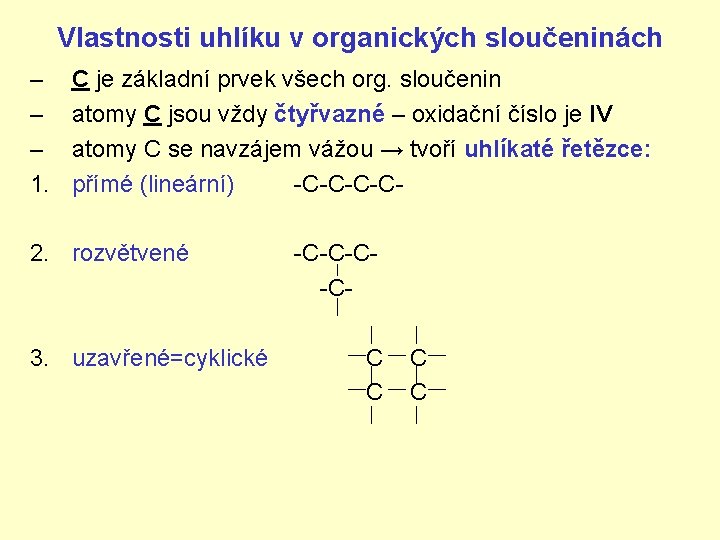
Vlastnosti uhlíku v organických sloučeninách – – – 1. C je základní prvek všech org. sloučenin atomy C jsou vždy čtyřvazné – oxidační číslo je IV atomy C se navzájem vážou → tvoří uhlíkaté řetězce: přímé (lineární) -C-C- 2. rozvětvené 3. uzavřené=cyklické -C-CC C

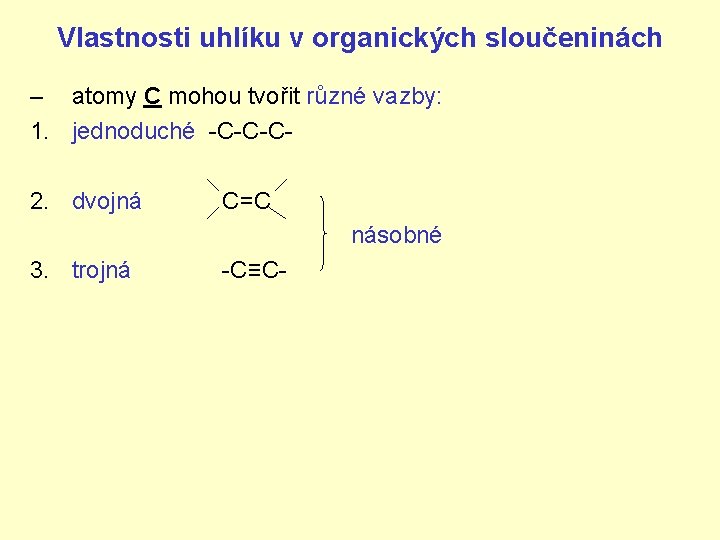
Vlastnosti uhlíku v organických sloučeninách – atomy C mohou tvořit různé vazby: 1. jednoduché -C-C-C 2. dvojná C=C násobné 3. trojná -C≡C-

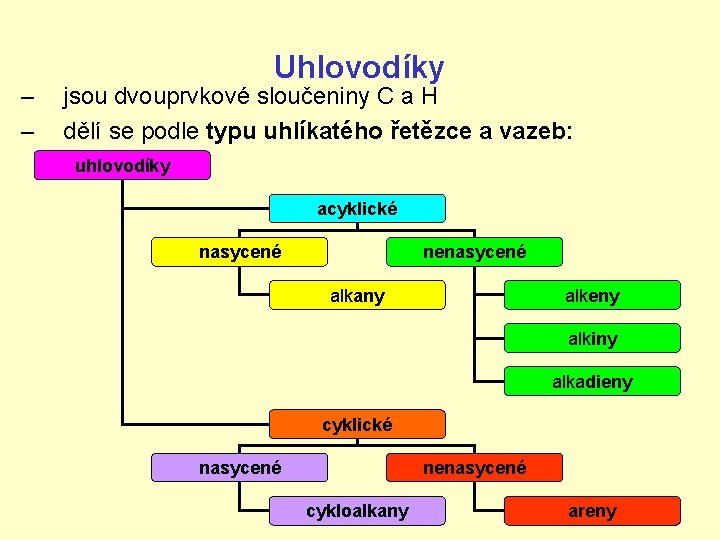
– – Uhlovodíky jsou dvouprvkové sloučeniny C a H dělí se podle typu uhlíkatého řetězce a vazeb: uhlovodíky acyklické nasycené nenasycené alkany alkeny alkiny alkadieny cyklické nasycené nenasycené cykloalkany areny

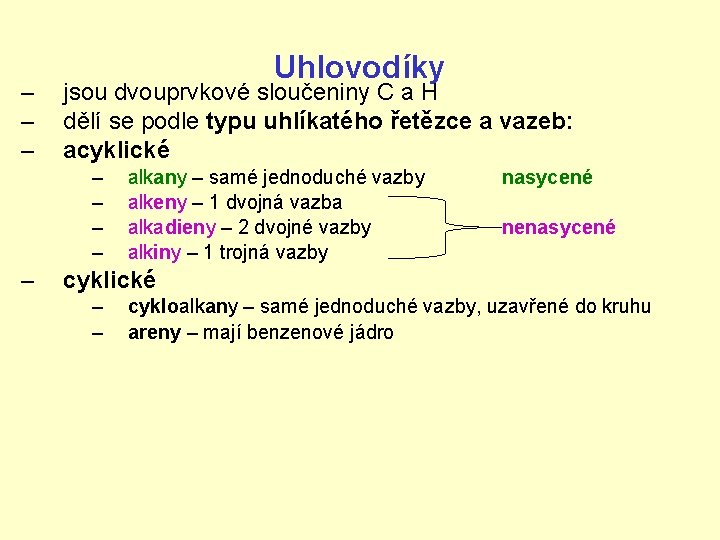
– – – Uhlovodíky jsou dvouprvkové sloučeniny C a H dělí se podle typu uhlíkatého řetězce a vazeb: acyklické – – – alkany – samé jednoduché vazby alkeny – 1 dvojná vazba alkadieny – 2 dvojné vazby alkiny – 1 trojná vazby nasycené nenasycené cyklické – – cykloalkany – samé jednoduché vazby, uzavřené do kruhu areny – mají benzenové jádro

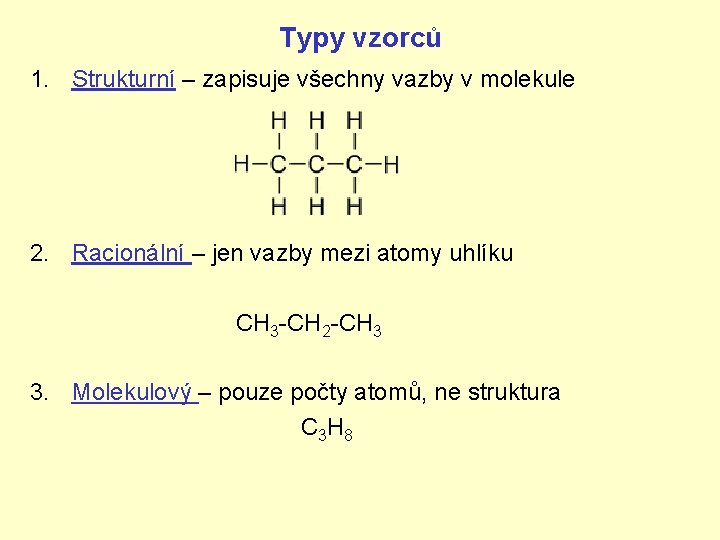
Typy vzorců 1. Strukturní – zapisuje všechny vazby v molekule 2. Racionální – jen vazby mezi atomy uhlíku CH 3 -CH 2 -CH 3 3. Molekulový – pouze počty atomů, ne struktura C 3 H 8

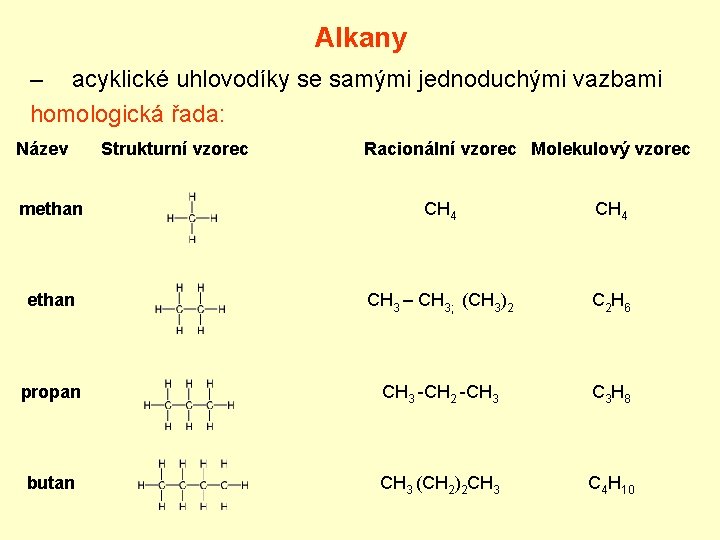
Alkany – acyklické uhlovodíky se samými jednoduchými vazbami homologická řada: Název Strukturní vzorec Racionální vzorec Molekulový vzorec methan CH 4 ethan CH 3 – CH 3; (CH 3)2 C 2 H 6 propan CH 3 -CH 2 -CH 3 C 3 H 8 butan CH 3 (CH 2)2 CH 3 C 4 H 10

Alkany – acyklické uhlovodíky se samými jednoduchými vazbami homologická řada: pentan hexan heptan oktan nonan dekan undekan dodekan obecný vzorec alkanů Cn. H 2 n+2

Vlastnosti alkanů – – 1 – 5 atomů C – plyny – nejvíce obsažené v zemním plynu 6 – 14 atomů C – kapaliny od 15 atomů C – pevné látky – nejvíce obsažené v ropě čisté alkany – bezbarvé, – vzájemně se mísí, – ve vodě nerozpustné – hořlavé

Zástupci alkanů Methan – na Uranu součást atmosféry nebo kapalný – tvoří oceány – součást zemního plynu (90%), bioplynu (60%) – bezbarvý plyn, snadno zápalný, nerozpustný ve vodě – těžší než vzduch, – v určitém poměru se vzduchem tvoří výbušnou směs užití: – palivo – výroba vodíku, acetylénu, čistých sazí

Alkany Propan a butan - kapalná směs stlačená v ocelových lahvích – palivo v domácnosti, v automobilech = LPG (ekolog. palivo, šetrné), náplň zapalovačů Oktan -oktanové číslo – určuje kvalitu benzínu





















