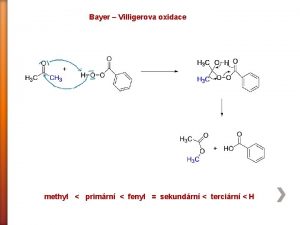
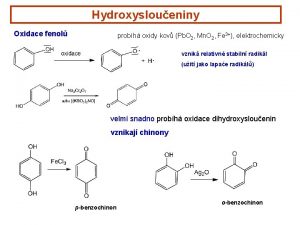
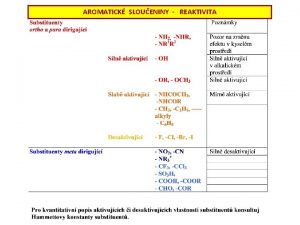
Obecn principy metabolismu Biologick oxidace makroergn sloueniny Biochemick

Obecné principy metabolismu Biologické oxidace, makroergní sloučeniny © Biochemický ústav LF MU 2013 - (H. P. ) 1
Metabolismus Soubor pochodů přeměny látek a energií v živých organismech Růst Rozmnožování Udržování struktury Udržování funkcí Reakce na prostředí 2
Látkový metabolismus Soubor pochodů přeměny látek v živých organismech (látková přeměna) Metabolické pochody spjaty s energií - pochody k ziskání energie - pochody využívající energii 3

ENERGIE Nezbytná pro každý živý organismus Potřeba energie: - Pohyb: (Mechanická práce-svaly, buněčné pohyby) - Transport molekul (iontů) přes membrány - Syntéza biomolekul - Další potřeby (udržování tělesné teploty apod) Zisk energie u lidského organismu: metabolismem živin Energetický metabolismus je metabolismus, ve kterém z chemické energie živin vzniká energie využitelná v organismu. 4
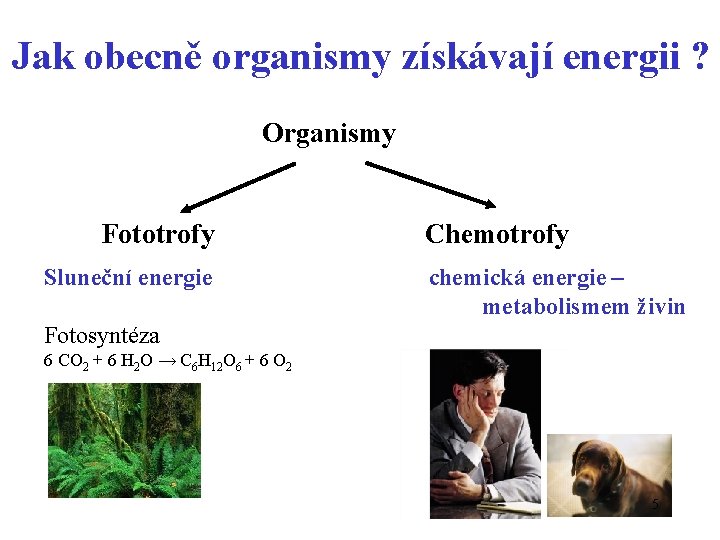
Jak obecně organismy získávají energii ? Organismy Fototrofy Sluneční energie Chemotrofy chemická energie – metabolismem živin Fotosyntéza 6 CO 2 + 6 H 2 O → C 6 H 12 O 6 + 6 O 2 5
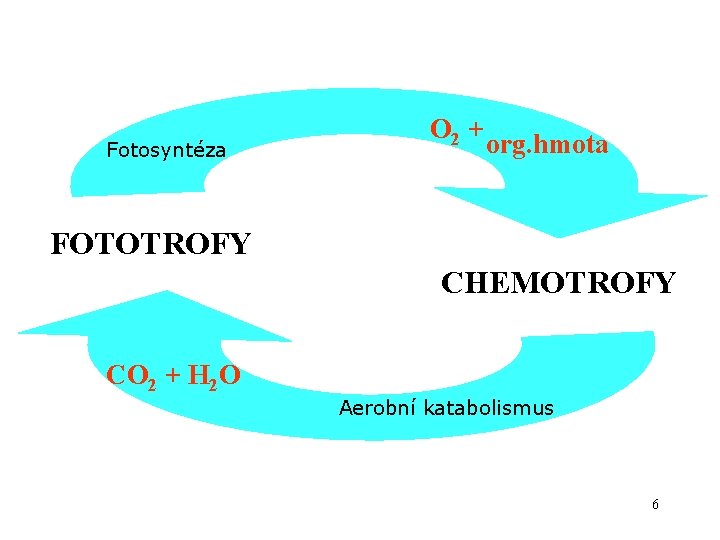
Fotosyntéza O 2 + org. hmota FOTOTROFY CHEMOTROFY CO 2 + H 2 O Aerobní katabolismus 6

Energie živých organismů má svůj původ ve sluneční energii, která je fotosyntézou transformována na do energii chemických vazeb. 7

Energie a chemická reakce • posouzení, zda chemická reakce se uskuteční dle energie • vyjadřujeme ji jako volnou energii (Gibsova energie: G) Gibsova energie: maximální energie, kterou soustava (na základě chemického děje) může využít k vykonání práce • symbol G kritérium spontánnosti reakcí (p, t je konstantní) 8
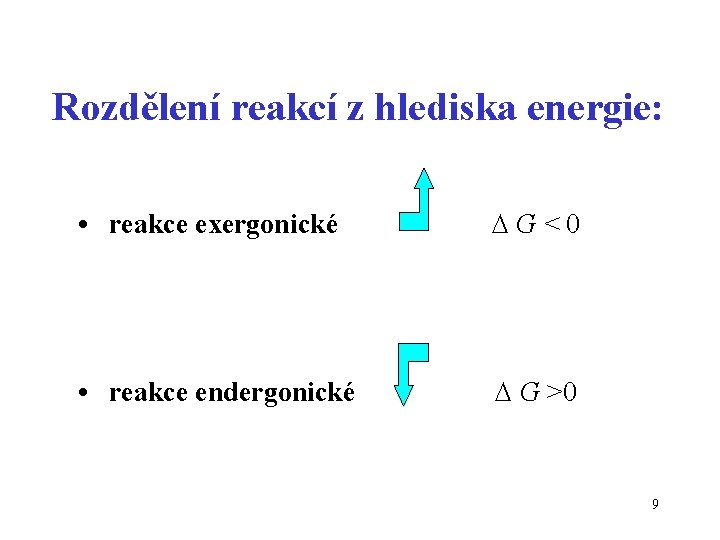
Rozdělení reakcí z hlediska energie: • reakce exergonické G<0 • reakce endergonické G >0 9
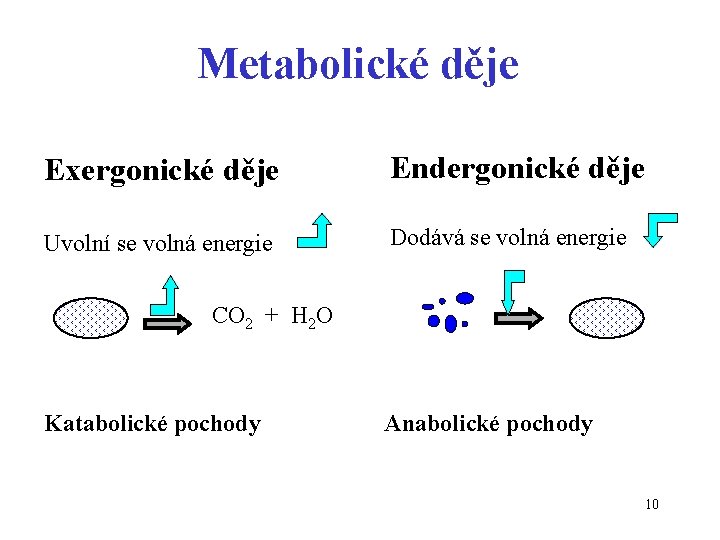
Metabolické děje Exergonické děje Endergonické děje Uvolní se volná energie Dodává se volná energie CO 2 + H 2 O Katabolické pochody Anabolické pochody 10
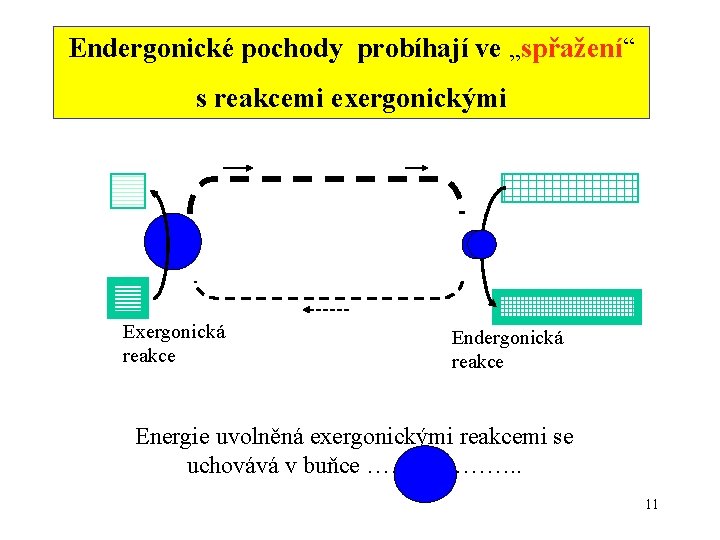
Endergonické pochody probíhají ve „spřažení“ s reakcemi exergonickými Exergonická reakce Endergonická reakce Energie uvolněná exergonickými reakcemi se uchovává v buňce ………………. . 11

Katabolismus Anabolismus Soubor degradačních procesů Soubor biosyntetických procesů Př: Trávení živin Př: Biosyntéza biomakromolekul Oba typy procesů probíhají současně, s různou intensitou 12

Uchovávání volné energie Energeticky bohaté sloučeniny • ve své struktuře uchovávají energii • při jejich rozkladu se energie uvolní 13
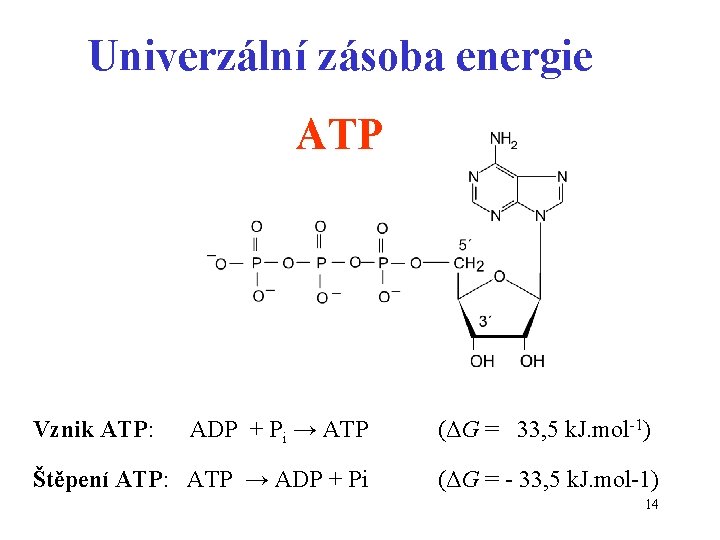
Univerzální zásoba energie ATP Vznik ATP: ADP + Pi → ATP Štěpení ATP: ATP → ADP + Pi (ΔG = 33, 5 k. J. mol-1) (ΔG = - 33, 5 k. J. mol-1) 14

Chemická energie ATP se využívá například na: • chemickou práci (syntézy, spřažení dvou reakcí) • mechanickou práci (pohyb molekul, buněk, organismu) • elektroosmotickou práci (transport iontů - viz tabulka) Průměrné koncentrace vybraných iontů (mmol/l): Tekutina Na+ K+ ECT 140 4 ICT 10 160 15
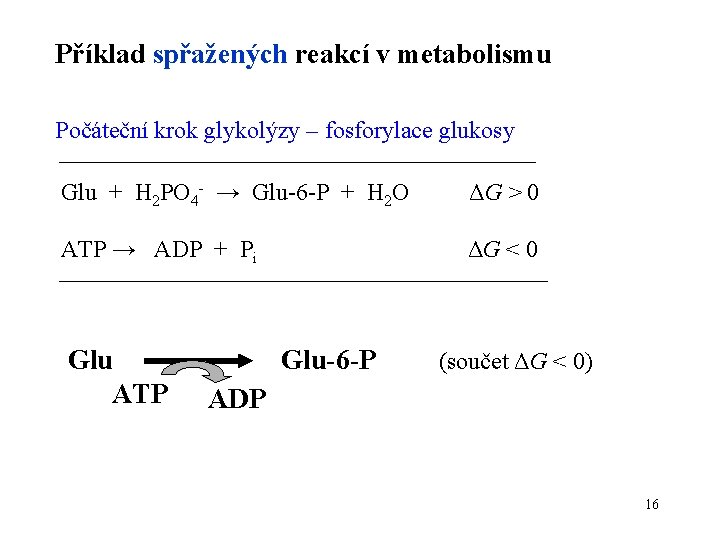
Příklad spřažených reakcí v metabolismu Počáteční krok glykolýzy – fosforylace glukosy Glu + H 2 PO 4 - → Glu-6 -P + H 2 O ΔG > 0 ATP → ADP + Pi ΔG < 0 Glu ATP Glu-6 -P (součet ΔG < 0) ADP 16

Další makroergní sloučeniny • pyrimidinové nukleosidtrifosfáty: UTP - pro aktivaci glukosy (syntéza glykogenu) CTP - aktivace cholinu při syntéze fosfolipidů • purinové nukleosidtrifosfáty GTP - při proteosyntéze • metabolity s vysokým stupněm energie kreatinfosfát – při svalové práci fosfoenolpyruvát – meziprodukt glykolýzy • thioestery sukcinyl-Co. A – při biosyntéze hemu 17

Biologické oxidace Oxidačně redukční reakce Katalyzovány enzymy - oxidoreduktasami Význam: - metabolismus živin - buněčná respirace 18

Opakování důležitých pojmů Oxidace Ztráta elektronů Redukce Příjem elektronů (př. Fe 2+ → Fe 3+) (př. Fe 3+ → Fe 2+ ) Ztráta 2 atomů vodíků (dehydrogenace) Příjem 2 atomů vodíků (hydrogenace) (př. laktát → pyruvát) Příjem kyslíku (př. pyruvát → laktát) Ztráta kyslíku 19

Oxidačně redukční reakce Při oxidaci látka A odevzdává elektrony a při redukci látka B elektrony přijímá, přičemž oba děje probíhají současně. Příklad: Ared + Box Aox + Bred Zn + Cu 2+ Zn 2+ + Cu 20

Oxidačně redukční reakce organických sloučenin Ared + Box Aox + Bred Příklad: dehydrogenace laktátu laktát + NAD+ pyruvát + NADH + H+ H Obecně: vodíkové atomy jsou při dehydrogenačních reakcích přenášeny na kofaktory - NAD+ a FAD (vznikají redukované kofaktory NADH a FADH 2) 21
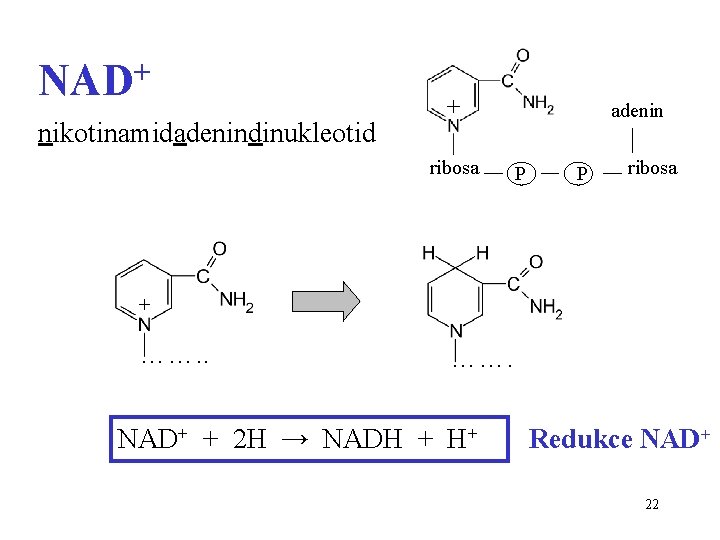
NAD+ nikotinamidadenindinukleotid + ribosa adenin P P ribosa + ……. NAD+ + 2 H → NADH + H+ Redukce NAD+ 22
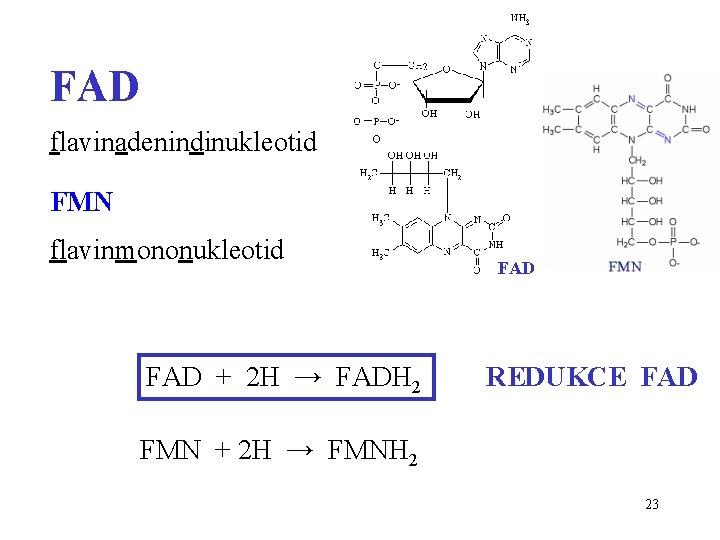
FAD flavinadenindinukleotid FMN flavinmononukleotid FAD + 2 H → FADH 2 FAD REDUKCE FAD FMN + 2 H → FMNH 2 23

Souvislost kofaktorů a vitaminů Viz. další přednáška 24

Oxidoreduktasy katalyzují oxidaci nebo redukci substrátu - dehydrogenasy: katalyzují transfer 2 H atomů Např. alkoholdehydrogenasa: ethanol + NAD+ acetaldehyd + NADH + H+ - oxygenasy: katalyzují zabudování jednoho nebo dvou O atomů do substrátu (monooxygenasy, dioxygenasy) - oxidasy: katalyzují transfer elektronů mezi substráty Např. cytochrom-c-oxidasa v respiračním řetězci - peroxidasy: katalyzují rozklad peroxidů Např. kataláza: H 2 O 2 → 2 H 2 O + O 2 25
! Princip odbourání živin postupná oxidace živin ! DEHYDROGENACE vzniká CO 2 + H 2 O ENERGIE (ATP) 26

Živiny slouží jako zdroj energie sacharidy lipidy bílkoviny postupná oxidace – formou dehydrogenace • vodíkové atomy převedeny na koenzymy - vznik NADH, FADH 2 - redukované kofaktory převedeny do dýchacího řetězce - oxidace redukovaných kofaktorů v dýchacím řetězci - vznik energie ve formě ATP (aerobní fosforylace) • uhlíkový skelet živin je postupnou oxidací převeden na CO 2 a H 2 O 27

Dýchací řetězec (DŘ, respirační řetězec) Dýchací řetězec je soustava redoxních dějů ve vnitřní mitochondriální membráně, která začíná oxidací NADH a končí redukcí O 2 na vodu. Aerobní fosforylace je děj, při kterém se energie získaná reoxidací redukovaných kofaktorů v DŘ využívá pro syntézu ATP 28

Hlavní rysy dýchacího řetězce • vnitřní mitochondriální membrána • systém (kaskáda, řetěz) oxidoredukčních enzymů s kofaktory enzymové komplexy I-IV dva pohyblivé přenašeče (koenzym Q, cyt c) kofaktory: cytochromy ubichinon (koenzym Q) FMN, FAD bílkoviny s nehemovým železem a sírou • konečná fáze přeměny vodíku z živin Spřažení dýchacího řetězce s aerobní fosforylací 29
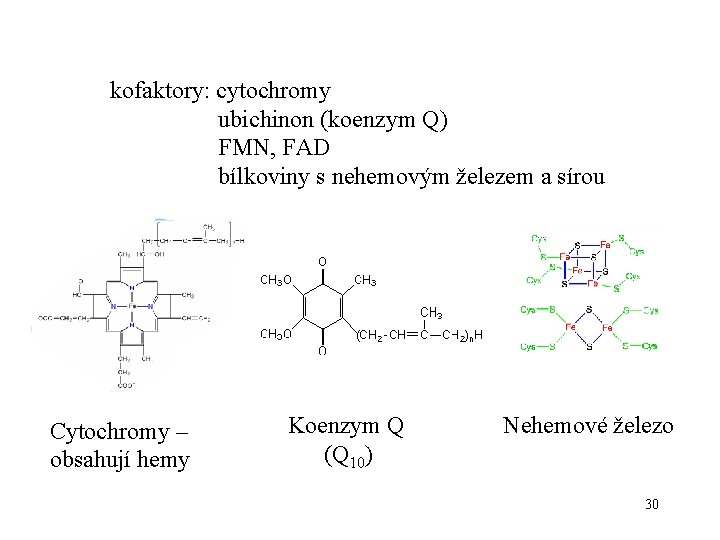
kofaktory: cytochromy ubichinon (koenzym Q) FMN, FAD bílkoviny s nehemovým železem a sírou Cytochromy – obsahují hemy Koenzym Q (Q 10) Nehemové železo 30
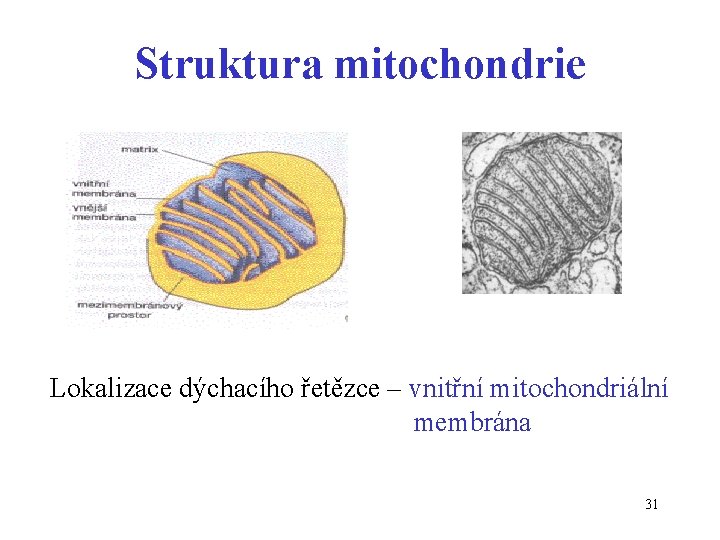
Struktura mitochondrie Lokalizace dýchacího řetězce – vnitřní mitochondriální membrána 31
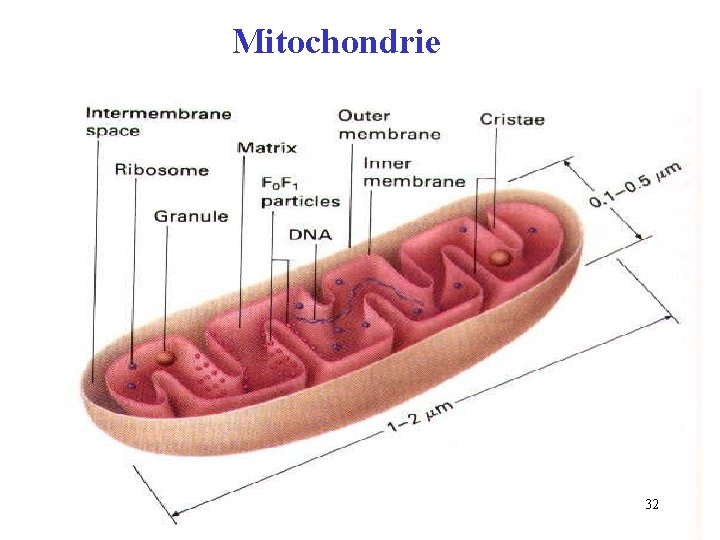
Mitochondrie 32

Vnitřní mitochondriální membrána • kristy • semipermeabilní • není propustná pro ionty • není propustná protony ! • obsahuje enzymové komplexy dýchacího řetězce, kofaktory • obsahuje transportní proteiny 33
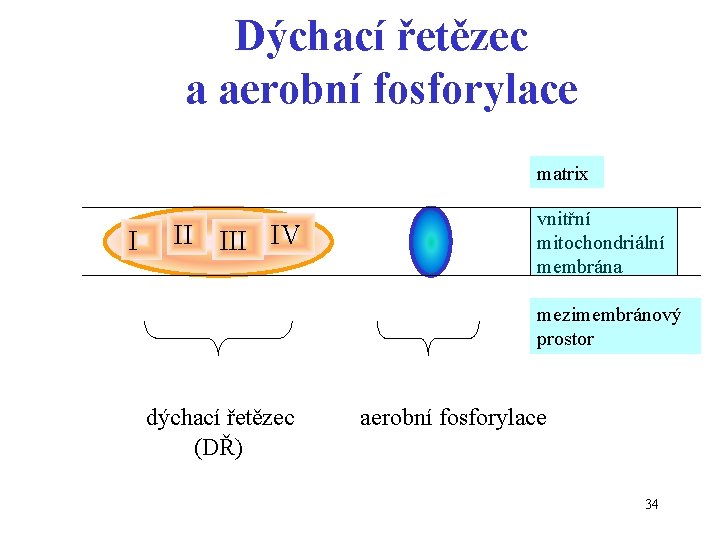
Dýchací řetězec a aerobní fosforylace matrix I II IV vnitřní mitochondriální membrána mezimembránový prostor dýchací řetězec (DŘ) aerobní fosforylace 34
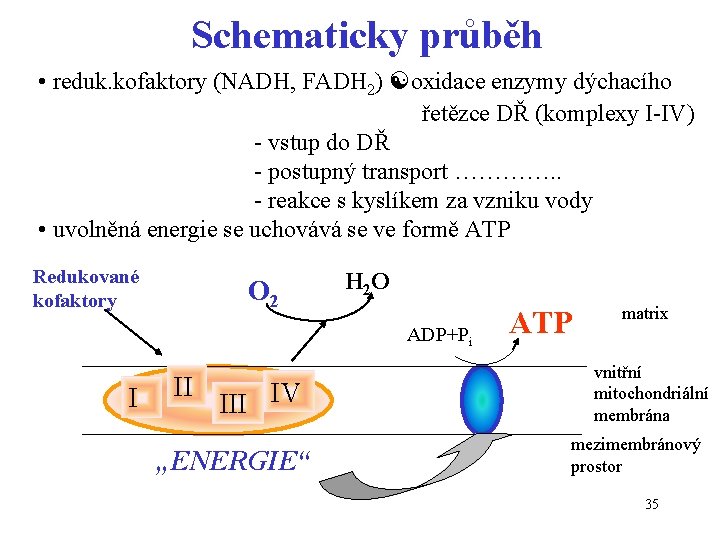
Schematicky průběh • reduk. kofaktory (NADH, FADH 2) oxidace enzymy dýchacího řetězce DŘ (komplexy I-IV) - vstup do DŘ - postupný transport …………. . - reakce s kyslíkem za vzniku vody • uvolněná energie se uchovává se ve formě ATP Redukované kofaktory O 2 H 2 O ADP+Pi I II IV „ENERGIE“ ATP matrix vnitřní mitochondriální membrána mezimembránový prostor 35
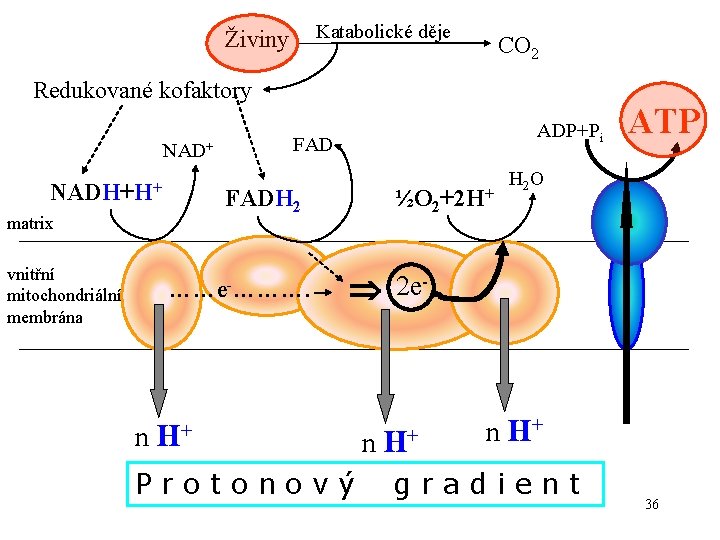
Katabolické děje Živiny CO 2 Redukované kofaktory NAD+ NADH+H+ FADH 2 matrix vnitřní mitochondriální membrána ……e-………. n ADP+Pi ½O 2+2 H+ ATP H 2 O 2 e- H+ Protonový n H+ gradient 36
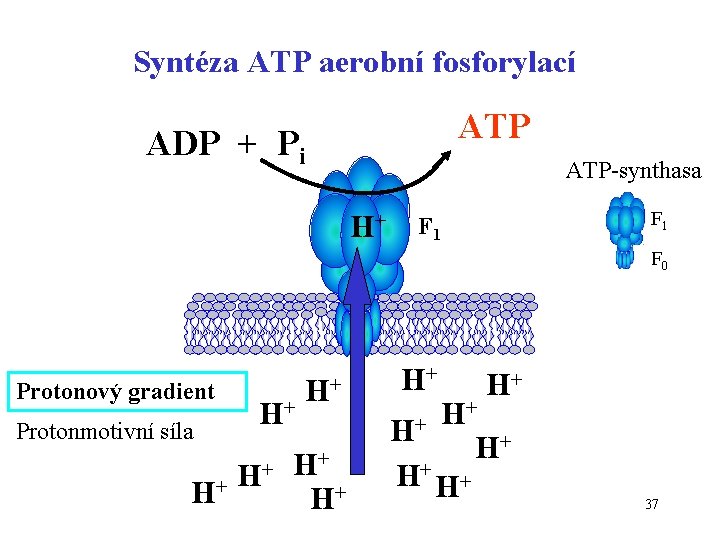
Syntéza ATP aerobní fosforylací ATP ADP + Pi ATP-synthasa H+ F 1 F 0 Protonový gradient Protonmotivní síla H+ H+ + H H+ H+ 37
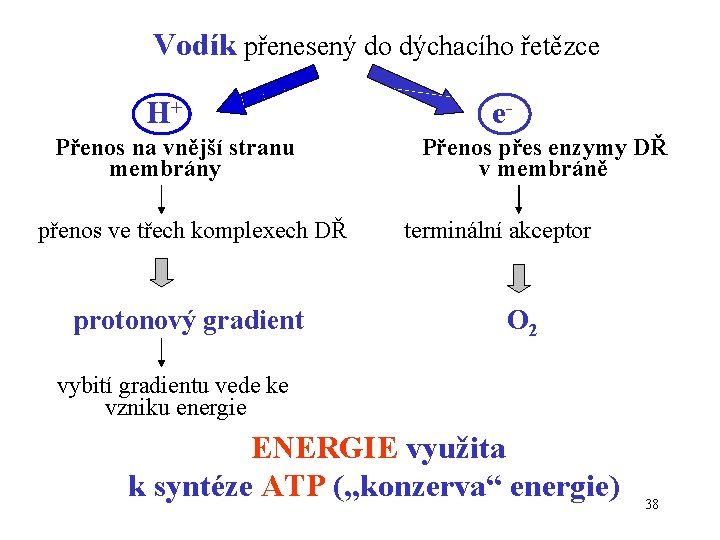
Vodík přenesený do dýchacího řetězce H+ Přenos na vnější stranu membrány přenos ve třech komplexech DŘ protonový gradient e. Přenos přes enzymy DŘ v membráně terminální akceptor O 2 vybití gradientu vede ke vzniku energie ENERGIE využita k syntéze ATP („konzerva“ energie) 38

Zisk energie v dýchacím řetězci Stechiometrie tvorby ATP při aerobní fosforylaci Oxidace Zisk ATP NADH 3 FADH 2 2 39

Spřažení DŘ a aerobní fosforylace DŘ spřažen s aerobní fosforylací: • vybití protonového gradientu přes ATP-syntázu vznik ATP (vnitřní mitochondriální membrána – nepropustná pro H+) Rozpojovače • Látky, které rozpojí DŘ od aerobní fosforylace (mohou vybít protonový gradient bez zisku chemické energie ATP) • uvolní se pouze teplo 40

Působení rozpojovačů • DŘ probíhá bez přerušení • aerobní fosforylace neprobíhá 41
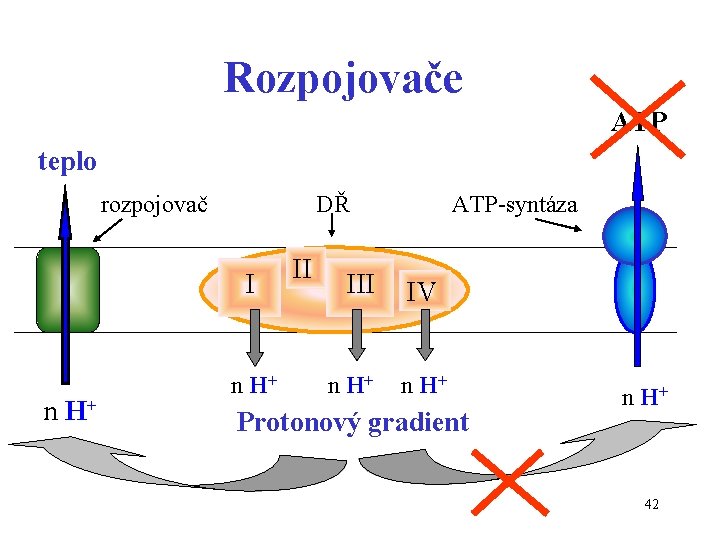
Rozpojovače ATP teplo rozpojovač DŘ I n H+ II III n H+ ATP-syntáza IV n H+ Protonový gradient n H+ 42

2, 4 -Dinitrofenol • pravý rozpojovač • otrava: zvýšená tělesná teplota, horečka, pocení, zrychlený dech • smrtelná dávka kolem 1 g • v letech 1920 -30 se užíval v dávce 2, 5 mg/kg jako „zázračný“ prostředek na hubnutí 43

Thermogenin • fyziologický rozpojovač • speciální bílkovina s kanálem pro H+ • vyskytuje se v hnědé tukové tkáni prokrvená, hodně mitochondrií • novorozenci, hibernující zvířata 44

Dva způsoby vzniku ATP Aerobní fosforylace • hlavní způsob vzniku ATP • navazuje na DŘ • na syntézu ATP se využije protonmotivní síla Substrátová fosforylace • ATP vzniká při konverzi makroergních meziproduktů při metabolismu živin sukcinyl-Co. A (CC) 1, 3 -bisfosfoglycerát (glykolýza) fosfoenolpyruvát (glykolýza) 45
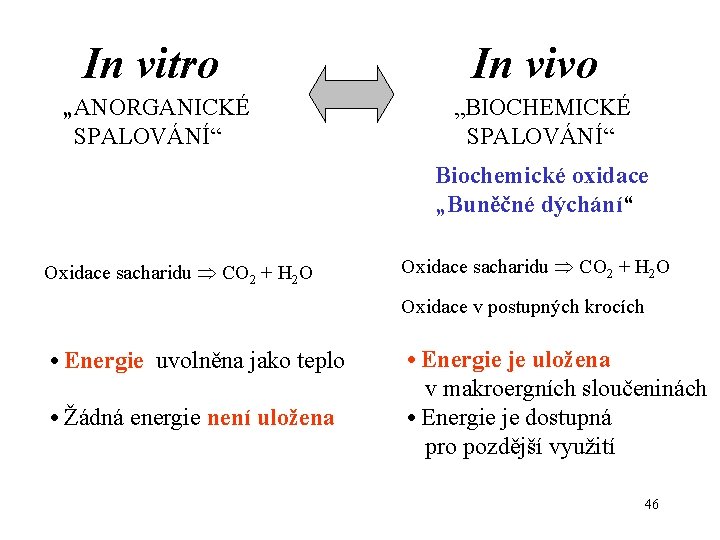
In vitro „ANORGANICKÉ SPALOVÁNÍ“ In vivo „BIOCHEMICKÉ SPALOVÁNÍ“ Biochemické oxidace „Buněčné dýchání“ Oxidace sacharidu CO 2 + H 2 O Oxidace v postupných krocích • Energie uvolněna jako teplo • Žádná energie není uložena • Energie je uložena v makroergních sloučeninách • Energie je dostupná pro pozdější využití 46
- Slides: 46