Oxidace a biosyntza mastnch kyselin ketogenese Oxidation and

Oxidace a biosyntéza mastných kyselin; ketogenese Oxidation and biosynthesis of fatty acids; ketogenesis Prof. Dr. V. Pelouch, CSc

Zopakuj • Lipidy jsou hetero. Lipidy genní skupinou sloučenin = všechny jsou hydrofobní. Jedná se hydrofobní často o estery (glyceestery rol a mastné kyseliny (MK) = (MK) TG, TG glycerofosfolipidy (glycerol, ( 2 x MK a 1 x kys. fosforečná), sfingolipids Recall • Lipids = heterogeni ous group of components: characteristic nents hydrophobicity. Esterification: glycerol : and fatty acids (FA) = TG, glycerophospholipids (glycerol, 2 x FA lipids and 1 x phosphoric acid), sfingolipids. . . )

Úvod • Mastné kyseliny (MK) jsou „volné“ = „volné“ nejsou esterifikovány; ale nejsou volné v krvi - jsou esterifikovány transportovány vždy ve vazbě na albumin, nebo vazbě na albumin cirkulují jako lipoproteinové komplexy: od místa vzniku v tukové tkáni (triacylglyceroly v adipovzniku cytech jsou hlavní reservoir energie pro organismus) k místu jejich spotřeby – tkáních (především v játrech a svalech) kde jsou kde degradovány; oxidace MK produkuje energii = ATP • MK jsou esterifikovány = triacylglyceroly (zásobesterifikovány ní látky), jsou součástí membránových lipidů = fosfolipidy, sfingolipidy, glykolipidy, prekursory glykolipidy prostaglandinů.

Introduction • Fatty acids (FA) exist „free“ in body = it means that they are unsterified. Plasma FA are transported in blood in binding with serum albumin or binding albumin in lipoprotein complexes on route from point of complexes origin ( origin triacylglycerols from adipocytes are major body energy reservoir) to their site of consumption (predominantly in muscles or liver); degraption liver dation of FA in tissues produced energy =ATP • FA are esterified – esterified triacylglycerol, structural , component of membranes: phospholipid, sphingolipids, glycolipids, precursor of glycolipids prostaglandins

Struktura MK • MK obsahuje různě dlouhý hydrofobní uhlíkatý řetězec a terminální hydrofilní –COOH skupinu řetězec hydrofilní (p. Ka = 4. 8), která je při fysiologickém p. H ionisována (-COO- ). MK vykazují proto amfipatické vlastnosti (= hydrofilní a hydrofobní vlastnosti). vlastnosti Běžné MK jsou však hydrofobní – 90% MK součástí esterů (triacylglycerol, cholesterylester, součástí esterů fosfolipidy): jsou obsaženy v lipoproteinových komplexech • 10% MK (neesterifikované) jsou transportovány 10% MK v krvi ve vazbě na albumin

Structure of FA • FA consists of hydrophobic hydrocarbon chain hydrocarbon with terminal hydrophilic -COOH (p. Ka =4. 8), at physiol. p. H this group is ionized (COO-); it means that FA have amphipathic nature (= both nature hydrophobic and hydrophilic properties). Most FA have hydrophobic nature = water insolubl. Therefore, in plasma FA 90% is transported in 90% form of FA esters (triacylglycerol, cholesteryl esters ester, phospholipids) in different lipoproteins. 10% = unesterified FA are transported in unesterified association with albumin

Struktura MK (nomenklatura) n 3 2 1 ω β α CH 3 -(CH 2)n - (CH 2) – COOH • 18: 0 znamená, že MK má osmnáct uhlíků a žádnou dvojnou vazbu (=nasycená mastná kyselina) • 18: 2 znamená, že MK má osmnáct uhlíků a dvě dvojné vazby (=nenasycená mastná kyselina- podle počtu dvojných vazeb máme mononenasycené (MUFA) a ( polynenasycené MK (PUFA) • Kde je dvojná vazba? Lokalizace vazba? • Použije se buď ∆ 9, 12 nebo (9, 12) znamená, že dvojná vazba vychází z uhlíků 9, 12 - viz číslování uhlíků uvedené výše. Jinou možností je použít vyjádření ω9 nebo n-9 číslo znamená, že první dvojná vazba se vyskytuje na uhlíku devět – počítáno od posledního („omega“ uhlíku) • ω3 or 6 mají specifické biologické vlastnosti

Structure of FA (nomenclature) n 3 2 1 ω β α CH 3 -(CH 2)n - (CH 2) - COOH • 18: 0 it means FA 18 C and no double bond (= sat. FA) . • 18: 2 it means FA 18 C and two double bonds (= unsat. FA) : mono- MUFA or polyunsaturated FA - PUFA) • Where is double bonds ? ? Localization • Using either ∆ 9, 12 or (9, 12) – it means double bond from C 9, 12 - see numbering above or used numbering from ωC. Then it will be ω9 or n-9: number corresponded that first double bond is comming from carbon nine (from last = omega C) • ω3 or 6 have specific biomedical imporance

Structure of FA, main FA (C 4 -C 10 in milk, C 16 or higher = structural lipids, TG…, (two categories: saturated/unsat

Nejdůležítější MK • Kyselina palmitová 16: 0 Kyselina stearová 18: 0 CH 3 -(CH 2)14 –COOH CH 3 -(CH 2)16 –COOH • Kyselina palmitooleova 16: 1 (9 c) ω7 CH 3 -(CH 2)5 –CH=CH-(CH 2)7 –COOH • Kyselina olejová 18: 1 (9 c) ω9 CH 3 -(CH 2)7 –CH=CH-(CH 2)7 –COOH • Kyselina linolová 18: 2 c 9, c 12, ω6 CH 3 -(CH 2)4 –CH=CH – CH 2 -CH=CH- (CH 2)7 –COOH • Kyselina linolenová 18: 3 c 9, c 12, c 15 ω3 CH 3 -(CH 2)-CH=CH-CH 2–CH=CH-CH 2 -CH=CH-(CH 2)7 –COOH • Kyselina arachidonová 20: 4 c 5, c 8, c 11, c 4 ω6 CH 3 -(CH 2)4 -CH=CH-CH 2 -CH=CH-(CH 2)7–COOH

Important FA • Palmitic acid 16: 0 Stearic acid 18: 0 CH 3 -(CH 2)14 –COOH CH 3 -(CH 2)16 –COOH • Palmitoleic acid 16: 1 (9 c) ω7 CH 3 -(CH 2)5 –CH=CH-(CH 2)7 –COOH • Oleic acid 18: 1 (9 c) ω9 CH 3 -(CH 2)7 –CH=CH-(CH 2)7 –COOH • α Linoleic acid 18: 2 c 9, c 12, ω6 CH 3 -(CH 2)4 –CH=CH – CH 2 -CH=CH- (CH 2)7 –COOH • Linoleic acid 18: 3 c 9, c 12, c 15 ω3 CH 3 -(CH 2)-CH=CH-CH 2–CH=CH-CH 2 -CH=CH-(CH 2)7 –COOH • Arachidonic acid 20: 4 c 5, c 8, c 11, c 4 ω6 CH 3 -(CH 2)4 -CH=CH-CH 2 -CH=CH-(CH 2)7–COOH

Syntéza MK MK probíhá v cytosolu Synthesis of FA in cytosol

První reakce • Acetylkoezym A je A uvolněn z mitochondrie jako citrát, citrát v cytosolu je rozložen na Ac. Ko. A a OA OA • Malonylkoenzym vzniká karboxylací Ac. Ko. A (biotin, ATP) (viz nasl. obr. ) • Multienzymový komplex / First reactions • Acetyl. Coenzym A is A released from mitochondria via citrate, citrate into cytosol, citrate is converted into Ac. Co. A and OA OA • Malonylcoenzyme A - A carboxyzation of Ac. Co. A (biotin, ATP) (next slide) • Reactions on multienzyme complex

FA synthase = multienzyme complex + ACP = acyl carrier protein, production of Ac. Co. A and malonyl. Co. A)

Další reakce • Vazby na dvě -SH skupiny: Ø Ac. Ko. A na cystein v betaacyl-acetylase Ø Malonyl-Ko. A na cystein pantothenatu v ACP • Kondenzace Ac. Ko. A a Malonyl-Ko. A -vazba na ACP (+decarboxylace) • CH 3 COCH 2 CO- S ACP / Next reactions Ø Binding on two –SH groups: Ø Ac. Co. A on cystein v on betaacyl-acetylase Ø Malonyl-Co. A on cystein of pantotheine in ACP in Condensation Ac. Co. A and malonyl. Co. A -binding on ACP (+decarboxylation) • CH 3 COCH 2 CO- S ACP

Další reakce / Next reactions • První redukce: • (NADPH) CH 3 COHCH 2 CO-S-ACP • dehydratace: CH 3 CH=CH CO- S-ACP • Druhá redukce: (NADPH) CH 3 CH 2 CO- S-ACP • Translokace butyryl na Cys v KS • Prodloužení: Děj pokračuje další vazbou malonyl. Ko. A na ACP až do vytvoření palmitatu (C 16) • First reduction: (NADPH) CH 3 COHCH 2 CO-S-AC • dehydratation: CH 3 CH=CH CO- S –ACP • Second reduction: (NADPH) CH 3 CH 2 CO- S-ACP • Translocation of butyryl group on Cys in KS • Prolongation: by the next binding of malonyl. Co. A on ACP up to formation of palmitate (C 16)

Cytosolic synthesis of palmitate reduction, dehydratation, reduction

Two reductions in synthesis of FA need NADHP
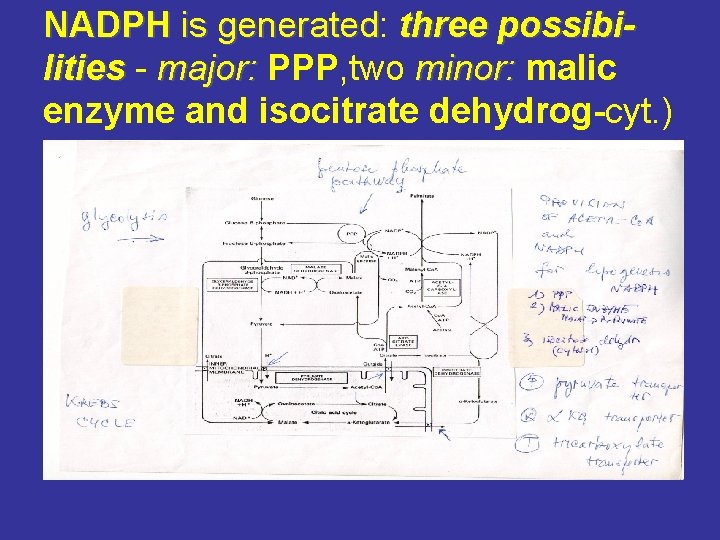
NADPH is generated: generated three possibilities - minor: malic lities major: PPP, two major: enzyme and isocitrate dehydrog-cyt. )

Degradace MK MK probíhá v mitochondrii Degradation of FA FA in mitochondia

Hormonal regulation of removal TG from adipocyte; FA in blood

TG from nutrition are hydrolyzed by c. AMP lipases

Transport MK /Transport of FA • Transport MK v krvi - • Transport of FA in MK FA ve vazbě na albumin blood stream - either (nebo v lipoproteiin binding on albumin nových komplexech); (or in lipoprotein nových lipoprotein complexes). • přestup MK do buňky (a v buňce) je • Transfer FA into ve vazbě na FABP = cells (and in cells) is FABP = „mastné kyseliny due to binding of FA vázající proteiny on diffferent FABP´= „fatty acids binding proteins“

Vstup do mitochondrie / Enter into mitochondria • Před vstupem do mitochondrie musí být mitochondrie MK aktivována: ATP a Ko. A = vzniká AMP + PP + acyl. Ko. A • acyl. Ko. A projde vnější mitochondriální membránu, přestup přes vnitřní membránu vyžaduje karnitinem • V mitochondriálním matrix degradace: beta oxidace • Before enter into mitochondria FA is activated chondria by ATP and Co. A = arise AMP + PP + acyl. Co. A • acyl. Co. A penetrates outer mitochondrial membrane, via inner mitochon ne, drial membrane only after binding with carnitine • In matrix of mitochondria degradation: beta oxidation
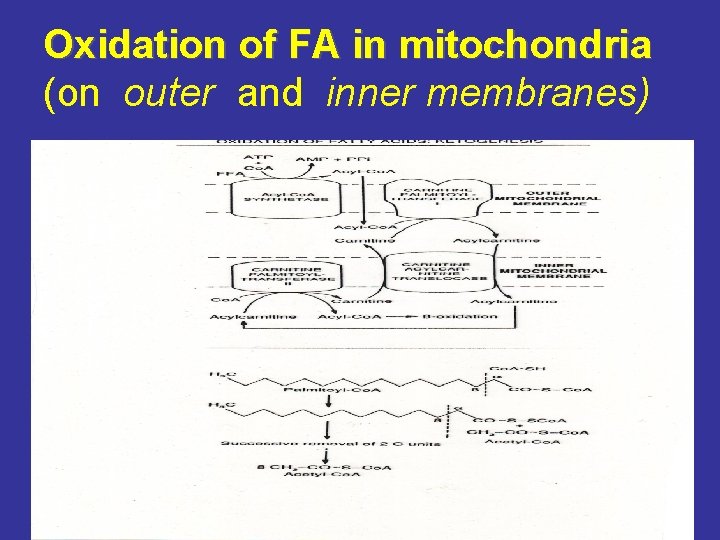
Oxidation of FA in mitochondria (on outer and inner membranes)

Principy beta oxidace /Principless of β - oxidation • • • Oxidace (FAD) Oxidace Hydratace Oxidace (NAD) Oxidace Thiolysa (Ko. A) Thiolysa Odštěpí se Ac. Ko. A a Ac. Ko. A tak zbývající acyl je o dva uhlíky kratší • Děj se opakuje až zůstane poslední C 2 = Ac. Ko. A • • • Oxidation (FAD) Oxidation Hydratation Oxidation (NAD) Oxidation Thiolysis (Co. A) Removal of Ac. Co. A and rest acyl is two carbon shorter • Repetion till last C 2 = C 2 Ac. Co. A

Beta oxidation - principless, oxidation and carnitine shuttle
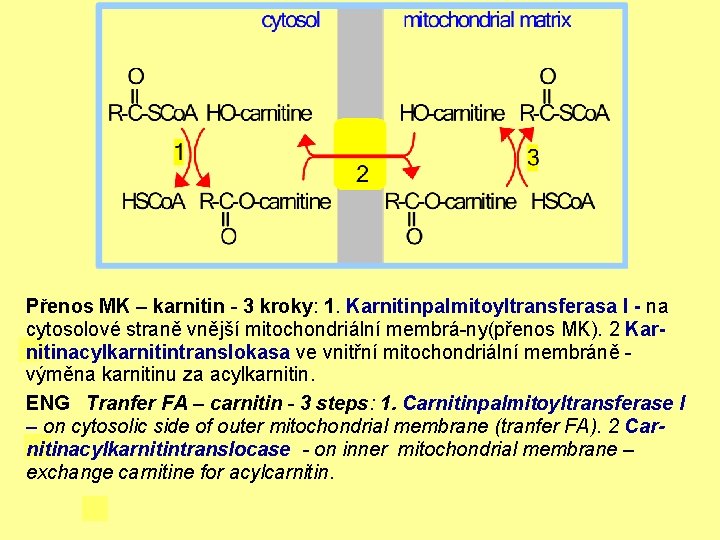
Přenos MK – karnitin - 3 kroky: 1. Karnitinpalmitoyltransferasa I - na cytosolové straně vnější mitochondriální membrá-ny(přenos MK). 2 Karnitinacylkarnitintranslokasa ve vnitřní mitochondriální membráně - výměna karnitinu za acylkarnitin. ENG Tranfer FA – carnitin - 3 steps: 1. Carnitinpalmitoyltransferase I – on cytosolic side of outer mitochondrial membrane (tranfer FA). 2 Carnitinacylkarnitintranslocase - on inner mitochondrial membrane – exchange carnitine for acylcarnitin.
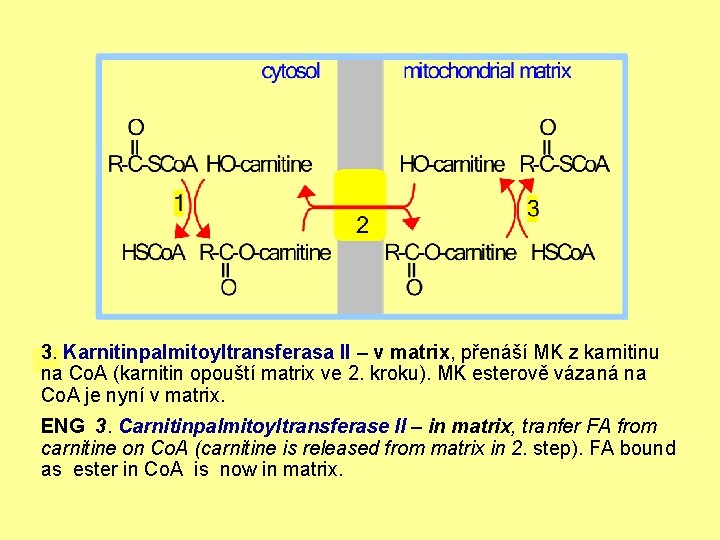
3. Karnitinpalmitoyltransferasa II – v matrix, přenáší MK z karnitinu na Co. A (karnitin opouští matrix ve 2. kroku). MK esterově vázaná na Co. A je nyní v matrix. ENG 3. Carnitinpalmitoyltransferase II – in matrix, tranfer FA from carnitine on Co. A (carnitine is released from matrix in 2. step). FA bound as ester in Co. A is now in matrix.

Energy yield from palmitoyl. Co. A (16 carbon FA) =129 ATP

Synthesis and degradation FA (differences)

Ø Oxidace MK s lichým počtem uhlíků Ø V posledním kole reakčního cyklu b-oxidace získáme, v případě MK s lichým počtem uhlíků, acetyl-Co. A & propionyl-Co. A. Propionyl-Co. A je přeměněn na succinyl-Co. A (karboxylace -vyžaduje biotin, succinyl-Co. A je substrátem citrátového cyklu), v Oxidation of FA with odd numbers of C v In last reaction of b-oxidation of FA with odd numbers of C is recovered acetyl-Co. A (= C 2) and propionyl. Co. A (= C 3)- Propionyl-Co. A is carboxylated (it needs biotin) to succinyl-Co. A (substrate in KC)

Ø Oxidace nenasycených MK Ø Většina nenasycených MK má cis konfiguraci dvojných vazeb. Tyto MK tudíž nejsou vhodnými substráty pro enoyl. Co. A- hydratasu (vyžaduje trans izomery): potřeba dalších enzymů isomerasa a reduktasa v Oxidation unsaturated FA ENG v Most unsaturated FA have cis configuration of double binding; it is not suitable for enzyme enoyl-Co. A- hydratase; (needs trans isomers) – therefore, two other enzymes are needed: isomerasa a reductase

w Oxidace MK s velmi dlouhými řetězci probíhá v peroxisomech FADH 2 - vzniká v 1. kroku oxidace MK - není reoxidován v dýchacím řetězci, ale reakcí s O 2: FADH 2 + O 2 FAD + H 2 O 2 - katalasa rozkládá H 2 O 2: 2 H 2 O 2 2 H 2 O + O 2 Reakce nevedou k tvorbě ATP; oxidace končí u oktanoyl. Co. A - odstraněn z peroxisomů vázaný na karnitin; oxidován v mitochondriích

w Oxidation of FA with very long numbers of carbon is realized in peroxisomes ENG FADH 2 - arised in first step of oxidation of FA - is not oxidized in respiratory chain but reaction with O 2: FADH 2 + O 2 FAD + H 2 O 2 - catalase - cleavage of H 2 O 2: 2 H 2 O 2 2 H 2 O + O 2 Reaction did not produced ATP; oxidation of this type of FA finished at oktanoyl-Co. A; this one is removed from peroxisomes (oktanoyl-Co. A is bound to carnitin) and then oktanoyl-Co. A is transfered into mitochondia for oxidation
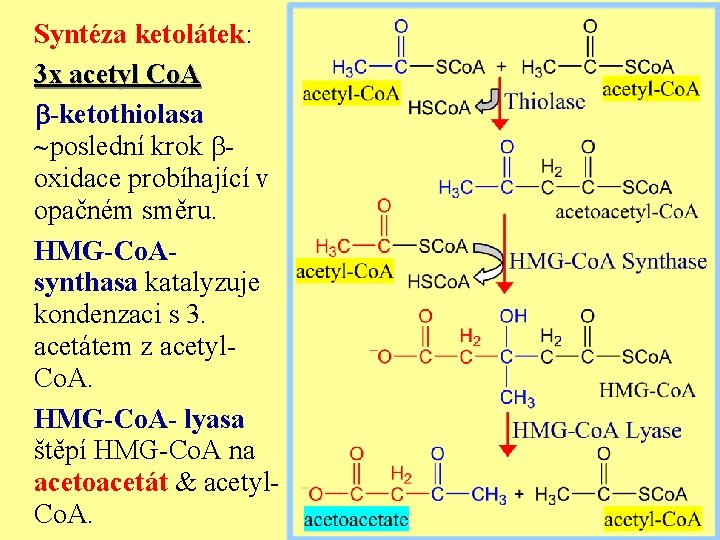
Syntéza ketolátek: 3 x acetyl Co. A b-ketothiolasa poslední krok boxidace probíhající v opačném směru. HMG-Co. Asynthasa katalyzuje kondenzaci s 3. acetátem z acetyl. Co. A. HMG-Co. A- lyasa štěpí HMG-Co. A na acetoacetát & acetyl. Co. A.
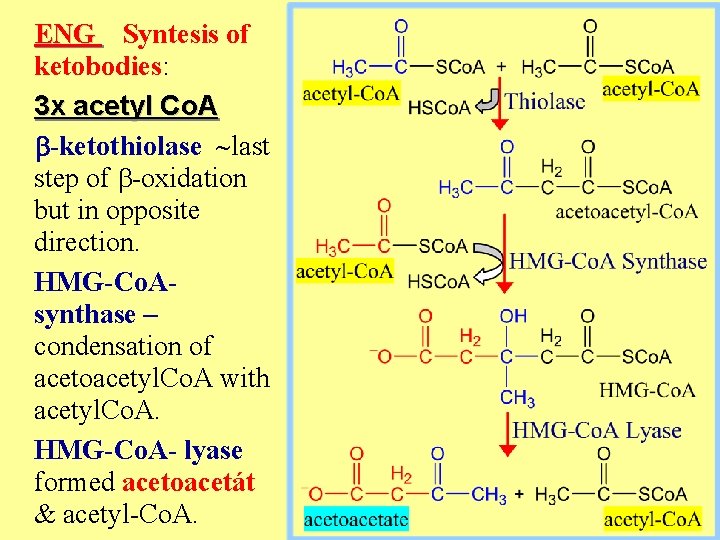
ENG Syntesis of ketobodies: 3 x acetyl Co. A b-ketothiolase last step of b-oxidation but in opposite direction. HMG-Co. Asynthase – condensation of acetoacetyl. Co. A with acetyl. Co. A. HMG-Co. A- lyase formed acetoacetát & acetyl-Co. A.

b-hydroxybutyrátdehydrogenasa katalyzuje vzájemnou reverzibilní přeměnu ketolátek: acetoacetátu and b-hydroxybutyrátu Ketolátky jsou krví transportovány do extrahepatálních tkání –zde jsou zpět přeměněny na acetyl-Co. A, který vstupuje do citrátového cyklu. Ketolátky tedy fungují jako alternativní zdroj energie. Ketoacidosa nastává v důsledku nadbytku ketolátek.
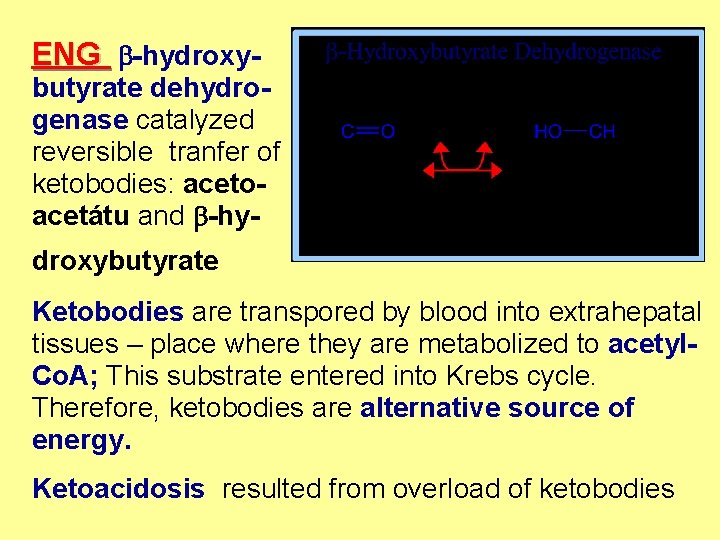
ENG b-hydroxy- butyrate dehydrogenase catalyzed reversible tranfer of ketobodies: acetoacetátu and b-hy- droxybutyrate Ketobodies are transpored by blood into extrahepatal tissues – place where they are metabolized to acetyl. Co. A; This substrate entered into Krebs cycle. Therefore, ketobodies are alternative source of energy. Ketoacidosis resulted from overload of ketobodies

Elongace -prodlužování řetězce MK- probíhá jak v mitochondriích tak v ER. w V mitochondriích probíhá elongace jako b-oxidace pouze opačně. V posledním kroku se elongace od boxidace odlišuje koenzymem (místo FADH 2 využívá NADPH) w V ER zahrnuje elongace kondenzaci malonyl-Co. A s acyl-Co. A. w Prodlužování řetězce MK se účastní enzymy elongasy ENG Elongation in both mitochondria (similar as betaoxidation but in opposite motion, last step is not FADH 2 but NADPH) and ER (condensation malonyl. Co. A and acetyl. Co. A) w Prolongation FA by different enzymes - elongases
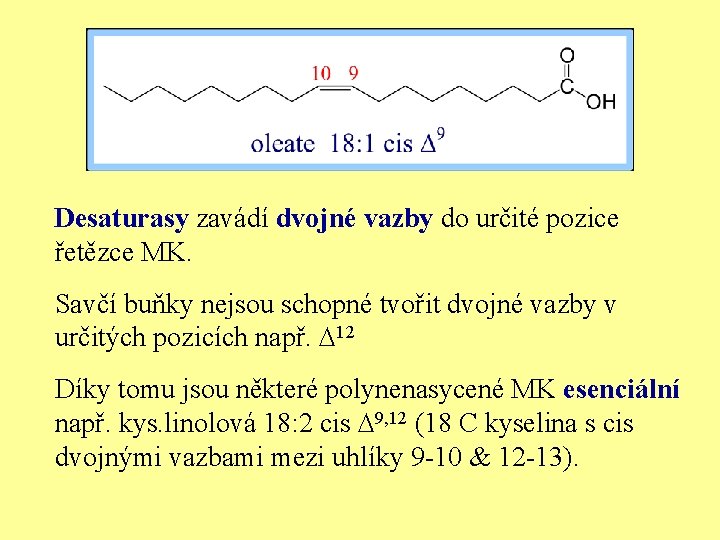
Desaturasy zavádí dvojné vazby do určité pozice řetězce MK. Savčí buňky nejsou schopné tvořit dvojné vazby v určitých pozicích např. D 12 Díky tomu jsou některé polynenasycené MK esenciální např. kys. linolová 18: 2 cis D 9, 12 (18 C kyselina s cis dvojnými vazbami mezi uhlíky 9 -10 & 12 -13).
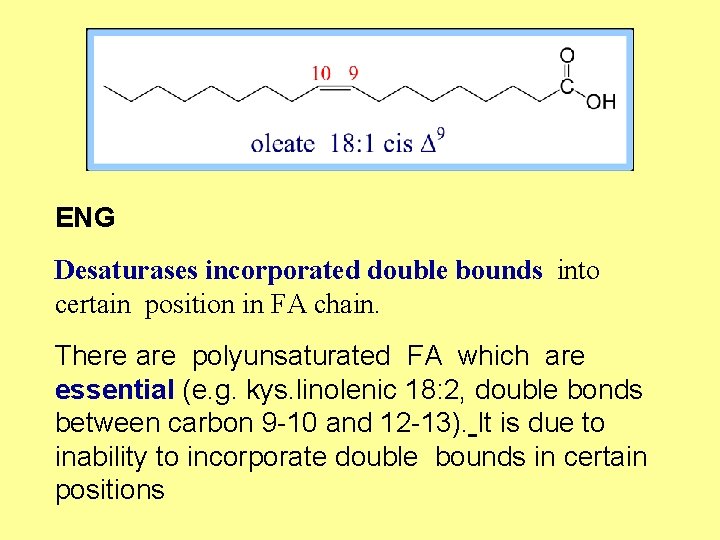
ENG Desaturases incorporated double bounds into certain position in FA chain. There are polyunsaturated FA which are essential (e. g. kys. linolenic 18: 2, double bonds between carbon 9 -10 and 12 -13). It is due to inability to incorporate double bounds in certain positions

MK – degradace/syntéza SUMMARY SOUHRN FA degradation/ synthesis Zatímco degradace MK probíhá v mitochondrii až k acetyl. Ko. A, vyžaduje řadu enzymů (FAD, NAD) tak syntéza MK probíhá v cytosolu na multienzymovém komplexu (NADPH) až do C 16, další elongace a -C=C- vyžaduje jiné enzymy Degradation of FA in mitochondria till acetyl. Co. A needs different enzymes (FAD, NAD), synthesis of FA in cytosol, multienzymes complex (NADPH) till C 16, next elongation and -C=C- needs other enzymes
- Slides: 43