Nzvoslov anorganickch slouenin Mgr Jakub Janek VY32INOVACECh 1

Názvosloví anorganických sloučenin Mgr. Jakub Janíček VY_32_INOVACE_Ch 1 r 0105

Názvosloví anorganických sloučenin • Přiřazení názvu příslušné sloučenině Název se skládá ze dvou částí Podstatné jméno oxid chlorid kyselina přídavné jméno uhličitý sodný sírová
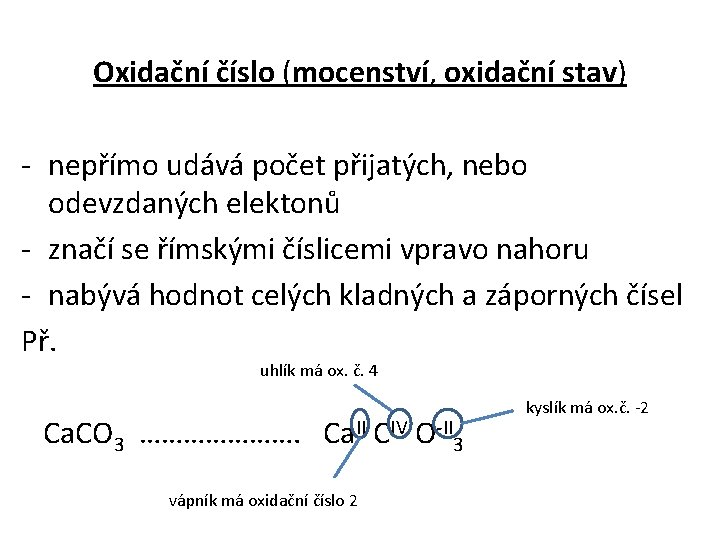
Oxidační číslo (mocenství, oxidační stav) - nepřímo udává počet přijatých, nebo odevzdaných elektonů - značí se římskými číslicemi vpravo nahoru - nabývá hodnot celých kladných a záporných čísel Př. uhlík má ox. č. 4 Ca. CO 3 …………………. Ca. II CIV O-II 3 vápník má oxidační číslo 2 kyslík má ox. č. -2
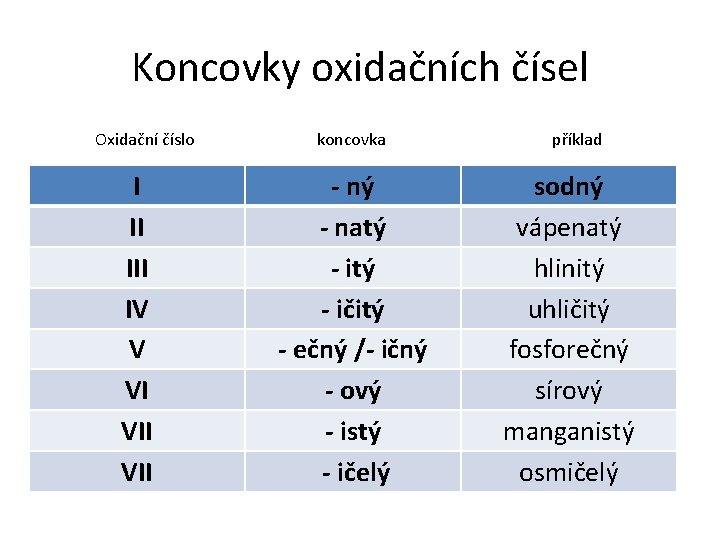
Koncovky oxidačních čísel Oxidační číslo I II IV V VI VII koncovka - ný - natý - ičitý - ečný /- ičný - ový - istý - ičelý příklad sodný vápenatý hlinitý uhličitý fosforečný sírový manganistý osmičelý

Názvosloví hydroxidů • Hydroxidy obsahují hydroxylovou skupinu s oxidačním číslem mínus jedna (OH)-I Nejprve napíšeme kov, poté OH skupinu, doplníme oxidační čísla + křížové pravidlo Př. Hydroxid vápenátý Ca(OH)2 II Ca (OH) jednička se nepíše automaticky se bere jeden vápník -I 2

Názvosloví oxidů • oxidy obsahují ve své molekule kyslík s oxidačním číslem mínus dvě O-II Nejprve napíšeme kov, poté kyslík, doplníme oxidační čísla + křížové pravidlo Pokud je počet obou prvků po křížovém pravidlu dělitelný dvěma – dojde ke zkrácení Př. oxid fosforečný oxid sírový V P 2 O -II 5 P 2 O 5 VI S 2 O -II 6 SO 3

Názvosloví sulfidů • sulfidy obsahují ve své molekule síru s oxidačním číslem mínus dvě S-II Nejprve napíšeme kov, poté síru, doplníme oxidační čísla + křížové pravidlo Pokud je počet obou prvků po křížovém pravidlu dělitelný dvěma – dojde ke zkrácení Př. sulfid sodný sulfid železnatý I Na 2 S -II Na 2 S II Fe 2 S -II 2 Fe. S
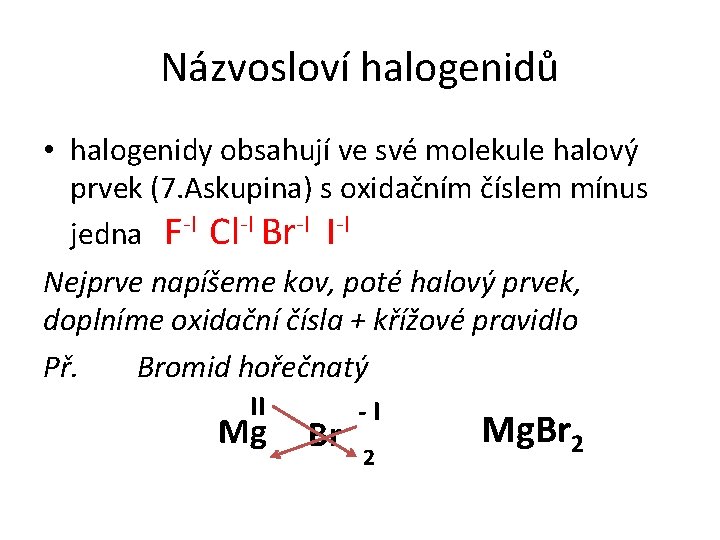
Názvosloví halogenidů • halogenidy obsahují ve své molekule halový prvek (7. Askupina) s oxidačním číslem mínus jedna F-I Cl-I Br-I I-I Nejprve napíšeme kov, poté halový prvek, doplníme oxidační čísla + křížové pravidlo Př. Bromid hořečnatý II Mg Br -I 2 Mg. Br 2
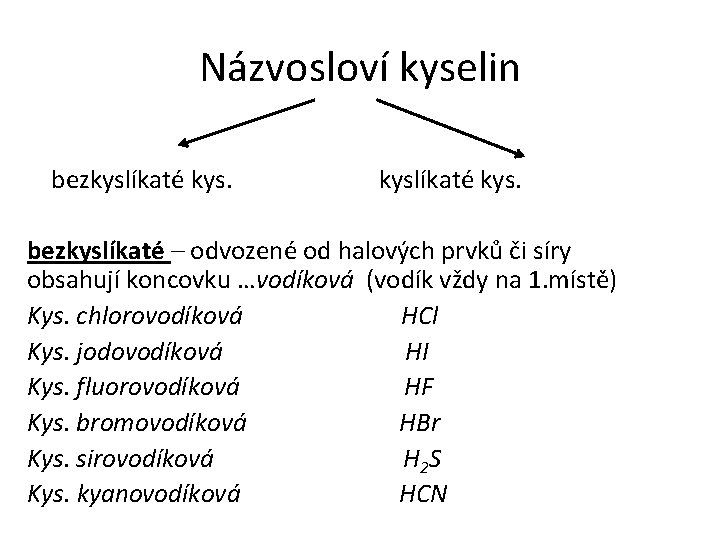
Názvosloví kyselin bezkyslíkaté kys. bezkyslíkaté – odvozené od halových prvků či síry obsahují koncovku …vodíková (vodík vždy na 1. místě) Kys. chlorovodíková HCl Kys. jodovodíková HI Kys. fluorovodíková HF Kys. bromovodíková HBr Kys. sirovodíková H 2 S Kys. kyanovodíková HCN
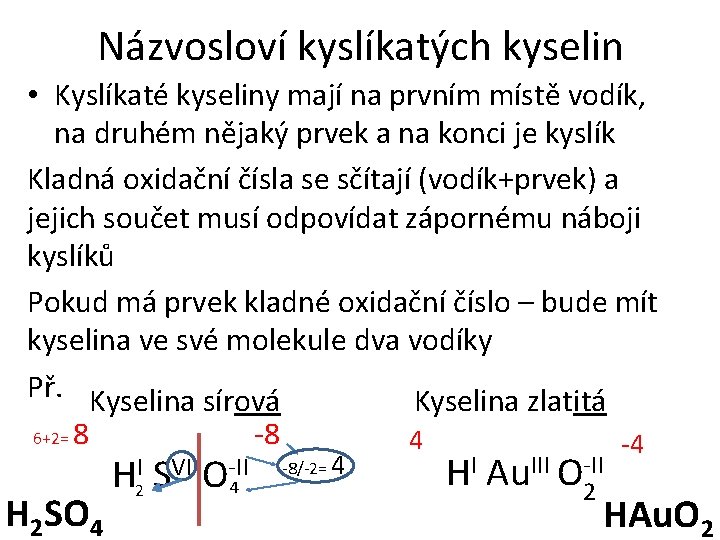
Názvosloví kyslíkatých kyselin • Kyslíkaté kyseliny mají na prvním místě vodík, na druhém nějaký prvek a na konci je kyslík Kladná oxidační čísla se sčítají (vodík+prvek) a jejich součet musí odpovídat zápornému náboji kyslíků Pokud má prvek kladné oxidační číslo – bude mít kyselina ve své molekule dva vodíky Př. Kyselina sírová Kyselina zlatitá 6+2= 8 -8 4 -4 H 2 SO 4 H 2 I SVI O-II 4 -8/-2= 4 HI Au. III O 2 -II HAu. O 2
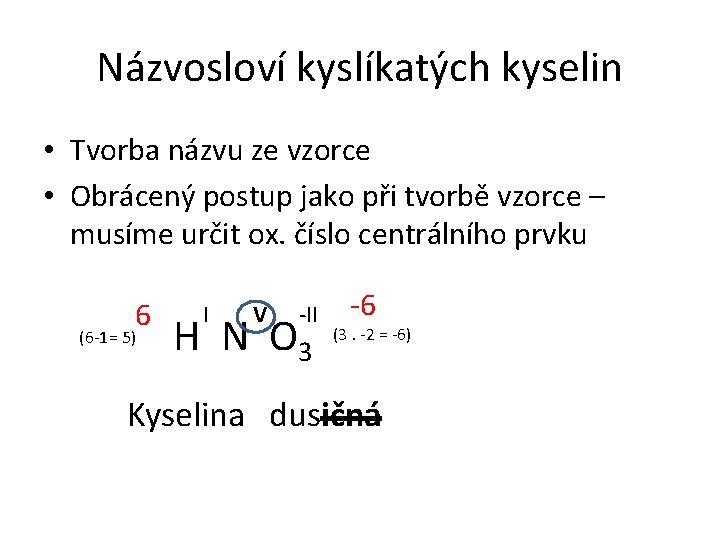
Názvosloví kyslíkatých kyselin • Tvorba názvu ze vzorce • Obrácený postup jako při tvorbě vzorce – musíme určit ox. číslo centrálního prvku 6 (6 -1= 5) I V -II H N O 3 -6 (3. -2 = -6) Kyselina dusičná

Názvosloví solí • Soli jsou odvozené od kyselin ( po nahrazení vodíku kovem) zbytky kyselin – záporný náboj je roven počtu odtrhnutých vodíků uhličitan …………. (CO 3)-II chlorečnan …………………. (Cl. O 3)-I síran ………… (SO 4)-II

Názvosloví solí • Nejprve napíšeme kov, který nahradil vodík a poté přidáme zbytek kyseliny. Napíšeme oxidační čísla a křížové pravidlo Př. dusičnan olovnatý Pb II (NO 3) -I 2 kys. dusičná HNO 3

Tvorba názvů solí Doplníme oxidační čísla a podle kyseliny odvodíme příslušnou sůl. Původní kyselina sírová H 2 SO 4 ……… síran (SO 4)-II Ca. II (SO 4)-II Síran vápenatý

Procvičování – doplňte názvy nebo vytvořte vzorec sloučeniny oxid železitý Na. OH sulfid hořečnatý H 2 S jodid stříbrný Si. O 2 kyselina jodistá BI 3 Manganistan draselný Ca. O kyselina jodovodíková HAu. O kyanid draselný Ca. CO 3
- Slides: 15