Roztoky Mgr Jakub Janek VY32INOVACECh 1 r 0111

Roztoky Mgr. Jakub Janíček VY_32_INOVACE_Ch 1 r 0111
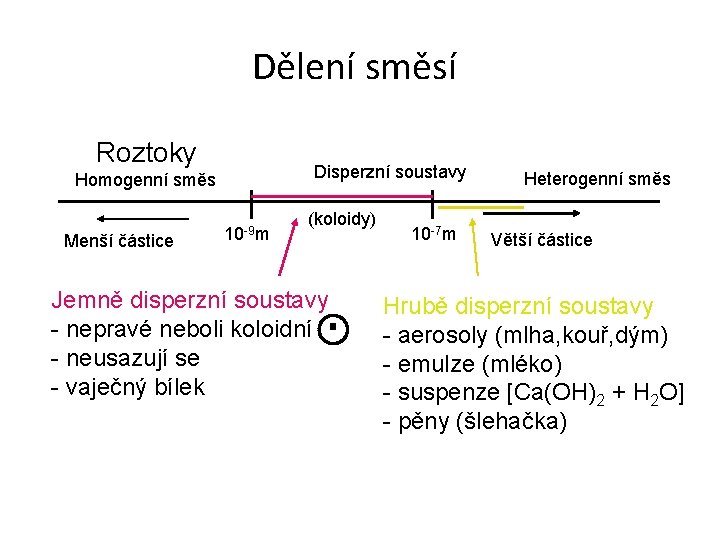
Dělení směsí Roztoky Disperzní soustavy Homogenní směs Menší částice 10 -9 m (koloidy) Jemně disperzní soustavy - nepravé neboli koloidní - neusazují se - vaječný bílek 10 -7 m Heterogenní směs Větší částice Hrubě disperzní soustavy - aerosoly (mlha, kouř, dým) - emulze (mléko) - suspenze [Ca(OH)2 + H 2 O] - pěny (šlehačka)

Roztok • Je homogenní směs dvou nebo více látek • Děj při němž vznikají roztoky = Rozpouštění (probíhá na molekulární úrovni) Složení roztoků – rozpouštědlo – látka, která je v nadbytku, většinou kapalina (H 2 O) - rozpuštěná l. – látka s určitou rozpustností pro dané rozpouštědlo

Rozpustnost látek Rozpustnost – schopnost l. rozpouštět se - udává se jako hmotnost látky rozpuštěné v 100 g rozpouštědla, při vzniku nasyceného roztoku (za dané teploty) – najdeme v tabulkách Př. Rozpustnosti některých látek v 100 g vody Název látky 0 o. C 20 o. C 100 o. C Na. Cl 36 g 40 g Na. OH 42 g 109 g 347 g

Na čem závisí rozpustnost látky? • rozpouštědle ( látka se jinak rozpouští v ethanolu a jinak ve vodě) • rozpouštěné látce ( Na. Cl má jinou než Na. OH) • přítomnosti dalších látek v roztoku ( Ag. Cl se více rozpouští v čisté vodě než v roztoku obsahujícím chloridy) • teplotě (rozpustnost plynů v kapalinách s rostoucí teplotou obyčejně klesá, rozpustnost pevných látek a kapalin v kapalinách s rostoucí teplotou většinou roste- ne vždy) • tlaku ( jen u plynů, s rostoucím tlakem roste rozpustnost)

Dělení roztoků Podle skupenství – pevné (slitiny kovů) kapalné (kyslík ve vodě) plynné (vzduch) Podle vodivosti – elektrolyt………. . Vede el. proud neelektrolyt……. Nevede el. proud Podle mísitelnosti – nemísitelné (voda + olej) neomezeně mísitelné (všechny plyny, voda + ethanol…) omezeně mísitelné (nenasycený, nasycený a přesycený roztok)

Možnosti omezeně mísitelných roztoků • Nenasycený roztok – roztok, ve kterém je za daných podmínek rozpuštěno méně látky než v roztoku nasyceném • Nasycený roztok - roztok, ve kterém se při určité teplotě již více látek nerozpustí • Přesycený roztok - roztok, ve kterém je za daných podmínek rozpuštěno více látky než v roztoku nasyceném (krystalky na dně)

Příklady 1) Kolik hydroxidu sodného je třeba rozpustit v 500 g vody, abychom získali nasycený roztok? Teplota v laboratoři je 20 o. C. (545 g) 2) Kolik soli je třeba nasypat do 5 l (5000 g) vody, aby nám nezamrzla (0 o. C)? Chceme vytvořit nasycený rotok! (1800 g)

Literatura: • Mareček, A. ; Honza, J. Chemie pro čtyřletá gymnázia 1. díl. Olomouc: Nakladatelství Olomouc, 1998, ISBN 80 -7182 -055 -5
- Slides: 9