NZEV KOLY ZKLADN KOLA KARLA KLE HOSTINN Autor











- Slides: 12

NÁZEV ŠKOLY: ZÁKLADNÍ ŠKOLA KARLA KLÍČE HOSTINNÉ Autor: Petrželová Eva Název: VY_32_INOVACE_03_A_12_Roztoky Téma: Organická a anorganická chemie Číslo projektu: CZ. 1. 07/1. 4. 00/21. 2131

ROZTOKY Vznik roztoků Nasycený roztok Nenasycený roztok Rozpustnost Dělení roztoků

VZNIK ROZTOKŮ Vznikají rozpuštěním látek v kapalině, která je rozpouštědlem Za rozpouštědlo bývá často považována látka, která je soustavně v nadbytku (často voda, ale i benzín, ethanol) Stejnorodé směsi neboli homogenní směsi dvou a více látek Děj, při kterém roztoky vznikají - rozpouštění

NASYCENÝ ROZTOK Nasycený roztok je takový roztok, v kterém se za daných podmínek už více rozpuštěné látky nerozpustí http: //www. zskunup. cz/images/bigimg/ 1289408525 -dsc-0025 -resize. jpg

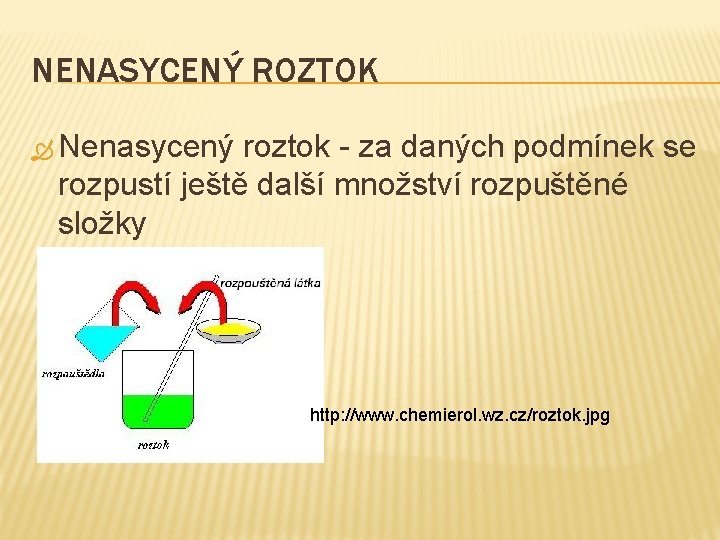
NENASYCENÝ ROZTOK Nenasycený roztok - za daných podmínek se rozpustí ještě další množství rozpuštěné složky http: //www. chemierol. wz. cz/roztok. jpg

ROZPUSTNOST Rozpustnost určité látky v daném rozpouštědle se většinou udává hmotností látky, která se za daných podmínek (teploty a tlaku) rozpustí v určitém váhovém nebo objemovém množství rozpouštědla za vzniku nasyceného roztoku Rozpustnost většiny pevných látek se s rostoucí teplotou rozpouštědla zvětšuje

DĚLENÍ ROZTOKU � Podle skupenství rozdělujeme roztoky: - pevné – slitiny kovů - kapalné – cukr rozpuštěný ve vodě - plynné – vzduch Rozpouštědlo – kapalina Rozpouštěná látka – plyn, kapalina, pevná látka

DĚLENÍ ROZTOKŮ Podle rozpuštěné látky: Roztoky elektrolitů – vznikají při rozpouštění iontových sloučenin, vzniklý roztok obsahuje volně pohyblivé, elek. nabité částice - vede elektrický proud Roztoky neelektrolitů – roztok jodu v chloridu uhličitém nebo roztok glukózy ve vodě - nevedou elektrický proud Roztoky potenciálních elektrolitů – obsahují polární vazbu

KONCENTRACE ROZTOKŮ � Můžeme vyjádřit pomocí: A) Hmotnostního zlomku : WA= m. A / m. R WA ……. hmotnostní zlomek m. A ……. hmotnost látky A m. R ……. hmotnost roztoku mr ……. . hmotnost rozpouštědla m. A + m r = m R

B) Hmotnostním procentem – w * 100 C) Objemovým procentem – objemové %= VA / VR * 100 D) Molární koncentrace – počet molů určité látky v rozpouštěné v 1 dm 3 roztoku C A= n A / V R CA…. . molární koncentrace látky A n. A …. počet molů látky A VR……celkový objem roztoku n= m /M

ZDROJE P. Beneš, V. Pumpr, J. Banýr, Základy chemie 1, pro druhý stupeň základní školy, nižší ročníky víceletých gymnázií a střední školy, FORTUNA Praha, 1993 A. Mareček, J. Honza, Chemie pro čtyřletá gymnázia -1. díl, Olomouc, 1998

� � � � � Anotace: Výklad Autor : Eva Petrželová Vytvořeno dne: 13. 8. 2012 Odpilotováno dne: ve třídě: osmá Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Téma: Organická a anorganická chemie Klíčová slova: roztoky, nasycené a nenasycené, koncentrace roztoků, dělení roztoků