MSZAKI FIZIKA ALAPJAI yi Istvn Egyetem s Kmia










- Slides: 15

MŰSZAKI FIZIKA ALAPJAI yi István Egyetem s Kémia Tanszék Az atommagok tulajdonságai és a magerők Dr. Giczi Ferenc Széchenyi István Egyetem Fizika és Kémia Tanszék 1

Az atommag szerkezete Az atomok felépítése, mérete elektronburok elektronok, me=9, 109· 10 -31 kg, qe=1, 6· 10 -19 C, ½ spin atommag Az atommagok alkotórészei (nukleonok) protonok, mp=1, 6726· 10 -27 kg, qp=1, 6· 10 -19 C, ½ spin neutronok, mn=1, 6749· 10 -27 kg, qn=0 C, ½ spin

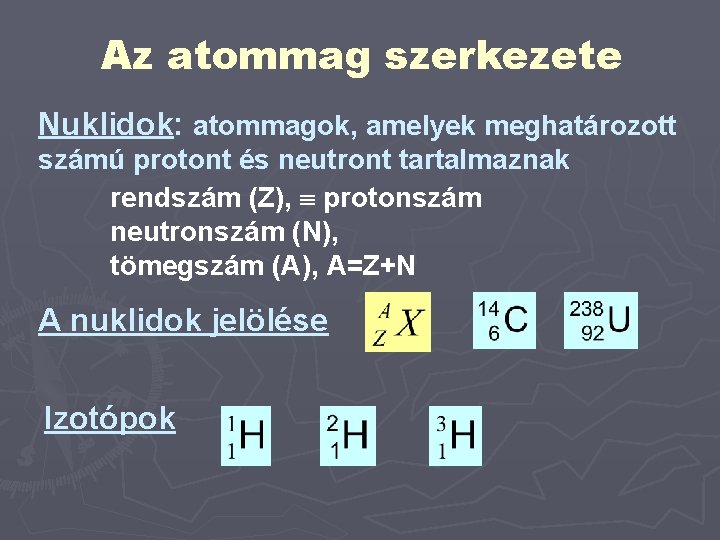
Az atommag szerkezete Nuklidok: atommagok, amelyek meghatározott számú protont és neutront tartalmaznak rendszám (Z), protonszám neutronszám (N), tömegszám (A), A=Z+N A nuklidok jelölése Izotópok

A magerők • Mintegy milliószor erősebbek, mint a Coulomb erők. • Kisebb a hatótávolságuk, mint a Coulomberőké (10 -15 m). • A magerők töltésfüggetlenek. • Az erőhatás független attól, hogy p-p, p-n vagy n-n között áll fenn a kölcsönhatás.

Az atommagok spinje és mágneses momentuma Az atommagok spinje (perdülete, imulzusmomentuma) az alkotórészek (protonok és neutronok) saját spinjéből és az atommagon belüli mozgásuk következtében előálló pályamomentumaikból tevődik össze (vektoriálisan).

Az atommagok spinje és mágneses momentuma Jelölés Spin (ps, ps) zérus spin (ps, pn) feles spin (pn, ps) feles spin (pn, pn) egész spin Példa • Az impulzusmomentummal nem rendelkező atommagoknak mágneses momentumuk sincsen. • Az impulzusmomentummal rendelkező atommagoknak mágneses momentumuk is van.

Az atommagok spinje és mágneses momentuma • Mágneses momentummal rendelkező atommagok külső mágneses térhez képest csak meghatározott irányokba állhatnak be. Átmenetek rádiófrekvenciás (MHz-es) váltakozó mágneses mezővel (mag-mágneses rezonancia, NMR).

Az atommagok tömege atomi tömegegység 1 u=M(12 C)/12=1, 6605· 10 -27 kg Példák: protonok, neutronok, mp=1, 6726· 10 -27 kg = 1, 007276 u mn=1, 6749· 10 -27 kg = 1, 008664 u elektronok, me=9, 109· 10 -31 kg = 5, 485· 10 -4 u

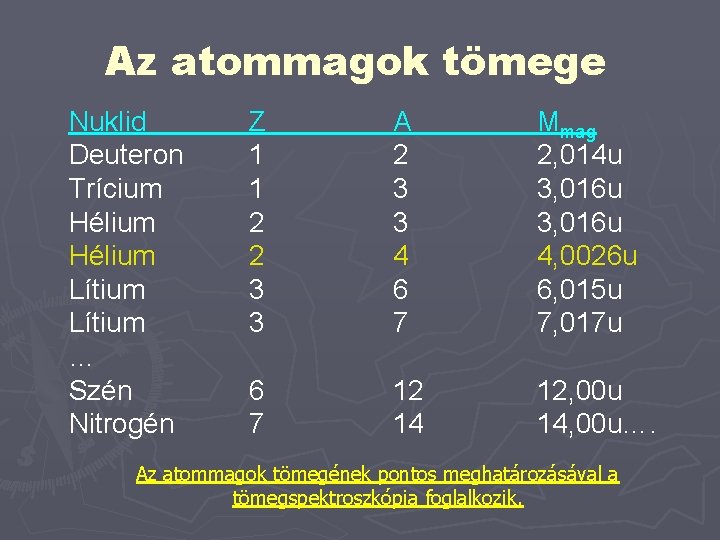
Az atommagok tömege Nuklid Deuteron Trícium Hélium Lítium … Szén Nitrogén Z 1 1 2 2 3 3 A 2 3 3 4 6 7 Mmag 2, 014 u 3, 016 u 4, 0026 u 6, 015 u 7, 017 u 6 7 12 14 12, 00 u 14, 00 u…. Az atommagok tömegének pontos meghatározásával a tömegspektroszkópia foglalkozik.

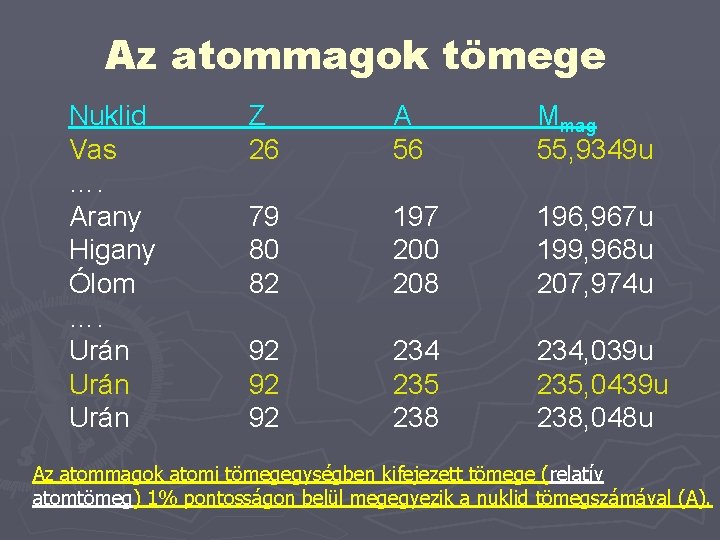
Az atommagok tömege Nuklid Vas …. Arany Higany Ólom …. Urán Z 26 A 56 Mmag 55, 9349 u 79 80 82 197 200 208 196, 967 u 199, 968 u 207, 974 u 92 92 92 234 235 238 234, 039 u 235, 0439 u 238, 048 u Az atommagok atomi tömegegységben kifejezett tömege (relatív atomtömeg) 1% pontosságon belül megegyezik a nuklid tömegszámával (A).

Az atommag mérete Az atommagok sugara a tömegszám köbgyökével arányos: Megjegyzés: Az atom sugara 10 -10 m (angström) nagyságrendű. Az atommagok sűrűsége állandó! Feladatok: • Számítsuk ki a vas (Z=26, A=56) atommagjának tömegét, térfogatát és sűrűségét. • Számítsuk ki általánosan az atommagok sűrűségét.

Az atommag kötési energiája Az atommagok tömege mindig kisebb, mint a nukleonok tömegének összege. Tömeghiány, tömegdefektus A m tömegváltozás mindig E energiaváltozással jár. A mag kötési energiája

Az egy nukleonra eső átlagos kötési energiája Az atommagok energiaállapotára, stabilitására vagy instabil voltára nagyon jellemző az egy nukleonra vonatkoztatott kötési energia. Feladat: • Mekkora a tömegdefektus és a kötési energia a Fe-56 nuklidokra? mp=1, 6726· 10 -27 kg mn=1, 6749· 10 -27 kg 1 u=1, 6605· 10 -27 kg

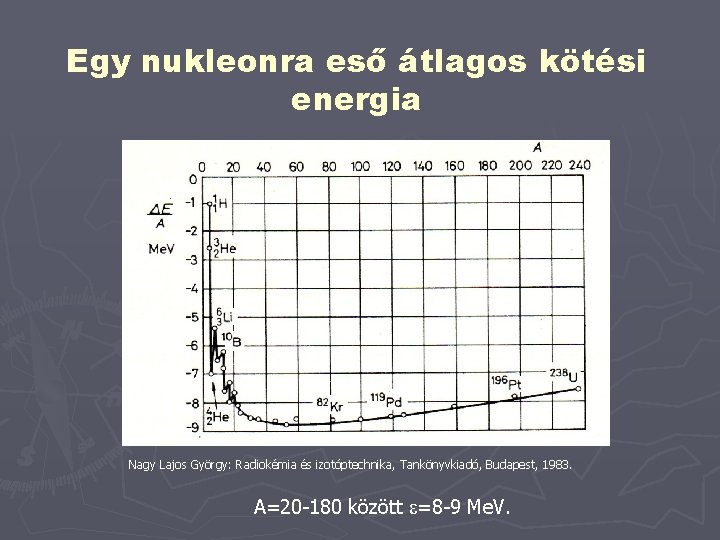
Egy nukleonra eső átlagos kötési energia Nagy Lajos György: Radiokémia és izotóptechnika, Tankönyvkiadó, Budapest, 1983. A=20 -180 között =8 -9 Me. V.

Köszönöm a figyelmüket! 18