Kyselinotvorn a hydroxidotvorn oxidy M Lukainov Hydroxidotvorn oxidy









- Slides: 10

Kyselinotvorné a hydroxidotvorné oxidy M. Lukačinová


Hydroxidotvorné oxidy �Oxid vápenatý patrí do skupiny oxidov, v ktorých sú s atómami kyslíka zlúčené atómy prvkov �s hodnotou elektronegativity rovnou 1 alebo menšou ako 1. Takéto oxidy reagujú s vodou za vzniku hydroxidov, preto ich nazývame hydroxidotvorné oxidy. Medzi ne patria predovšetkým oxidy prvkov I. A a II. A skupiny periodickej sústavy.

Kyselinotvorné oxidy. �Oxid siričitý patrí do skupiny oxidov, v ktorých sú atómami kyslíka zlúčené atómy prvkov �s hodnotou elektronegativity väčšou ako 2. �Väčšina týchto oxidov reaguje s vodou za vzniku kyseliny, preto ich nazývame kyselinotvorné oxidy.

Amfotérne oxidy �Oxid hlinitý patrí do skupiny oxidov, v ktorých sú s atómami kyslíka zlúčené atómy prvkov � s hodnotou elektronegativity väčšou ako 1, ale najviac rovnou 2. �Takýchto oxidov, ktoré nereagujú s vodou je väčšina. � Oxid hlinitý je amfotérny oxid hliníka s chemickým vzorcom Al 2 O 3, ktorý sa v prírode vyskytuje napr. ako minerál korund, prípadne ako jeho drahokamové odrody rubín či zafír. Priemyslene ho získavame z bauxitu a je hlavnou surovinou používanou pri výrobe hliníka.

Zásadotvorné oxidy reagujú: � � 1) s vodou (len rozpustné vo vode); vznikajú vo vode rozpustné hydroxidy: K 2 O + H 2 O ==> 2 KOH - hydroxid draselný � � � � Poznámka: Oxidy kovových prvkov sa vo vode takmer vôbec nerozpúšťajú, zato však reagujú so silnými kyselinami aj so silnými zásadami. Takéto oxidy sa nazývajú amfoterné. � 2) s kyselinotvornými oxidmi; vzniká soľ kyseliny, ktorá odpovedá kyselinotvornému oxidu: Sr. O + N 2 O 5 ==> Sr(NO 3)2 - dusičnan strontnatý 3) s amfoternými oxidmi; vzniká soľ kyseliny, ktorá odpovedá amfotérnemu oxidu: Ca. O + Zn. O ==> Ca. Zn. O 2 - zinočnatan vápenatý 4) s kyselinami; vzniká soľ a voda: Cr. O + H 2 SO 4 ==> Cr. SO 4 + H 2 O - síran chrómnatý + voda

Kyselinotvorné oxidy reagujú: � � 1) s vodou vzniká kyselina: P 2 O 5 + H 2 O ==> 2 HPO 3 - kyselina fosforečná � Existujú však aj oxidy, ktoré s vodou nereagujú ako napríklad Si. O 2, B 2 O 3 � � 2) so zásadotvornými oxidmi; vzniká soľ: N 2 O 3 + Li 2 O ==> 2 Li. NO 2 - dusitan lítny � � 3) s hydroxidmi; vzniká soľ a voda: V 2 O 5 + Ba(OH)2 ==> Ba(VO 3)2 + H 2 O - vanadičnan bárnatý + voda

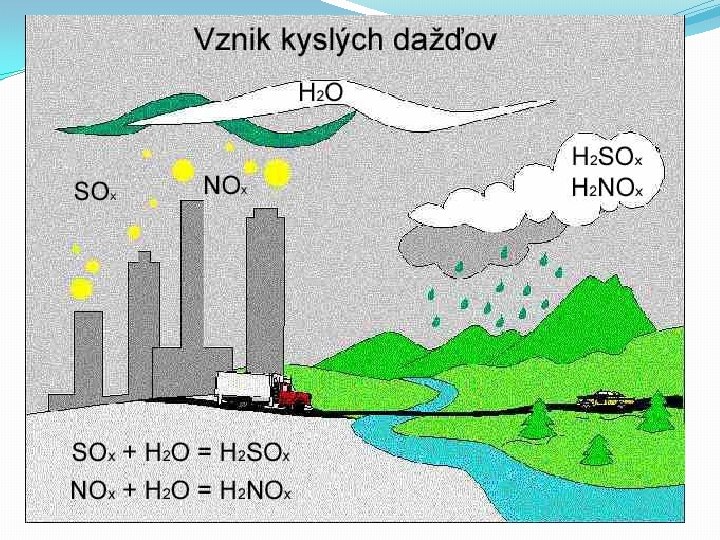
Použitie hydroxidotvorných a zásadotvorných oxidov: � � Uvedené vlastnosti oxidov sa využívajú v priemyselnej výrobe. Napríklad kyselina sírová sa vyrába reakciou oxidu sírového s vodou, reakciou oxidu vápenatého s vodou sa vyrába hydroxid vápenatý (hasené vápno). � � Reakcie niektorých kyselinotvorných oxidov s vodou majú aj škodlivý dôsledok na prírodu a životné prostredie. Napríklad oxid siričitý, ktorý vzniká pri spaľovaní uhlia s obsahom síry v tepelných elektrárňach, v priemysle, ale aj v domácnostiach, vytvára s vodnou parou vo vzduchu kyselinu siričitú. � � Oxidy dusíka z výfukových plynov áut reagujú s vodnou parou. Vznikajú tzv. kyslé dažde, ktoré škodlivo pôsobia nielen na organizmy, ale aj na stavby a priemyselné zariadenie.


Zopakuj si: �Ako vznikajú kyslé dažde? �Aké sú to kyselinotvorné oxidy? �Aké sú to hydroxidotvorné oxidy?



















