Z Beneov Jirskova 888 CHEMIE Klasifikace oxid 8

ZŠ Benešov, Jiráskova 888 CHEMIE Klasifikace oxidů – 8. ročník Mgr. Jitka Říhová
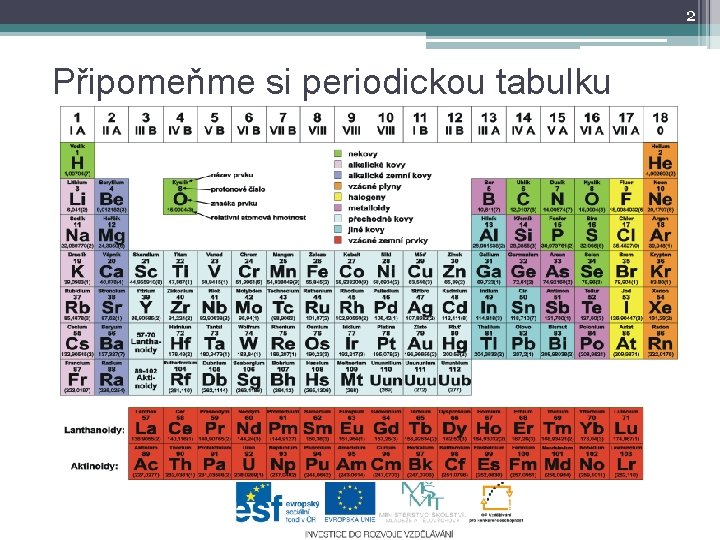
2 Připomeňme si periodickou tabulku

3 Klasifikace - třídění oxidů • Kyselinotvorné oxidy SO 2, SO 3, CO 2, NO 2, . . • Zásadotvorné oxidy Li 2 O, Ba. O, Mg. O, Fe. O • Amfoterní oxidy Zn. O, Sn. O, Pb. O, Al 2 O 3, Cr 2 O 3

4 Kyselinotvorné oxidy • Reagují s vodou za vzniku kyseliny CO 2 + H 2 O = H 2 CO 3 • Elektronegativita prvku tvořící oxid je větší než 2 (prvky v pravé části period. tabulky) - N, C, S, P • Ochotně reagují s hydroxidy, vzniká voda a sůl SO 2 + 2 Na. OH = H 2 O + Na 2 SO 3

5 Zásadotvorné oxidy • Reagují s vodou za vzniku hydroxidu K 2 O + H 2 O = 2 KOH • Elektronegativita prvku tvořící oxid je menší než 1 (většina prvků 1. a 2. skupiny v per. tabulce- K, Ca, . . ) • Ochotně reagují s kyselinami, vzniká voda a sůl Cr. O + H 2 SO 4 = Cr. SO 4 + H 2 O

6 Amfoterní oxidy • S vodou nereagují • Elektronegativita prvku tvořící oxid je mezi 1 - 2 • Reagují s hydroxidy- vzniká sůl kyseliny, která odpovídá amfoternímu oxidu + voda: Zn. O + 2 Na. OH = Na 2 Zn. O 2 + H 2 O - zinečnatan sodný + voda • Reagují s kyselinami vzniká sůl a voda: 2 Al 2 O 3 + 3 H 2 SO 4 = Al 2(SO 4)3 + 3 H 2 O - síran hlinitý + voda

7 Dokonči a uprav reakce 1. SO 3 + H 2 O = 2. Ca. O + H 2 O = 3. Zn. O + H 2 O = 4. Na 2 O + H 2 O = 5. CO 2 + KOH = 6. Li 2 O + HCl = 7. SO 2 + Sn(OH)2 = 8. K 2 O + H 2 SO 4 =

8 Správná řešení 1. SO 3 + H 2 O = H 2 SO 4 2. Ca. O + H 2 O = Ca(OH)2 3. Zn. O + H 2 O = nereaguje 4. Na 2 O + H 2 O =2 Na. OH 5. CO 2 +2 KOH = H 2 O + K 2 CO 3 6. Li 2 O + 2 HCl = H 2 O + 2 Li. Cl 7. SO 2 + Sn(OH)2 = H 2 O + Sn. SO 3 8. K 2 O + H 2 SO 4 = H 2 O + K 2 SO 4

9 Použitá literatura Učebnice základy chemie 1( Beneš, Pumpr, Banýr) http: //xantina. hyperlink. cz/odpovedi/odpov_koxidy. html http: //www. labo. cz/mft/pt. htm http: //xantina. hyperlink. cz/cvic_zoxidy. html http: //xantina. hyperlink. cz/aoxidy. html
- Slides: 9