KRSTAL KMYASI q Minerallerin zelliklerinin ou byk lde

KRİSTAL KİMYASI q Minerallerin özelliklerinin çoğu, büyük ölçüde kimya bileşimlerine bağlıdır. Bu nedenle kimyasal bileşim, minerallerde temel önem taşır q Ancak minerallerin özellikleri, kimyasal bileşimden başka, minerali meydana getiren atom ve iyonların geometrik düzenlemeleri ile bunları bir arada tutan elektriksel yüklerin tabiatına da bağlıdır q Böylece mineralleri anlamak için, bunların kimyası, bağlantı ve yapılarının da göz önüne alınması gereklidir q Bir bilim dalı olan kristal kimyasının amacı, kristalen maddenin kimyasal bileşimi, iç yapısı ve fiziksel özellikleri arasındaki ilişkileri açıklamaktır

ATOM q Atom, maddenin karakteristik element özelliklerini taşıyan en küçük parçasıdır q Çekirdek: Proton ve nötronlar Proton; + yüklü Nötron; nötr Etrafında: elektronlar Elektron; - yüklü q Nötr bir atomda, proton sayısı = elektron sayısı = atom sayısı (= Z) q Protonlar + nötronlar = karakteristik kütlesi / kütle sayısı
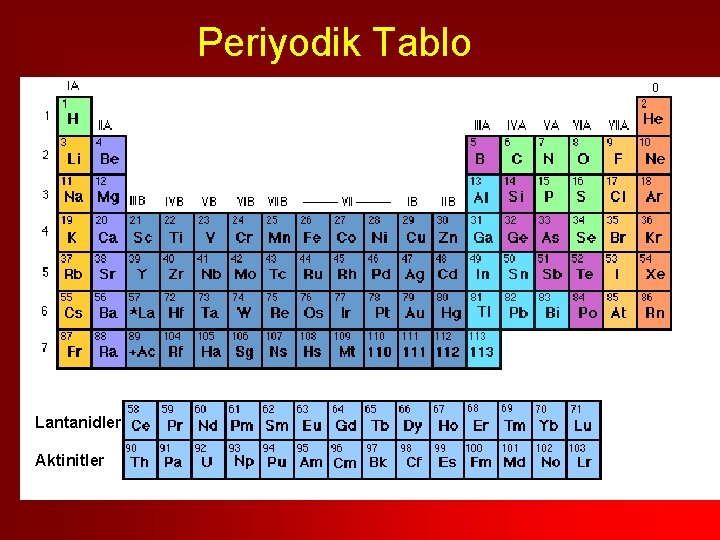
Periyodik Tablo Lantanidler Aktinitler

İYON • Elementler, elektron vermeye eğilimli olanlar ve elektron alma yeteneği olanlar olmak üzere iki gruba ayrılabilirler Metaller elektron verici Metal olmayanlar elektron alıcı • Bir atomun elektron konfigürasyonundan bir veya daha fazla elektron eksilirse katyon, eklenirse bir anyon meydana gelir X atom – e– X + katyon X atom + e– X– anyon

• Bir iyonun yarıçapı, kristalden kristale farklı olabilir Bu durum, bağ türüne ve çevreleyen atomların sayısına bağlıdır K+ 6 ‘lı koordinasyondaki 8’ lı koordinasyonda 10 ‘lu koordinasyonda yarıçapı 1. 38 Å yarıçapı 1. 51 Å yarıçapı 1. 59 Å • Çevreleyen anyonlar, merkezdeki katyonun genişlemesini ve yarıçapının büyümesine neden olurlar • Katyonların yarıçapları, aynı elementlerin metalik yarıçaplarından daima daha küçüktür • Anyonlar nötr atomlarından daha büyüktür

• Aynı sütundaki elementlerde atom sayısı büyüdükçe iyonik yarıçaplar da büyür • Aynı elektron yapılı pozitif iyonlarda ise yük arttıkça yarıçap küçülür • Farklı valans durumları gösteren bir elementin daha yüksek yüklü olan pozitif iyonunun yarıçapı daha küçüktür Mn 2+ = 0. 83 Å, Mn 3+ = 0. 65 Å, Mn 4+ = 0. 53 Å • Çok sayıdaki komşu iyonlar, merkezdeki iyonu daha fazla genişletir az sayıdaki iyonlar biraz büzülmesini sağlarlar
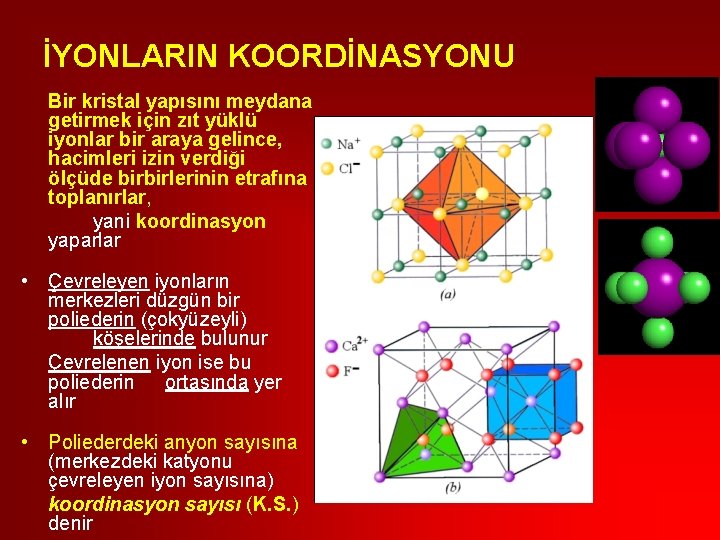
İYONLARIN KOORDİNASYONU Bir kristal yapısını meydana getirmek için zıt yüklü iyonlar bir araya gelince, hacimleri izin verdiği ölçüde birbirlerinin etrafına toplanırlar, yani koordinasyon yaparlar • Çevreleyen iyonların merkezleri düzgün bir poliederin (çokyüzeyli) köşelerinde bulunur Çevrelenen iyon ise bu poliederin ortasında yer alır • Poliederdeki anyon sayısına (merkezdeki katyonu çevreleyen iyon sayısına) koordinasyon sayısı (K. S. ) denir

Yarıçap Oranı • Bir kristal yapısında en büyük güçler, yakın konumlarda olan iyonlar arasındadır Bunlar ilk koordinasyon kabuğunu meydana getirirler • Bu kabuğun geometrik düzenlenmesi dolayısıyla koordinasyon sayısı, çevrelenen iyonun boyutuna bağlıdır • Çevreleyen ve çevrelenen iyonların birbirine göreceli boyutları yarıçap oranı ile ifade edilir Yarıçap oranı: RA : RX RA merkezdeki katyonun yarıçapı RX çevreleyen iyonun yarıçapı
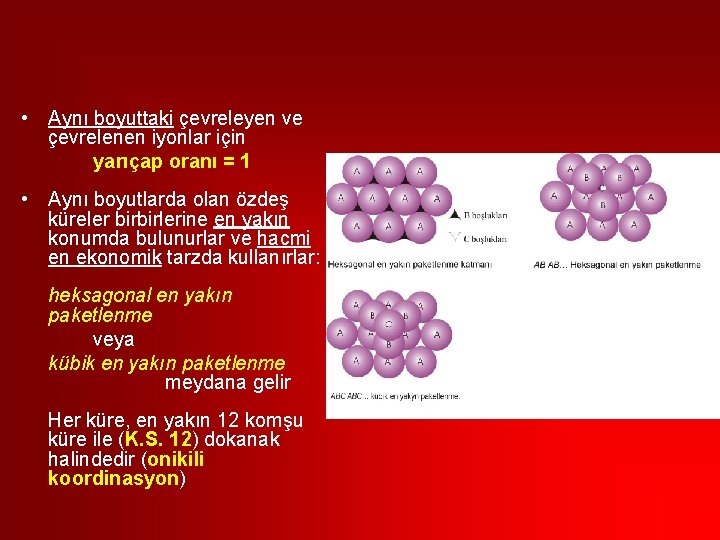
• Aynı boyuttaki çevreleyen ve çevrelenen iyonlar için yarıçap oranı = 1 • Aynı boyutlarda olan özdeş küreler birbirlerine en yakın konumda bulunurlar ve hacmi en ekonomik tarzda kullanırlar: heksagonal en yakın paketlenme veya kübik en yakın paketlenme meydana gelir Her küre, en yakın 12 komşu küre ile (K. S. 12) dokanak halindedir (onikili koordinasyon)
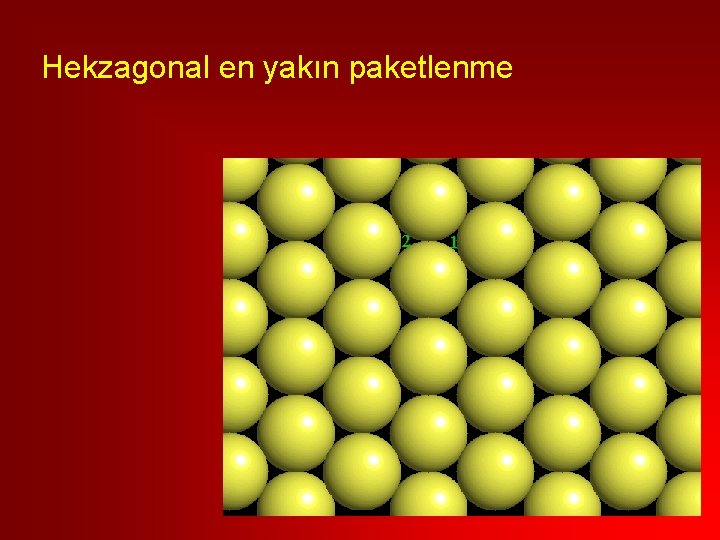
Hekzagonal en yakın paketlenme 2 1

1


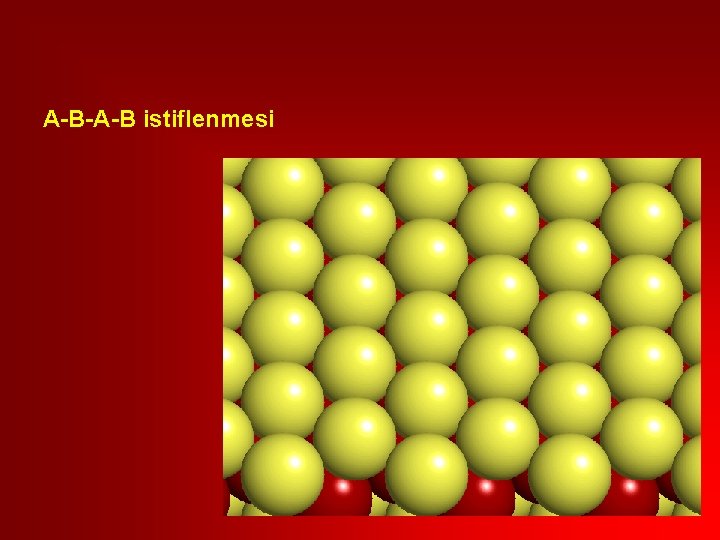
A-B-A-B istiflenmesi

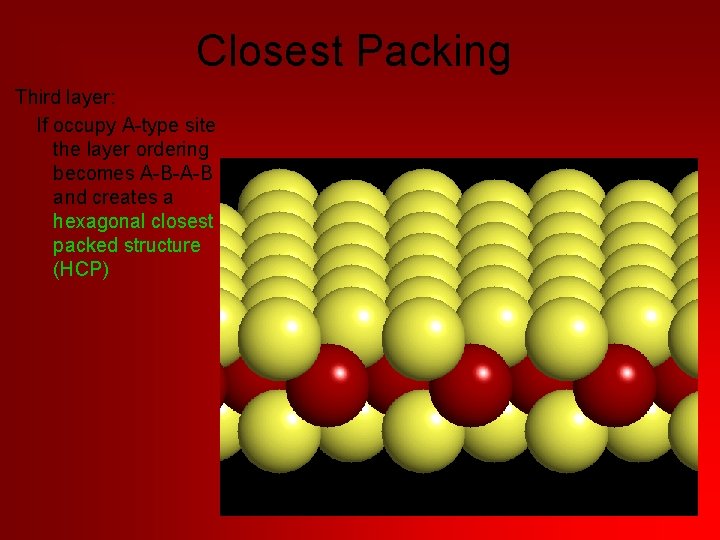
Closest Packing Third layer: If occupy A-type site the layer ordering becomes A-B-A-B and creates a hexagonal closest packed structure (HCP)

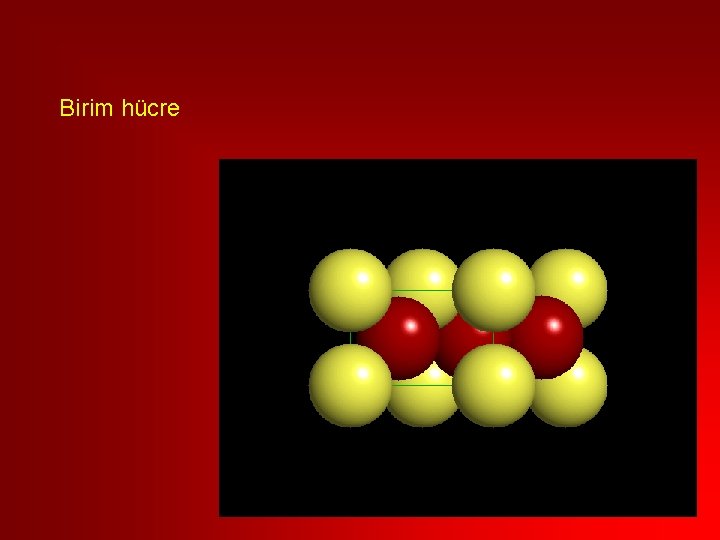
Birim hücre
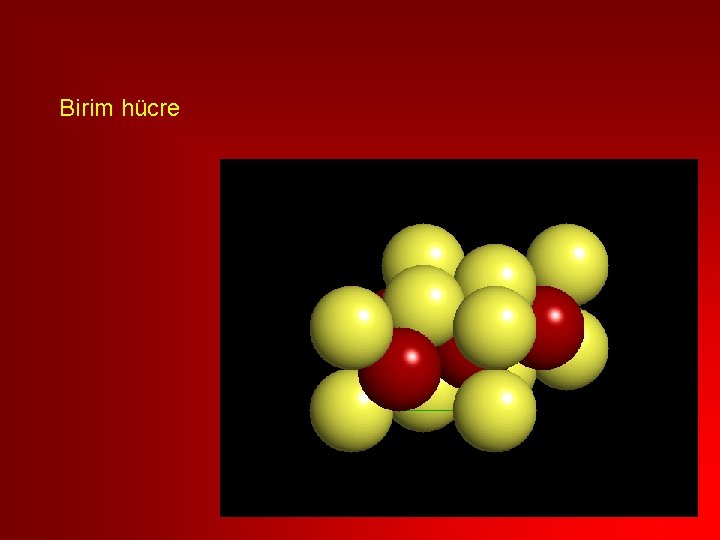
Birim hücre
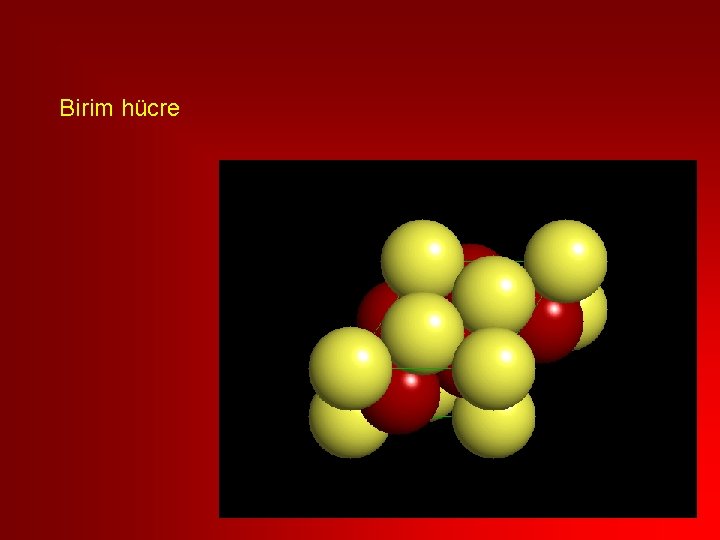
Birim hücre
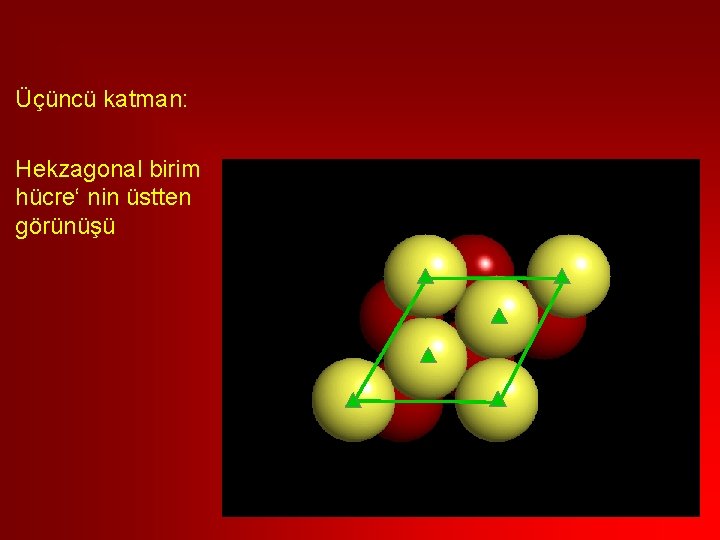
Üçüncü katman: Hekzagonal birim hücre‘ nin üstten görünüşü

Kübik en yakın paketlenme A ve B katmanlarının üzerinde c boşluklarına gelecek tarzda üçüncü bir katman yerleştirilirse





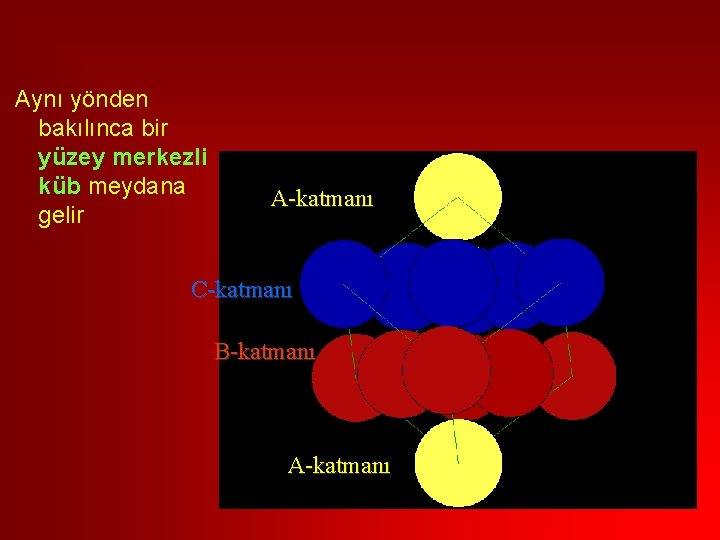
Aynı yönden bakılınca bir yüzey merkezli küb meydana gelir A-katmanı C-katmanı B-katmanı A-katmanı

Üstten görünecek tarzda döndürülürse:

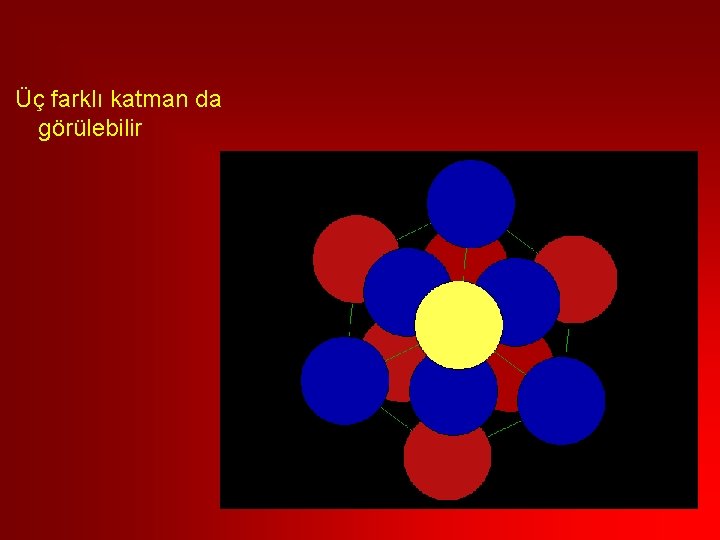
Üç farklı katman da görülebilir

Sekizli koordinasyon (kübik koordinasyon ): 1. 000 - 0. 732 yarıçap oranlarında kararlı Hacim merkezli küb






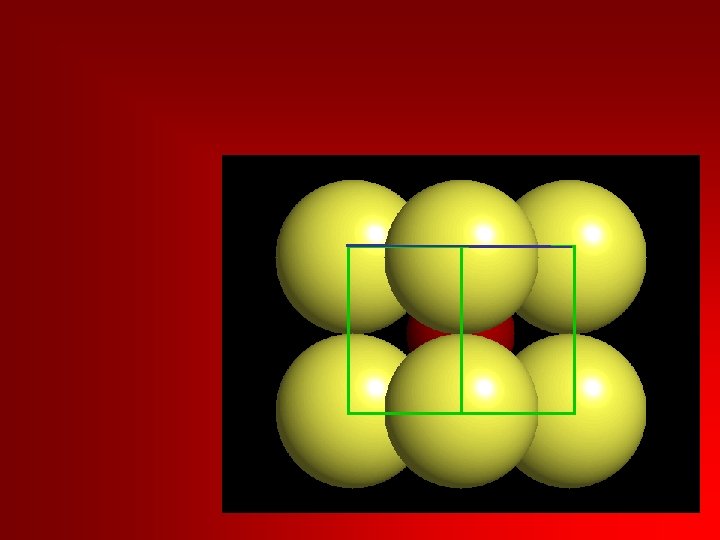

Altılı koordinasyon (oktaedral koordinasyon): 0. 732 - 0. 414 yarıçap oranları için kararlı Halit, kalsit, spinel ve bir çok silikat





Dörtlü koordinasyon (tetraedral koordinasyon): 0. 414 - 0. 225 yarıçap oranları için kararlı Si. O 4 tetraederlerinde







Üçlü koordinasyon (üçgen koordinasyon): 0. 225 - 0. 155 yarıçap oranları için kararlı CO 3, NO 3 ve BO 3 gruplarında

İkili koordinasyon (lineer koordinasyon): 0. 155 ’tan küçük yarıçap oranları için kararlı Uranil grubu (UO 2)2+, nitrit grubu (NO 2)2–, kuprit (Cu 2 O)

KRİSTALLERDE BAĞ GÜÇLERİ • Kristal yapılarında atomları, iyonları veya iyonik grupları bağlayan güçler elektriksel niteliktedir • Bu güçlerin türü ve şiddetleri, minerallerin fiziksel ve kimyasal özelliklerini büyük ölçüde denetler • Sertlik, dilinim, ergime, elektrik ve ısı iletkenliği, sıkışabilme ve ısı genleşme katsayısı doğrudan bağ güçleri ile ilgilidir

İyonik Bağ • Zıt yüklü iyonlar arasındaki çekimle iyonik (veya elektrostatik) bağ meydana gelir. Bu bağın bir metal atomunun metal olmayan bir atomla elektron değiştirmesi ile meydana gelir • İyonik bağlı kristaller: orta derecede sertlik ve özgül ağırlık gösterirler ergime noktaları oldukça yüksek, ısı ve elektriği zayıf iletirler • İyonik bağı meydana getiren elektrostatik yük iyonun üzerine yayılmıştır. Bu nedenle, bir katyon etrafında mümkün olduğu kadar çok anyon yerleşebilir Meydana gelen kristaller yüksek simetri gösterirler

İyonik bağın dayanımı: u = (A q 1 • q 2) / r Coulomb çekim gücü gibidir • Li. F bir istisnadır. Bunun sebebi yapıda yer alan çok küçük F anyonlarının birbirini itmesidir.

Kovalent Bağ • En güçlü bağ türüdür. Kovalent bağı meydana getiren elektriksel güçler, elektronların ortak olarak kullanıldığı kesimde yoğunlaşmıştır • Bağlantı yüksek derecede yönlüdür ve meydana gelen kristallerin simetri derecesi iyonik bağlantılı kristallerden daha düşüktür • Kovalent bağlantılı mineraller: Çözünmezler, büyük kararlılık ve yüksek ergime noktaları gösterirler, katı ve çözelti halindeyken elektriği iletmezler

Metalik Bağ • Metallerdeki yapısal birimler; atom çekirdekleri ile “valans olmayan” elektron yörüngeleridir Elektronların çoğunun herhangi birey çekirdekle ilgisi yoktur Bağ mekanizmasını bozmadan yapı içinde serbestçe kayarlar veya yapının dışına tamamen çıkabilirler • Elektron yörüngeleri dolu olan çekirdekler ve - elektron bulutu arasındaki çekici güçler, yapıyı bir arada tutar Buna metalik bağ denir • Metalik bağlantı nedeniyle metaller: yüksek plastiklik, dövülebilme, çekilebilme, iletkenlik ve düşük sertlik özellikleri gösterirler

van der Waals Bağı • Cl 2 gibi nötr moleküllerin bir ucunda küçük bir + yük yoğunlaşması, diğer ucuda da buna eşit miktarda + yük eksilmesi meydana gelebilir • Etkileşen atomların yörüngelerinde yer alan elektronlar, ani ve zayıf dipol çekimi meydana getirecek tarzda hareketlerini senkronize ederler. Bu zayıf dipol, komşu atomlarda da aynı etkiyi yapar ve sonuçta tüm moleküller zayıf bir dipol etkisiyle yapıda bağlanırlar • Kristal oluşurken bu moleküller negatif kutupları komşu moleküllerin pozitif kutuplarına karşı gelecek tarzda dizilirler • Nötr molekülleri ve yüksüz yapısal birimleri yüzeylerindeki zayıf kalıntı yükleriyle bir yapıda tutan zayıf bağlara van der Waals bağları denir • Bunlar en zayıf kimyasal bağlardır. Genellikle organik bileşikler ve katılaştırılmış gazlarda bulunurlar. Minerallerde seyrek olarak bulunurlar ve kolayca ayrılan dilinim ve düşük sertlikteki zonları denetlerler
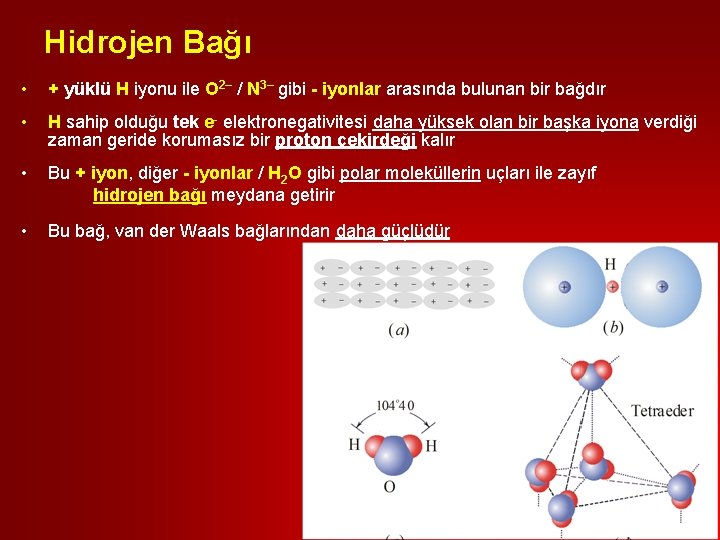
Hidrojen Bağı • + yüklü H iyonu ile O 2– / N 3– gibi - iyonlar arasında bulunan bir bağdır • H sahip olduğu tek e- elektronegativitesi daha yüksek olan bir başka iyona verdiği zaman geride korumasız bir proton çekirdeği kalır • Bu + iyon, diğer - iyonlar / H 2 O gibi polar moleküllerin uçları ile zayıf hidrojen bağı meydana getirir • Bu bağ, van der Waals bağlarından daha güçlüdür

• Olağanüstü çeşitlilik ve karmaşıklık gösteren doğal maddelerde tek tipte bağlantı seyrek olarak bulunur • Minerallerin pek çoğunda iki / daha fazla bağ tipi birlikte yer alır Bu durumda kristal, farklı bağların özelliklerini ortak olarak kullanır ve sıkça kuvvetli yönlenmiş özellikler gösterir
- Slides: 61