IDELN PLYN Pi odvozovn zkon platnch pro plyn

















- Slides: 24

IDEÁLNÍ PLYN

Při odvozování zákonů platných pro plyn je často vhodné nahradit plyn (např. kyslík, dusík) zjednodušeným modelem, který nazýváme ideální plyn.

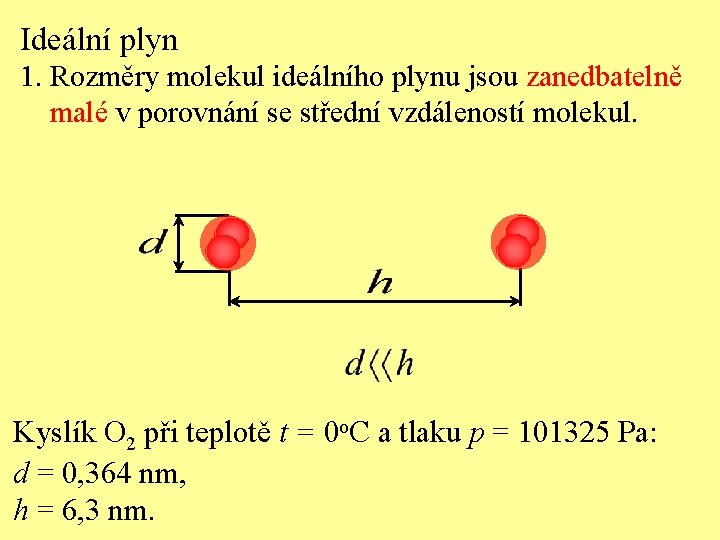
Ideální plyn 1. Rozměry molekul ideálního plynu jsou zanedbatelně malé v porovnání se střední vzdáleností molekul. Kyslík O 2 při teplotě t = 0 o. C a tlaku p = 101325 Pa: d = 0, 364 nm, h = 6, 3 nm.

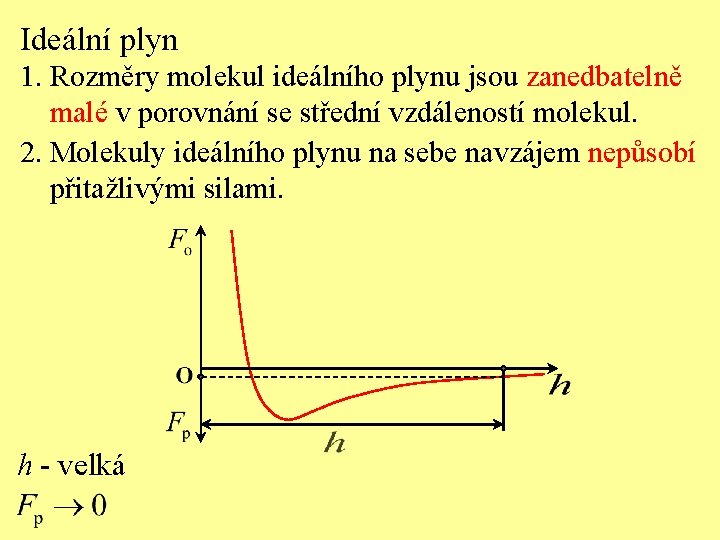
Ideální plyn 1. Rozměry molekul ideálního plynu jsou zanedbatelně malé v porovnání se střední vzdáleností molekul. 2. Molekuly ideálního plynu na sebe navzájem nepůsobí přitažlivými silami. h - velká

Ideální plyn 1. Rozměry molekul ideálního plynu jsou zanedbatelně malé v porovnání se střední vzdáleností molekul. 2. Molekuly ideálního plynu na sebe nepůsobí navzájem přitažlivými silami. 3. Vzájemné srážky molekul ideálního plynu a srážky molekul se stěnou nádoby jsou dokonale pružné. Rychlosti molekuly před nárazem a po nárazu jsou stejné.

Vnitřní energie ideálního plynu s dvouatomovými molekulami: posuvný + rotační + kmitavý Energie soustavy molekul se rovná součtu kinetických energií posuvného pohybu molekul a energie jejich rotačního a kmitavého pohybu. Potenciální energie soustavy molekul je nulová.

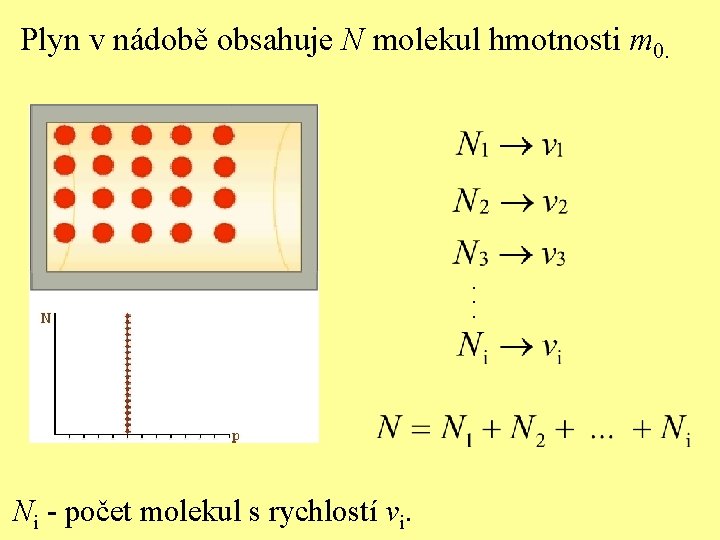
Plyn v nádobě obsahuje N molekul hmotnosti m 0. . Ni - počet molekul s rychlostí vi.

Kinetická energie molekuly s rychlostí v 1 je vyjádřená vztahem: Kinetická energie N 1 molekul s rychlostí v 1: . . .

Kinetická energie všech N molekul N - je celkový počet molekul

Kinetická energie všech N molekul Nahradíme všechny rychlosti molekul rychlostí vk. . . tak, že Ek. N se nezmění Pro rychlost molekul vk 2 platí vztah:

Střední kvadratická rychlost Druhá mocnina střední kvadratické rychlosti se rovná součtu druhých mocnin rychlostí všech molekul děleným počtem molekul. Střední kvadratická rychlost je rychlost, kterou lze nahradit rychlosti pohybu všech molekul, přičemž se celková kinetická energie molekul nezmění. (statistická veličina)

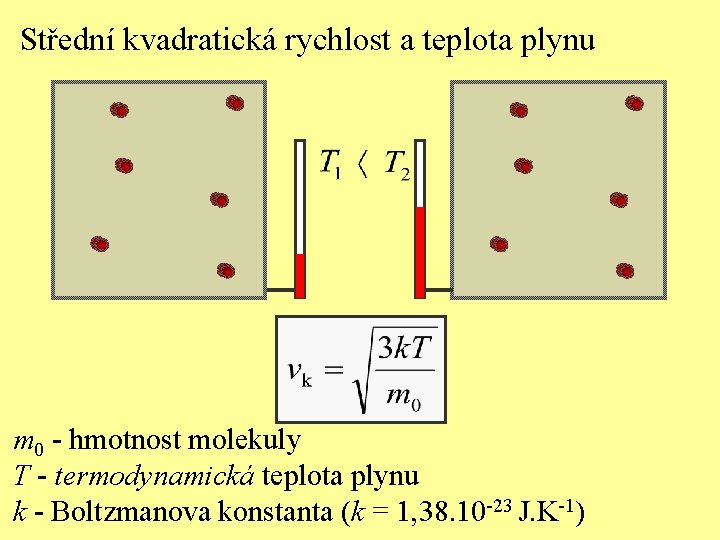
Střední kvadratická rychlost a teplota plynu m 0 - hmotnost molekuly T - termodynamická teplota plynu k - Boltzmanova konstanta (k = 1, 38. 10 -23 J. K-1)
Teoreticky dokázal vztah James Clark Maxwell (1831 - 1879), skotský fyzik

Kinetická energie molekul ideálního plynu Umocníme a násobíme m 0 Molekuly ideálního plynu mají v důsledku neuspořádaného pohybu střední kinetickou energii, která je přímo úměrná termodynamické teplotě plynu.

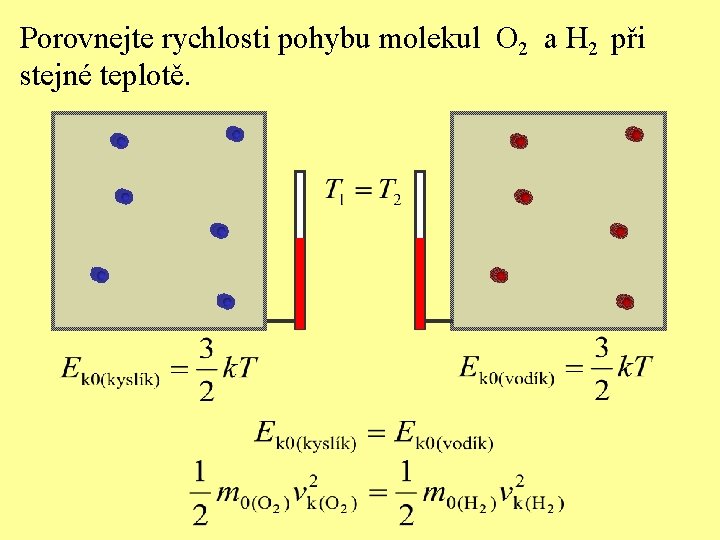
Porovnejte rychlosti pohybu molekul O 2 a H 2 při stejné teplotě.

Řešte úlohu: Vypočítejte střední kvadratickou rychlost molekul kyslíku při teplotách -100 o. C; 100 o. C. vk= 367 m. s-1, 461 m. s-1, 539 m. s-1

Řešte úlohu: Vzorek argonu s hmotností 100 g má teplotu 20 o. C. Vypočítejte celkovou kinetickou energii všech jeho molekul při neuspořádaném posuvném pohybu. Ek= 9, 1. 103 J

Test Pro ideální plyn platí: a) Rozměry molekul jsou porovnatelné se střední vzájemnou vzdáleností molekul. b) Molekuly ideálního plynu na sebe navzájem působí přitažlivými silami. c) Srážky molekul ideálního plynu jsou dokonale pružné. d) Molekuly ideálního plynu na sebe navzájem působí odpudivými silami. 1

Test Vnitřní energie ideálního plynu zahrnuje: a) energii vyplývající z posuvného pohybu molekul, b) energii vyplývající ze vzájemného pohybu molekul, c) energii vyplývající z rotačního pohybu molekul, d) energii vyplývající z kmitavého pohybu molekul. 2

Test Střední kvadratická rychlost pohybu molekul je rychlost, kterou nahradíme-li všechny rychlosti pohybu molekul: a) jejich kinetická energie se nezmění, b) jejich potenciální energie se nezmění, c) celková kinetická energie plynu se nezmění, d) celková kinetická energie plynu se změní. 3

Test Vztah mezi střední kvadratickou rychlostí vk pohybu molekul ideálního plynu a jeho termodynamickou teplotou T je vyjádřen rovnicí: 4

Test Molekuly ideálního plynu mají v důsledku neuspořádaného pohybu střední kinetickou energii, která je: a) přímo úměrná jeho celsiově teplotě, b) nepřímo úměrná jeho termodynamické teplotě, c) přímo úměrná jeho termodynamické teplotě, d) nepřímo úměrná jeho celsiově teplotě. 5

Test Vztah mezi střední kinetickou energii Ek 0 molekuly ideálního plynu a jeho termodynamickou teplotou T je vyjádřen veličinovou rovnicí: 6

Test Je-li teplota dvou ideálních plynů stejná, pak pro velikost rychlosti pohybu jejich molekul platí: a) je stejná, b) molekuly s větší hmotností se pohybují s větší rychlostí, c) molekuly s větší hmotností se pohybují s menší rychlostí, d) molekuly s menší hmotností se pohybují s větší rychlostí. 7