Hoofdstuk 15 Paragraaf 4 Reactiesnelheid De snelheid van


![Voor de reactie: I 3⁻(aq) geldt: s =. . . k. [I 3⁻] I Voor de reactie: I 3⁻(aq) geldt: s =. . . k. [I 3⁻] I](https://slidetodoc.com/presentation_image_h/08549fb8517acb3e6a3266936bbc4114/image-3.jpg)








- Slides: 16

Hoofdstuk 15 Paragraaf 4 Reactiesnelheid

De snelheid van een reactie is o. a. afhankelijk van de concentratie(s). . . . . van de beginstof(fen) De reactiesnelheid (s) is het aantal mol van een stof dat per seconde. . . reactieruimte. . . en per liter verdwijnt of ontstaat De eenheid van de reactiesnelheid is mol. . . . L⁻ 1 s⁻ 1 In een reactiesnelheids. . . vergelijking komen alleen. . stof(fen) voor de concentratie(s) van de begin
![Voor de reactie I 3aq geldt s k I 3 I Voor de reactie: I 3⁻(aq) geldt: s =. . . k. [I 3⁻] I](https://slidetodoc.com/presentation_image_h/08549fb8517acb3e6a3266936bbc4114/image-3.jpg)
Voor de reactie: I 3⁻(aq) geldt: s =. . . k. [I 3⁻] I 2(aq) + I⁻(aq) waarin s de reactiesnelheid en k de reactiesnelheidsconstante is Voor de reactie: H 2(g) + Cl 2(g) 2 HCl(g) geldt: s = k. . . . . [H 2]. [Cl 2] Voor de reactie: 2 HBr(g) geldt: s =. . . k. [HBr]2 H 2(g) + Br 2(g)

Veel reacties verlopen niet in één stap Het reactiemechanisme. . . . van een reactie geeft het verloop van de elkaar opvolgende reacties weer De langzaamste. . . . stap bepaalt dan de reactiesnelheid van de totale reactie

Voor de reactie: (CH 3)3 C-Cl + OH⁻ (CH 3)3 C-OH + Cl⁻ Zou je verwachten: s = k. . . . . [ (CH 3)3 C-Cl ]. [OH⁻] Uit metingen blijkt echter: s =. . . k. [ (CH 3)3 C-Cl ] Deze reactie verloopt in twee stappen: + + Cl⁻ Stap 1: (CH 3)3 C-Cl (CH. . . . . ) C 3 3 + + OH⁻ ) C. . . . . Stap 2: (CH 3 3 (CH 3)3 C-OH . . Stap 1 is de langzaamste stap Vandaar dat: s =. . . k. [ (CH 3)3 C-Cl ]

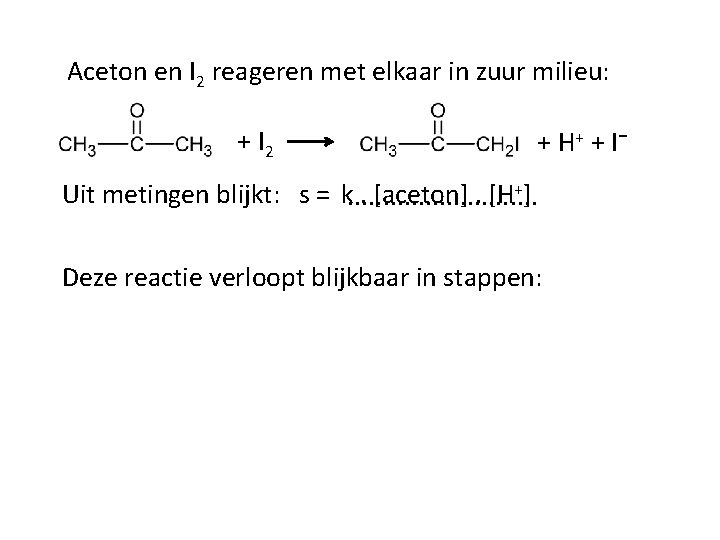
Aceton en I 2 reageren met elkaar in zuur milieu: + I 2 + H+ + I⁻ . [aceton]. [H+] Uit metingen blijkt: s = k. . . . Deze reactie verloopt blijkbaar in stappen:

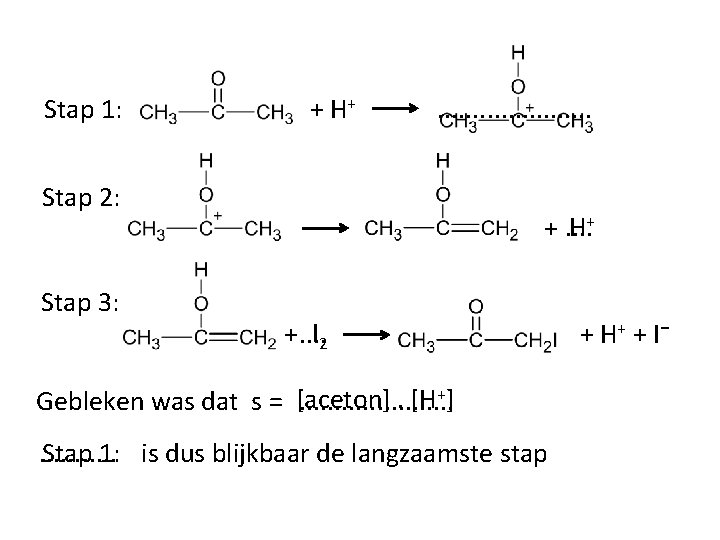
Stap 1: + H+ . . Stap 2: Stap 3: H+ +. . I 2 +. . . [H+]. . . . . Gebleken was dat s = [aceton] Stap 1: is dus blijkbaar de langzaamste stap. . . + H+ + I⁻

Reactiesnelheid en evenwicht In de chemische industrie werkt men vaak met evenwichtsreacties. Het rendement is daardoor relatief. . . . laag Als voorbeeld nemen we de productie van ammoniak (NH 3) uit. . N 2 en. . H 2 N. . . 2(g) + 3 H 2(g) 2 NH 3(g) ΔE = -. . . . a k. J. . .

N 2(g) + 3 H 2(g) 2 NH 3(g) ΔE = - a k. J Bij de productie van ammoniak werkt men met: 1. Een hoge druk 2. Een hoge temperatuur Welke voor- en nadelen hebben een hoge druk? Welke voor- en nadelen hebben een hoge temperatuur?

N 2(g) + 3 H 2(g) 2 NH 3(g) ΔE = - a k. J Voordelen hoge druk: ● Reactiesnelheid is. . . . hoger ● Insteltijd van het evenwicht is. . korter ● Rendement is hoger. . (evenwicht verschuift naar. . rechts ) Nadelen hoge druk: ● Risico bij. . . . . calamiteiten ● Hoge investerings. . . . . kosten ● Kost veel energie. . .

N 2(g) + 3 H 2(g) 2 NH 3(g) ΔE = - a k. J Voordelen hoge temperatuur: . . . . ● Reactiesnelheid is hoger ● Insteltijd van het evenwicht is. . korter Nadelen hoge temperatuur: energie ● Kost veel. . . ● Rendement is lager. . (evenwicht verschuift naar de. . . . . endotherme kant)

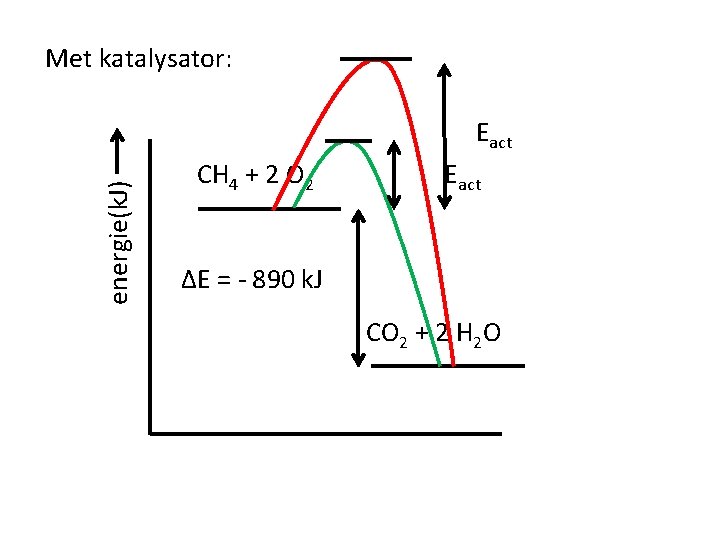
Wat doet een katalysator? Een katalysator …………… verlaagt de activeringsenergie

Met katalysator: energie(k. J) Eact CH 4 + 2 O 2 Eact ΔE = - 890 k. J CO 2 + 2 H 2 O

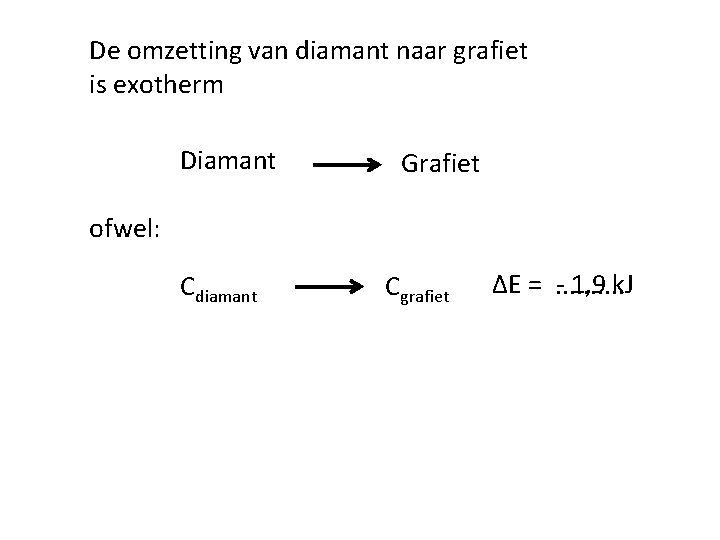
De omzetting van diamant naar grafiet is exotherm Diamant Grafiet ofwel: Cdiamant Cgrafiet ΔE =. . - 1, 9 k. J

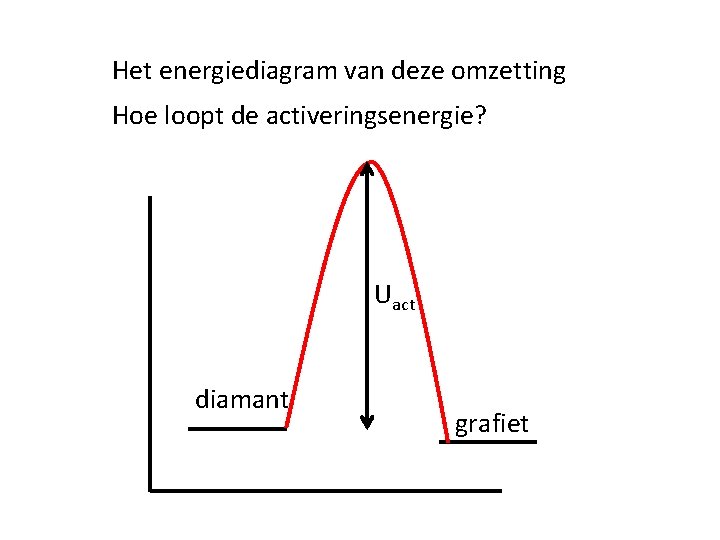
Het energiediagram van deze omzetting Hoe loopt de activeringsenergie? Uact diamant grafiet

Hoe hoger de activeringsenergie, des te ……. . lager de reactiesnelheid is