Genetyka guza chromochonnego Zoliwy guz chromochonny Mariola PCZKOWSKA



![Ostre rozwarstwienie aorty Obrzęk płuc [Azizi et al. , 1994] [Wark et al. , Ostre rozwarstwienie aorty Obrzęk płuc [Azizi et al. , 1994] [Wark et al. ,](https://slidetodoc.com/presentation_image/4a4b31a1d11dacd5fb9864972f2219f7/image-6.jpg)





![Pozytronowa Tomografia Emisyjna (PET) [18 F]DA, [18 F]DOPA Wysoka przydatność Guzy pozanadnerczowe i przerzuty Pozytronowa Tomografia Emisyjna (PET) [18 F]DA, [18 F]DOPA Wysoka przydatność Guzy pozanadnerczowe i przerzuty](https://slidetodoc.com/presentation_image/4a4b31a1d11dacd5fb9864972f2219f7/image-15.jpg)












































- Slides: 94

Genetyka guza chromochłonnego Złośliwy guz chromochłonny Mariola PĘCZKOWSKA

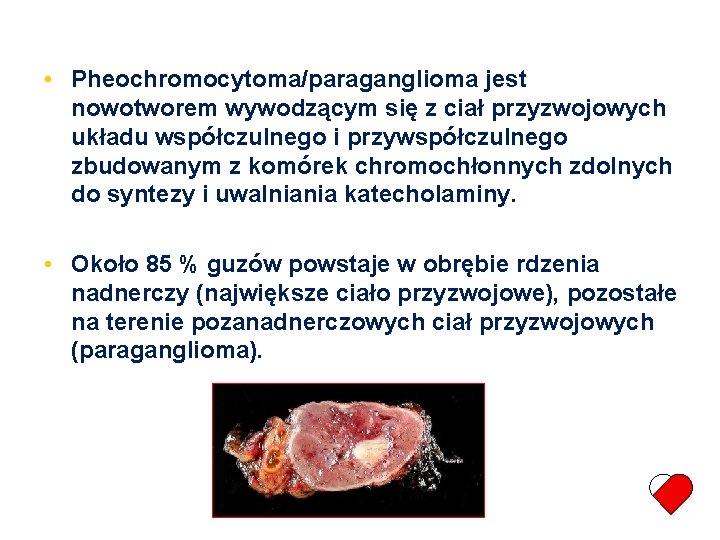
• Pheochromocytoma/paraganglioma jest nowotworem wywodzącym się z ciał przyzwojowych układu współczulnego i przywspółczulnego zbudowanym z komórek chromochłonnych zdolnych do syntezy i uwalniania katecholaminy. • Około 85 % guzów powstaje w obrębie rdzenia nadnerczy (największe ciało przyzwojowe), pozostałe na terenie pozanadnerczowych ciał przyzwojowych (paraganglioma).

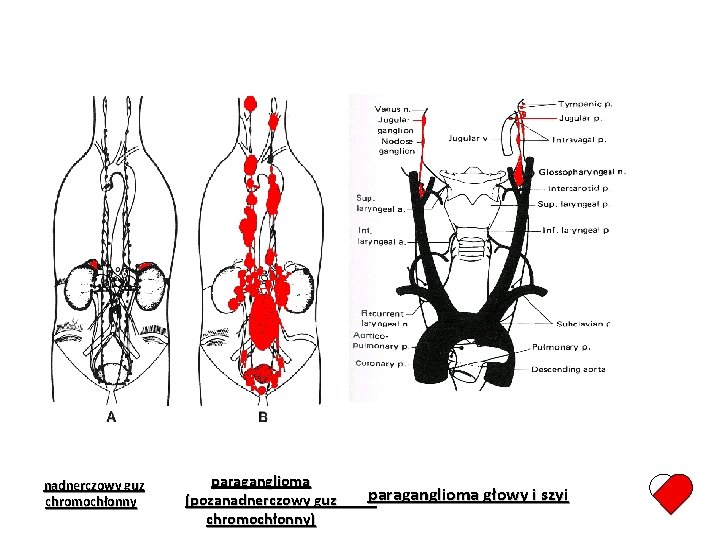
nadnerczowy guz chromochłonny paraganglioma (pozanadnerczowy guz chromochłonny) paraganglioma głowy i szyi

Guz chromochłonny Manger , Gifford Clin Exp Pheochromocytoma , 1996 Zasłużona nazwa ‘ great mimic ‘ Bardzo duża różnorodność objawów [ > 70 ! ] Nadmiar katecholamin i/lub nadciśnienie tętnicze Bóle głowy, pocenie się, kołatanie serca, niepokój, ból w klatce piersiowej, bóle brzucha, utrata masy ciała, zaparcia, inne Powikłania Układ sercowo-naczyniowy Współistniejące choroby / zespoły Rak rdzeniasty tarczycy Nerwiakowłókniakowatość Choroba von Hippel Lindau Inne Ucisk / naciekanie struktur przylegających

Częstość występowania objawów Doświadczenie wielu ośrodków Utrwalone nadciśnienie tętnicze 80 – 92 % Napadowe nadciśnienie 56 – 60 % Bóle głowy 43 – 82 % Nadmierne pocenie się 37 – 89 % Uczucie kołatania serca 44 – 84 % Januszewicz W i wsp. , 2002
![Ostre rozwarstwienie aorty Obrzęk płuc Azizi et al 1994 Wark et al Ostre rozwarstwienie aorty Obrzęk płuc [Azizi et al. , 1994] [Wark et al. ,](https://slidetodoc.com/presentation_image/4a4b31a1d11dacd5fb9864972f2219f7/image-6.jpg)
Ostre rozwarstwienie aorty Obrzęk płuc [Azizi et al. , 1994] [Wark et al. , 1978] Wstrząs kardiogenny Zatrzymanie akcji serca [Grasselli et al. , 2008] [Paschalis-Purtak et al. , 2004] Niewydolność serca [Col et al. , 1999] OBJAWY ZE STRONY UKŁADU S-N MOGĄ BYĆ PIERWSZYMI OBJAWAMI PHEO Klasyczna / odwrócona kardiomiopatia takotsubo [various] - WYNIKAJĄ Z NADMIARU KATECHOLAMIN Zapalenie mięśnia serca Kardiomiopatia [Mootha et al. , 2000] [Baratella et al. , 1998] Zawał serca Nawracające komorowe zaburzenia rytmu serca [Mc. Neill et al. , 1992] Rzucawka torsades de Pointes [Hudsmith et al. , 2006] [Methe et al. , 2007]

Kiedy należy podejrzewać pheo w praktyce ? Nadciśnienie z dużą zmiennością wartości RR Na przemian występujące – zwyżki RR i hipotensja Hipotonia ortostatyczna i / lub tachykardia po pionizacji Paradoksalna reakcja na leki hipotensyjne / wprowadzenie do znieczulenia ogólnego Zmienność rytmu serca Tachykardia / zab. rytmu serca Retinopatia nadciśnieniowa [III-IV] / encefalopatia Manger, Gifford. Clinical and Experimental Pheochromocytoma, Blackwell Science , Second edition , 1996

Przypadek

53 -letni mężczyzna z pogorszeniem kontroli NT 53 -letni mężczyzna 2 -letni wywiad NT Od tygodnia pogorszenie kontroli NT z napadowymi zwyżkami RR, bóle głowy Zieleń P, Klisiewicz A, Januszewicz A i wsp. J Hum Hypertens 2010

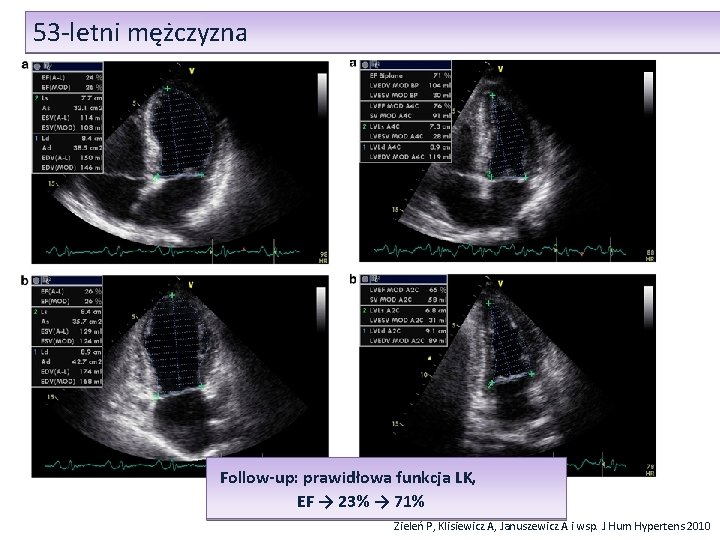
53 -letni mężczyzna Przy przyjęciu: - Ból w klatce piersiowej, RR 180/100 mm. Hg EKG - ↑ST – II, III, a. VF ↑Troponina I Koronarografia – prawidłowa Echokardiografia „DYŻUR” – akineza koniuszka i segmentów środkowych, hiperkineza segmentów podstawnych z EF - 23% TYPOWY OBRAZ KARDIOMIOPATII TAKO-TSUBO Zieleń P, Klisiewicz A, Januszewicz A i wsp. J Hum Hypertens 2010

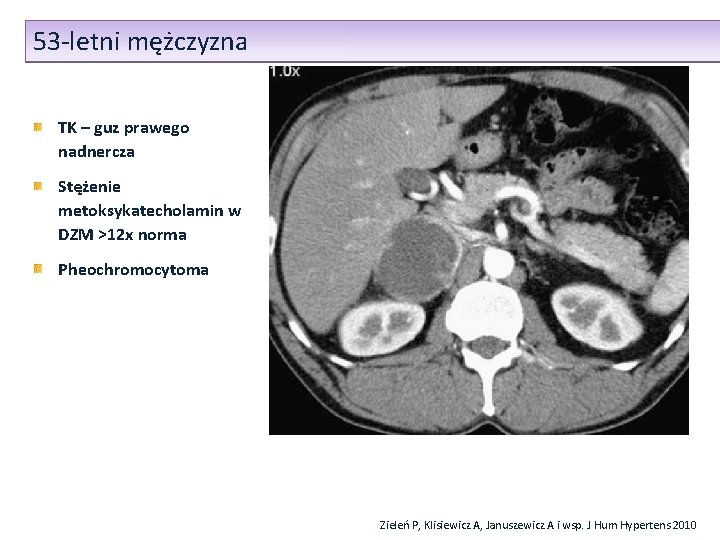
53 -letni mężczyzna TK – guz prawego nadnercza Stężenie metoksykatecholamin w DZM >12 x norma Pheochromocytoma Zieleń P, Klisiewicz A, Januszewicz A i wsp. J Hum Hypertens 2010

53 -letni mężczyzna Follow-up: prawidłowa funkcja LK, EF → 23% → 71% Zieleń P, Klisiewicz A, Januszewicz A i wsp. J Hum Hypertens 2010

Postępowanie z chorym z guzem chromochłonnym – Zalecenia PTNT 2006 Diagnostyka biochemiczna Najbardziej przydatna metoda: Oznaczanie frakcjonowanych metoksykatecholamin w osoczu i/lub moczu Najbardziej miarodajna: Oznaczanie metoksykatecholamin w moczu Niższa czułość i specyficzność: Oznaczanie katecholamin w moczu Oznaczanie kwasu wanilinomigdałowego - mniejsza wartość diagnostyczna

Pheochromocytoma Rezonans magnetyczny (MRI) Pozytronowa tomografia emisyjna (PET) 18 F-DOPA 18 F-Dopamina Tomografia komputerowa (CT) Scyntygrafia MIGB (131 I; 123 I) Scyntygrafia receptorowa Analog somatostatyny (Ind, Technet)
![Pozytronowa Tomografia Emisyjna PET 18 FDA 18 FDOPA Wysoka przydatność Guzy pozanadnerczowe i przerzuty Pozytronowa Tomografia Emisyjna (PET) [18 F]DA, [18 F]DOPA Wysoka przydatność Guzy pozanadnerczowe i przerzuty](https://slidetodoc.com/presentation_image/4a4b31a1d11dacd5fb9864972f2219f7/image-15.jpg)
Pozytronowa Tomografia Emisyjna (PET) [18 F]DA, [18 F]DOPA Wysoka przydatność Guzy pozanadnerczowe i przerzuty Małe guzy, guzy uwarunkowane genetycznie Bardzo ograniczona dostępność Koszt badania

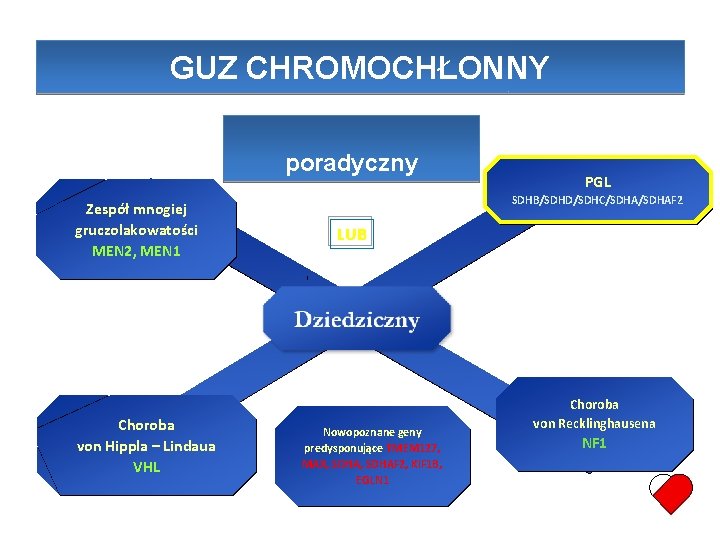
GUZ CHROMOCHŁONNY S poradyczny Zespół mnogiej gruczolakowatości MEN 2, MEN 1 Choroba von Hippla – Lindaua VHL PGL SDHB/SDHD/SDHC/SDHAF 2 LUB Nowopoznane geny predysponujące TMEM 127, MAX, SDHAF 2, KIF 1 B, EGLN 1 Choroba von Recklinghausena NF 1

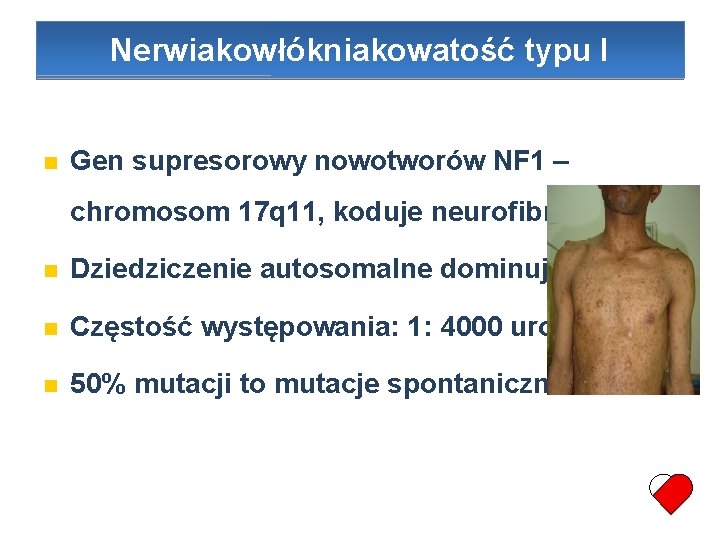
Nerwiakowłókniakowatość typu I Gen supresorowy nowotworów NF 1 – chromosom 17 q 11, koduje neurofibrominę Dziedziczenie autosomalne dominujące Częstość występowania: 1: 4000 urodzeń 50% mutacji to mutacje spontaniczne

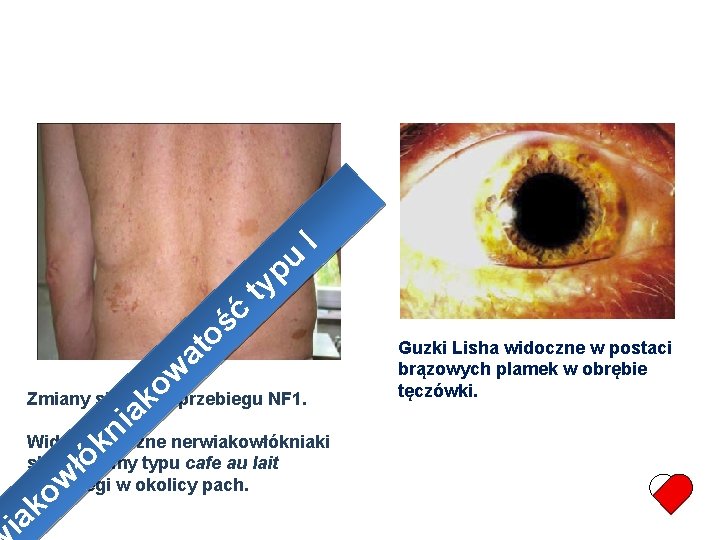
• Kryteria rozpoznania wg NIH (obecność dwóch objawów) I 6 lub więcej plam typu café au lait u p 2 lub więcej nerwiakowłókniaków jakiegokolwiek typu lub jeden ty ć splotowaty ś opach lub pachwin t Piegi w okolicy a w ocznego Glejak nerwu o k a i więcej guzków Lischa (hamartoma tęczówki) Dwa lub n k Zmiany łó w układzie kostnym w o k ia

u p y I t ć ś o t a w o Zmiany skórnekw przebiegu NF 1. a i nliczne nerwiakowłókniaki Widoczne k ó typu cafe au lait skóry, łplamy orazw piegi w okolicy pach. o k ia Guzki Lisha widoczne w postaci brązowych plamek w obrębie tęczówki.

Guz chromochłonny w NF 1 • Częstość występowania – ok. 5%. • Wiek w chwili rozpoznania pheo – podobny jak w przypadkach sporadycznych – najczęściej 4 -5 dekada życia • Częściej niż w przypadkach sporadycznych – obustronny (ok. 20%) • Częściej niż w przypadkach sporadycznych - złośliwy (ok. 10)

70 chorych z NF 1 Liczba nowotworów w latach 1978 -1989 w porównaniu do populacji ogólnej Złosliwe nowotwory występują częściej niż w populacji ogólnej Zöller MET et al. Cancer 1997; 79: 2125– 31.

Nerwiakowłókniakowatość typu I • Nowotwory towarzyszące NF 1: Pheochromocytoma – 5 - 20% Złośliwe guzy z osłonek nerwów obwodowych (malignant peripheral nerve sheath tumor) Nowotwory układu pokarmowego – najczęściej guzy neuroendokrynne Guzy mózgu – glejaki, gwiaździaki, oponiaki Białaczka Zespoły mielodysplastyczne

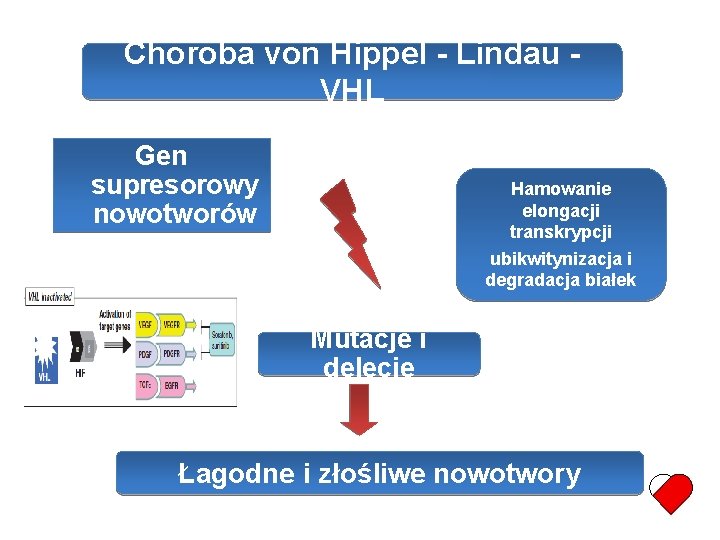
Choroba von Hippel - Lindau VHL Gen supresorowy nowotworów Hamowanie elongacji transkrypcji ubikwitynizacja i degradacja białek Mutacje i delecje Łagodne i złośliwe nowotwory

Choroba von Hippel - Lindau - VHL Gen supresorowy nowotworów VHL – chromosom 3 p 25. 3, koduje białko VHL Dziedziczenie autosomalne dominujące Częstość występowania: 1: 36. 000 urodzeń

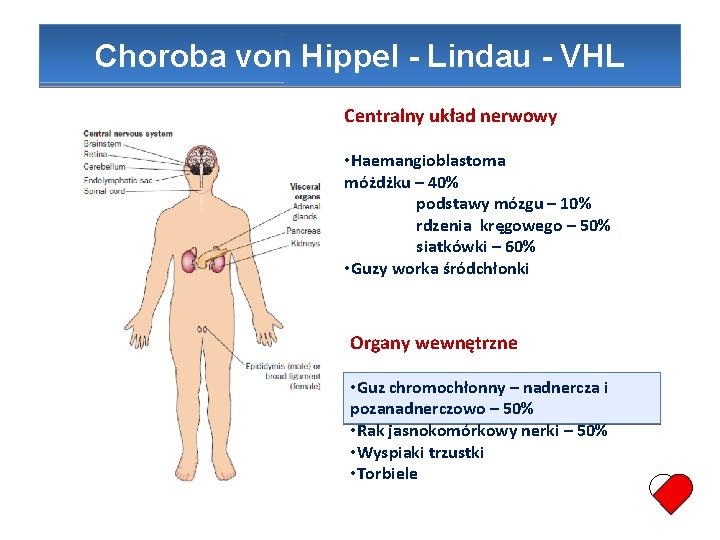
Choroba von Hippel - Lindau - VHL Centralny układ nerwowy • Haemangioblastoma móżdżku – 40% podstawy mózgu – 10% rdzenia kręgowego – 50% siatkówki – 60% • Guzy worka śródchłonki Organy wewnętrzne • Guz chromochłonny – nadnercza i pozanadnerczowo – 50% • Rak jasnokomórkowy nerki – 50% • Wyspiaki trzustki • Torbiele

Guz chromochłonny w chorobie VHL Guz chromochłonny w VHL • Wiek w chwili rozpoznania – 1 -2 dekada życia (średni wiek – 29 lat) • Najczęściej w nadnerczach, często obustronnie (ok. 40%) • W ok. 40% przypadków wieloogniskowy i pozanadnerczowy • Najczęściej są to guzy łagodne

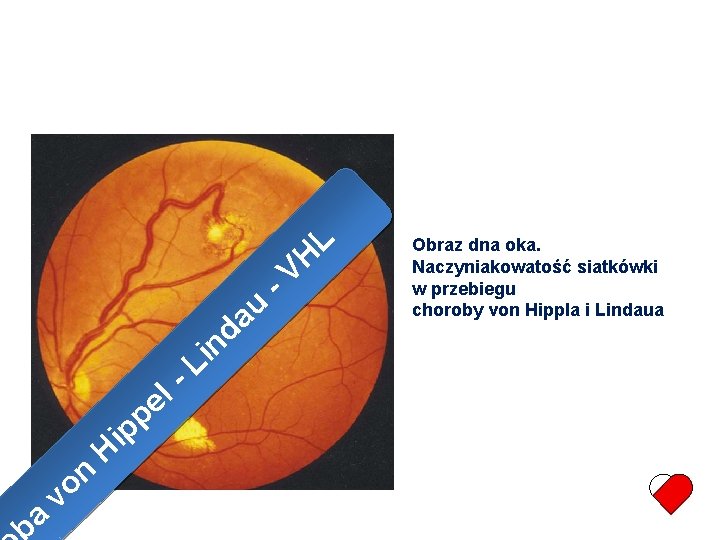
L L H H VV e i u b a o r d no i h - c. L w l e y n p i o ł H h ocn mv o ra Obraz dna oka. Naczyniakowatość siatkówki w przebiegu choroby von Hippla i Lindaua

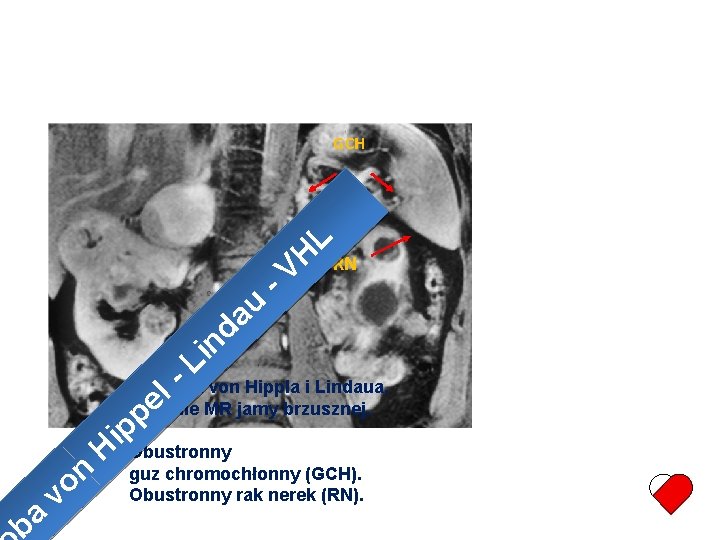
GCH L u a d l e - H V RN n i L Choroba von Hippla i Lindaua. Badanie MR jamy brzusznej. ba v on H p p i Obustronny guz chromochłonny (GCH). Obustronny rak nerek (RN).

Zespół gruczolakowatości wydzielniczej typu 2 Protoonkogen RET – chromosom 10 q 11. 21 Mutacje aktywujące funkcję produktu białkowego Dziedziczenie autosomalnie dominujące Produkt genu: kinaza tyrozynowa – receptor błony komórkowej

Zespół gruczolakowatości wydzielniczej typu 2 MEN 2 A, MEN 2 B, FMTC – rodzinny rak rdzeniasty tarczy Dziedziczenie autosomalne dominujące Częstość występowania: 1: 40. 000 urodzeń

Zespół gruczolakowatości wydzielniczej typu 2 • Cechy kliniczne Rak rdzeniasty tarczycy – 100% Guz chromochłonny – powyżej 50% Nadczynność przytarczyc (tylko MEN 2 A) – 15 – 30% W przypadku MEN 2 B charakterystyczne cechy fenotypowe

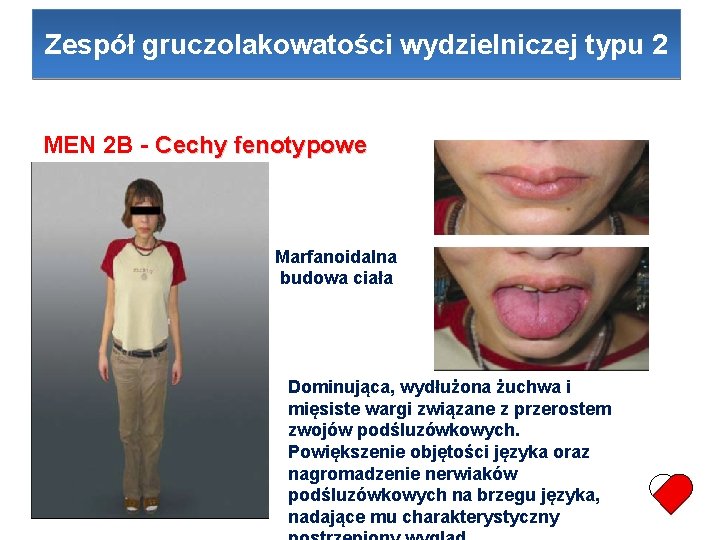
Zespół gruczolakowatości wydzielniczej typu 2 MEN 2 B - Cechy fenotypowe Marfanoidalna budowa ciała Dominująca, wydłużona żuchwa i mięsiste wargi związane z przerostem zwojów podśluzówkowych. Powiększenie objętości języka oraz nagromadzenie nerwiaków podśluzówkowych na brzegu języka, nadające mu charakterystyczny

Zespół gruczolakowatości wydzielniczej typu 2 • 1. 2. 3. Ścisła korelacja fenotyp/genotyp ! FMTC: kodon: 609, 768, 790, 791, 804, 891 MEN 2 A: kodon: 611, 618, 620, 634 choroba Hirschprunga: kodon 609, 611, 618, 620 – exon 10 liszaj skórny amyloidowy: kodon 634 nadczynność przytarczyc: głównie kodon 634 pheochromocytoma: głównie kodon 634 MEN 2 B: kodon: 883, 918 (90% wszystkich przypadków MEN 2 B), 922

Zespół paraganglioma - pheochromocytoma Mutacje genów kodujących podjednostki dehydrogenazy bursztynianowej: geny SDHA, SDHAF 2, SDHB, SDHC, SDHD. Geny supresorowe nowotworów Dziedziczenie autosomalne dominujące SDHD – imprinting matczyny – aktywna choroba dziedziczy się od ojca.

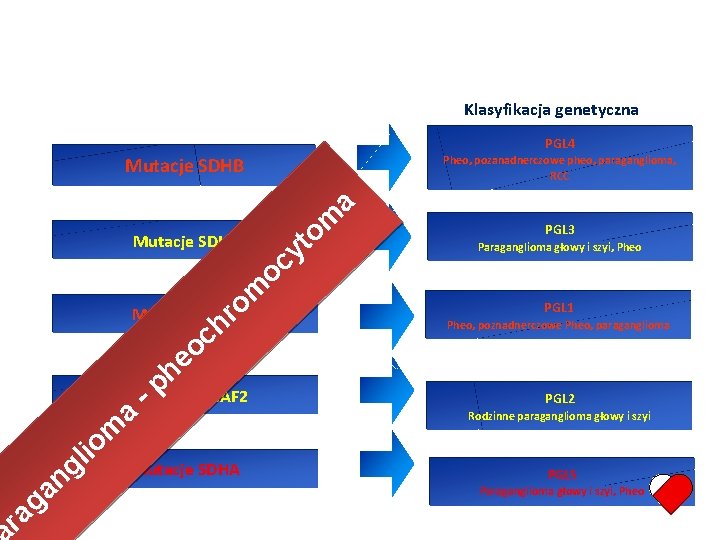
Klasyfikacja genetyczna PGL 4 Pheo, pozanadnerczowe pheo, paraganglioma, RCC Mutacje SDHB a om Mutacje SDHC o om hr Mutacje SDHD c o e i l g n a g ra h p Mutacje - SDHAF 2 a om Mutacje SDHA t y c PGL 3 Paraganglioma głowy i szyi, Pheo PGL 1 Pheo, poznadnerczowe Pheo, paraganglioma PGL 2 Rodzinne paraganglioma głowy i szyi PGL 5 Paraganglioma głowy i szyi, Pheo

• 8% - 12% sporadycznych pheochromocytoma – mutacja genów SDH – a. N Engl J Med. , 2002, JAMA 2004 m o t y c o genów SDH – niepełna – • Penetracja mutacji m o r mutacji może nie mieć objawów część nosicieli h c o chorobyhe p • Ekspresja – bardzo zróżnicowana – u części a m o chorych obserwuje się pojedyncze zmiany, inni i l g n rozwijają mnogie guzy na wielu poziomach. a g a r

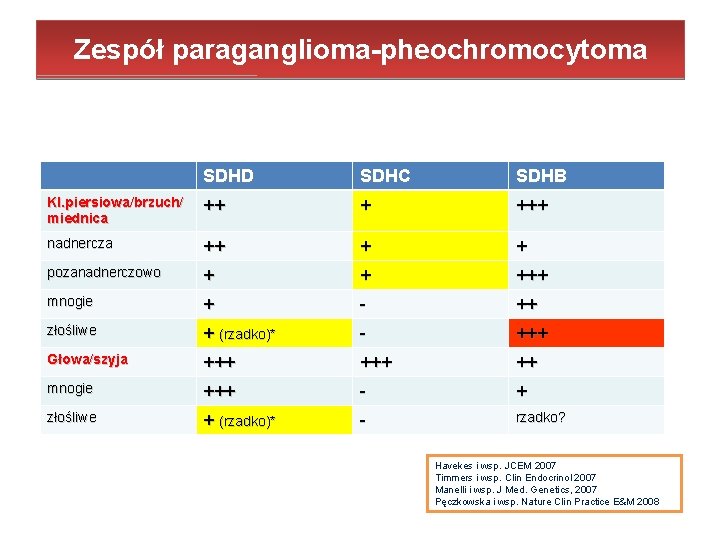
Zespół paraganglioma-pheochromocytoma SDHD SDHC SDHB Kl. piersiowa/brzuch/ miednica ++ + +++ nadnercza ++ + + pozanadnerczowo + + +++ mnogie + - ++ złośliwe + (rzadko)* - +++ Głowa/szyja +++ ++ mnogie +++ - + złośliwe + (rzadko)* - rzadko? *D 92 Y, G 148 D, Y 114 X, 85 X, W 43 X, IVS 2+5 G>T, C 11 X Havekes i wsp. JCEM 2007 Timmers i wsp. Clin Endocrinol 2007 Manelli i wsp. J Med. Genetics, 2007 Pęczkowska i wsp. Nature Clin Practice E&M 2008

• Obecność mutacji genu SDHB jest głównym niekorzystnym czynnikiem rokowniczym w złośliwym guzie chromochłonnym Badanie retrospektywne 54 chorych ze złośliwym guzem chromochłonnym/paraganglioma o om a om t y c r h c o e a om i l g n a g ra h p - Średni czas przeżycia: 42 miesiące (SDHB +) versus 244 miesiące (SDHB -) Gimenez-Roqueplo i wsp. J Clin Endocrinol Metab 2002, Gimenez-Roqueplo i wsp. Cancer Res 2003, Amar i wsp. J Clin Oncol 2005, Amar i wsp. J Clin Endocrinol Metab 2007

• SDHx – inne związki Sporadyczny guz pęcherza moczowego – somatyczna mutacja SDHB. • • • • Nederveen i wsp. NEJM 2007 a om t (KIT, PDGFRA): PGL, GIST – Zespół Carney – Stratakis y SDHB/C/D oc m o r Mc. Whinney i wsp. NEJM 2007 h c Cowden like (multiple hamartoma syndrome) – Zespół Cowden/ o gen PTEN: nowotwory sutka, tarczycy i endometrium. e h U 10/375 PTEN ujemnych chorych – mutacje SDHD i SDHB – p - tarczycy i nerki rak sutka, a om Ni i wsp. AJHG 2008 i l g jasnokomórkowy nerki, rak tarczycy – SDHB Rak n • a Vaharanta i wsp. AJHG 2004 g ra

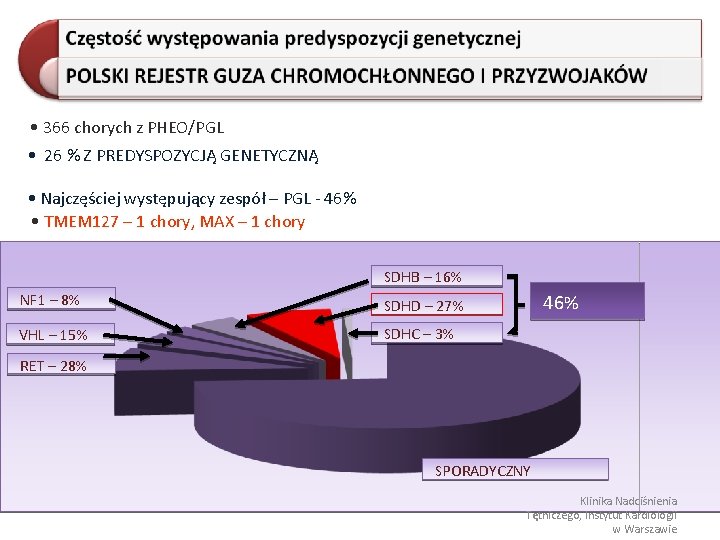
• 366 chorych z PHEO/PGL • 26 % Z PREDYSPOZYCJĄ GENETYCZNĄ • Najczęściej występujący zespół – PGL - 46% • TMEM 127 – 1 chory, MAX – 1 chory SDHB – 16% NF 1 – 8% SDHD – 27% VHL – 15% SDHC – 3% 46% RET – 28% SPORADYCZNY Klinika Nadciśnienia Tętniczego, Instytut Kardiologii w Warszawie

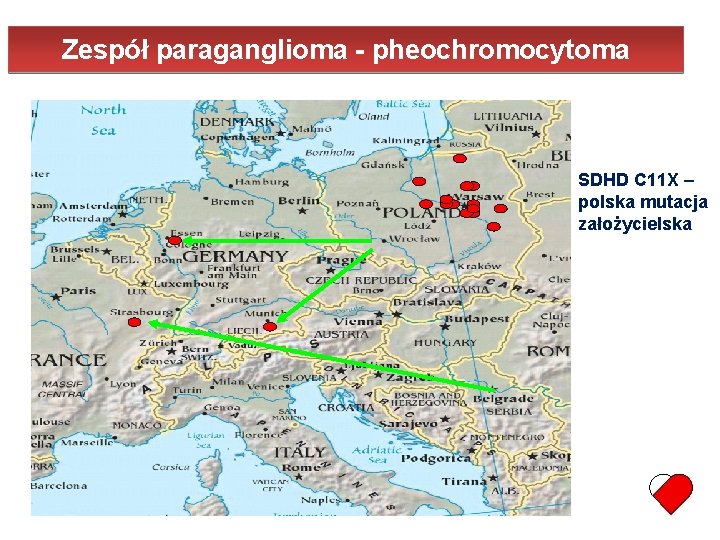
Zespół paraganglioma - pheochromocytoma SDHD C 11 X – polska mutacja założycielska

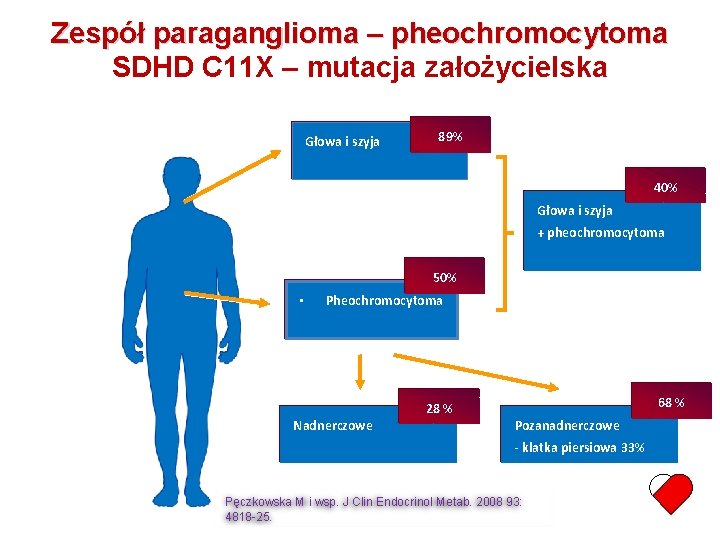
Zespół paraganglioma – pheochromocytoma SDHD C 11 X – mutacja założycielska Głowa i szyja 89% 40% Głowa i szyja + pheochromocytoma 50% • Pheochromocytoma Nadnerczowe 28 % 68 % Pozanadnerczowe - klatka piersiowa 33% Pęczkowska M i wsp. J Clin Endocrinol Metab. 2008 93: 4818 -25.

Przypadek

Przypadek 33 -letni mężczyzna Nadciśnienie tętnicze – od 3 lat Objawy – okresowo: bóle głowy, kołatanie serca – w okresie ostatnich dwóch tygodni: krótkie epizody zwyżek RR z towarzyszącym zblednięciem i niepokojem Obecne leczenie Inhibitor konwertazy, antagonista wapnia, diuretyk tiazydopodobny

33 -letni chory z NT Badanie przedmiotowe: BMI – 27, 4 kg/m 2 Badania laboratoryjne Stężenie glukozy na czczo ↑ Obwód pasa - 94 cm HR - 88/min RR (pozycja siedząca) - 150/105 mm. Hg EKG Prawidłowe

33 -letni chory z NT Wydalanie metoksykatecholamin z moczem: 8538, 9345, 9761 µg/24 h (norma <1000) Stężenie metoksykatecholamin we krwi: - normetanefryna – 3283 pg/m. L (norma <112) - metanefryna – 25 pg/ml (norma <61)

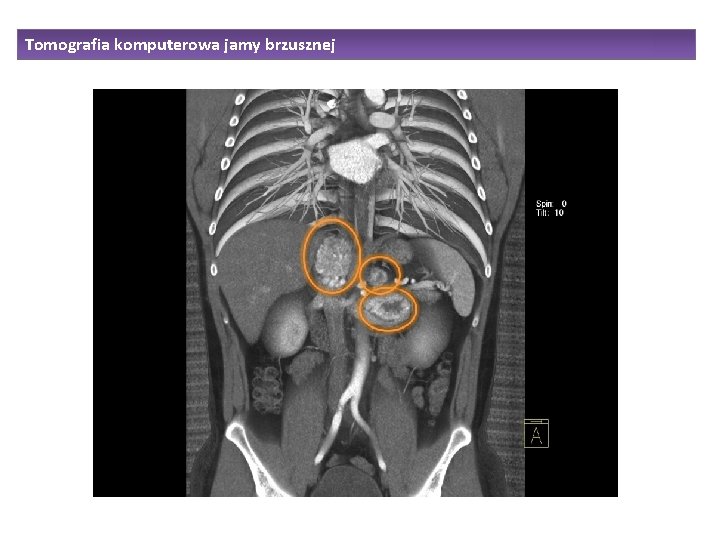
33 -letni chory z NT Wydalanie metoksykatecholamin z moczem: 8538, 9345, 9761 µg/24 h (norma <1000) Stężenie metoksykatecholamin we krwi: - normetanefryna – 3283 pg/m. L (norma <112) - metanefryna – 25 pg/ml (norma <61) USG jamy brzusznej: 3 guzy w obrębie jamy brzusznej Modyfikacja leczenia: - dołączono alfa-adrenolityk, następnie beta-adrenolityk

Tomografia komputerowa jamy brzusznej

Scyntygrafia z zastosowanie I 123 -MIBG

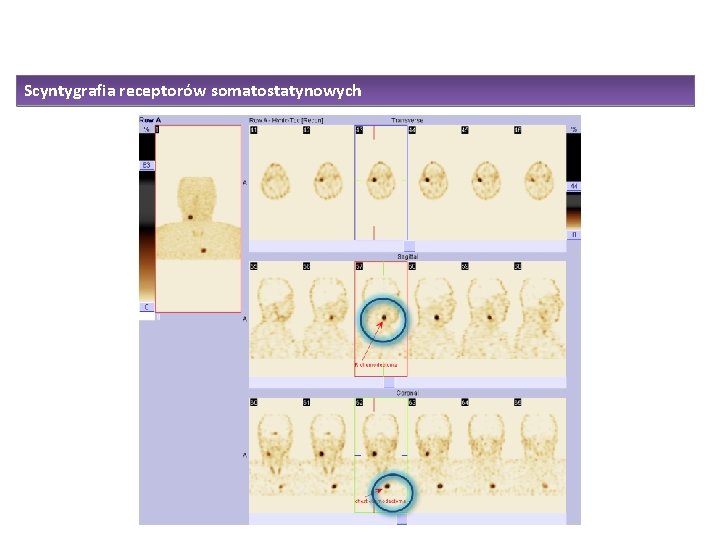
Scyntygrafia receptorów somatostatynowych

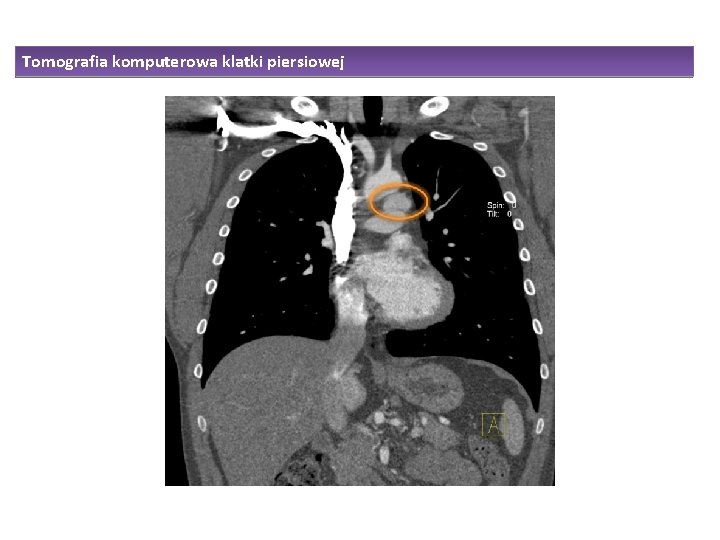
Tomografia komputerowa klatki piersiowej

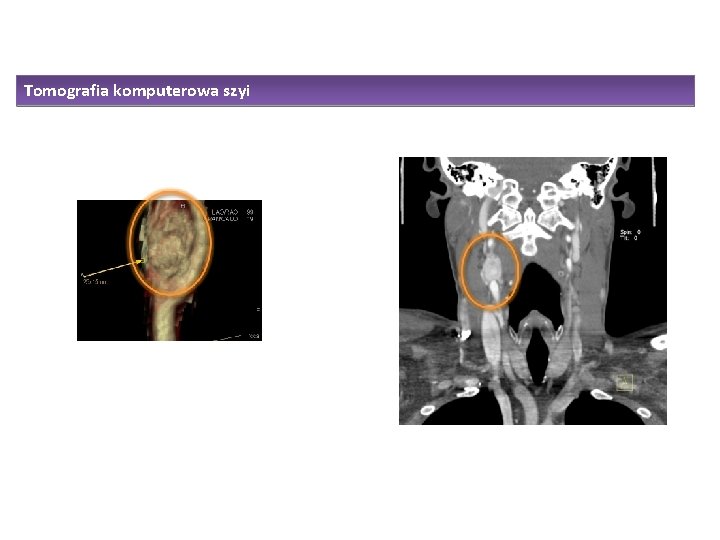
Tomografia komputerowa szyi

Zabieg operacyjny - usunięto 3 guzy - paraganglioma Badania genetyczne

Badania genetyczne - mutacja genu SDHD - c. 33 C→A (p. Cys 11 X)


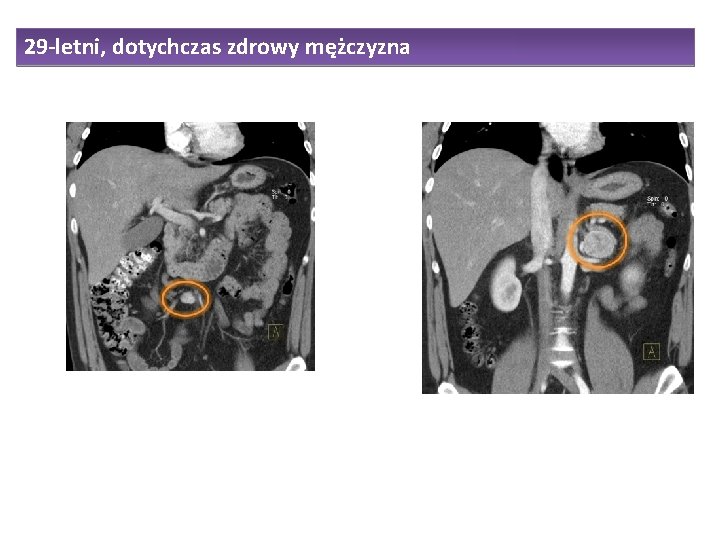
29 -letni, dotychczas zdrowy mężczyzna Podwyższone RR w pomiarach klinicznych i ABPM Wydalanie metoksykatecholamin z moczem: 2973, 3133 µg/24 h (norma <1000) Stężenie metoksykatecholamin we krwi: - normetanefryna – 1239 pg/m. L (norma <112) - metanefryna – 28 pg/ml (norma <61)

29 -letni, dotychczas zdrowy mężczyzna

3 paraganglioma - j. brzuszna Paraganglioma – klp Kłębczak prawej t. szyjnej Pheochromocytoma lewego nadnercza, paraganglioma j. brzusznej Przyzwojaki w obrębie głowy i szyi


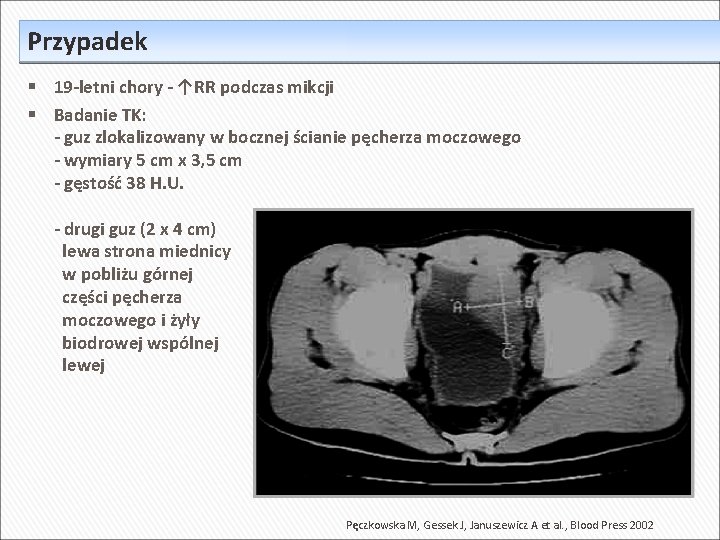
Przypadek 19 -letni chory - ↑RR podczas mikcji Badanie TK: - guz zlokalizowany w bocznej ścianie pęcherza moczowego - wymiary 5 cm x 3, 5 cm - gęstość 38 H. U. - drugi guz (2 x 4 cm) lewa strona miednicy w pobliżu górnej części pęcherza moczowego i żyły biodrowej wspólnej lewej Pęczkowska M, Gessek J, Januszewicz A et al. , Blood Press 2002

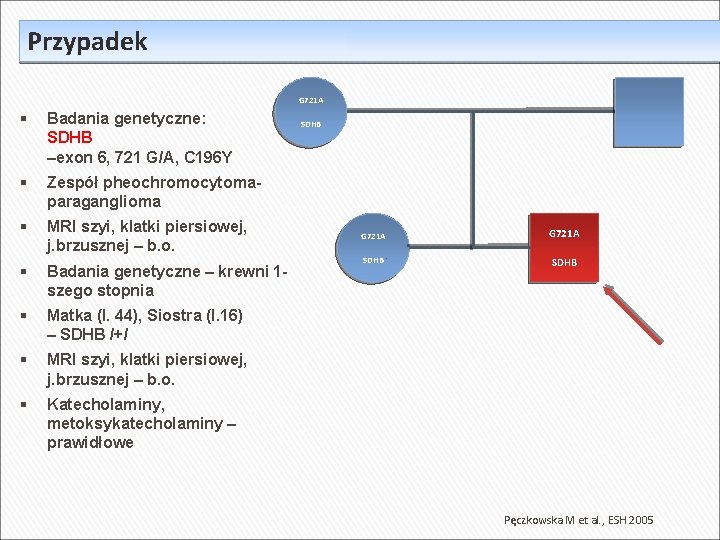
Przypadek G 721 A Badania genetyczne: SDHB –exon 6, 721 G/A, C 196 Y Zespół pheochromocytomaparaganglioma MRI szyi, klatki piersiowej, j. brzusznej – b. o. Badania genetyczne – krewni 1 szego stopnia Matka (l. 44), Siostra (l. 16) – SDHB /+/ MRI szyi, klatki piersiowej, j. brzusznej – b. o. Katecholaminy, metoksykatecholaminy – prawidłowe SDHB G 721 A SDHB Pęczkowska M et al. , ESH 2005

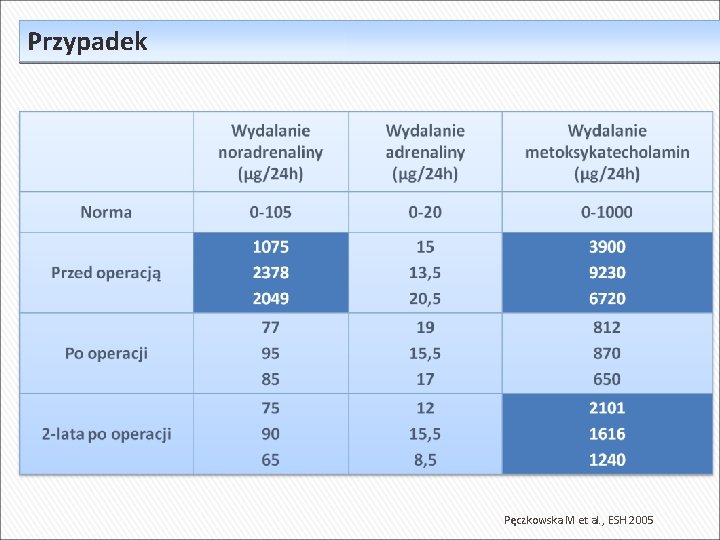
Przypadek Pęczkowska M et al. , ESH 2005

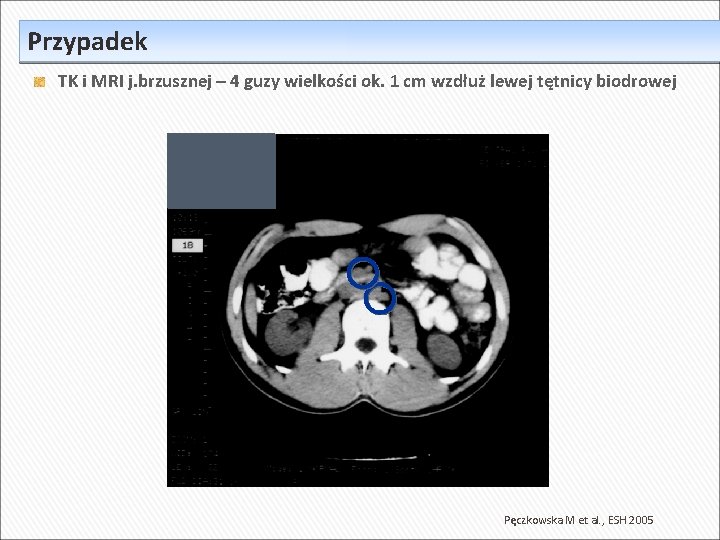
Przypadek TK i MRI j. brzusznej – 4 guzy wielkości ok. 1 cm wzdłuż lewej tętnicy biodrowej Pęczkowska M et al. , ESH 2005

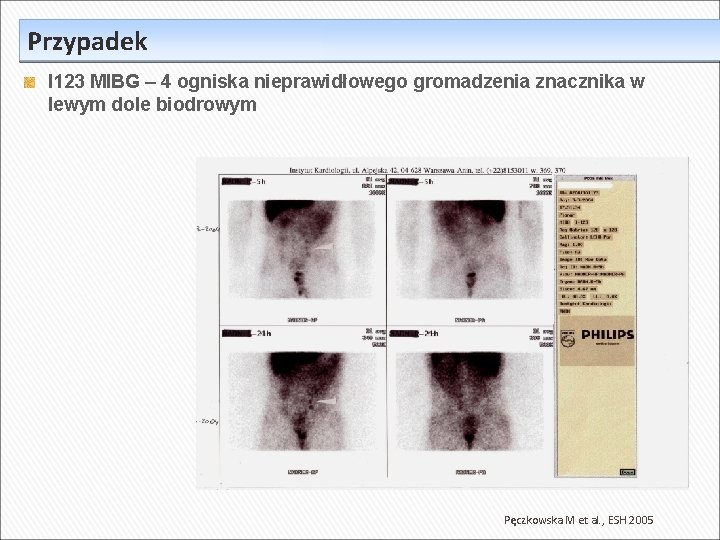
Przypadek I 123 MIBG – 4 ogniska nieprawidłowego gromadzenia znacznika w lewym dole biodrowym Pęczkowska M et al. , ESH 2005

Przypadek Operacyjne usunięcie guzów z okolicy lewej tętnicy biodrowej Badanie hist-pat - pheochromocytoma Pęczkowska M et al. , ESH 2005

Przypadek 2 lata później - nieznacznie podwyższone wydalanie metoksykatecholamin z moczem Dalsza diagnostyka obrazowa: - 2 guzy o typie paraganglioma w lewym dole biodrowym

We recommend a surveillance protocol that includes: annual history and physical examination, annual biochemical testing, MRI of the neck, chest, abdomen, and pelvis every 1– 2 yrs Timmers HJLM et al. Endocrine-Related Cancer 2009

Nowe geny predysponujące Gen KIF 1 B, chromosom 1 p. 36, 22 Gen supresorowy nowotworów, koduje kinezy uczestniczące w apoptozie Dziedziczenie autosomalnie dominujące Opisano dwa przypadki Predysponuje do pheochromocytoma, ganglioneuroma, leiomiosarkoma, raka płuc

Gen EGLN 1, chromosom 1 q 42. 1 Gen supresorowy nowotworów, koduje e białko EGLN 1 – hydroksylazę prolinową c ą j odpowiedzialną za hydroksylację HIF- 1α u n 1 przypadek, nawrotowe o p pheochromocytoma, czerwienica. s y n e g r p y d e

TMEM 127, chromosom 2 q 11. 2 Gen supresorowy nowotworów, reguluje negatywnie kompleks kinazy m. TOR. e c ą Dziedziczenie autosomalnie dominujące j u n Częstość występowania (143 chorych) – o ok. 2%, 96% PHEO, 39% - obustronne, p s y 9% - HNP, sporadycznie – d pozanadnerczowe e r p Inne nowotowory: MTC, rak sutka, zespoły y n e mielodysplastyczne g

MAX – chromosom 14 p. 23. 3 Gen supresorowy nowotworów, koduje e czynnik transkrypcyjny MAX c ą j Dziedziczenie autosomalnie dominujące u n o PHEO – częstość występowania w grupie p s 1694 chorych – 1, 12% y d nadnerczowe (50% - obustronnie) i e r p pozanadnerczowe, 10% - złośliwe. y n e g

Miejsce badań DNA w guzie chromochłonnym • SKALA PROBLEMU Neumann, H. P. H. et al. N Engl J Med 2002; 346: 1459 -1466

Miejsce badań DNA w guzie chromochłonnym Mutacje germinalne 4 genów 271 niespokrewnionych chorych z pozornie sporadycznym guzem chromochłonnym 66 (24%) nosiciele germinalnej mutacji Neumann, H. P. H. et al. N Engl J Med 2002; 346: 1459 -1466

Miejsce badań DNA w guzie chromochłonnym Czy istnieją cechy kliniczne pozwalające podejrzewać tło genetyczne choroby?

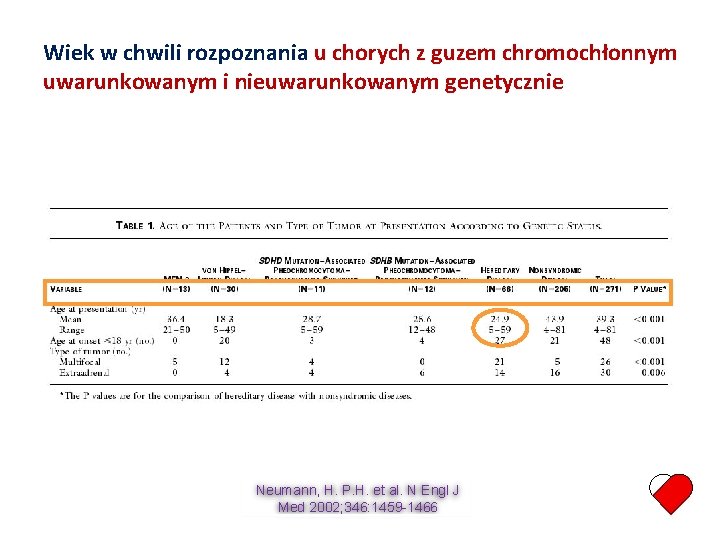
Wiek w chwili rozpoznania u chorych z guzem chromochłonnym uwarunkowanym i nieuwarunkowanym genetycznie Neumann, H. P. H. et al. N Engl J Med 2002; 346: 1459 -1466

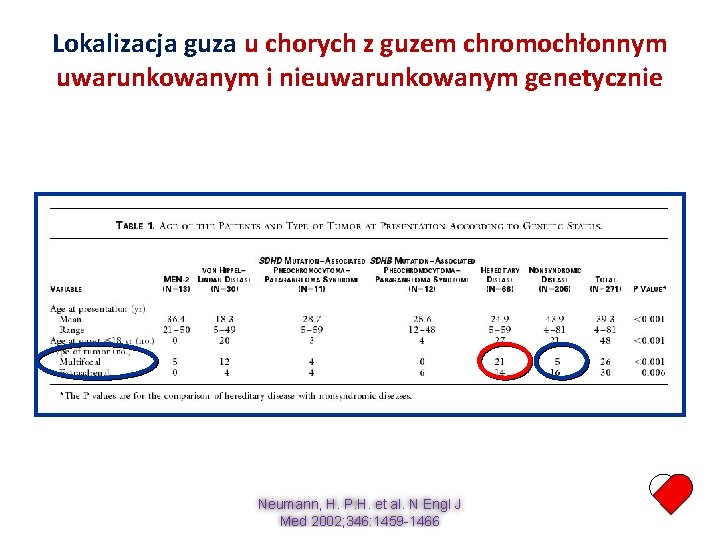
Lokalizacja guza u chorych z guzem chromochłonnym uwarunkowanym i nieuwarunkowanym genetycznie Neumann, H. P. H. et al. N Engl J Med 2002; 346: 1459 -1466

Miejsce badań DNA w guzie chromochłonnym znaczenie kliniczne Identyfikacja mutacji określonego genu pozwala ustalić rozpoznanie zespołu genetycznego ukierunkowanie diagnostyki oraz aktywnej obserwacji Zależności genotyp-fenotyp – ocena profilu ryzyka i wybór strategii postępowania

Lenders JW


Złośliwy guz chromochłonny Pewne kryterium rozpoznania: obecność przerzutów odległych: kości, wątroba, płuca.

Złośliwy guz chromochłonny - rokowanie • Przerzuty – w chwili rozpoznania, lub po pewnym czasie od usunięcia guza pierwotnego – średni czas – ok. 5 lat • Całkowite 5 letnie przeżycie - 34 -60% • Przeżycie zależy od lokalizacji przerzutów: – short-term survivors – wątroba, płuca – long-term survivors – kości

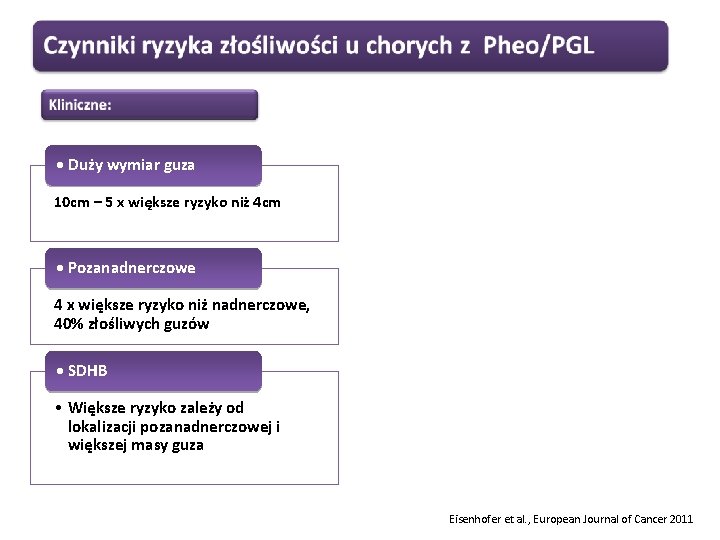
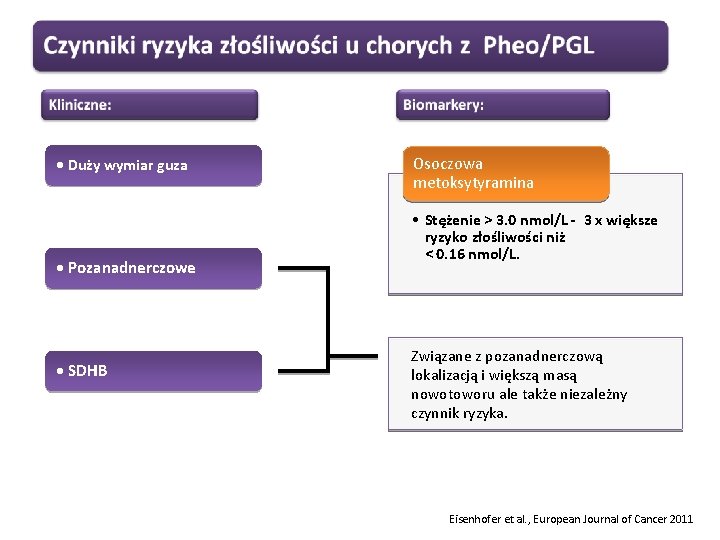
• Duży wymiar guza 10 cm – 5 x większe ryzyko niż 4 cm • Pozanadnerczowe 4 x większe ryzyko niż nadnerczowe, 40% złośliwych guzów • SDHB • Większe ryzyko zależy od lokalizacji pozanadnerczowej i większej masy guza Eisenhofer et al. , European Journal of Cancer 2011

• Duży wymiar guza • Pozanadnerczowe • SDHB Osoczowa metoksytyramina • Stężenie > 3. 0 nmol/L - 3 x większe ryzyko złośliwości niż < 0. 16 nmol/L. Związane z pozanadnerczową lokalizacją i większą masą nowotoworu ale także niezależny czynnik ryzyka. Eisenhofer et al. , European Journal of Cancer 2011

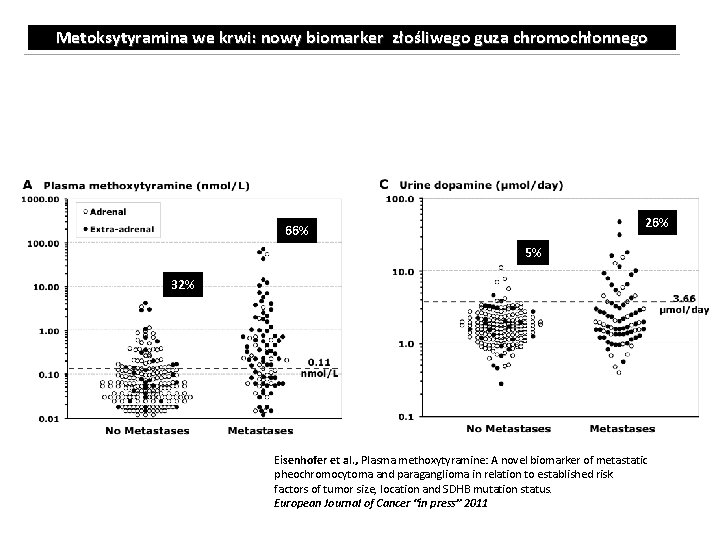
Metoksytyramina we krwi: nowy biomarker złośliwego guza chromochłonnego 26% 35% 66% 5% 32% 8% Eisenhofer et al. , Plasma methoxytyramine: A novel biomarker of metastatic pheochromocytoma and paraganglioma in relation to established risk factors of tumor size, location and SDHB mutation status. European Journal of Cancer “in press” 2011

Złośliwy guz chromochłonny Markery molekularne: białko szoku cieplnego (hsp 90), odwrotna transkryptaza ludzkiej telomerazy (h. TERT), naczyniowy czynnik wzrostu śródbłonka (VEGF), receptor naczyniowego czynnika wzrostu śródbłonka (VEGFR 2), białko indukowane hipoksją (HIF-2 -alfa), cyklooksygenaza-2, tenascyna C, N-kadheryna oraz peptyd EM 66 (secretogranin II-derived peptide EM 66). Zwiększona ekspresja w tkance guza

Złośliwy guz chromochłonny - kryteria histologiczne PASS (Pheochromocytoma of the Adrenal Gland Scaled Score) • • • Inwazja naczyń - 1 Naciekanie torebki guza - 1 Naciekanie okołonadnerczowej tkanki tłuszczowej - 2 Obecność dużych gniazd komórkowych lub rozlany charakter wzrostu - 2 Zwiększona aktywność mitotyczna - 2 Atypowe mitozy - 2 Pojawienie się martwicy - 2 Obecność komórek wrzecionowatych - 2 Duży pleomorfizm komórkowy - 1 Hyperchromazja jąder komórkowych - 1 Monotonia komórkowa - 2 Utkanie bogatokomórkowe - 2 Suma punktów skali PASS dzieli guzy chromochłonne na te o potencjalnej złośliwości (PASS ≥ 4) i łagodne (PASS < 4).

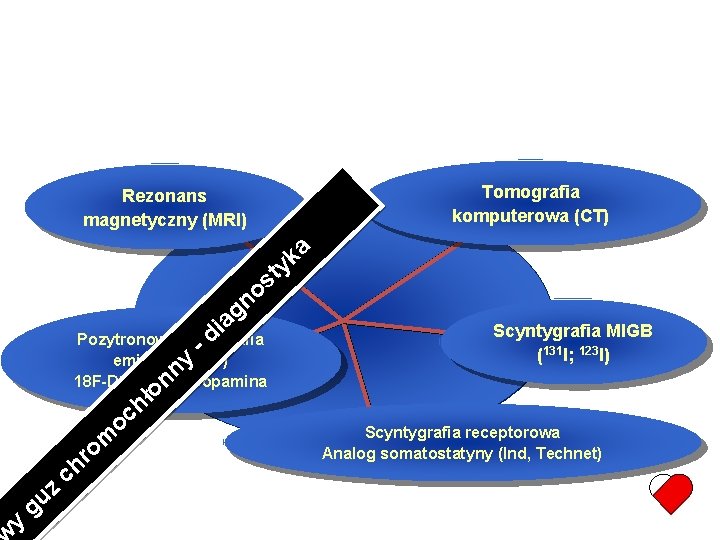
Tomografia komputerowa (CT) Rezonans magnetyczny (MRI) a k y t s o n g y z u g a i d Pozytronowa tomografia emisyjna y (PET) n 18 F-DOPA 18 F-Dopamina on ł h c o m o r ch Scyntygrafia MIGB (131 I; 123 I) Scyntygrafia receptorowa Analog somatostatyny (Ind, Technet)

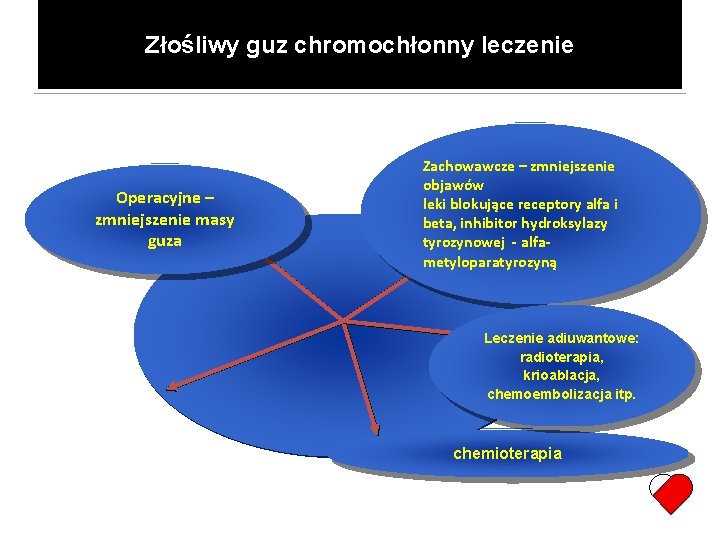
Złośliwy guz chromochłonny leczenie Operacyjne – zmniejszenie masy guza Zachowawcze – zmniejszenie objawów leki blokujące receptory alfa i beta, inhibitor hydroksylazy tyrozynowej - alfametyloparatyrozyną Leczenie adiuwantowe: radioterapia, krioablacja, chemoembolizacja itp. chemioterapia

Złośliwy guz chromochłonny - leczenie radioizotopowe Leczenie I-131 -MIGB – wyniki (116 chorych z 24 ośrodków) regresja nowotworu – 30% odpowiedź hormonalna – 45% zmniejszenie objawów – 76% Loh KC i wsp. J Endocrinol Invest, 1997

Złośliwy guz chromochłonny - leczenie radioizotopowe Leczenie dużymi dawkami I-131 -MIGB – wyniki (30 chorych) regresja nowotworu – 67% przeżycie 5 – letnie – 75% Działanie toksyczne na szpik kostny.

Złośliwy guz chromochłonny - leczenie chemiczne Podstawą nowych metod chemioterapii są badania molekularne w dziedzicznych postaciach obejmujące profil ekspresji genów w tkance guza Ekspresja genów związanych z aktywacją szlaków zależnych od kinaz Ekspresja genów związanych z hipoksją i angiogenezą (zależne od HIF-1). RET, NF 1, KIF 1 B, TMEM 127, MAX VHL, SDHx GUZY SPORADYCZNE

Złośliwy guz chromochłonny chemiczne - leczenie • Nowe metody terapeutyczne: Talidomid (działanie antyangiogenne VEGF, b. FGF) +Temozolomid Imatinib (inhibitor kinazy tyrozynowej) Sunitinib (inhibitor kinazy tyrozynowej) Everolimus (inhibitor m. TOR) Obiecujący lek – Sunitinib

Złośliwy guz chromochłonny - leczenie chemiczne • Protokół Averbucha ( cyklofosfamid, vinkrystyna, dakarbazyna) - odpowiedź hormonalna – 52 -76% - regresja nowotworu – 47 - 56% - mediana przeżycia – 65 -216 miesięcy. Nomura K i wsp. J Clin Endocrinol Metab, 2009; Huang H i wsp. Cancer, 2008, Rao F i wsp. Hypertension 2000; Patel S i wsp. Cancer, 1995; Averbuch S i wsp. Ann Intern Med. , 1988

DZIĘKUJĘ ZA UWAGĘ