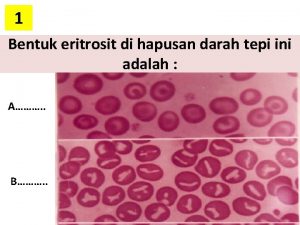
Eritrosit membrannn permeabilitesi ve hemoliz Eritrositlerin ozmotik frajilitesinin

Eritrosit membranının permeabilitesi ve hemoliz Eritrositlerin ozmotik frajilitesinin ölçülmesi, kantitatif frajilite testi Serumun edilmesi tampon gücünün test

HEMOLİZ • Eritrosit zarının yırtılması sonucunda, Hb molekülünün Eritrositler içinde bulunan hemoglobinin eritrosit hücre dışına çıkmasıdır. membranının parçalanması sonucunda plazmaya geçmesine hemoliz denir Hemoliz 2 şekilde oluşur 1) Hemositoliz 2) Osmotik Hemoliz

HEMOLİZ Ozmotik Hemoliz: Eritrositler hipotonik sıvıya konulduklarında içeri giren su dolayısıyla şişerler. Bu şişme sonucu hücre zarı üstünde oluşan yüksek basınç nedeniyle zarın yırtılmasına ve hemoglobin molekülünün dışarı çıkmasına yol açar. Hemositoliz (eritrosit membran harabiyeti): Bazı mekanik, fiziksel ve kimyasal etmenlerle zar yapısının bozulmasıyla görülen hemolizdir (Donma-çözünme, sıcaklık, akrep-yılan zehirleri, bazı bakteri toksinleri, eter, gliserin, asetik asit gibi maddeler bu tip hemolize neden olur). Hemoliz, izotonik ortamda eritrosit membranı haraplanmadan oluşabilir, üre gibi membrandan kolaylıkla geçen küçük moleküller hücre içinde ozmotik basıncı artırıp suyu hücre içine çekerek hücrenin şişip yırtılmasına neden olabilir.

OSMOLARİTE-TONİSİTE Osmolarite (Osm), çözeltinin (örn; plazma) bir litresindeki daha fazla disosiye olamayan parçacıkların toplam mol sayısıdır. Bir çözeltinin plazmaya göre osmolaritesini belirtmek için tonisite terimi kullanılır. İzotonik: Plazma ile aynı osmolariteye (300 m. Osm = 0. 3 Osm sahip çözeltiler (örn: %0. 9 Na. Cl) Hipertonik: Hipotonik: Plazmadan daha büyük osmolaritede Plazmadan daha düşük osmolaritede

HEMOLİZİN İNCELENMESİ Gerekli eriyikler (her biri 0. 3 Osm olmak üzere): Na. Cl (%0. 9) Gliserin Üre Na asetat Asetik asit Eter (0. 3 Osm %0. 9 Na. Cl içinde) Saf su Pıhtılaşması önlenmiş kan (Sodyum Sitratlı –[Ca bağlar] kan
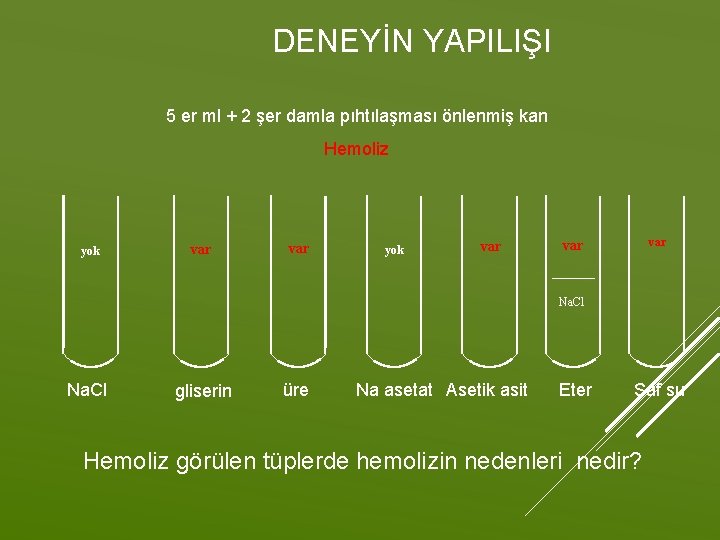
DENEYİN YAPILIŞI 5 er ml + 2 şer damla pıhtılaşması önlenmiş kan Hemoliz yok var var var Na. Cl gliserin üre Na asetat Asetik asit Eter Saf su Hemoliz görülen tüplerde hemolizin nedenleri nedir?

Ozmotik frajilite Eritrositlerin hipotonik solüsyonlara direncini araştıran testtir. Eritrositlerin yüzey alanı- hacim ilişkisini değerlendirir. Yüzey alanının hacme oranı azalmışsa (sferosit) ozmotik frajilite artmıştır. Hipotonik solüsyonlara direnç azalmıştır. Heparinize kan , azalan konsantrasyonlarda Na. Cl çözeltisine konarak oda ısısında bekletilir. Tüplerde gözlenen hemoliz , eritrositlerin hipotonik hasara hassasiyet derecesinin göstergesidir. OZMOTİK FRAJİLİTE

Normal eritrositler %0. 9 (izotonik), 0. 8, 0. 7, 0. 6, 0. 5 Na. Cl çözeltilerinde su alıp şişmelerine rağmen hemolize uğramazlar. Çünkü: zarları esnektir eritrositler sitoplazmik materyal miktarının hücre içi hacmine oranla düşük olması sebebiyle içi boş bir torba gibi davranabilirler. Çözeltinin konsantrasyonu %0. 5 ten daha düşük olunca normal eritrositlerde de hemoliz görülmeye başlar. Bazı anemi tiplerinde eritrositler %0. 7 lik tuz çözeltisinde bile hemolize uğrayabilirler (ör: Herediter sferositoz). Osmotik frajilite artmıştır. Hipokrom-mikrositer anemiler (Demir eksikliği, talassemi gibi) de ozmotik frajilite azalır.

Eritrositlerin membran proteinlerinin defektleri sonucu, morfolojik olarak bikonkav ve santral solukluğu olan disk şeklinden, küre şeklini almaları ile hemolize eğilim artar Eritrositlerin kapillerlerden geçerken şekil değiştirebilme özelliğinin azalması sonucu dalakta daha kolay yakalanır ve yıkılırlar. HEMOLİZ NEDENİ OLARAK MEMBRAN DEFEKTİ (HEREDİTER SFEROSİTOZ)
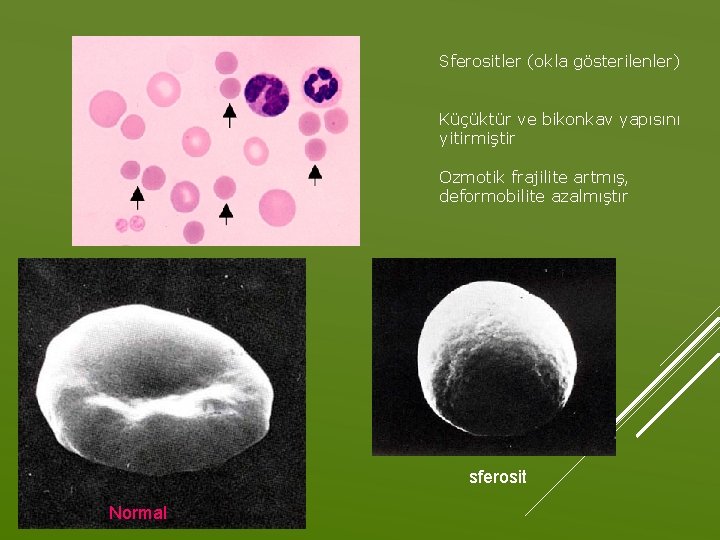
Sferositler (okla gösterilenler) Küçüktür ve bikonkav yapısını yitirmiştir Ozmotik frajilite artmış, deformobilite azalmıştır sferosit Normal

Gerekli materyal %1 Na. Cl çözeltisi distile su, test tüpleri, heparinize kan, santrifüj Hb ölçüm cihazı DENEYİN YAPILIŞI
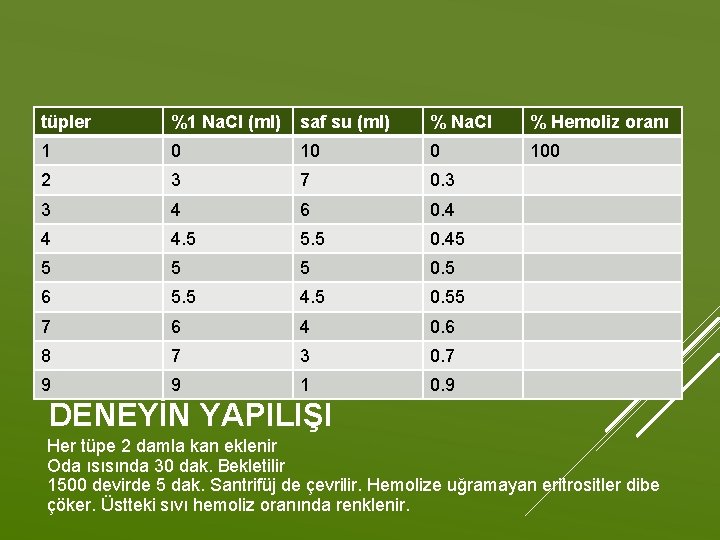
tüpler %1 Na. Cl (ml) saf su (ml) % Na. Cl % Hemoliz oranı 1 0 100 2 3 7 0. 3 3 4 6 0. 4 4 4. 5 5. 5 0. 45 5 0. 5 6 5. 5 4. 5 0. 55 7 6 4 0. 6 8 7 3 0. 7 9 9 1 0. 9 DENEYİN YAPILIŞI Her tüpe 2 damla kan eklenir Oda ısısında 30 dak. Bekletilir 1500 devirde 5 dak. Santrifüj de çevrilir. Hemolize uğramayan eritrositler dibe çöker. Üstteki sıvı hemoliz oranında renklenir.
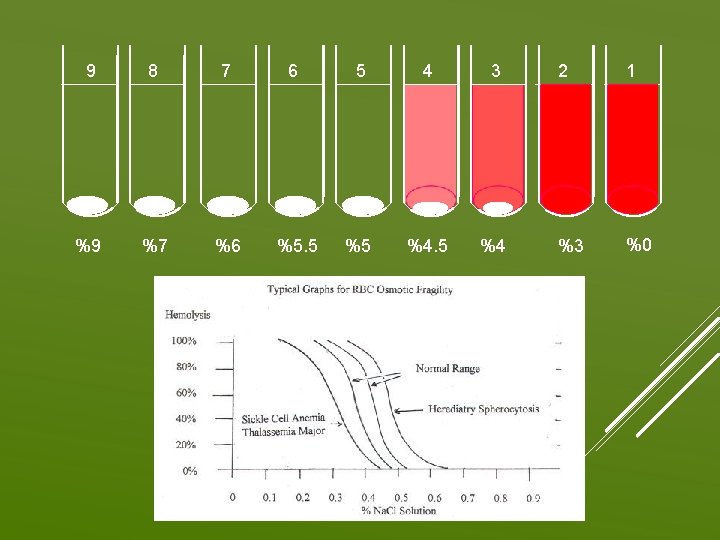
9 8 7 6 5 4 3 %9 %7 %6 %5. 5 %5 %4 2 1 %3 %0
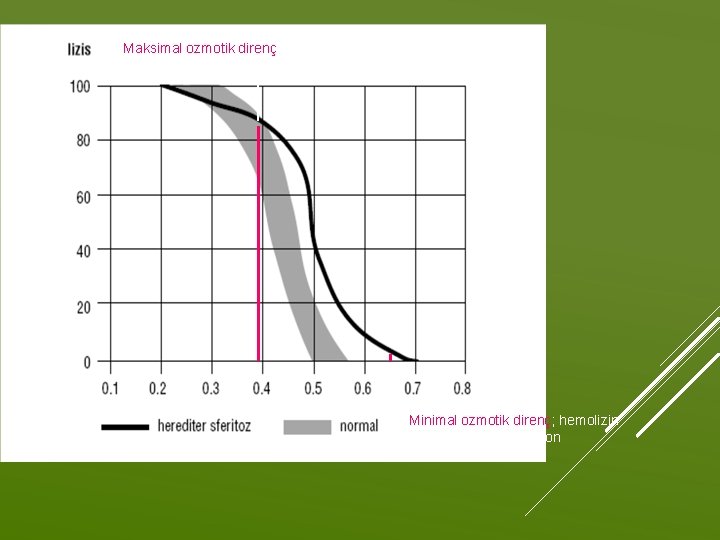
Maksimal ozmotik direnç; hemolizin tamamlandığı konsantrasyon Minimal ozmotik direnç; hemolizin başladığı konsantrasyon

Homeostasis: Vücut fonksiyonlarının normal sürdürülebilmesi için iç ortamın bazı parametreler açısından sabit ve dengede tutulması Vücutta sabit tutulan fizyolojik parametrelerin en önemlilerinden biri (H+) yoğunluğudur.

p. H bir çözeltinin asit veya alkali derecesini tarif eden ölçü birimidir. Çözeltinin içindeki H iyonlarının yoğunluğuna göre ölçüm yapılır 0'dan 14'e kadar olan bir skalada ölçülür. Kanın p. H’ı 7. 4 tür ve bunun sabit tutulması şarttır. Çünkü; Protein moleküllerinin yapısı, Enzim aktiviteleri Eloktrolit dağılımı Membran geçirgenliği p. H’a bağlıdır. Bu nedenle; H+ vücut sıvılarında sıkı bir şekilde regüle edilir. Bu regülasyona “asit-baz dengesi ” adı verilir. “Hayat aslında Hidrojene karşı bir mücadeledir”
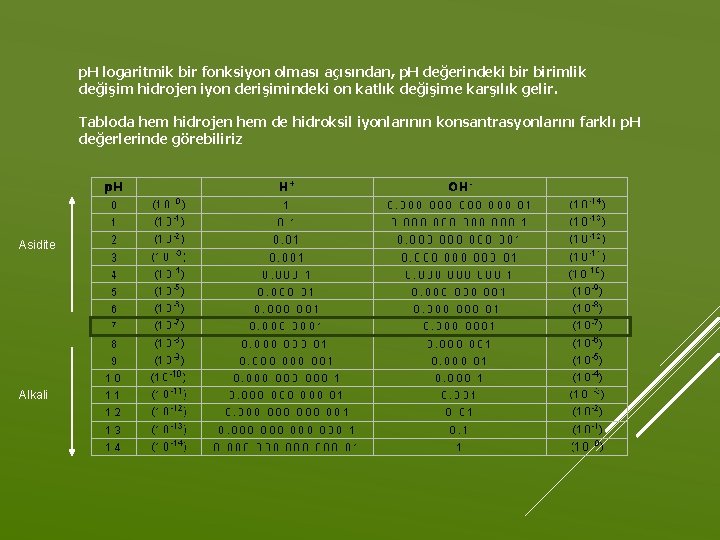
p. H logaritmik bir fonksiyon olması açısından, p. H değerindeki birimlik değişim hidrojen iyon derişimindeki on katlık değişime karşılık gelir. Tabloda hem hidrojen hem de hidroksil iyonlarının konsantrasyonlarını farklı p. H değerlerinde görebiliriz Asidite Alkali
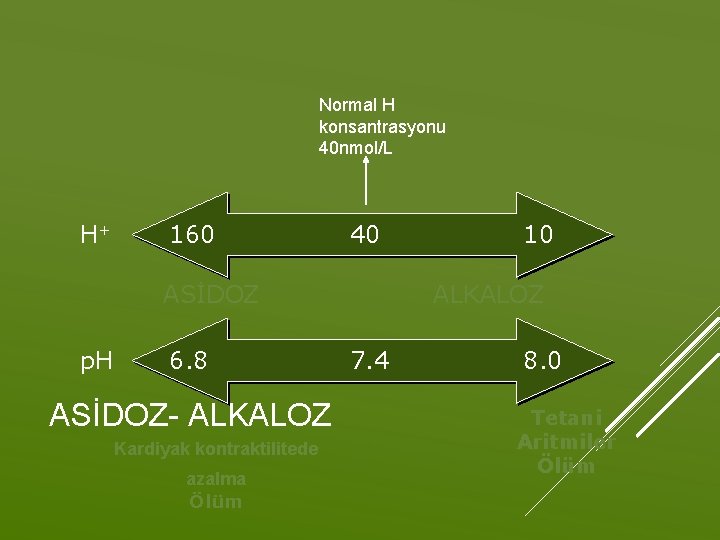
Normal H konsantrasyonu 40 nmol/L H+ 160 40 ASİDOZ p. H 6. 8 ASİDOZ- ALKALOZ Kardiyak kontraktilitede azalma Ölüm 10 ALKALOZ 7. 4 8. 0 Tetani Aritmiler Ölüm
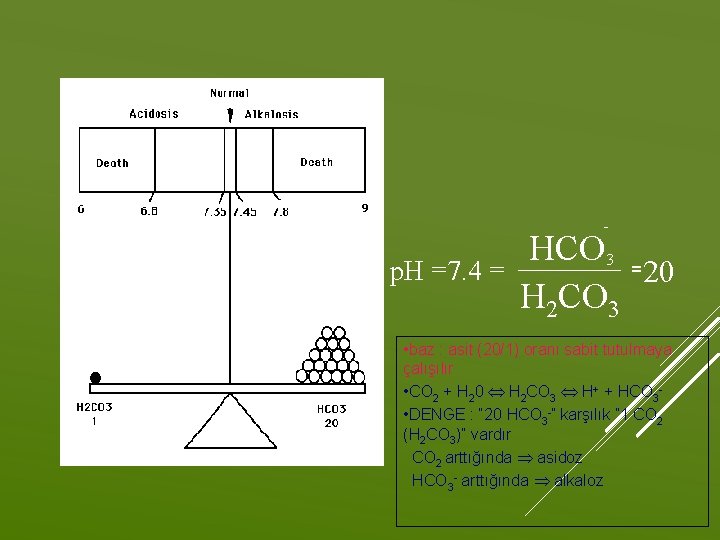
- p. H =7. 4 = HCO 3 = 20 H 2 CO 3 • baz : asit (20/1) oranı sabit tutulmaya çalışılır • CO 2 + H 20 Û H 2 CO 3 Û H+ + HCO 3 • DENGE : “ 20 HCO 3 -” karşılık ” 1 CO 2 (H 2 CO 3)” vardır CO 2 arttığında Þ asidoz HCO 3 - arttığında Þ alkaloz

PH NIN SABİT TUTULMASI BAŞLICA 3 MEKANİZMA İLE SAĞLANIR 1 -Kimyasal Tampon Sistemi (Saniyeler içerisinde etkisini gösterir) 2 -Solunum sistemi; Akciğerler yoluyla CO 2 atılımının kontrolu (Dakikalar içerisinde etkisini gösterir) 3 -Üriner sistem; Böbrekler gerekirse geri emmek ve gerekirse salgılamak yoluyla H+ ve HCO 3 - iyonlarının kandaki konsantrasyonlarını düzenleme yeteneğine sahiptir (Saatler, günler içerisinde etkisini gösterir).

VÜCUTTAKİ TAMPON SİSTEMLERİ Yer Tampon sistemi Yorum Kan Bikarbonat Metabolik asitler için önemli Hemoglobin Metabolik asitler için önemli Plazma proteinleri Minor tampon Fosfatlar Konsantrasyonu çok düşük Hücre içi Proteinler Önemli tampon Fosfatlar Önemli tampon İdrar Fosfatlar Titre edilebilen asitlerin çoğu için önemli Amonyak Önemli - NH 4+ formasyonu Ca karbonat Uzun süreli metabolik asidoz Kemik

TAMPON SİSTEMLERİ Bulundukları ortama eklenen H+ veya OH- iyonlarının etkisini azaltarak, p. H değişikliğini önlerler. Tampon sistemleri zayıf asit veya baz ile bunların tuzlarının kombinasyonundan oluşur. Bu tamponların etkinliği bulundukları ortamdaki konsantrasyonlarına bağlıdır. Vücudun tamponlama kapasitesinin % 53’ ünü bikarbonat, % 35’ini Hb, %12’sini de fosfatlar, plazma proteinleri ve amonyum oluşturur.

Zayıf asit ve baz çiftleri en iyi tamponlardır Bir tampon sistemi için eşitlik şudur; HA(zayıf asit) Bu sistemi içeren çözeltiye kuvvetli asit eklenirse denge sola kayar. H konsantrasyonu azalır, Baz eklenirse H ve OH tepkimeye girer. H 2 O oluşturur. Öte yandan HA ayrışarakda H nin çok düşmesini sınırlar H+A(anyon) Örnek; HCO 3/H 2 CO 3 tampon sistemi(kanın önemli tampon sistemi); H 2 CO 3 H+HCO 3 TAMPON SİSTEMİH 2 CO 3 NASILCO 2+H 2 O Asit fazla ise ; H+HCO 3 ÇALIŞIR Baz fazla ise; OH+H 2 CO 3 HCO 3 +H 2 O böbrekten Akciğerlerden
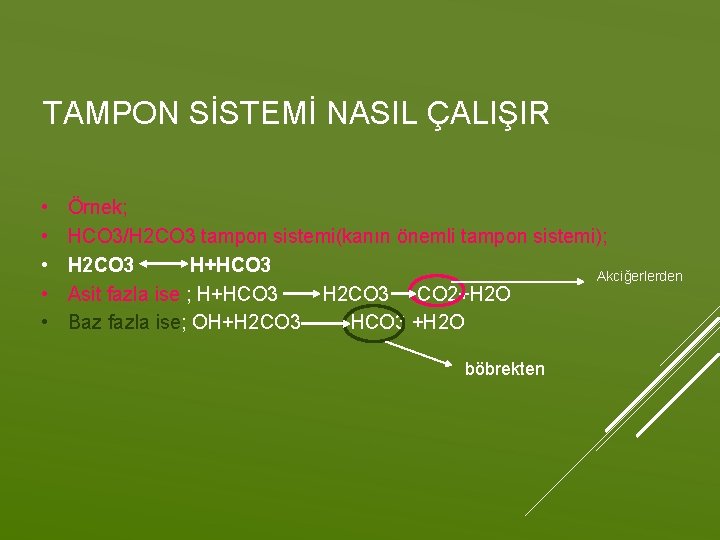
TAMPON SİSTEMİ NASIL ÇALIŞIR • • • Örnek; HCO 3/H 2 CO 3 tampon sistemi(kanın önemli tampon sistemi); H 2 CO 3 H+HCO 3 Akciğerlerden Asit fazla ise ; H+HCO 3 H 2 CO 3 CO 2+H 2 O Baz fazla ise; OH+H 2 CO 3 HCO 3 +H 2 O böbrekten

Gerekli malzeme; Ayıraçlar Fenolftalein (baz indikatörü): p. H 8. 3 -10. 2 arasında eflatun renk verir Metil oranj (asit indikatörü): metil oranj p. H 34. 4 arasında kırmızı renk verir İnsan serumu 0. 1 N Na. OH, 0. 1 N HCl SERUMUN TAMPON GÜCÜNÜN TEST EDİLMESİ

Pıhtılaşmış kan
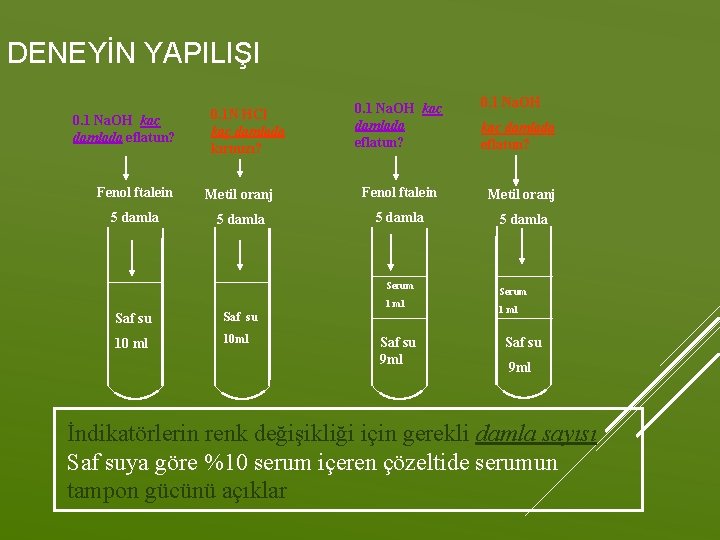
DENEYİN YAPILIŞI 0. 1 Na. OH kaç damlada eflatun? 0. 1 N HCl kaç damlada kırmızı? 0. 1 Na. OH kaç damlada eflatun? Fenol ftalein Metil oranj 5 damla Serum 1 ml Saf su 10 ml 10 ml Saf su 9 ml Serum 1 ml Saf su 9 ml İndikatörlerin renk değişikliği için gerekli damla sayısı Saf suya göre %10 serum içeren çözeltide serumun tampon gücünü açıklar
- Slides: 27