ELEKTROCHEMIE PRMYSLOV VYUIT ELEKTROCHEMIE ELEKTROLZA dj probhajc na

ELEKTROCHEMIE PRŮMYSLOVÉ VYUŽITÍ ELEKTROCHEMIE

ELEKTROLÝZA � děj probíhající na elektrodách při průchodu elektrického proudu vodivým roztokem nebo taveninou � vodivý roztok nebo tavenina obsahují volně pohyblivé ionty � kationt: kladně nabitá částice � aniont: záporně nabitá částice � katoda (K): záporná elektroda (přitahuje kationty) � anoda (A): kladná elektroda (přitahuje anionty)
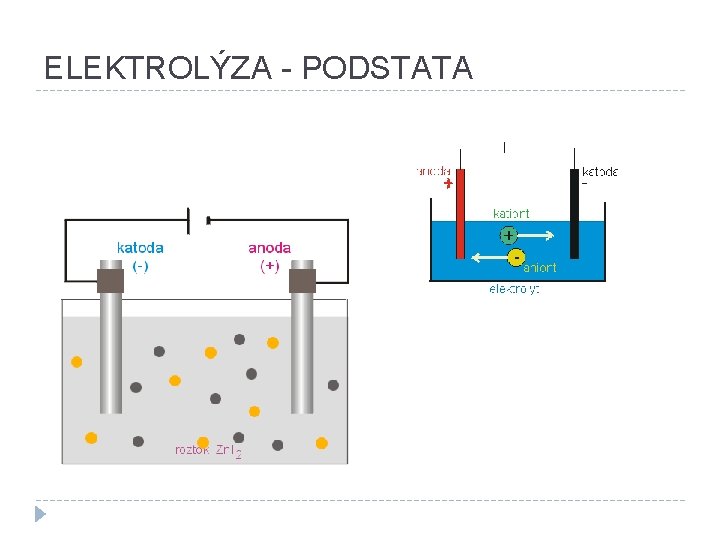
ELEKTROLÝZA - PODSTATA

ELEKTROLÝZA ROZTOKU Na. Cl výroba průmyslově významných chemikálií uhlíkové elektrody, roztok Na. Cl (ionty Na 1+, Cl 1 - ) � reakce na anodě A: oxidace chloridových aniontů → vznik molekul Cl₂ → viditelné bublinky chloru � reakce na katodě K: redukce sodíkových kationtů → sodík vylučovaný na katodě okamžitě reaguje za vzniku H₂ viditelné bublinky vodíku � v nádobce se hromadí hydroxid sodný

ELEKTROLÝZA Cu. SO 4 výroba průmyslově významných chemikálií uhlíkové elektrody, roztok Cu. SO 4 (ionty Cu 2+ , SO 42 - ) � reakce na anodě A: anionty SO 42 - reagují s H 2 O a zároveň odevzdají anodě dva elektrony reakcí vzniká kyselina sírová a bublinky kyslíku � reakce na katodě K: kationty Cu 2+ se na katodě redukují na atomy Cu → na katodě pozorujeme vyloučenou měď

CHEMICKÉ REAKCE JAKO ZDROJ ELEKTRICKÉ ENERGIE � proud elektronů v redoxní reakci může být zdrojem elektrické energie galvanický článek � zařízení, které jako zdroj elektrické energie využívá redoxní reakce � přeměňuje chemickou energii na elektrickou � používá se tam, kde nelze použít elektrický proud ze sítě např. kapesní svítilny, hodinky, myši, tranzistory

CHEMICKÉ REAKCE JAKO ZDROJ ELEKTRICKÉ ENERGIE 2 druhy galvanických článků primární články � poskytují velmi drahou energii � po proběhnutí chemické reakce jsou znehodnocené – vybité � nejběžnější je tzv. suchý článek

CHEMICKÉ REAKCE JAKO ZDROJ ELEKTRICKÉ ENERGIE sekundární články - akumulátory � mohou se mnohokrát opakovaně vybíjet a nabíjet � při nabíjení probíhá opačná reakce – el. proud se dodává � použití je hospodárné

KOROZE � proces, který probíhá na povrchu některých kovů za působení vzdušného kyslíku, vody � vzniká vrstva látek, která mění vlastnosti kovů � vzniká galvanický článek, který proces koroze urychluje a prohlubuje a) korozí vzniká souvislá vrstva, která brání další oxidaci např. Zn, Al, Cu

KOROZE b) korozí vzniká pórovitá vrstva, která kov nechrání, např. Fe ochrana před korozí zabránění přístupu vlhkosti a vzdušného kyslíku olej, vazelína, nátěry, smalt, pokovování stálejším kovem – Zn, Cu, Cr (pasivace)
- Slides: 10












