TECHNICK VYUIT ELEKTROLZY Chemick zmny probhajc na elektrodch

TECHNICKÉ VYUŽITÍ ELEKTROLÝZY

Chemické změny probíhající na elektrodách je možné v praxi využít různým způsobem: 1. galvanické články, 2. elektrometalurgie, 3. galvanostegie, 4. elektrolytický kondenzátor, 5. zábrana před vlhnutím zdiva, 6. koroze, atd.
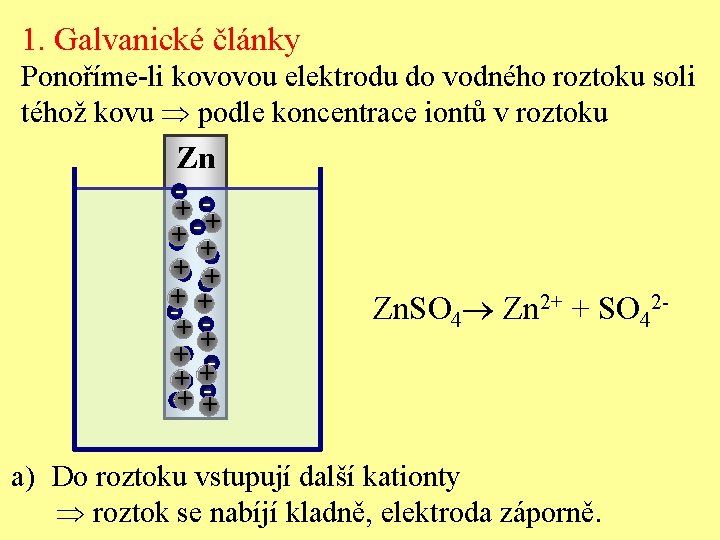
1. Galvanické články Ponoříme-li kovovou elektrodu do vodného roztoku soli téhož kovu podle koncentrace iontů v roztoku Zn - + -+ + - ++- + -+ ++ + +- +- +-+ + Zn. SO 4 Zn 2+ + SO 42 - a) Do roztoku vstupují další kationty roztok se nabíjí kladně, elektroda záporně.
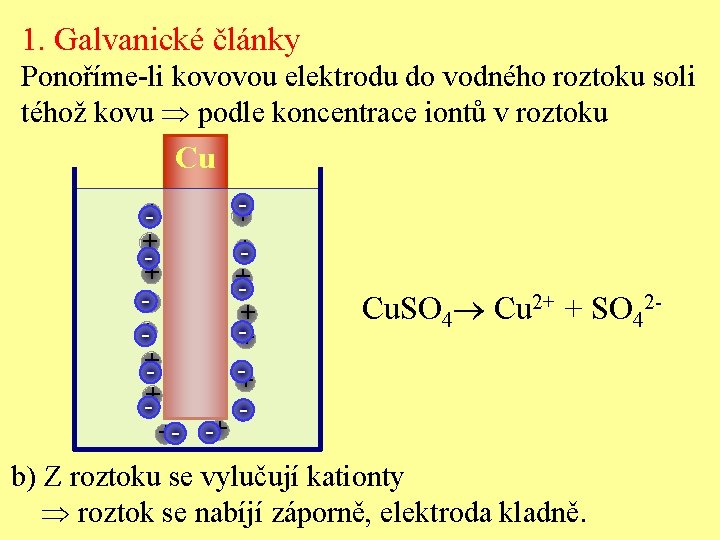
1. Galvanické články Ponoříme-li kovovou elektrodu do vodného roztoku soli téhož kovu podle koncentrace iontů v roztoku Cu + + + -+ -+ +- +++ - + -+ -+ Cu. SO 4 Cu 2+ + SO 42 - -+ - b) Z roztoku se vylučují kationty roztok se nabíjí záporně, elektroda kladně.

1. Galvanické články Ponoříme-li kovovou elektrodu do vodného roztoku soli téhož kovu podle koncentrace iontů v roztoku a) do roztoku vstupují kationty - roztok se nabíjí +, elektroda b) z roztoku se vylučují kationty - roztok se nabíjí -, elektroda + + a – náboje se navzájem přitahují na rozhraní kovu a elektrolytu vzniká tzv. elektrická dvojvrstva elektrické pole brání přechodu dalších iontů vzniká rovnovážný stav Elektrické napětí dvojvrstvy - tzv. elektrodový potenciál

1. Galvanické články Ponoříme-li kovovou elektrodu do vodného roztoku soli téhož kovu podle koncentrace iontů v roztoku a) do roztoku vstupují kationty - roztok se nabíjí +, elektroda b) z roztoku se vylučují kationty - roztok se nabíjí -, elektroda + + a – náboje se navzájem přitahují na rozhraní kovu a elektrolytu vzniká tzv. elektrická dvojvrstva elektrické pole brání přechodu dalších iontů vzniká rovnovážný stav Ponoření elektrody do jiného elektrolytu než do soli téhož kovu = obdobná situace také vylučování iontů do elektrolytu také vznik dvojvrstvy

1. Galvanické články 2 stejné elektrody v daném elektrolytu stejné elektrodové potenciály napětí mezi elektrodami = 0 V 2 chemicky různé elektrody v daném elektrolytu obecně různé elektrodové potenciály napětí mezi elektrodami ≠ 0 V – tzv. elektromotorické napětí
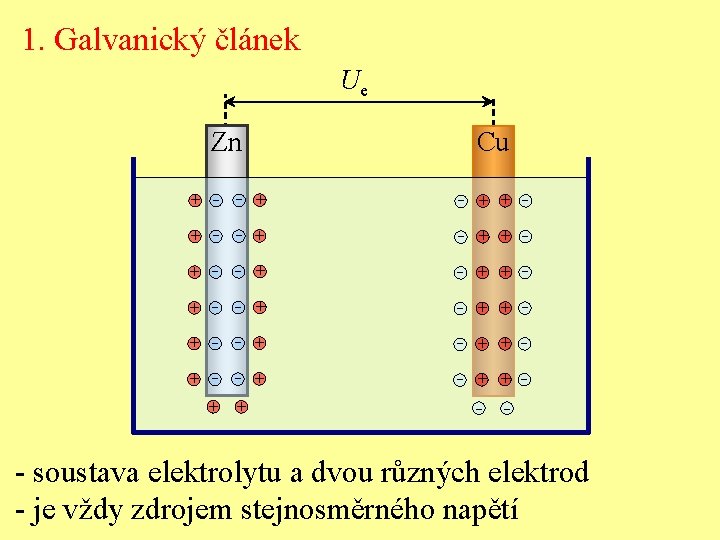
1. Galvanický článek Ue Zn Cu + - - + - + + - + - - + - + + - - - soustava elektrolytu a dvou různých elektrod - je vždy zdrojem stejnosměrného napětí

Stahy svalstva při doteku dvěma různými kovy Luigi Galvani (1737 -1798), italský lékař a přírodovědec
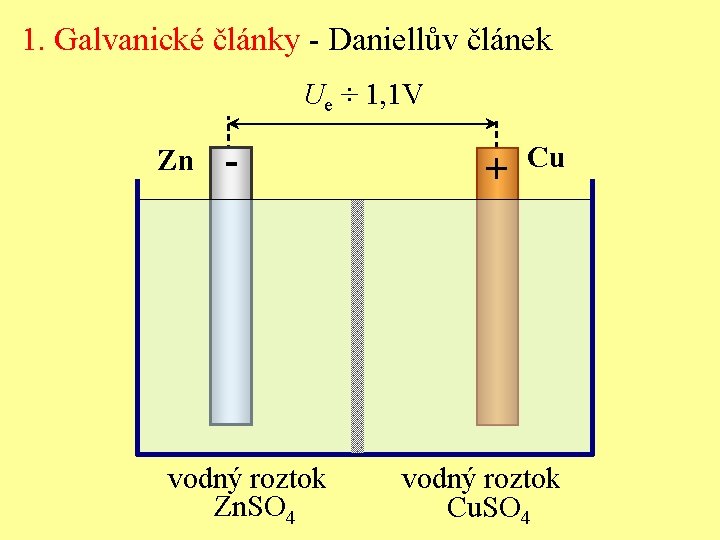
1. Galvanické články - Daniellův článek Ue ÷ 1, 1 V Zn - vodný roztok Zn. SO 4 + Cu vodný roztok Cu. SO 4
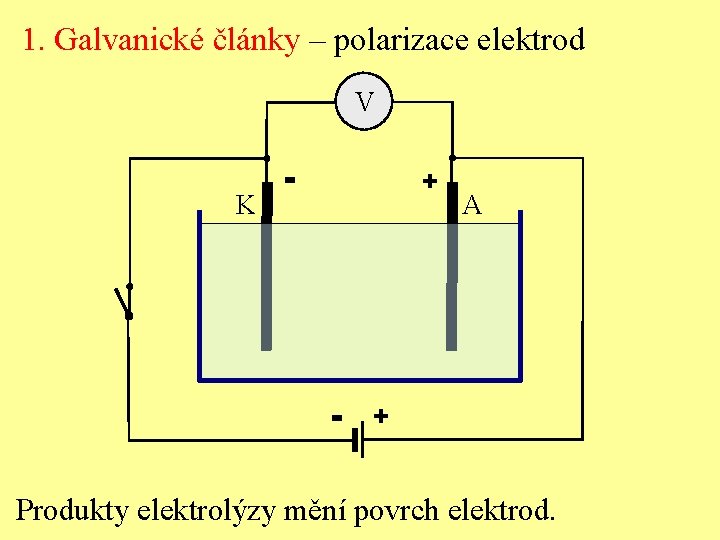
1. Galvanické články – polarizace elektrod V K - + - A + Produkty elektrolýzy mění povrch elektrod.

1. Galvanické články – polarizace elektrod Necháme určitou dobu probíhat elektrolýzu → odpojíme zdroj → místo něj zapojíme voltmetr ukáže, že anoda má vyšší potenciál než katoda připojeným obvodem teče proud opačným směrem uvnitř elektrolytu teče proud také = vlastní proud článku uvnitř elektrolytu je + na katodě, - na anodě → nastala tzv. polarizace elektrod → vznikl tzv. polarizační článek → napětí mezi A a K – tzv. polarizační napětí - tento jev se nazývá elektrolytická polarizace (elektrolýzou dochází ke změně chemického charakteru elektrod vznik nových dvojvrstev)

1. Galvanické články – polarizace elektrod Spojíme vodivě póly galvanického článku v článku probíhá elektrolýza způsobená vlastním proudem článku může nastat polarizace elektrod napětí článku postupně klesá – nestálý článek

1. Galvanické články – polarizace elektrod Voltův článek (Ue= 1 V): - Zn (H 2 SO 4 +H 2 O) Cu+ Elektrolýzou vzniká polarizační článek s elektromotorickým napětím opačné polarity. +Zn (H 2 SO 4 +H 2 O) H 2 - Vhodnou sestavou lze získat články, které se nepolarizují.

Sestrojil první zdroj dlouhotrvajícího elektrického proudu Allesandro Volta (1745 -1827), italský fyzik
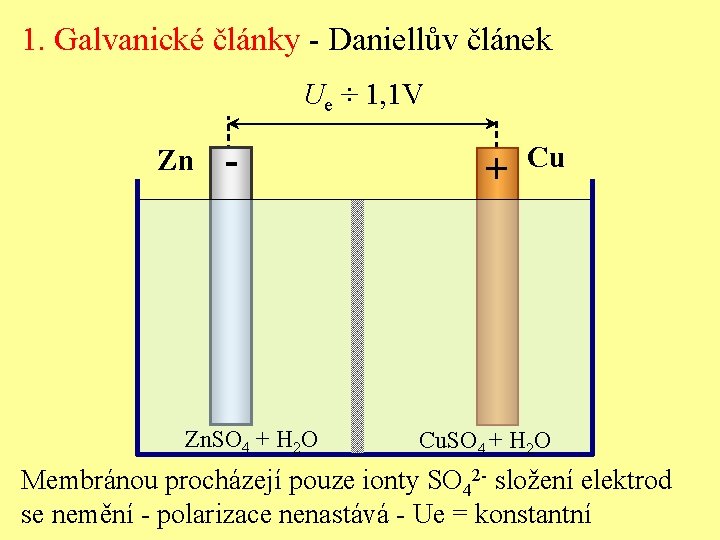
1. Galvanické články - Daniellův článek Ue ÷ 1, 1 V Zn - Zn. SO 4 + H 2 O + Cu Cu. SO 4 + H 2 O Membránou procházejí pouze ionty SO 42 - složení elektrod se nemění - polarizace nenastává - Ue = konstantní

1. Galvanické články - suchý článek Leclancheův článek (Ue= 1, 5 V): Složení: - uhlíková tyčka s mosaznou čepičkou (+), - salmiak (NH 4 Cl) zahuštěný škrobovým mazem, - zinková nádoba tvaru válečku (-).

1. Galvanické články - suchý článek Leclancheův článek (Ue= 1, 5 V): Složení: - uhlíková tyčka s mosaznou čepičkou (+), - salmiak (NH 4 Cl) zahuštěný škrobovým mazem, - zinková nádoba tvaru válečku (-). Depolarizátor = burel (Mn. O 2) - silné okysličovadlo - okysličuje vzniklý vodík na vodu - brání polarizaci uhlíkové elektrody.

1. Galvanické články - suchý článek Plochá baterie - tři suché články spojeny za sebou.

1. Galvanické články - akumulátor Primární galvanický článek – probíhají v něm nevratné elektrochemické děje Sekundární galvanický článek – probíhající elektrochemické děje jsou vratné – tzv. akumulátor Kapacita akumulátoru – součin proudu a doby, po kterou lze tento proud odebírat = náboj – jednotka A·h
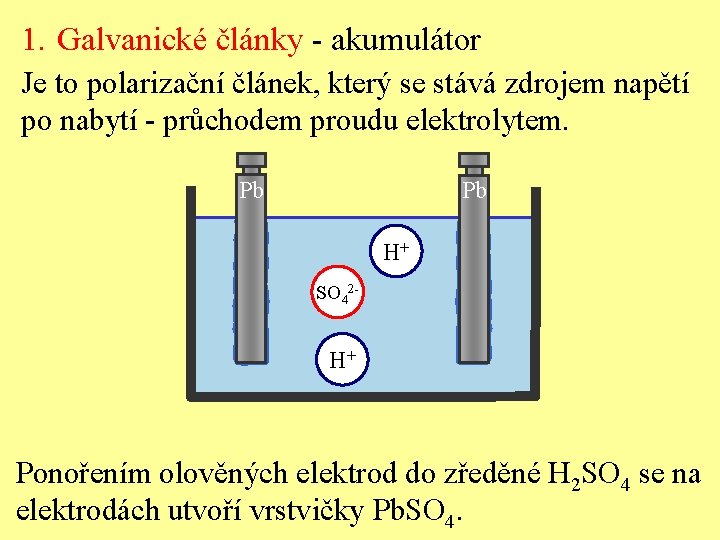
1. Galvanické články - akumulátor Je to polarizační článek, který se stává zdrojem napětí po nabytí - průchodem proudu elektrolytem. Pb Pb H+ SO 42 - H+ Ponořením olověných elektrod do zředěné H 2 SO 4 se na elektrodách utvoří vrstvičky Pb. SO 4.
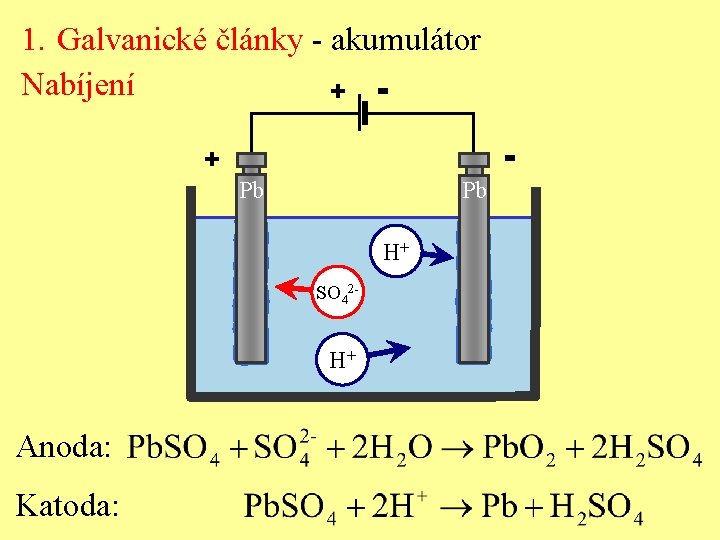
1. Galvanické články - akumulátor Nabíjení + + Pb Pb H+ SO 42 - H+ Anoda: Katoda: -
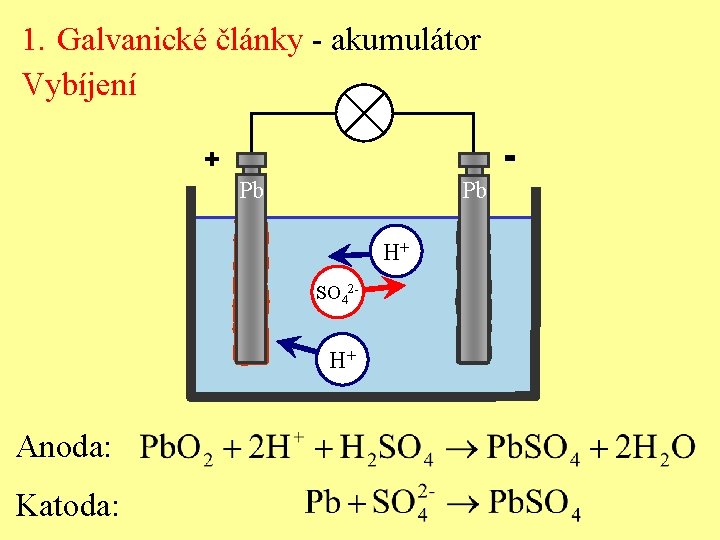
1. Galvanické články - akumulátor Vybíjení + Pb Pb H+ SO 42 - H+ Anoda: Katoda: -

1. Galvanické články Akumulátor Ni. Fe K – Fe A – Ni Elektrolyt - roztok 21% KOH + 5% Li. OH Ue = 1, 3 V Oproti olověnému -má větší kapacitu - má větší životnost -vydrží déle v nenabitém stavu -má větší vnitřní odpor

1. Galvanické články - akumulátorová baterie Akumulátorová baterie - jsou akumulátory spojeny za sebou.
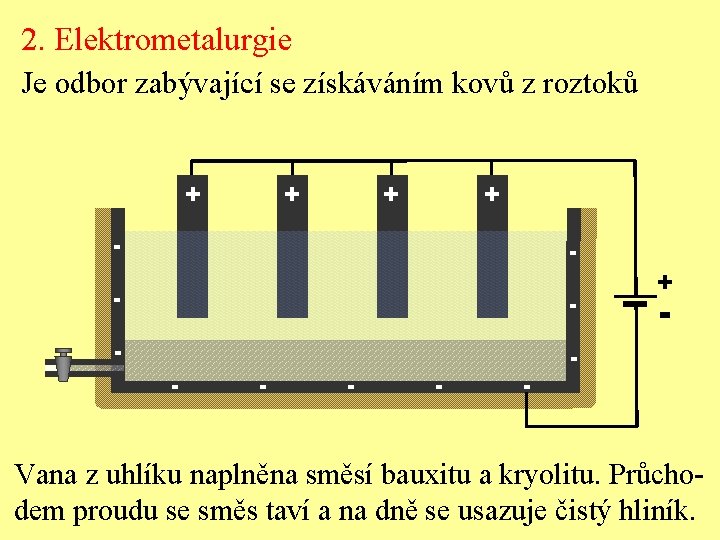
2. Elektrometalurgie Je odbor zabývající se získáváním kovů z roztoků + + - - - + + + Vana z uhlíku naplněna směsí bauxitu a kryolitu. Průchodem proudu se směs taví a na dně se usazuje čistý hliník.
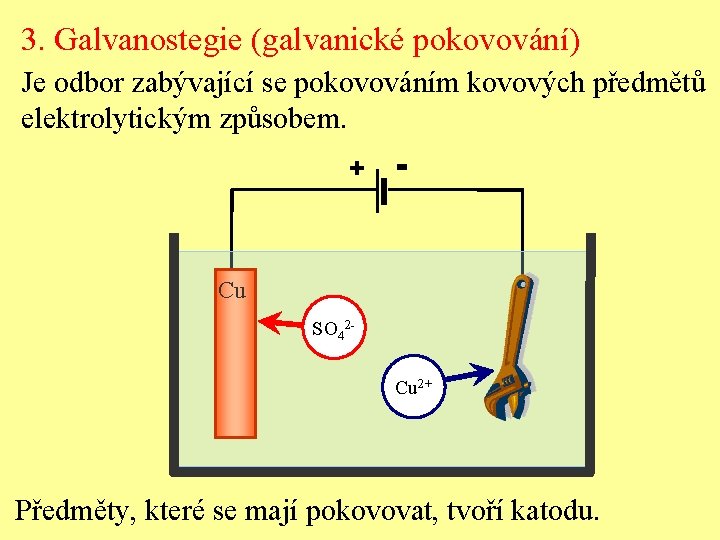
3. Galvanostegie (galvanické pokovování) Je odbor zabývající se pokovováním kovových předmětů elektrolytickým způsobem. + - Cu SO 42 Cu 2+ Předměty, které se mají pokovovat, tvoří katodu.

3. Galvanostegie (galvanické pokovování)
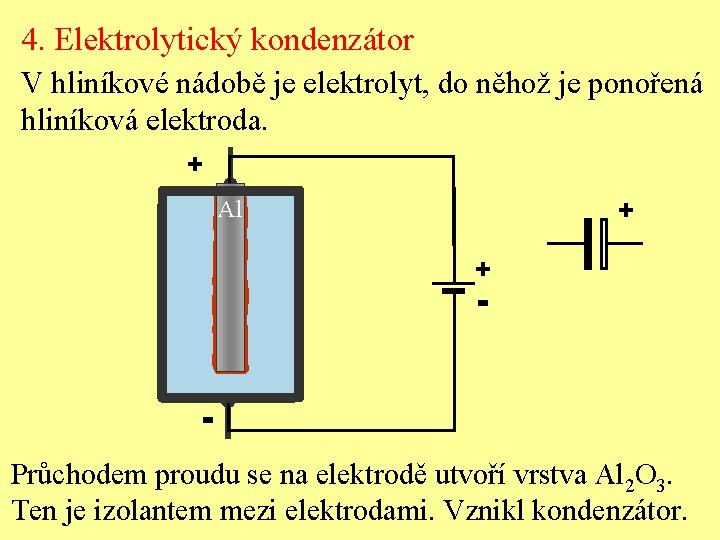
4. Elektrolytický kondenzátor V hliníkové nádobě je elektrolyt, do něhož je ponořená hliníková elektroda. + + Al + - Průchodem proudu se na elektrodě utvoří vrstva Al 2 O 3. Ten je izolantem mezi elektrodami. Vznikl kondenzátor.
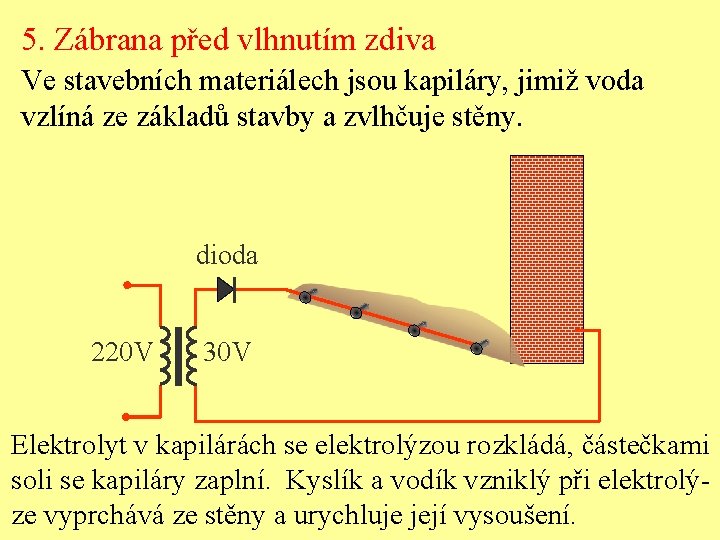
5. Zábrana před vlhnutím zdiva Ve stavebních materiálech jsou kapiláry, jimiž voda vzlíná ze základů stavby a zvlhčuje stěny. dioda 220 V 30 V Elektrolyt v kapilárách se elektrolýzou rozkládá, částečkami soli se kapiláry zaplní. Kyslík a vodík vzniklý při elektrolýze vyprchává ze stěny a urychluje její vysoušení.

6. Koroze Porušení povrchu kovu chemickým nebo elektrochemickým působením. Nejčastějším typem koroze je oxidace kovů účinkem vzdušného kyslíku a vlhkostí vzduchu. Kov, který tvoří anodu se naleptává.
- Slides: 31