Elektrolza Hradec 2018 Karel Heman Pbram Elektrolza Elektrolza

Elektrolýza Hradec 2018 Karel Heřman, Příbram
Elektrolýza

Elektrolýza • Základní pojmy : – Elektrolyt – Elektrody – Elektrolytická disociace – Elektrolýza

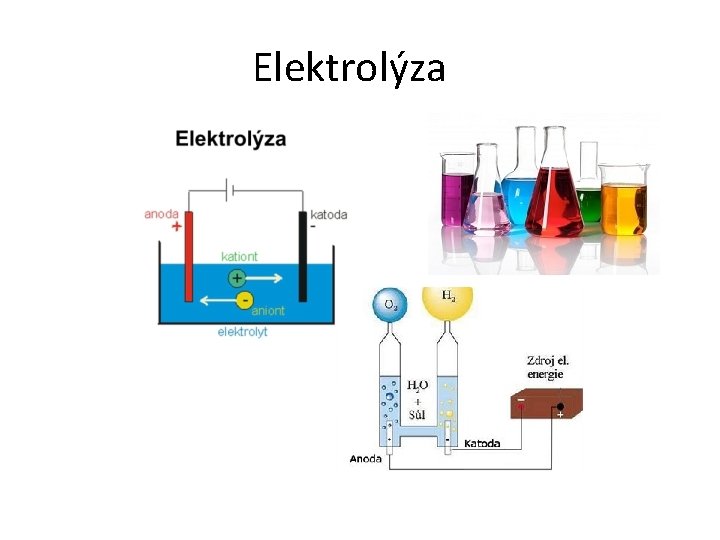
Elektrolýza je děj, který probíhá na elektrodách při průchodu stejnosměrného el. proudu elektrolytem Elektrolyt je roztok nebo tavenina – obsahuje volně pohyblivé ionty (kationty, anionty), díky kterým vedou el. proud Elektroda je propojení pevného obvodu a elektrolytu Elektrolytická disociace je proces vzniku iontů v roztoku

Elektrolýza Alessandro Volta (1745 -1827 Trocha Historie • • Celým jménem Alessandro Giuseppe Antonio Anastasio Volta Vynalezl elektrický článek, kondenzátor Pracoval jako profesor na univerzitě v Pávii Jeho příznivcem byl i Napoleon Luigi Galvani (1737 -1798) Celý život prožil v italské Boloni Studoval technologii, později medicínu Prováděl pokusy s živočišnou elektřinou

Elektrolýza Trocha Historie Anglický fyzik, chemik a velký experimentátor Michael Faraday se narodil 22. září 1791 nedaleko Londýna (v Newington Butts) v chudé rodině kováře (James Faraday). • Michael Faraday objevil elektromagnetickou indukci, elektromagnetické rotace, magneto-optický efekt, diamagnetismus a mnoho dalších jevů. • Základní zákony elektrolýzy. • Třísvazkový soubor experimentálních výzkumů o elektřině Experimental Researches in Electricity.

Faradayovy zákony pro elektrolýzu • 1. Faradayův zákon: Hmotnost m vyloučené látky je přímo úměrná součinu stálého proudu I a doby t, po kterou proud elektrolytem procházel m = A. I. t • 2. Faradayův zákon: Elektrochemický ekvivalent látky vypočteme, jestliže její molární hmotnost vydělíme Faradayovou konstantou a počtem elektronů potřebných k vyloučení jedné molekuly: [kde F je Faradayova konstanta F = 9, 6481× 104 C. mol− 1 a z je počet (mocenství) elektronů, které jsou potřeba při vyloučení jedné molekuly (např. pro Cu 2+ → Cu je z = 2, pro Ag+ → Ag je z = 1)]

Faradayovy zákony pro elektrolýzu Látková množství různých látek vyloučených při elektrolýze týmž nábojem jsou chemicky ekvivalentní. (Mohou se navzájem nahradit v chemické sloučenině nebo se mohou bezezbytku sloučit. ) - Veličina F = NAe ≈ 9, 6485· 104 C·mol-1 je Faradayova konstanta - Konstanta úměrnosti A, která je pro danou látku charakteristická, se nazývá elektrochemický ekvivalent látky; jednotkou je kg·C-1

Technické využití elektrolýzy • Vylučování kovů na katodě při elektrolýze se užívá v elektrometalurgii k získávání kovů z roztoků, v galvanostegii k pokovování, v galvanoplastice k vytváření odlitků, matric na výrobu gramofonových desek apod. • Velké použití má elektrolytický kondenzátor, který tvoří dvě hliníkové nebo tantalové fólie, mezi nimiž je vrstva papíru napuštěná elektrolytem, na jedné fólii se elektrochemicky vytvoří tenká vrstva oxidu, která slouží jako dielektrikum, vzhledem k malé tloušťce dielektrika mají tyto kondenzátory poměrně velkou kapacitu – řádově 10 -6 F až 10 -2 F • Zoxidovaná fólie elektrolytického kondenzátoru musí být zapojována do místa s vyšším potenciálem, jinak by se kondenzátor zničil (může dojít i k výbuchu, při němž se kondenzátor roztrhne)

Co nás čeká? • • Základní elektrolýza Odpor elektrolytu „Elektrolytický dělič napětí“ Ohmův zákon v elektrolýze I. typ Ohmův zákon v elektrolýze II. typ (Hofmannův př. ) Vliv mg pole na pohyb iontů v elektrolytu Elektrolytický motor Elektrolýza v injekční stříkačce
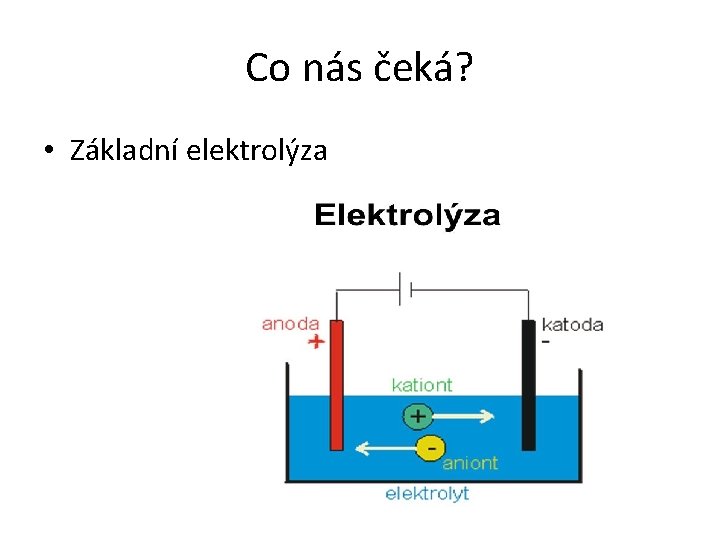
Co nás čeká? • Základní elektrolýza

Co nás čeká? • Odpor elektrolytu Závislost na – vzdálenosti elektrod - ploše elektrod - typu elektrolytu (množství iontů v něm )
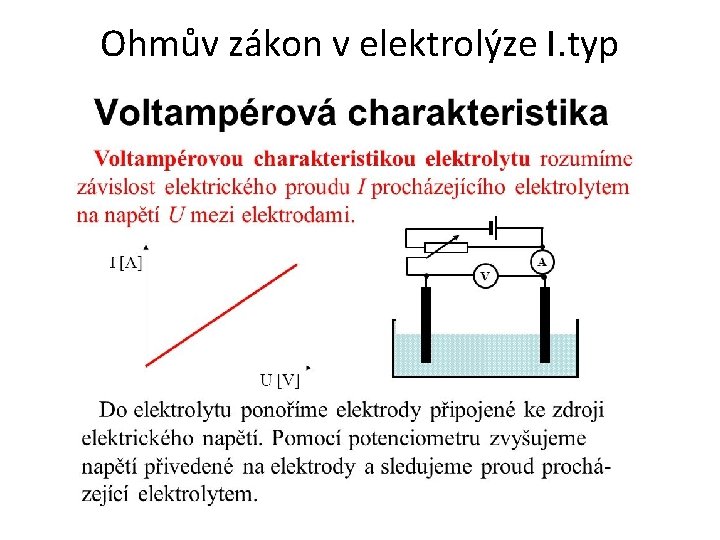
Ohmův zákon v elektrolýze I. typ
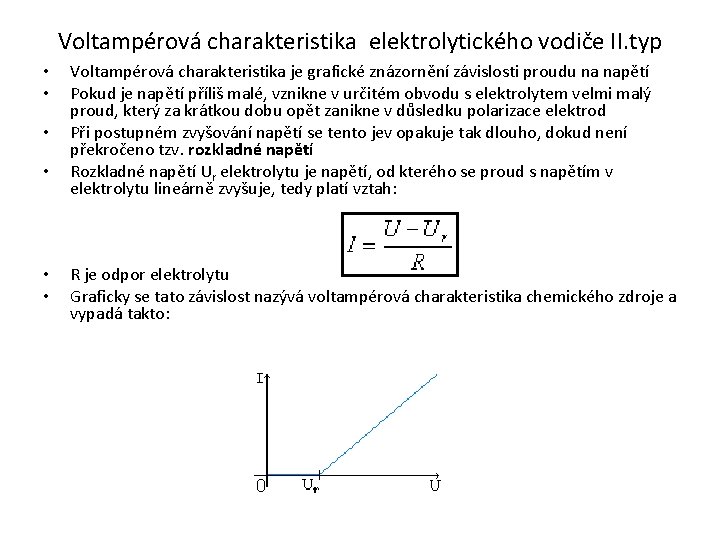
Voltampérová charakteristika elektrolytického vodiče II. typ • • • Voltampérová charakteristika je grafické znázornění závislosti proudu na napětí Pokud je napětí příliš malé, vznikne v určitém obvodu s elektrolytem velmi malý proud, který za krátkou dobu opět zanikne v důsledku polarizace elektrod Při postupném zvyšování napětí se tento jev opakuje tak dlouho, dokud není překročeno tzv. rozkladné napětí Rozkladné napětí Ur elektrolytu je napětí, od kterého se proud s napětím v elektrolytu lineárně zvyšuje, tedy platí vztah: R je odpor elektrolytu Graficky se tato závislost nazývá voltampérová charakteristika chemického zdroje a vypadá takto:

II. Typ

Co nás čeká? • Vliv mg pole na pohyb iontů v elektrolytu • Elektrolytický motor

Co nás čeká? • Elektrolýza v injekční stříkačce
- Slides: 17