ELEKTROLZA Elektrolza je redoxn dj probhajc na elektrodch

ELEKTROLÝZA

Elektrolýza je redoxní děj probíhající na elektrodách při průchodu stejnosměrného proudu roztokem nebo taveninou, který musí obsahovat volně pohyblivé ionty (kationty, anionty). Elektrolýza je přeměna elektrické energie na chemickou.

Elektrolýza Kationty se pohybují k záporně nabité elektrodě katodě. Anionty se pohybují ke kladně nabité elektrodě anodě. Elektrolýza se průmyslově využívá k výrobě kovů, pokovování a k čištění kovů.
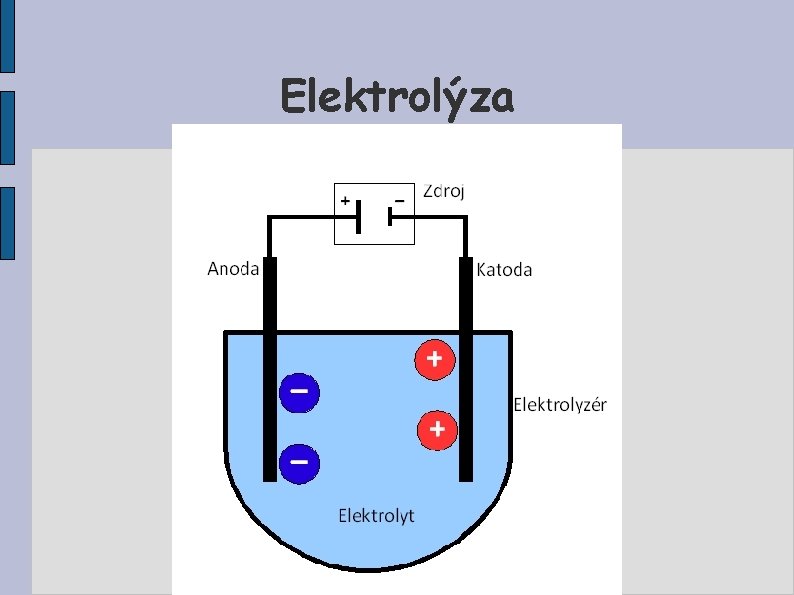
Elektrolýza

Výroba mědi Elektrolýza roztoku chloridu měďnatého Cu. Cl 2. Roztok Cu. Cl 2 + uhlíkové elektrody (4 – 6 V) Cu. Cl 2 Cu 2+ + 2 Cl 1 Anoda: 2 Cl 1 - - 2 e. Katoda: Cu 2+ + 2 e- Cl 20 oxidace Cu 0 redukce

Výroba hliníku Elektrolýza taveniny oxidu hlinitého Al 2 O 3 (bauxit). Roztok Al 2 O 3 + uhlíkové elektrody Al 2 O 3 2 Al 3+ + 3 O 2 Anoda: 3 O 2 - - 6 e. Katoda: 2 Al 3+ + 6 e- O 0 Al 0 oxidace redukce

Výroba zinku Elektrolýza roztoku jodidu zinečnatého Zn. I 2. Roztok Zn. I 2 + uhlíkové elektrody (9 – 12 V) Zn. I 2 Zn 2+ + 2 I 1 Anoda: 2 I 1 - - 2 e. Katoda: Zn 2+ + 2 e- I 20 Zn 0 oxidace redukce

Elektrolýza roztoku chloridu sodného (výroba chloru, vodíku a hyd. sodného) Vodný roztok Na. Cl + uhlíkové elektrody 2 Na. Cl + 2 H 2 O Cl 2 + H 2 + 2 Na. OH 2 Na+ + 2 Cl- + 2 H+ + 2 OH 2 Na. OH Anoda: 2 Cl- - 2 e. Cl 2 oxidace + Katoda: 2 H + 2 e. H 2 redukce Vznik roztoku hydroxidu sodného: 2 Na+ + 2 OH 2 Na. OH (odpařováním vznikne čistý hydroxid sodný)

Použité zdroje: BENEŠ, Pavel a kol. Základy praktické chemie pro 9. ročník základní školy. Praha: Fortuna, 2003. ISBN 80 -7168 -880 -0. Wikipedie, Internetová encyklopedie [online]. Praha, 2002 [cit. 2011 -07 -15]. Dostupné z WWW: <http: //www. wikipedia. cz>. Snímek 1: Domáca elektrolýza | Zábavná chémia: [online]. 2011 [cit. 2011 -08 -22]. Domáca elektrolýza | Zábavná chémia: . Dostupné z WWW: <http: //nd 04. jxs. cz/527/666/776523 c 6 d 4_71407492_o 2. jpg >. Snímek 3: Sbírka řešených úloh z fyziky: [online]. 2011 [cit. 2011 -08 -22]. Sbírka řešených úloh z fyziky: . Dostupné z WWW: <http: //fyzikalniulohy. cz/_upload/00157/elektrolyza. gif>. Snímek 4: Wikipedie, otevřená encyklopedie: [online]. 2011 [cit. 2011 -08 -22]. Elektrolýza - Wikipedie: . Dostupné z WWW: <http: //upload. wikimedia. org/wikipedia/commons/3/3 b/Elektrol%C 3%BDza. jpeg>.
- Slides: 9