Cap 8 I composti chimici inorganici Gli elementi









- Slides: 17

Cap. 8 I composti chimici inorganici

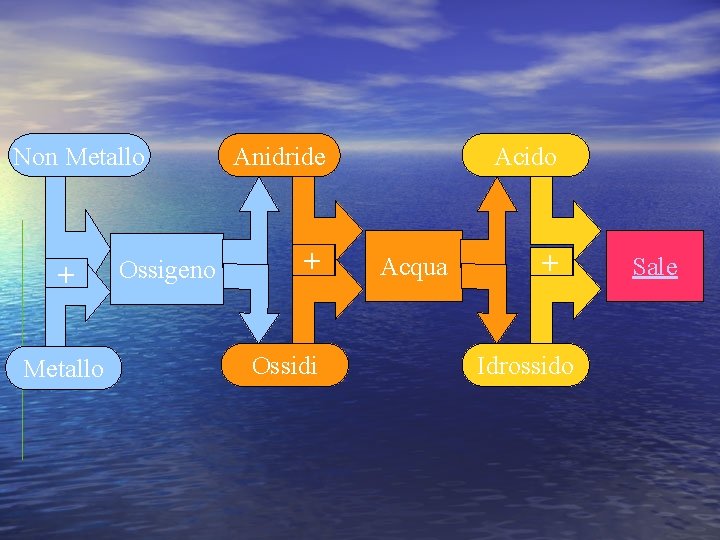
Gli elementi si possono suddividere in due gruppi metalli e non metalli Combinando un non metallo con l’ossigeno otteniamo un’anidride Combinando un metallo con l’ossigeno otteniamo un ossido Combinando un non metallo con l’acqua otteniamo un ossiacido o acido Combinando un metallo con l’acqua otteniamo un idrossido o base Combinando un idrossido con l’idracido otteniamo un sale con una reazione di condensazione che libera una molecola di acqua

Non Metallo + Metallo Ossigeno Anidride + Ossidi Acido Acqua + Idrossido Sale

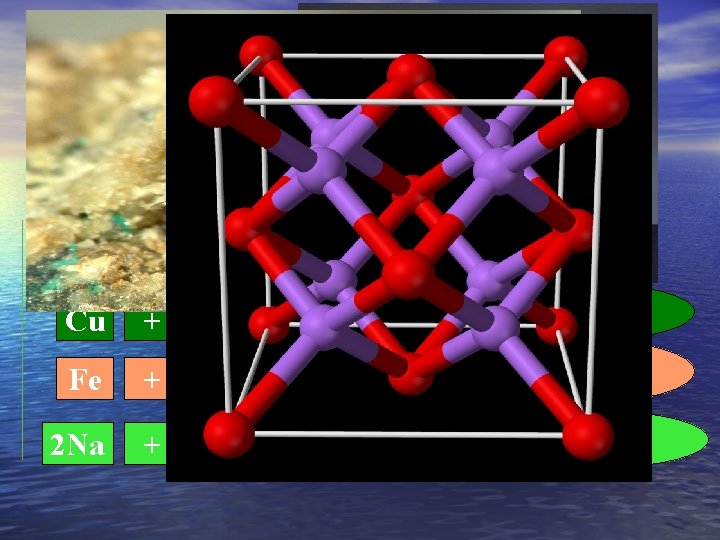
Gli Ossidi • Gli ossidi derivano dalla reazione di un metallo con l'ossigeno (reazione di ossidazione) Ca + O Ca. O (Ossido di calcio) Cu + O Cu. O Fe + O Fe. O 2 Na + O Tenorite Ossido di Na 2 O rame Ossido di ferro Ossido di sodio

Uraninite UO 2 Ematite Fe 2 O 3 Brookite Ti. O 2 Cuprite Cu 2 O Anatasio Ti. O 2 Rutilo Baddeleyte Ti. O 2 Zr O 2

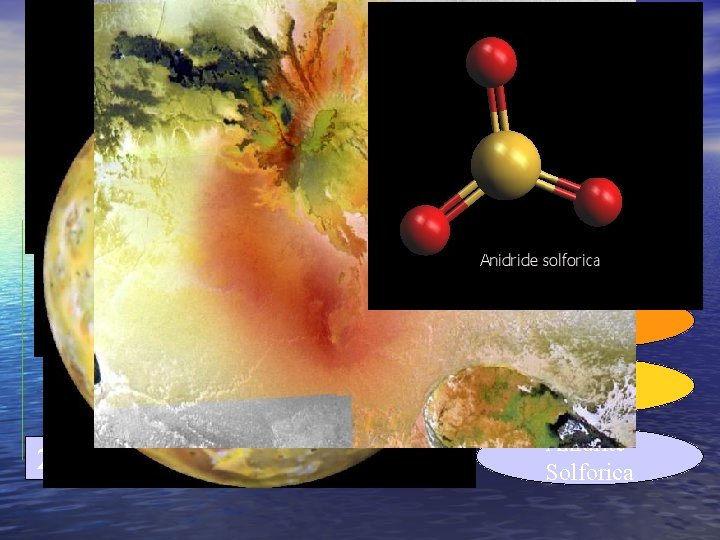
Le Anidridi • Le Anidridi derivano dalla reazione di un non metallo con l'ossigeno • Mentre gli ossidi sono generalmente solidi le anidridi sono gassose C S 2 S + + O 2 + 3 O 2 CO 2 Anidride carbonica SO 2 Anidrite Solforosa 2 SO 3 Anidrite Solforica

Le Basi o idrossidi • Le basi si ottengono facendo reagire gli ossidi con l'acqua Ca. O + H 2 O Ca(OH)2 Idrossido di calcio La Caratteristica degli idrossidi è quella di Portlandite Ca(OH)2 possedere un gruppi (OH) detto radicale ossidrilico di valenza 1 Gli idrossidi saranno formati da un metallo e gruppi (OH)

Fe. O Al 2 O 3 Na 2 O B 2 O 3 + H 2 O + 3 H 2 O + H 2 O Brucite Bernalite + 3 H 2 O Fe(OH)2 2 Al(OH)3 2 Na(OH) 2 B (OH)3 Idrossido di ferro Idrossido di alluminio Idrossido di sodio Gibsite Idrossido di boro

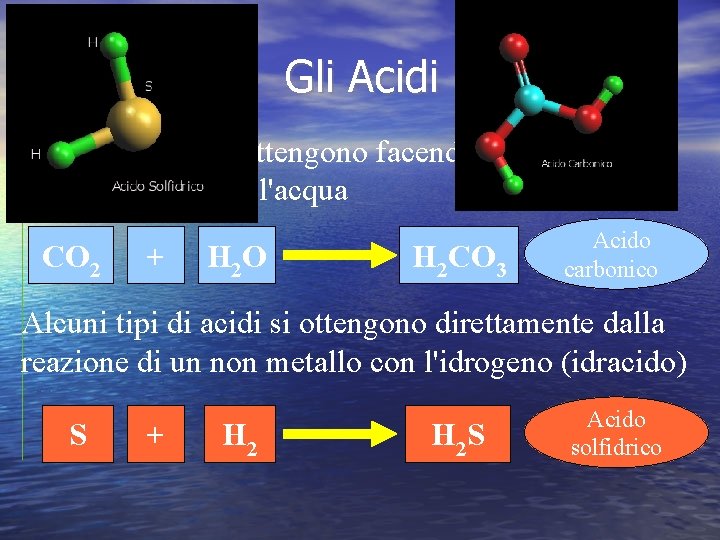
Gli Acidi Gli acidi si ottengono facendo reagire un anidride con l'acqua CO 2 + H 2 O H 2 CO 3 Acido carbonico Alcuni tipi di acidi si ottengono direttamente dalla reazione di un non metallo con l'idrogeno (idracido) S + H 2 S Acido solfidrico

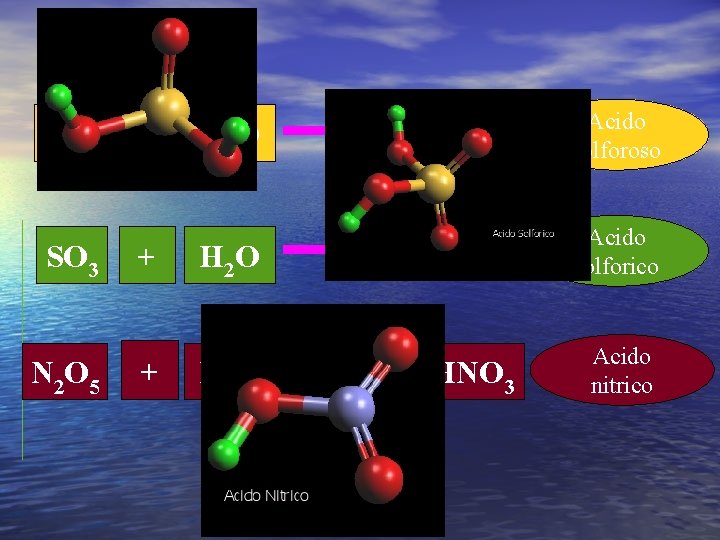
SO 2 SO 3 N 2 O 5 + + + H 2 O H 2 SO 3 Acido solforoso H 2 SO 4 Acido solforico 2 HNO 3 Acido nitrico

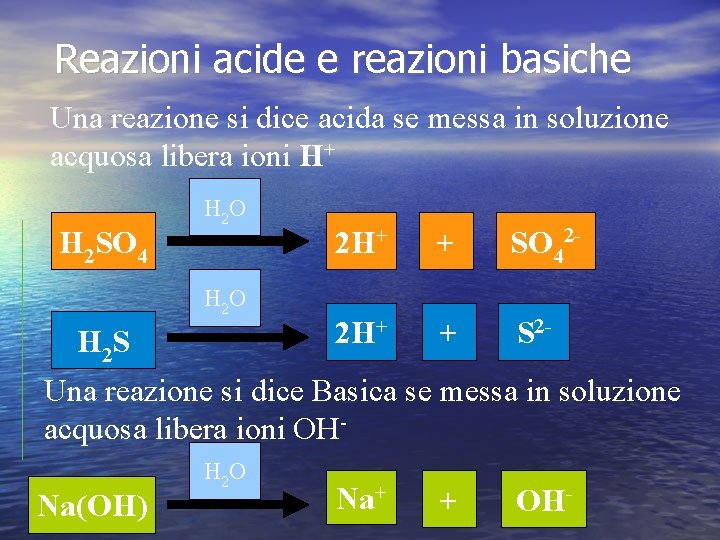
Reazioni acide e reazioni basiche Una reazione si dice acida se messa in soluzione acquosa libera ioni H+ H 2 SO 4 H 2 O H 2 S 2 H+ + SO 42 - 2 H+ + S 2 - Una reazione si dice Basica se messa in soluzione acquosa libera ioni OHNa(OH) H 2 O Na+ + OH-

I Sali I sali si ottengono facendo reagire un acido con una base Un sale si ottiene anche facendo reagire un metallo con l'acido base + acido = sale + acqua metallo + acido = sale + idrogeno

Halite + gesso Siderite + Ca. CO H 2 O Ca(OH)2 + H 2 CO 3 Ca(OH)2 + 2 HF Ca. F 2 + H 2 O Na. OH + HCl Na. Cl + H 2 O Fe + H 2 CO 3 Fe. CO 3 + H 2 3 Fluorite Calcite

Riassumiamo • calcio + ossigeno ossido di calcio • potassio + ossigeno ossido di potassio • Ossido di calcio + acqua idrossido di calcio • Ossido di potassio + acqua idrossido di potassio • Carbonio + ossigeno anidride carbonica • Zolfo +6 + ossigeno –> anidride solforica • Anidride carbonica + acqua acido carbonico • Anidride solforica + acqua acido solforico • Acido cloridrico + idrossido di sodio cloruro di sodio + acqua • Acido solforico + idrossido di calcio solfato di calcio + acqua

Acidi basi e sapore • Molte sostanze che a noi piacciono sono acide (limonata, aranciata, coca – cola) • Normalmente noi riconosciamo le sostanze acide dal sapore aspro • Non sono molti gli alimenti basici, un esempio è il caffè che e amaro • L’acqua che non ha sapore è neutra H 2 O H+ + OH- Una soluzione si dice neutra se libera esattamente lo stesso numero di ioni H+ e OH-

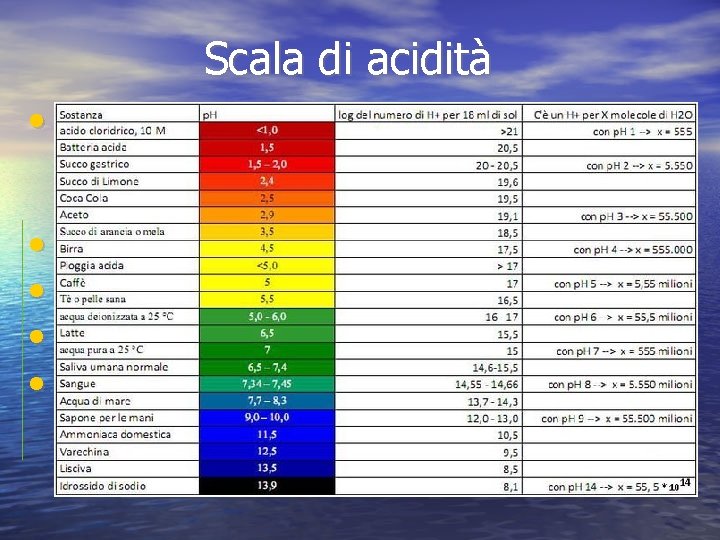
Scala di acidità • La scala di acidità (p. H) va da 0 a 14 a seconda del grado di acidità o basicità di una soluzione • Per p. H < 7 la soluzione è acida • Per p. H = 7 la soluzione è neutra • Per p. H > 7 la soluzione è basica • Per sapere se una soluzione è acida o basica si usano gli indicatori (cartine di tornasole)

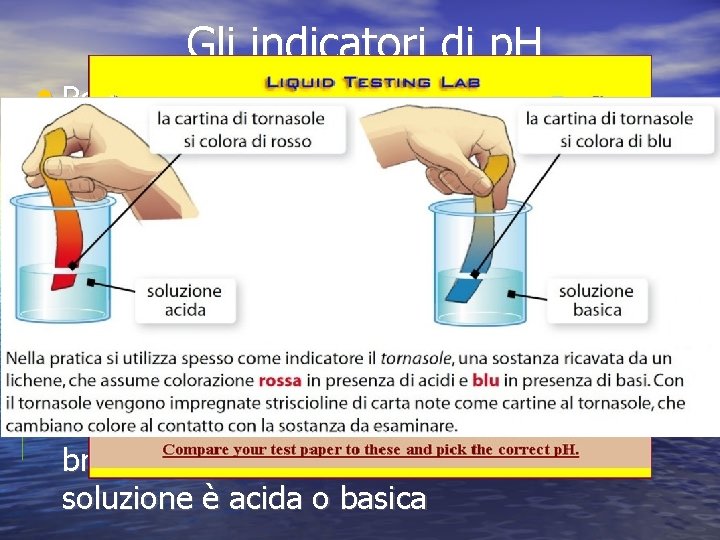
Gli indicatori di p. H • Per sapere il p. H di una soluzione si usano gli indicatori universali che è una cartina in grado di cambiare colore quando viene a contatto con una soluzione • Si bagna la cartina, si fa asciugare, poi si confronta il colore ottenuto con una scala cromatica e si stabilisce il valore del p. H • Altri tipi di indicatori come la cartina di tornasole, il metilarancio e il blu di bromotimolo ci dicono solo se una soluzione è acida o basica