BLEK FORMLLERNN YAZILMASI VE ADLANDIRILMASI METALLER AMETALLER SOYGAZLAR

BİLEŞİK FORMÜLLERİNİN YAZILMASI VE ADLANDIRILMASI
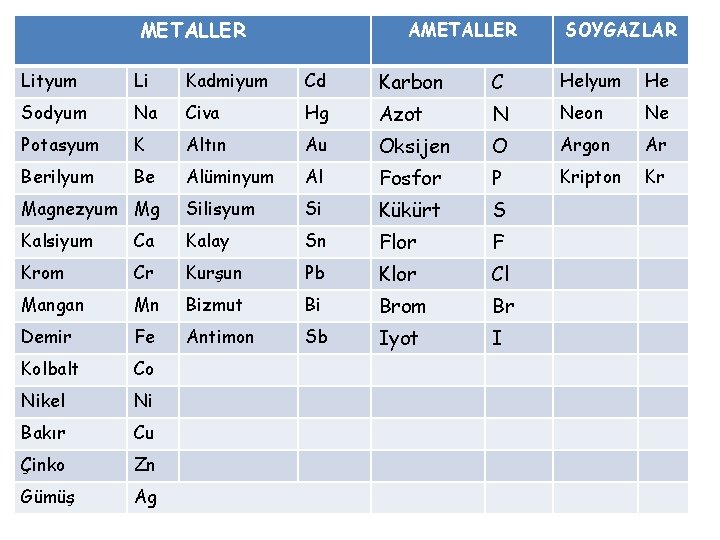
METALLER AMETALLER SOYGAZLAR Lityum Li Kadmiyum Cd Karbon C Helyum He Sodyum Na Civa Hg Azot N Neon Ne Potasyum K Altın Au Oksijen O Argon Ar Berilyum Be Alüminyum Al Fosfor P Kripton Kr Magnezyum Mg Silisyum Si Kükürt S Kalsiyum Ca Kalay Sn Flor F Krom Cr Kurşun Pb Klor Cl Mangan Mn Bizmut Bi Brom Br Demir Fe Antimon Sb Iyot I Kolbalt Co Nikel Ni Bakır Cu Çinko Zn Gümüş Ag
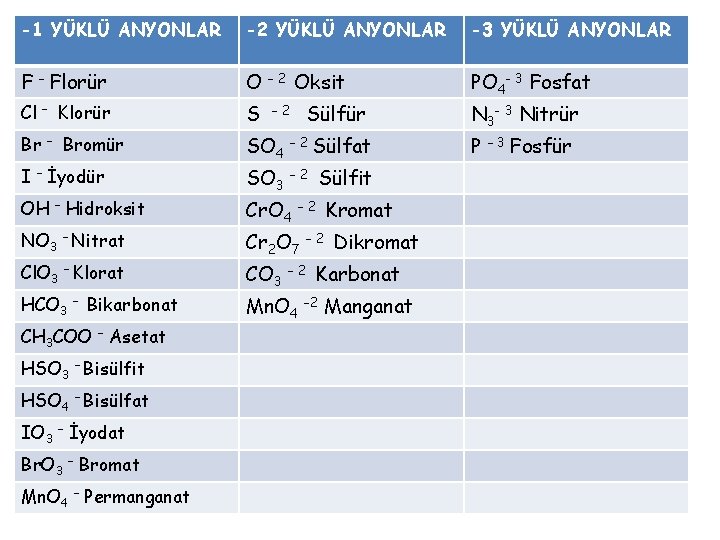
-1 YÜKLÜ ANYONLAR -2 YÜKLÜ ANYONLAR -3 YÜKLÜ ANYONLAR F – Florür O – 2 Oksit PO 4 - 3 Fosfat Cl S N 3 - 3 Nitrür – Klorür – 2 Sülfür Br – Bromür SO 4 – 2 Sülfat I – İyodür SO 3 – 2 Sülfit OH – Hidroksit Cr. O 4 – 2 Kromat NO 3 – Nitrat Cr 2 O 7 – 2 Dikromat Cl. O 3 – Klorat CO 3 – 2 Karbonat HCO 3 – Bikarbonat Mn. O 4 – 2 Manganat CH 3 COO – Asetat HSO 3 – Bisülfit HSO 4 – Bisülfat IO 3 – İyodat Br. O 3 – Bromat Mn. O 4 – Permanganat P – 3 Fosfür
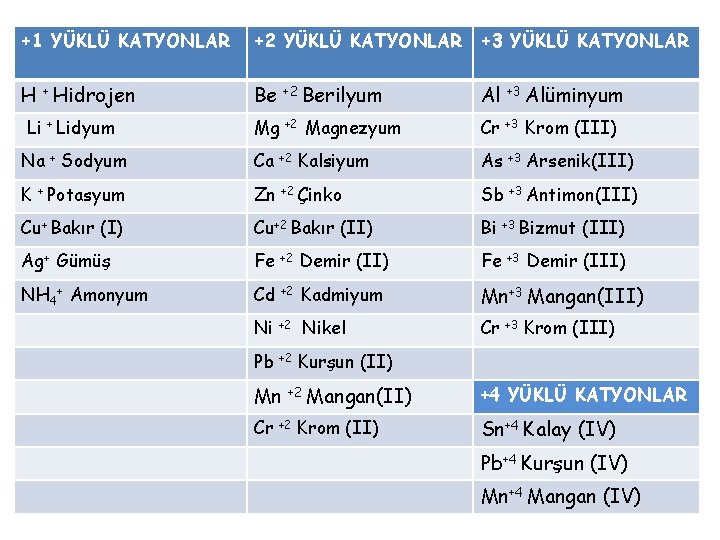
+1 YÜKLÜ KATYONLAR +2 YÜKLÜ KATYONLAR +3 YÜKLÜ KATYONLAR H + Hidrojen Be +2 Berilyum Al Li + Lidyum Mg +2 Magnezyum Cr +3 Krom (III) Na + Sodyum Ca K + Potasyum Zn +2 Çinko Sb +3 Antimon(III) Cu+ Bakır (I) Cu+2 Bakır (II) Bi +3 Bizmut (III) Ag+ Gümüş Fe Fe NH 4+ Amonyum Cd +2 Kadmiyum Mn+3 Mangan(III) Ni +2 Nikel Cr +3 Krom (III) +2 +2 Kalsiyum Demir (II) As +3 +3 +3 Alüminyum Arsenik(III) Demir (III) Pb +2 Kurşun (II) Mn +2 Mangan(II) Cr +2 Krom (II) +4 YÜKLÜ KATYONLAR Sn+4 Kalay (IV) Pb+4 Kurşun (IV) Mn+4 Mangan (IV)

BİLEŞİKLER En az 2 farklı cins atomdan oluşmuş maddelere denir. Kimyasal yöntemlerle daha basit bileşenlerine ayrıştırılabilir. Bileşiklerin Genel Özellikleri: • Homojen maddedirler. • Bileşikteki elementlerin kütleleri arasında sabit bir oran vardır. • Bileşikler formülle gösterilir. • Bir bileşiğin molekül formülünden, bileşiği oluşturan elementlerin cinsleri, sayıları ve birleşme oranları anlaşılır. • Bileşiklerin ayırt edici özellikleri vardır. • Bileşiği oluşturan elementler, kendi kimyasal özelliklerini kaybederler. • Bileşikler, bileşenlerine ancak kimyasal yollarla ayrıştırılabilirler.

Moleküller kendini meydana getiren atomlardan farklı kimyasal özellik gösterirler. Bu yüzden bileşik kedini oluşturan farklı özelliktedir. Bileşikler katı sıvı ve gaz fazında bulunabilirler. Bileşiği elementten ayıran temel özellik; kimyasal reaksiyonlarla daha basit yapıda maddelere, hatta elementlere ayrışabilmeleridir. Bileşiği karışımdan ayıran temel özellik ise; saf olması, yapısında elementlerin belli oranlarda bulunması, kendini meydana getiren elementlerden tamamen farklı fiziksel kimyasal özellik göstermesidir. ve

BİLEŞİK FORMÜLLERİ Bir bileşiğin moleküllerindeki atomlar ve bunların sayıları farklı şekilde gösterilebilir. Molekül şekil olarak modellerle gösterilebileceği gibi açık, yarı açık ve kapalı formüllerle de gösterilebilir. Açık formüllere yarı formülde denir. Bunlara atomların birbiriyle yaptıkları bağlar da belirtilebilmektedir. Fakat reaksiyon kimyasında daha çok kapalı formül kullanılır. Al. Cl 3 yazılışında atomların ad ve sayıları belirtilmiştir. Al. Cl 3 molekülü; bir alüminyum ve 3 adet klor atomundan oluşur.

Kaba formülle molekül formülü arasındaki farkın anlaşılmasında yarar vardır. Kaba formül sadece bileşiği oluşturan elementlerin bileşikteki bağıl atom sayıları arasındaki oranı gösterir. Fakat gerçekte bileşiğin moleküllerinde kaçar atom bulunduğunu ifade etmez. Molekül formülü ise bileşiğin molekülündeki atomların gerçek sayısını gösterir. Gerçek formül veya kimyasal formül olarak da adlandırılır.

BİLEŞİKLERİN ADLANDIRILMASI 1 -Metal-Ametal İkili Bileşiklerinin Adlandırılması İyonik karakterli metal-ametal ikili bileşiklerinin adlandırılmasında şu kural izlenir; 1) Metalin adı olduğu gibi söylenir, 2) Ametalin adının sonuna “ür” eki getirilir. ***Not: Farklı değerliklere sahip metal iyonları farklı formüllere sahip bileşikler oluşturacağı için, bunların isimlendirilmesinde, metal iyonunun yükseltgenme basamağı da belirtilir.

Dikkat edilmesi gereken nokta, bileşiklerin oluşumunda elektriksel olarak nötralliğin sağlanmış olduğudur. Na. Cl: Sodyum klorür Kalsiyum Nitrür: Ca 3 N 2 Mg. I 2: Magnezyum iyodür Alüminyum oksit: Al 2 O 3 Farklı değerlikler içeren metal-ametal ikili bileşiklerinin adlandırılması Fe. Cl 3: Demir(III) klorür Fe. Cl 2: Demir (II) klorür Sn(NO 3)2: Kalay (II) nitrat Sn(NO 3)4: Kalay (IV) nitrat

2 -İki Ametalden Oluşan Bileşiklerinin Adlandırılması Bu bileşikler adlandırılırken; 1. Ametalin sayısı + Adı + 2. Ametalin sayısı + Adı + “ür” Eki Sayıların Latince Karşılıkları; 1. Mono 6. Hekza 2. Di 7. Hepta 3. Tri 8. Okta 4. Tetra 9. Nona 5. Penta 10. Deka

NO: Azot monoksit N 2 O 3: Di azot trioksit PCl 3 : Fosfor triklorür P 4 S 3 : Tetrafosfor trisülfür
- Slides: 12