Thrapie gnique Gne mdicament Stratgies potentielles de Thrapie








- Slides: 23

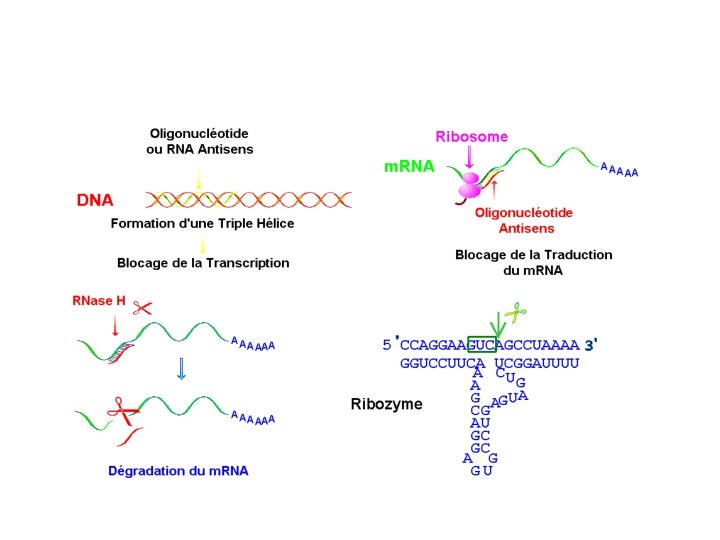
Thérapie génique : Gène médicament





Stratégies potentielles de Thérapie génique des Cancers 1 : association avec une "chimiothérapie" 2 : immunothérapie 3 : virus compétent pour la réplication

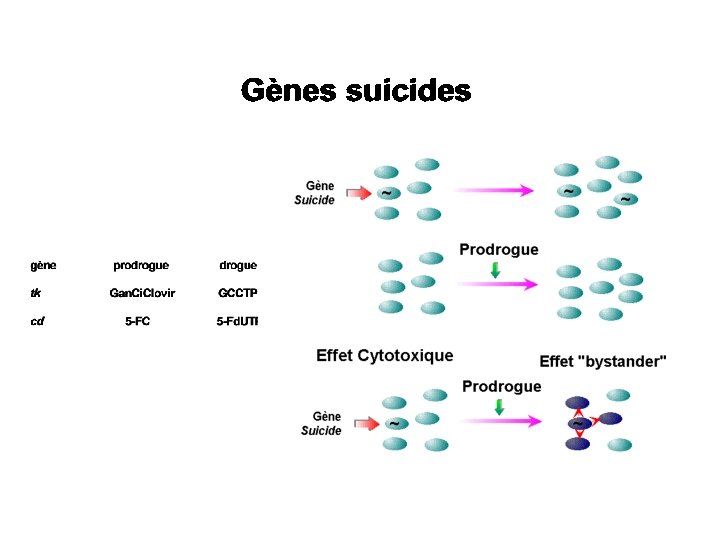
Transférer un gène Suicide dans la Tumeur par exemple: Transgène codant HSV-TK et traitement par Gancyclovir Transférer un gène de Toxine sous contrôle d'un Promoteur Tumeur-Spécifique Transférer un Gène Suppresseur de Tumeur normal par exemple: le gène P 53, dans les tumeurs Chimio ou Radio résistantes Protéger des Cellules Souches de la Chimiothérapie Par exemple: Transgène MDR 1




Critères d’un vecteur idéal • ciblage cellulaire • expression «cellule spécifique» • pas d’effet sur les cellules non-cibles

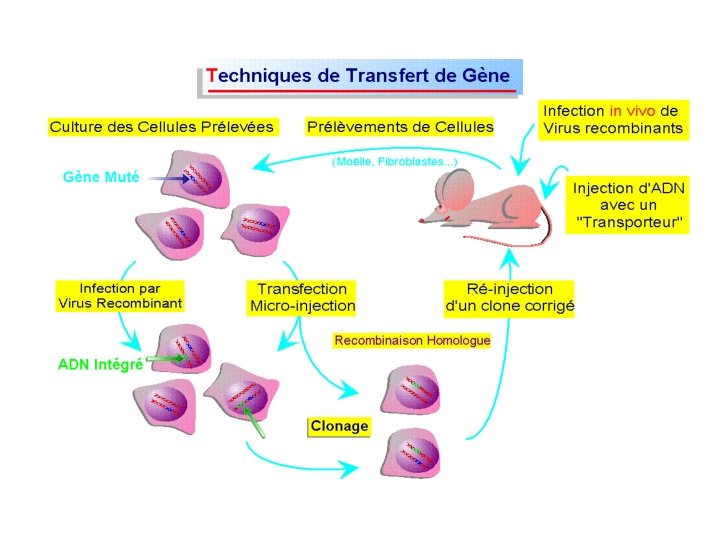
Procédés de transfert de gène dans les cellules cibles: - méthodes non virales : lipofection, injection directe d ’ADN. - utilisation de vecteurs viraux : rétrovirus adénovirus AAV

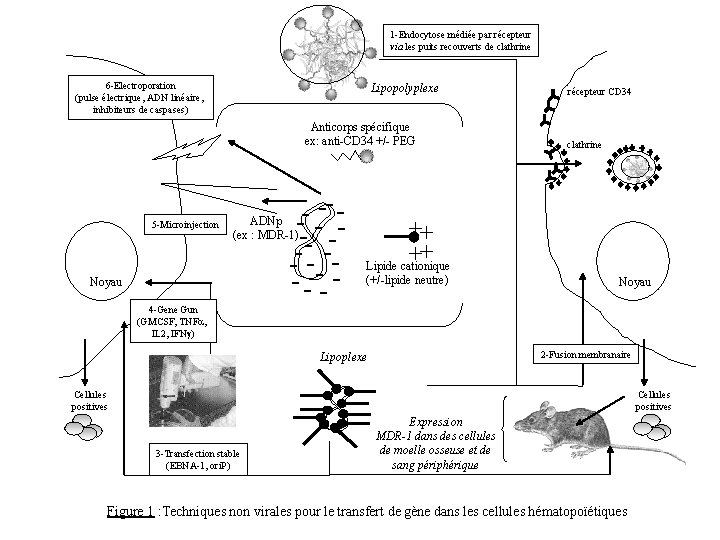
1 -Endocytose médiée par récepteur via les puits recouverts de clathrine 6 -Electroporation (pulse électrique, ADN linéaire, inhibiteurs de caspases) Lipopolyplexe Anticorps spécifique ex: anti-CD 34 +/- PEG 5 -Microinjection Noyau 4 -Gene Gun (GMCSF, TNF , IL 2, IFN ) ADNp (ex : MDR-1) - - -- ------ - récepteur CD 34 clathrine ++ ++ Lipide cationique (+/-lipide neutre) Noyau 2 -Fusion membranaire Lipoplexe Cellules positives 3 -Transfection stable (EBNA-1, ori. P) Expression MDR-1 dans des cellules de moelle osseuse et de sang périphérique Figure 1 : Techniques non virales pour le transfert de gène dans les cellules hématopoïétiques

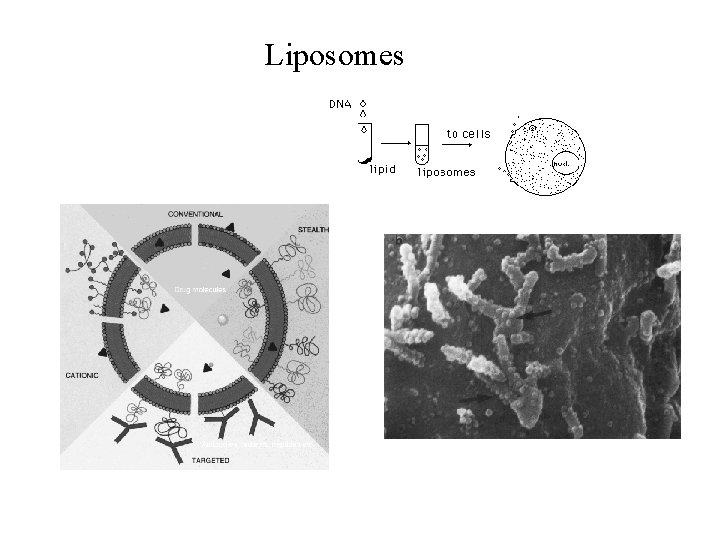
Liposomes

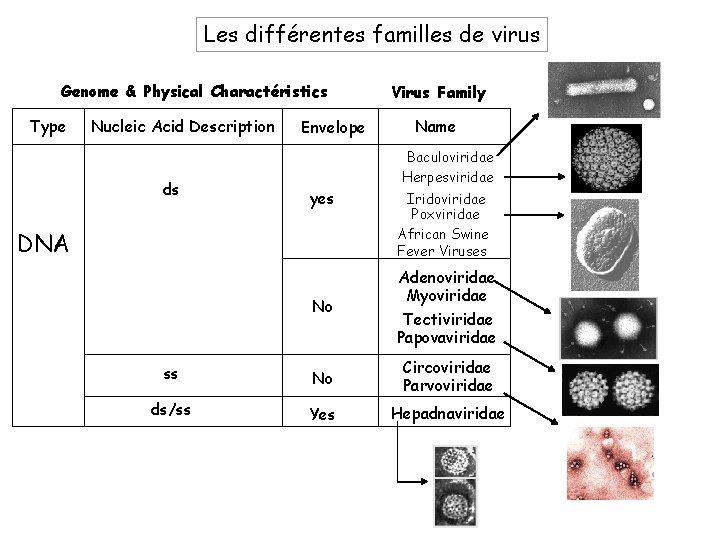
Les différentes familles de virus Genome & Physical Charactéristics Type Nucleic Acid Description ds Envelope Virus Family Name Baculoviridae Herpesviridae yes DNA Iridoviridae Poxviridae African Swine Fever Viruses No Adenoviridae Myoviridae Tectiviridae Papovaviridae ss No Circoviridae Parvoviridae ds/ss Yes Hepadnaviridae

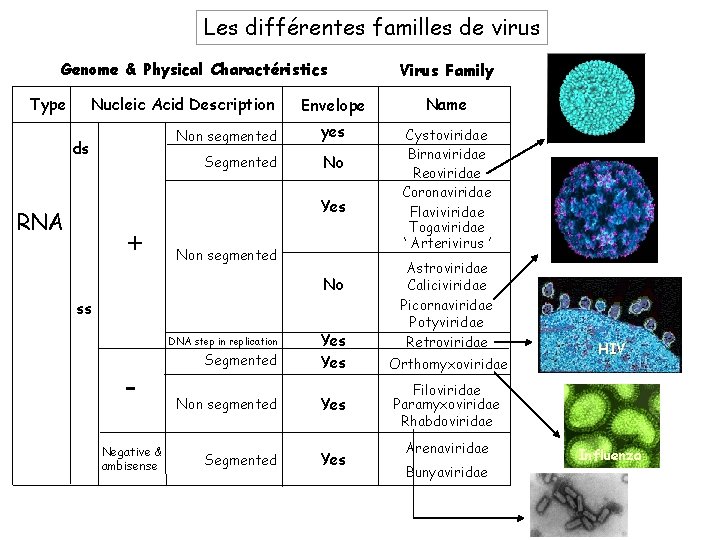
Les différentes familles de virus Genome & Physical Charactéristics Type Nucleic Acid Description ds Envelope Name Non segmented yes Segmented No Cystoviridae Birnaviridae Reoviridae Coronaviridae Flaviviridae Togaviridae ‘ Arterivirus ’ Yes RNA + Non segmented No ss DNA step in replication Negative & ambisense Virus Family Segmented Yes Non segmented Yes Segmented Yes Astroviridae Caliciviridae Picornaviridae Potyviridae Retroviridae Orthomyxoviridae HIV Filoviridae Paramyxoviridae Rhabdoviridae Arenaviridae Bunyaviridae Influenza

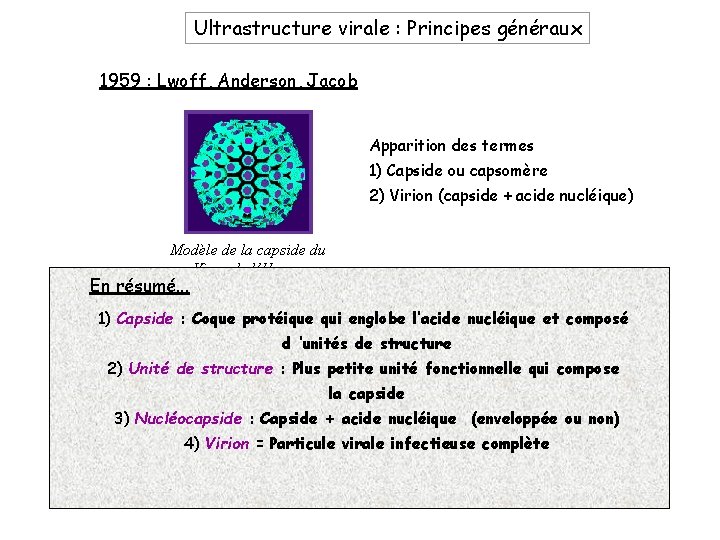
Ultrastructure virale : Principes généraux 1959 : Lwoff, Anderson, Jacob Apparition des termes 1) Capside ou capsomère 2) Virion (capside + acide nucléique) Modèle de la capside du Virus de l’Herpes En résumé. . . 1) Capside protéique qui englobe l’acide nucléique et composé 1956 : Crick : et. Coque Watson d ’unités de structure 1) plusieurs : Plus petite unité fonctionnelle qui compose 2)Existence Unité dedestructure sous-unités identiques la capside 2) Environnement identiques pour chaque sous-unité: : Capside + acide nucléique (enveloppée ou non) 3) Nucléocapside Symétrie cubique 4) Virion = Particule virale infectieuse complète Symétrie icosahédrique

Les pathologies virales http: //www. virology. net : 185 pathologies conséquentes à des infections par des virus, des bactéries, des champignons ou des levures Environ 46 % des infections sont d’origine virale ex: Conjonctivite (adénovirus, virus de l ’Herpes), Fièvre hémorragique d ’Ebola (virus d ’Ebola), HIV, Hépatite (virus de l ’hépatite A, B, C, D, E), Varicelle (varicella zoster virus), Gastroentérite (norwalk virus) Infection : Interaction virus/cellule hôte ex: cellules épithéliales

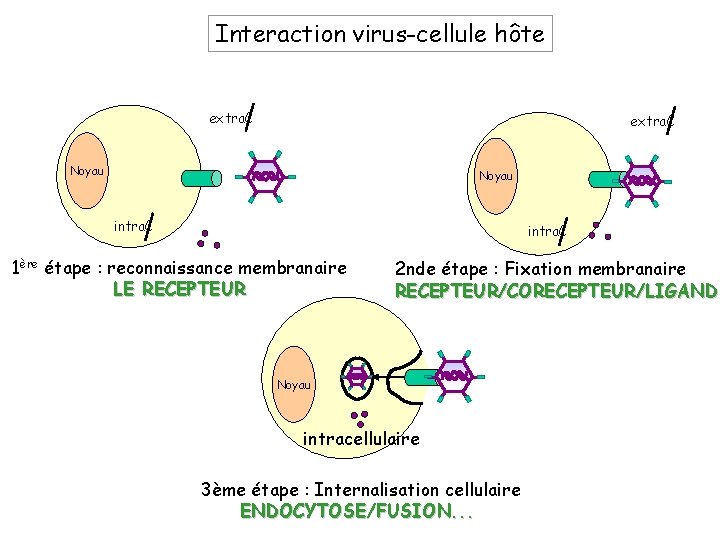
Interaction virus-cellule hôte extra. C Noyau intra. C 1ère étape : reconnaissance membranaire LE RECEPTEUR 2 nde étape : Fixation membranaire RECEPTEUR/CORECEPTEUR/LIGAND Noyau intracellulaire 3ème étape : Internalisation cellulaire ENDOCYTOSE/FUSION. . .

Récepteurs et virus Virus Protéine virale Récepteur cellulaire Picornaviridae Rhinovirus humain 14, 91. . . Protéine de la capside VP 1, 2, 3 ICAM-1 Coronaviridae Gastroentérite porcine. . . Glycoprotéine d’enveloppe S Aminopeptidase N Rhabdoviridae Virus rabique Glycoprotéine d’enveloppe G Récepteur -adrénergique, Glycoprotéine sialysées, NCAM (CD 56) Paramyxoviridae Virus de la rougeole, Virus Carré Glycoprotéine d’enveloppe H CD 46 humain, SLAM humain CD 9 canin Glycoprotéine d’enveloppe gp 120 CD 4 et corécepteurs (récepteurs de chémokines) Protéine de la capside : fibre h. CAR et corécepteurs (intégrines), Héparanes sulfates, 2 CMHI Glycoprotéine d’enveloppe gp 350/220 CD 21 Rétroviridae Virus VIH Adenoviridae Adénovirus humain de sérotype 5 Herpesviridae Virus d’Epstein-Barr …etc

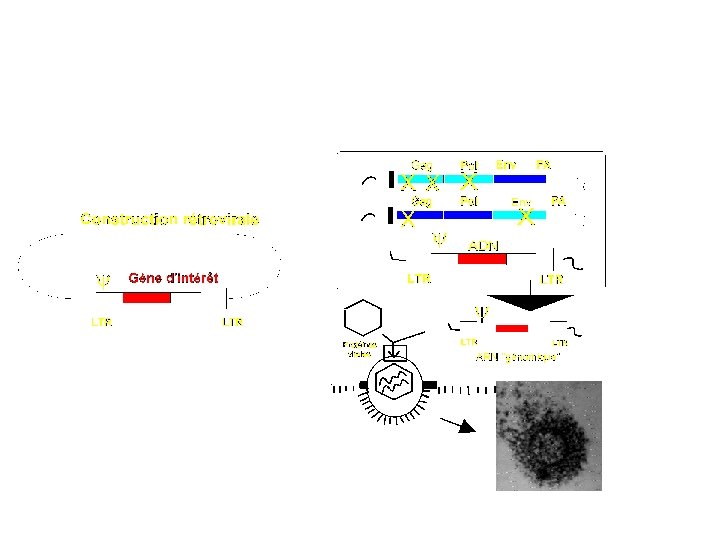
Virus : vecteur de thérapie génique Utilisation des propriétés naturelles des virus Faculté de reproduction élevée : production d’un vecteur rentable Reconnaissance membranire de récepteurs +/-spécifiques Spectre cellulaire +/- étendu Infection naturelle et efficace des cellules hôtes : transfert élevé de leur matériel génétique dans les noyaux cellulaire. Expression des protéines correspondantes Développement de vecteurs de thérapie génique Création de virus dits ‘ recombinant ’ Modifications génétiques des virus : délétions de certaines régions impliquées dans la réplication des virus (ex : E 1 pour les adénovirus ou gal, pol env pour les rétrovirus)


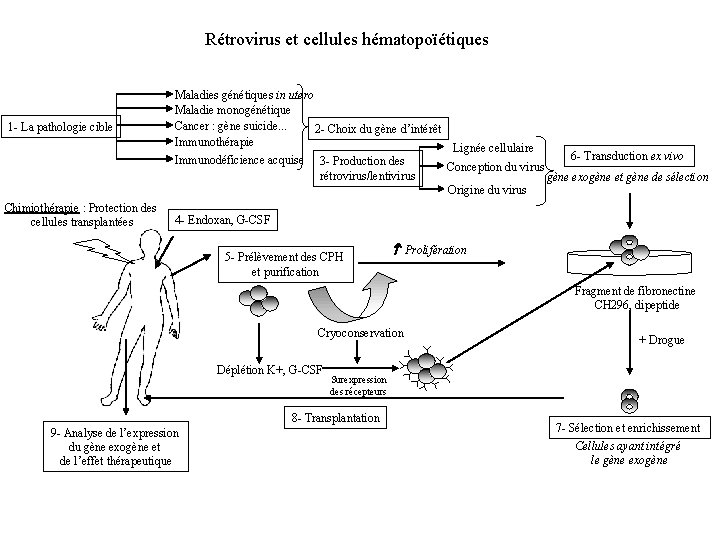
Rétrovirus et cellules hématopoïétiques 1 - La pathologie cible Chimiothérapie : Protection des cellules transplantées Maladies génétiques in utero Maladie monogénétique Cancer : gène suicide. . . 2 - Choix du gène d’intérêt Immunothérapie Lignée cellulaire 6 - Transduction ex vivo Immunodéficience acquise 3 - Production des Conception du virus rétrovirus/lentivirus gène exogène et gène de sélection Origine du virus 4 - Endoxan, G-CSF 5 - Prélèvement des CPH et purification Prolifération Fragment de fibronectine CH 296, dipeptide Cryoconservation Déplétion K+, G-CSF Surexpression des récepteurs 8 - Transplantation 9 - Analyse de l’expression du gène exogène et de l’effet thérapeutique + Drogue 7 - Sélection et enrichissement Cellules ayant intégré le gène exogène