Gnexpresszi szablyozsa szintetikus oligonukleotidokkal fehrjk m RNS sejtmag
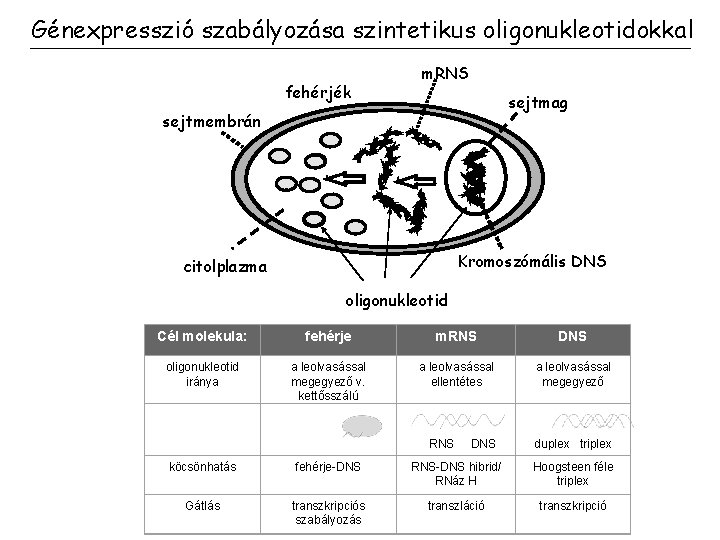
Génexpresszió szabályozása szintetikus oligonukleotidokkal fehérjék m. RNS sejtmag sejtmembrán Kromoszómális DNS citolplazma oligonukleotid Cél molekula: fehérje m. RNS DNS oligonukleotid iránya a leolvasással megegyezõ v. kettõsszálú a leolvasással ellentétes a leolvasással megegyezõ RNS DNS duplex triplex köcsönhatás fehérje-DNS RNS-DNS hibrid/ RNáz H Hoogsteen féle triplex Gátlás transzkripciós szabályozás transzláció transzkripció
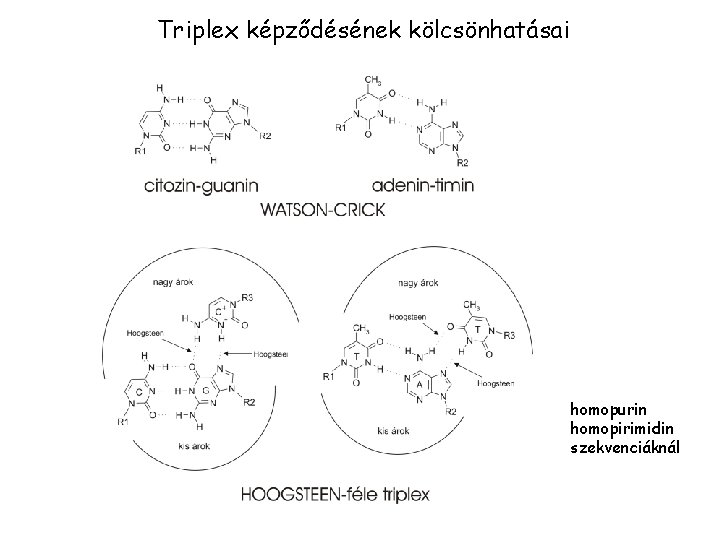
Triplex képződésének kölcsönhatásai homopurin homopirimidin szekvenciáknál
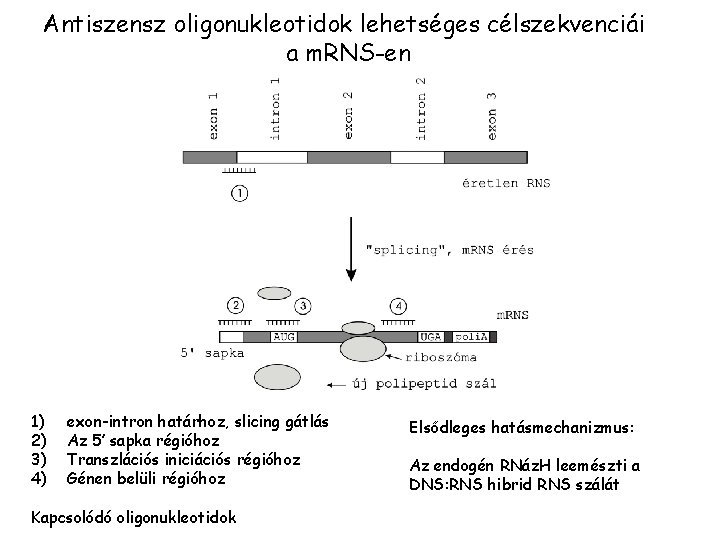
Antiszensz oligonukleotidok lehetséges célszekvenciái a m. RNS-en 1) 2) 3) 4) exon-intron határhoz, slicing gátlás Az 5’ sapka régióhoz Transzlációs iniciációs régióhoz Génen belüli régióhoz Kapcsolódó oligonukleotidok Elsődleges hatásmechanizmus: Az endogén RNáz. H leemészti a DNS: RNS hibrid RNS szálát
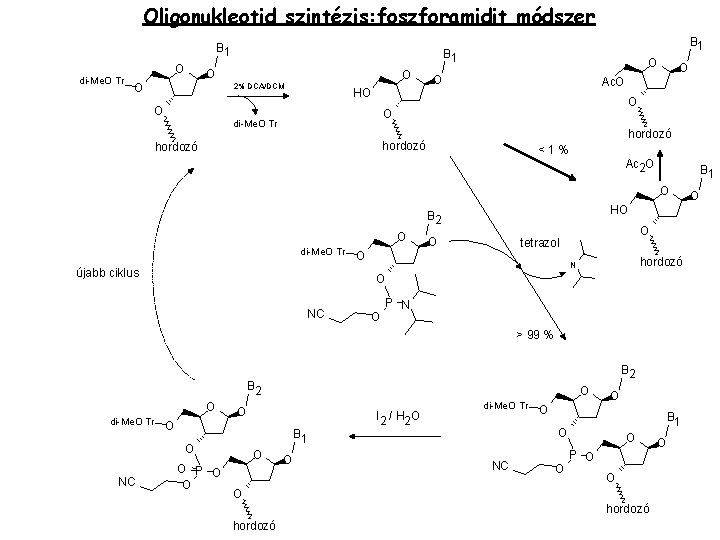
Oligonukleotid szintézis: foszforamidit módszer B 1 di-Me. O Tr O O O B 1 O 2% DCA/DCM O O Ac. O HO O di-Me. O Tr hordozó O <1% Ac 2 O B 1 O HO B 2 O di-Me. O Tr újabb ciklus O O tetrazol O hordozó N O NC O P N > 99 % B 2 O di-Me. O Tr O I 2 / H 2 O O O P O O di-Me. O Tr O O B 1 O NC O O P O O O hordozó O O
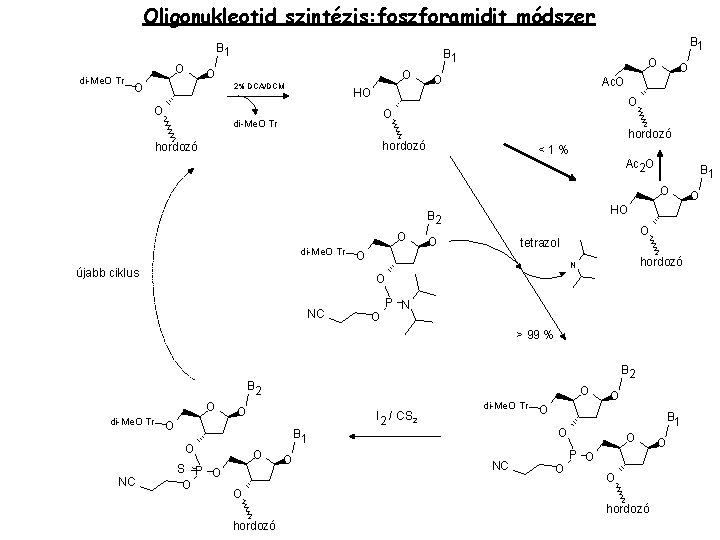
Oligonukleotid szintézis: foszforamidit módszer B 1 di-Me. O Tr O O O B 1 O 2% DCA/DCM O O Ac. O HO O di-Me. O Tr hordozó O <1% Ac 2 O B 1 O HO B 2 O di-Me. O Tr újabb ciklus O O tetrazol O hordozó N O NC O P N > 99 % B 2 O di-Me. O Tr O I 2 / CS 2 O S P O O di-Me. O Tr O O B 1 O NC O O P O O O hordozó O O
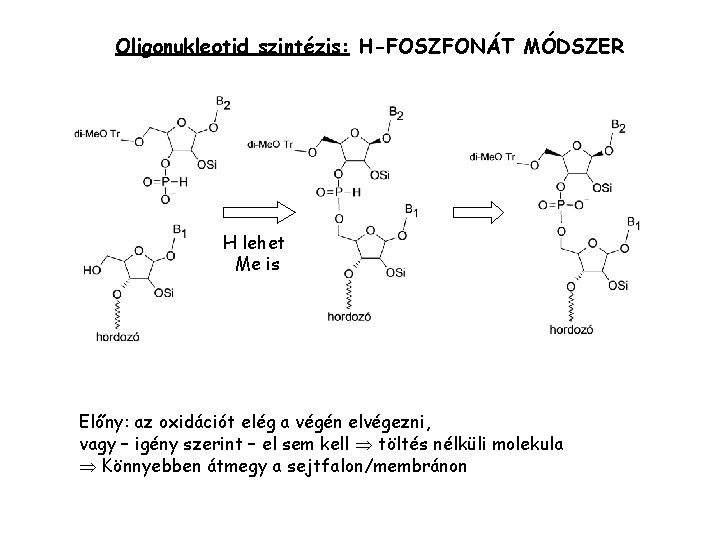
Oligonukleotid szintézis: H-FOSZFONÁT MÓDSZER H lehet Me is Előny: az oxidációt elég a végén elvégezni, vagy – igény szerint – el sem kell töltés nélküli molekula Könnyebben átmegy a sejtfalon/membránon
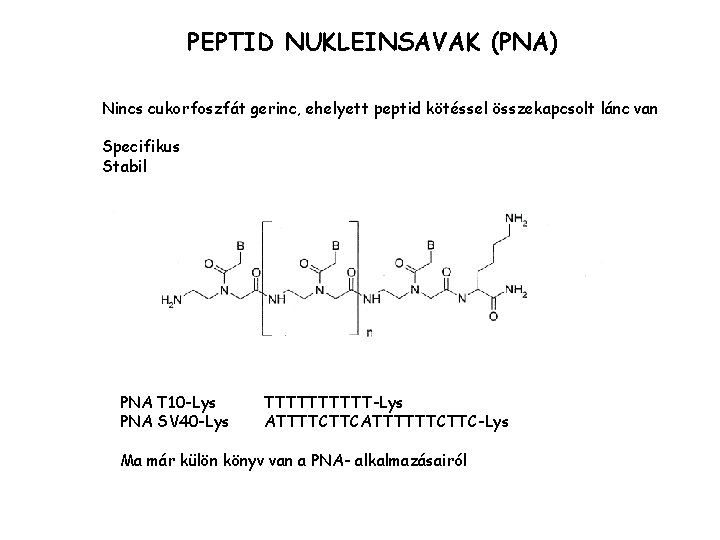
PEPTID NUKLEINSAVAK (PNA) Nincs cukorfoszfát gerinc, ehelyett peptid kötéssel összekapcsolt lánc van Specifikus Stabil PNA T 10 -Lys PNA SV 40 -Lys TTTTT-Lys ATTTTCTTCATTTTTTCTTC-Lys Ma már külön könyv van a PNA- alkalmazásairól
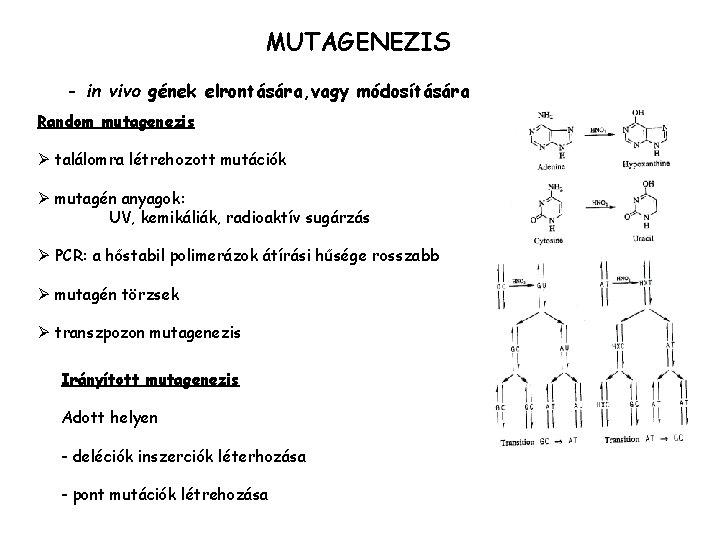
MUTAGENEZIS - in vivo gének elrontására, vagy módosítására Random mutagenezis Ø találomra létrehozott mutációk Ø mutagén anyagok: UV, kemikáliák, radioaktív sugárzás Ø PCR: a hőstabil polimerázok átírási hűsége rosszabb Ø mutagén törzsek Ø transzpozon mutagenezis Irányított mutagenezis Adott helyen - deléciók inszerciók léterhozása - pont mutációk létrehozása
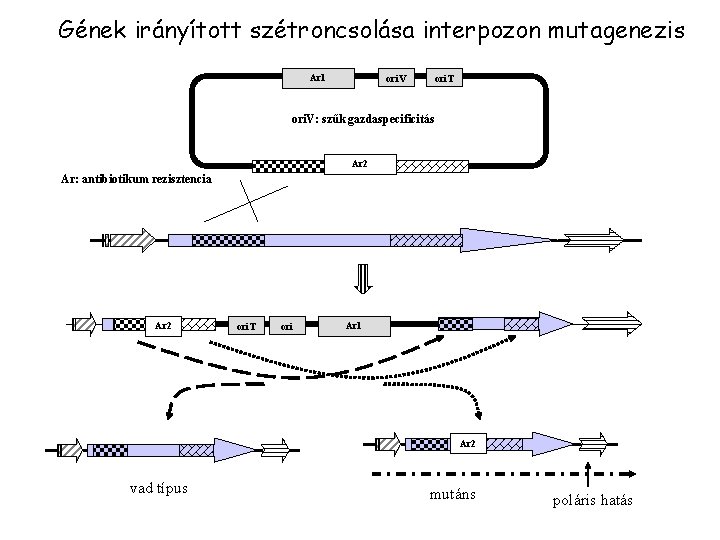
Gének irányított szétroncsolása interpozon mutagenezis Ar 1 ori. V ori. T ori. V: szűk gazdaspecificitás Ar 2 Ar: antibiotikum rezisztencia Ar 2 ori. T ori Ar 1 Ar 2 vad típus mutáns poláris hatás
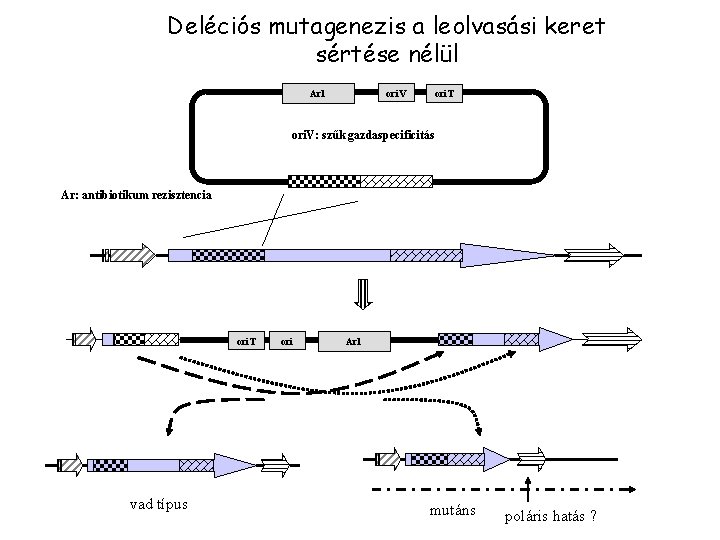
Deléciós mutagenezis a leolvasási keret sértése nélül Ar 1 ori. V ori. T ori. V: szűk gazdaspecificitás Ar: antibiotikum rezisztencia ori. T vad típus ori Ar 1 mutáns poláris hatás ?
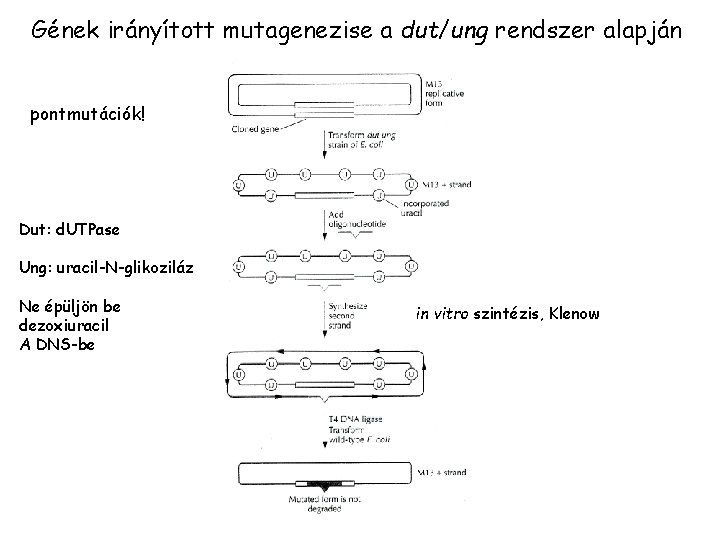
Gének irányított mutagenezise a dut/ung rendszer alapján pontmutációk! Dut: d. UTPase Ung: uracil-N-glikoziláz Ne épüljön be dezoxiuracil A DNS-be in vitro szintézis, Klenow
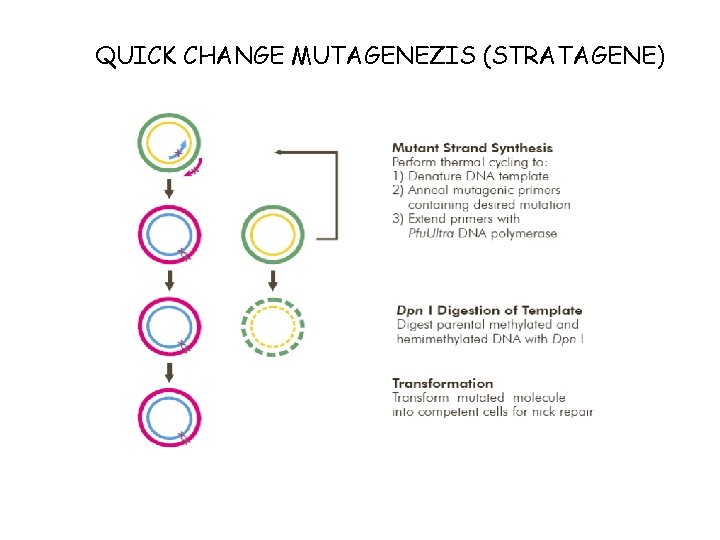
QUICK CHANGE MUTAGENEZIS (STRATAGENE)

FEHÉRJE TERMELTETÉS VAN GÉNÜNK: Legyen az prokarióta vagy eukarióta természetes vagy szintetikus vad típusú vagy mutáns
FEHÉRJE TERMELTETŐ RENDSZEREK PROKARIÓTÁK E. coli ismert, Bármilyen fehérje, feltéve, ha - nem túl nagy - nem túl kicsi - nem túl hidrofób - nincs túl sok cisztein benne szekréciós rendszere minimális Bacillus subtilis jól ismert, ha nem is annyira, mint az E. coli van szekréciós rendszere EUKARIÓTÁK élesztő ügyorsan szaporodó eukarióta sejtvonal, üsok ismeretanyag üviszonylag könnyű kezelhetőség üposzttranszlációs modifikációk lehetősége emlős sejtvonalak v minden fajta fehérje termeltethető bennük v tranziens expressziós rendszerek viszonylag gyors, de korlátozott lehetôségek, v stabil expressziós rendszerek v hosszú, fáradságos optimalizálást igényel

Escherichia coli ELŐNYÖK ü óriási mennyiségű ismeretanyag ü könnyű kezelhetőség, gyors növekedési sebesség, viszonylag olcsó médium ü nagy mennyiségű biomassza gazdaságos előállítása ü ismert szelekciós rendszerek ü legtöbb expressziós rendszer HÁTRÁNYOK § általában nem szekretál § a sejten belül redukáló atmoszféra diszulfid hidak kialakulása gátolt § az eukariota poszttranszlációs módosítások általában nem megvalósíthatóak § nem alakul ki a megfelelő aktiv szerkezet, rossz folding

STRATÉGIÁK TÚLTERMELTETÉSRE KONSTITUTÍV PROMÓTER INDUKÁLT TERMELTETÉS Ø a fehérje a teljes növekedési fázis alatt expresszálódik a promoter represszált állapotban van a növekedés egy bizonyos fázisáig Ø nagy sejttömeg elérése után a fehérje visszanyerése Ø nem igazán használatos, toxicitási problémák miatt valamilyen indukcióval derepresszió további növesztés fehérje visszanyerése legáltalánosabban használt stratégia toxicitás sok esetben megoldható
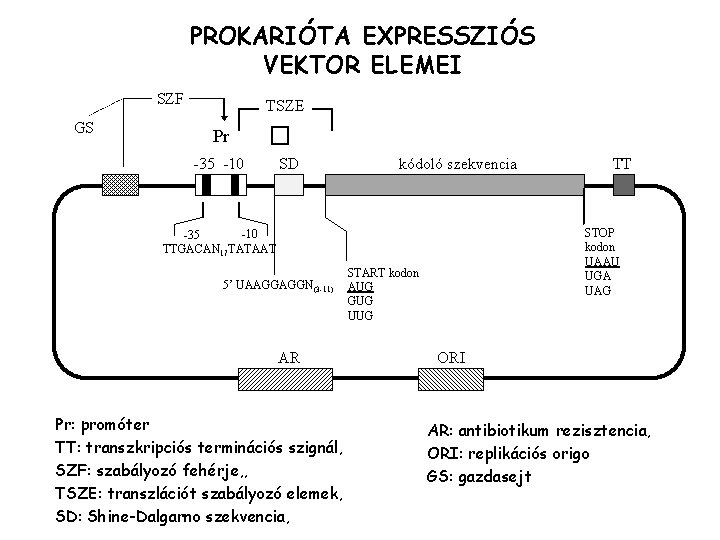
PROKARIÓTA EXPRESSZIÓS VEKTOR ELEMEI SZF GS TSZE Pr � -35 -10 SD kódoló szekvencia STOP kodon UAAU UGA UAG -10 -35 TTGACAN 17 TATAAT 5’ UAAGGAGGN(3 -11) AR Pr: promóter TT: transzkripciós terminációs szignál, SZF: szabályozó fehérje, , TSZE: transzlációt szabályozó elemek, SD: Shine-Dalgarno szekvencia, TT START kodon AUG GUG UUG ORI AR: antibiotikum rezisztencia, ORI: replikációs origo GS: gazdasejt
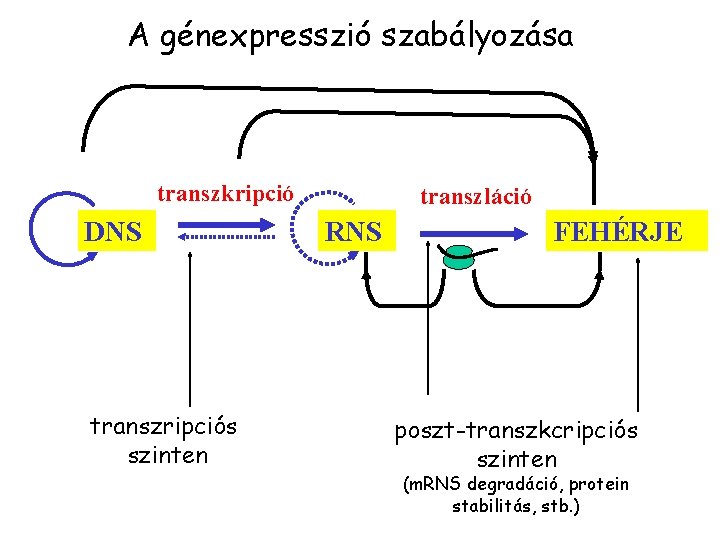
A génexpresszió szabályozása transzkripció DNS transzripciós szinten transzláció RNS FEHÉRJE poszt-transzkcripciós szinten (m. RNS degradáció, protein stabilitás, stb. )

Különböző faktorok relatív hatása a fehérje termeltetésre E. coli-ban Ø Promóter indukálhatóság kb. 1000 x Ø Gazdasejt kb. 1000 x Ø A m. RNS 5’ struktúrája kb. 100 x Ø Transzláció kb. 100 x Ø növekedési sebesség (m. RNS stabilitás) kb. 50 x
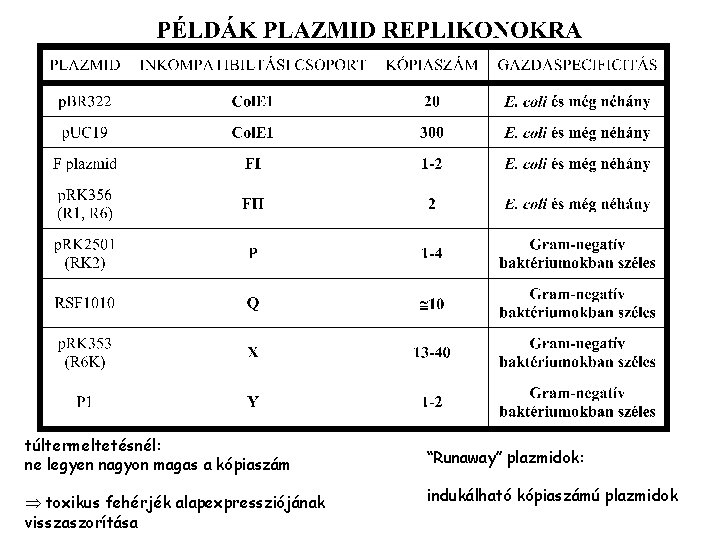
túltermeltetésnél: ne legyen nagyon magas a kópiaszám toxikus fehérjék alapexpressziójának visszaszorítása “Runaway” plazmidok: indukálható kópiaszámú plazmidok

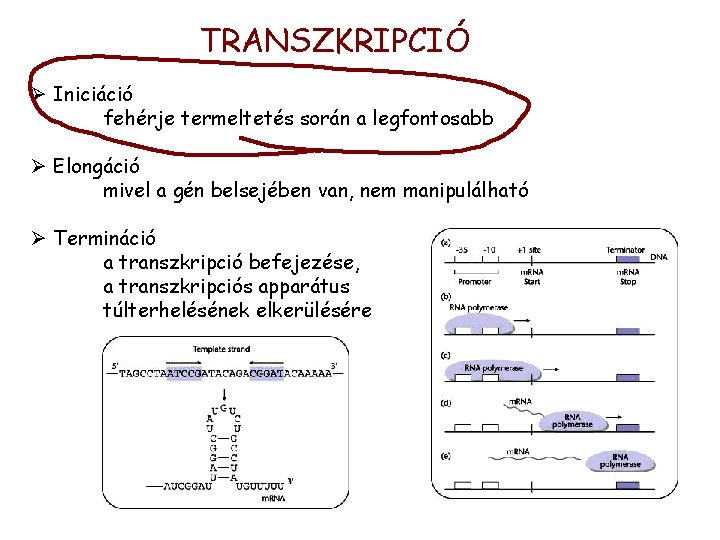
TRANSZKRIPCIÓ Ø Iniciáció fehérje termeltetés során a legfontosabb Ø Elongáció mivel a gén belsejében van, nem manipulálható Ø Termináció a transzkripció befejezése, a transzkripciós apparátus túlterhelésének elkerülésére
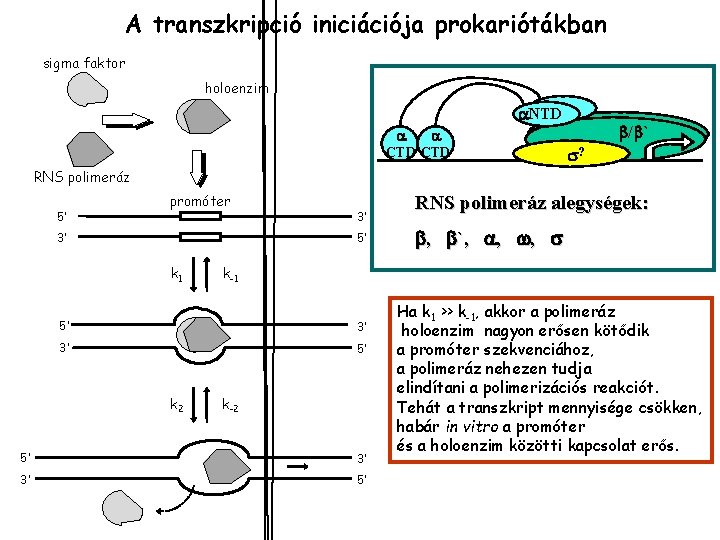
A transzkripció iniciációja prokariótákban sigma faktor holoenzim NTD CTD / ` ? RNS polimeráz 5’ promóter 3’ 3’ 5’ k 1 , `, , , k-1 5’ 3’ 3’ 5’ k 2 RNS polimeráz alegységek: k-2 5’ 3’ 3’ 5’ Ha k 1 >> k-1, akkor a polimeráz holoenzim nagyon erősen kötődik a promóter szekvenciához, a polimeráz nehezen tudja elindítani a polimerizációs reakciót. Tehát a transzkript mennyisége csökken, habár in vitro a promóter és a holoenzim közötti kapcsolat erős.
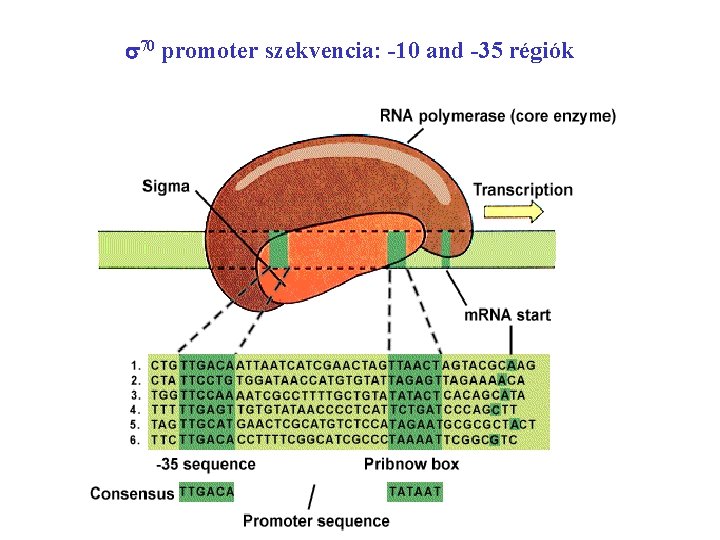
70 promoter szekvencia: -10 and -35 régiók
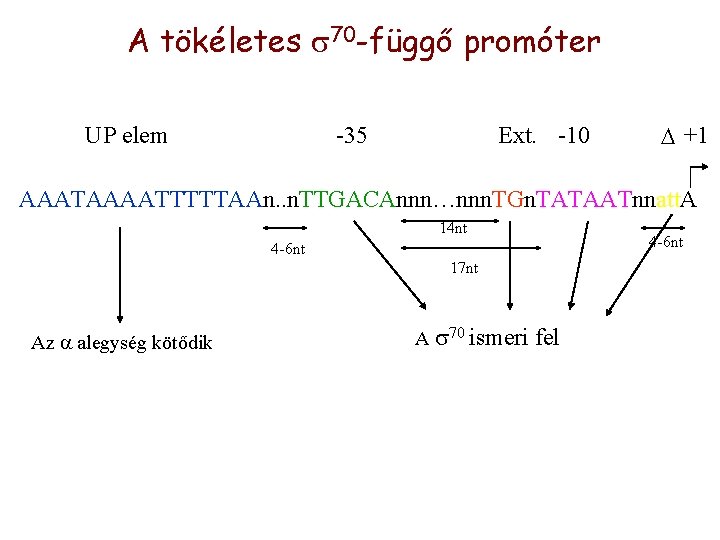
A tökéletes 70 -függő promóter UP elem -35 Ext. -10 D +1 AAATAAAATTTTTAAn. . n. TTGACAnnn…nnn. TGn. TATAATnnatt. A 14 nt 4 -6 nt 17 nt Az alegység kötődik A 70 ismeri fel
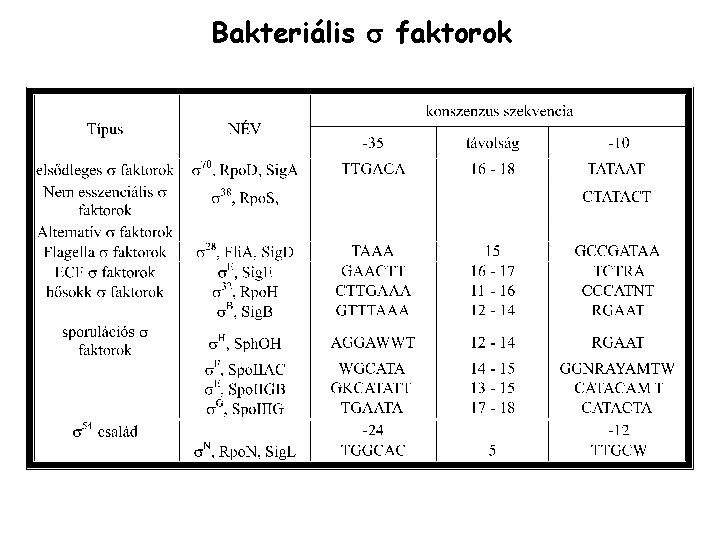
Bakteriális faktorok
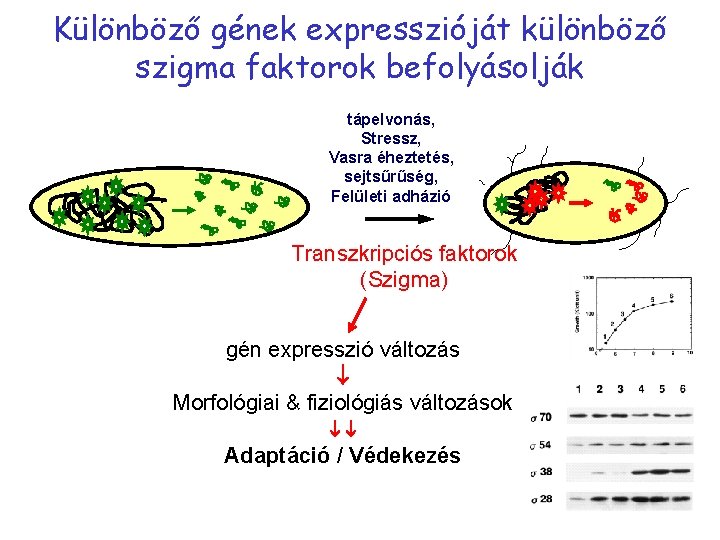
Különböző gének expresszióját különböző szigma faktorok befolyásolják tápelvonás, Stressz, Vasra éheztetés, sejtsűrűség, Felületi adházió Transzkripciós faktorok (Szigma) gén expresszió változás Morfológiai & fiziológiás változások Adaptáció / Védekezés
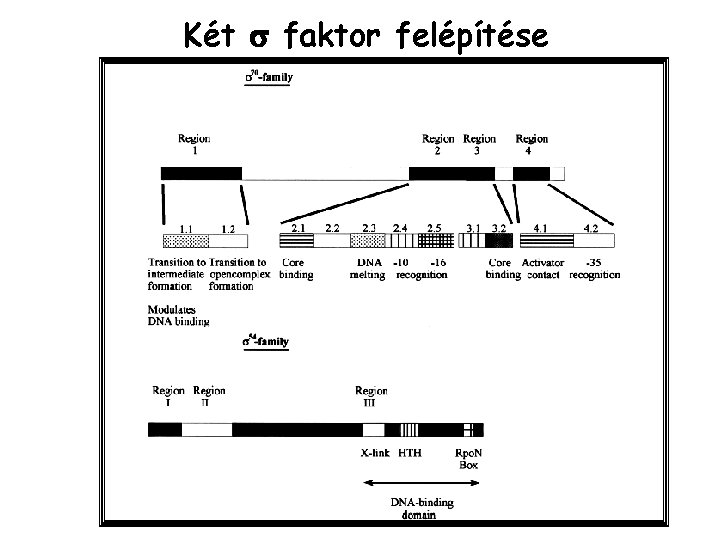
Két faktor felépítése
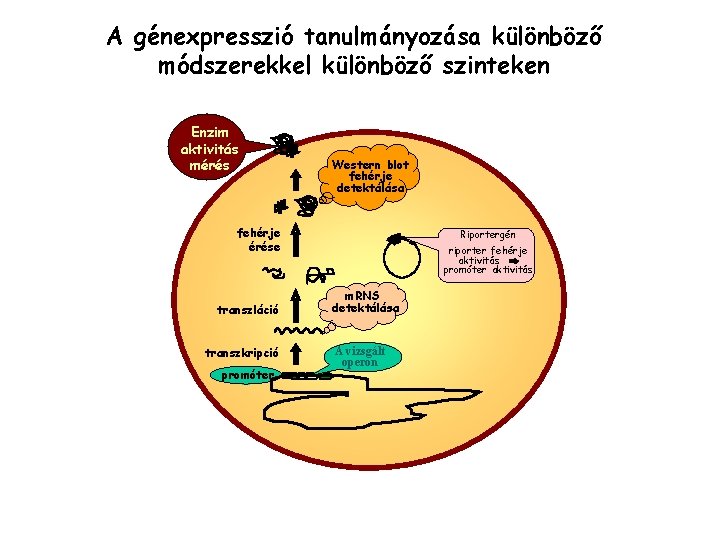
A génexpresszió tanulmányozása különböző módszerekkel különböző szinteken Enzim aktivitás mérés Western blot fehérje detektálása fehérje érése transzláció transzkripció promóter Riportergén riporter fehérje aktivitás promóter aktivitás m. RNS detektálása A vizsgált operon
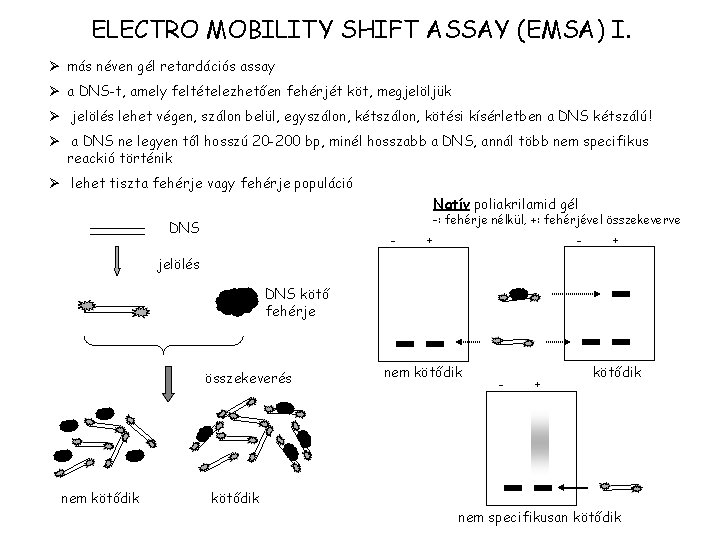
ELECTRO MOBILITY SHIFT ASSAY (EMSA) I. Ø más néven gél retardációs assay Ø a DNS-t, amely feltételezhetően fehérjét köt, megjelöljük Ø jelölés lehet végen, szálon belül, egyszálon, kétszálon, kötési kísérletben a DNS kétszálú! Ø a DNS ne legyen től hosszú 20 -200 bp, minél hosszabb a DNS, annál több nem specifikus reackió történik Ø lehet tiszta fehérje vagy fehérje populáció Natív poliakrilamid gél -: fehérje nélkül, +: fehérjével összekeverve DNS - + jelölés DNS kötő fehérje összekeverés nem kötődik - + kötődik nem specifikusan kötődik
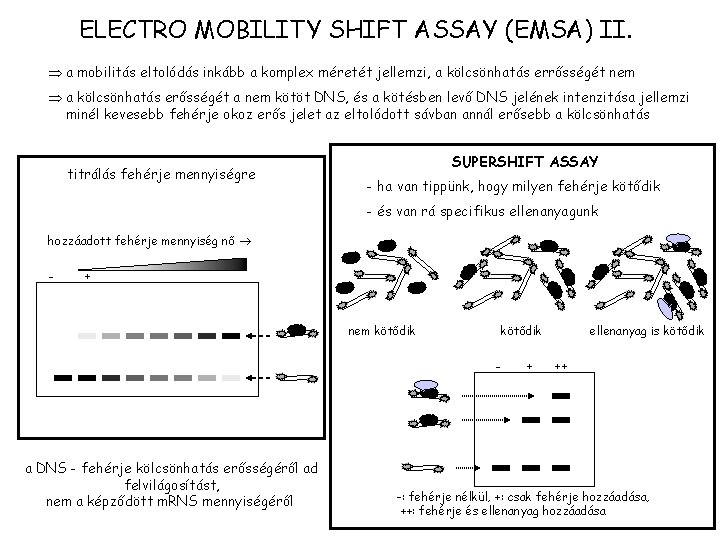
ELECTRO MOBILITY SHIFT ASSAY (EMSA) II. a mobilitás eltolódás inkább a komplex méretét jellemzi, a kölcsönhatás errősségét nem a kölcsönhatás erősségét a nem kötöt DNS, és a kötésben levő DNS jelének intenzitása jellemzi minél kevesebb fehérje okoz erős jelet az eltolódott sávban annál erősebb a kölcsönhatás titrálás fehérje mennyiségre SUPERSHIFT ASSAY - ha van tippünk, hogy milyen fehérje kötődik - és van rá specifikus ellenanyagunk hozzáadott fehérje mennyiség nő - + nem kötődik - a DNS - fehérje kölcsönhatás erősségéről ad felvilágosítást, nem a képződött m. RNS mennyiségéről + ellenanyag is kötődik ++ -: fehérje nélkül, +: csak fehérje hozzáadása, ++: fehérje és ellenanyag hozzáadása
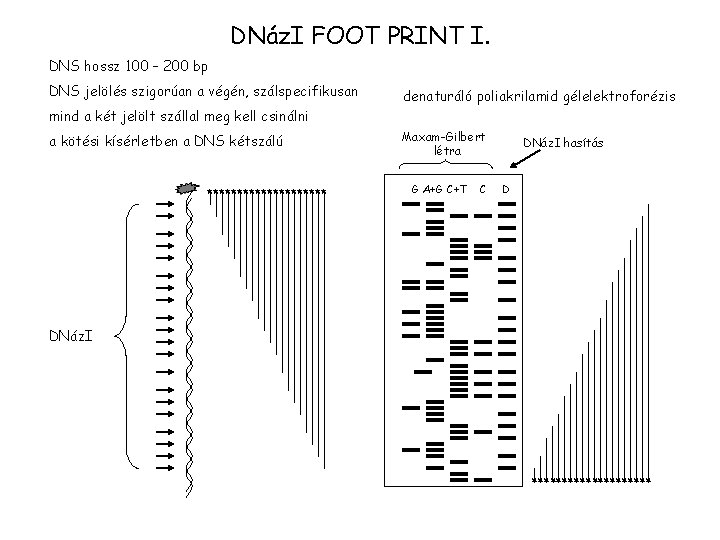
DNáz. I FOOT PRINT I. DNS hossz 100 – 200 bp DNS jelölés szigorúan a végén, szálspecifikusan denaturáló poliakrilamid gélelektroforézis mind a két jelölt szállal meg kell csinálni a kötési kísérletben a DNS kétszálú ********** Maxam-Gilbert létra G A+G C+T C DNáz. I hasítás D DNáz. I **********
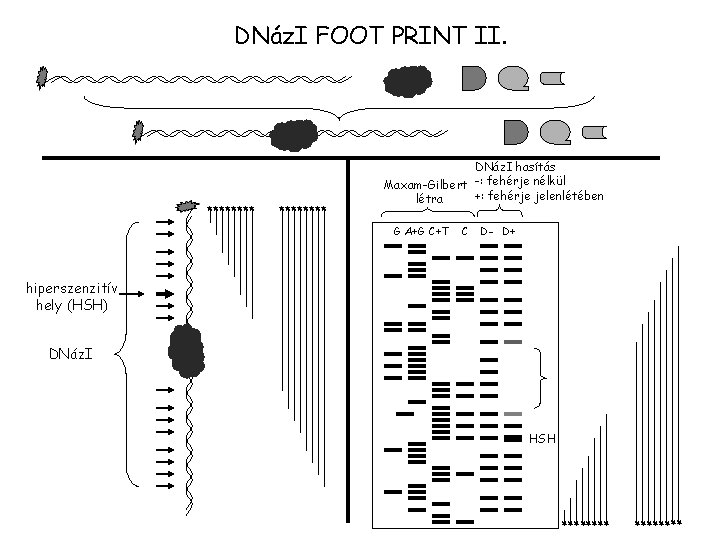
DNáz. I FOOT PRINT II. ******** DNáz. I hasítás Maxam-Gilbert -: fehérje nélkül +: fehérje jelenlétében létra G A+G C+T C D- D+ hiperszenzitív hely (HSH) DNáz. I HSH ********
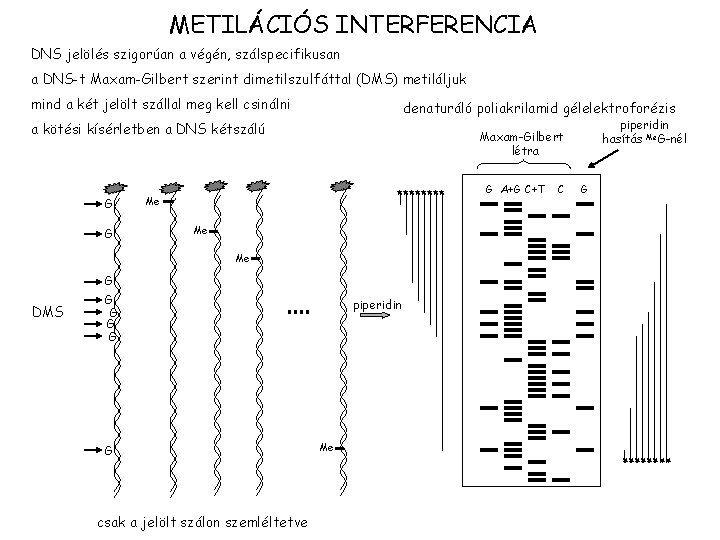
METILÁCIÓS INTERFERENCIA DNS jelölés szigorúan a végén, szálspecifikusan a DNS-t Maxam-Gilbert szerint dimetilszulfáttal (DMS) metiláljuk mind a két jelölt szállal meg kell csinálni denaturáló poliakrilamid gélelektroforézis a kötési kísérletben a DNS kétszálú G G piperidin hasítás Me. G-nél Maxam-Gilbert létra **** Me G A+G C+T C G Me Me G G G csak a jelölt szálon szemléltetve piperidin Me **** DMS
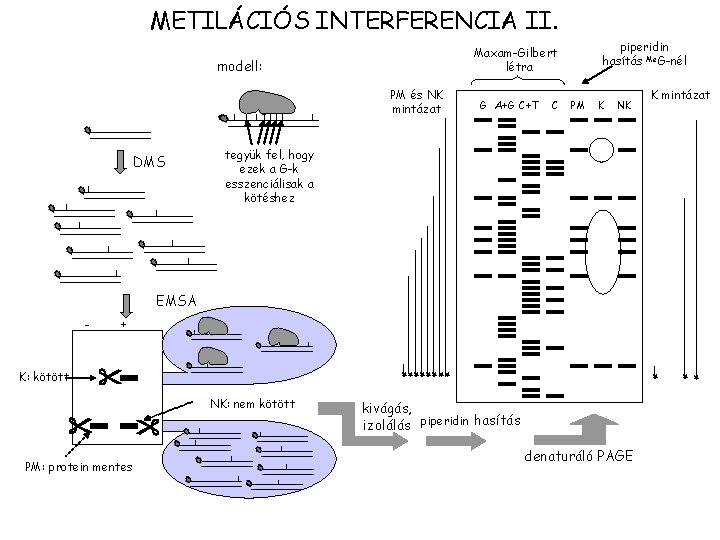
METILÁCIÓS INTERFERENCIA II. modell: PM és NK mintázat DMS piperidin hasítás Me. G-nél Maxam-Gilbert létra G A+G C+T C PM K NK K mintázat tegyük fel, hogy ezek a G-k esszenciálisak a kötéshez EMSA **** NK: nem kötött PM: protein mentes * K: kötött + kivágás, izolálás piperidin hasítás denaturáló PAGE ** -
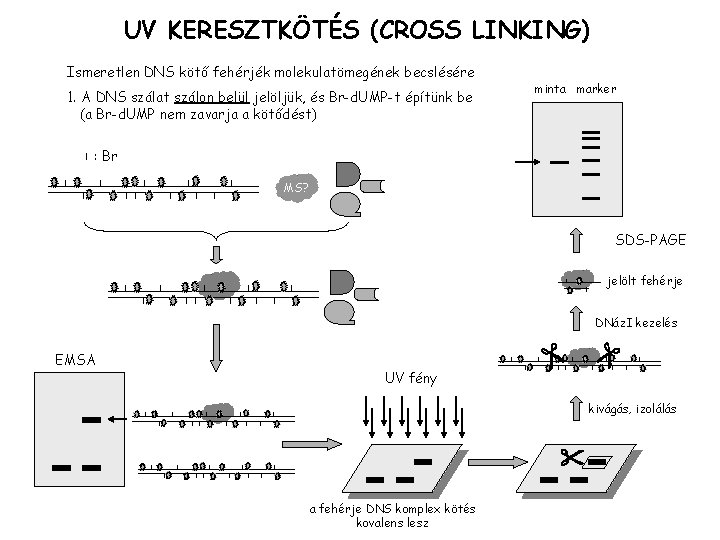
UV KERESZTKÖTÉS (CROSS LINKING) Ismeretlen DNS kötő fehérjék molekulatömegének becslésére 1. A DNS szálat szálon belül jelöljük, és Br-d. UMP-t építünk be (a Br-d. UMP nem zavarja a kötődést) minta marker : Br MS? SDS-PAGE jelölt fehérje DNáz. I kezelés UV fény EMSA kivágás, izolálás a fehérje DNS komplex kötés kovalens lesz

A m. RNS mennyiségének meghatározása - Northern-blot és hibridizáció - reverz-transzkripció kapcsolt kvantitatív PCR - korrekt, de belső összehasonlító standardokat igényel
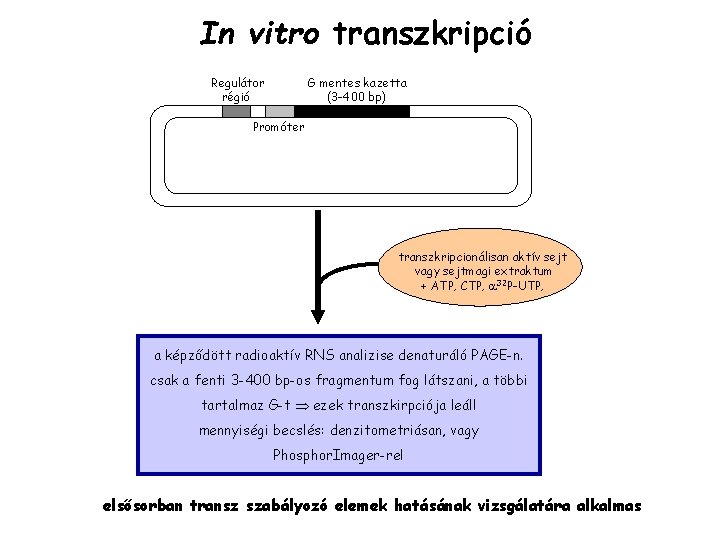
In vitro transzkripció Regulátor régió G mentes kazetta (3 -400 bp) Promóter transzkripcionálisan aktív sejt vagy sejtmagi extraktum + ATP, CTP, 32 P-UTP, a képződött radioaktív RNS analizise denaturáló PAGE-n. csak a fenti 3 -400 bp-os fragmentum fog látszani, a többi tartalmaz G-t ezek transzkirpciója leáll mennyiségi becslés: denzitometriásan, vagy Phosphor. Imager-rel elsősorban transz szabályozó elemek hatásának vizsgálatára alkalmas
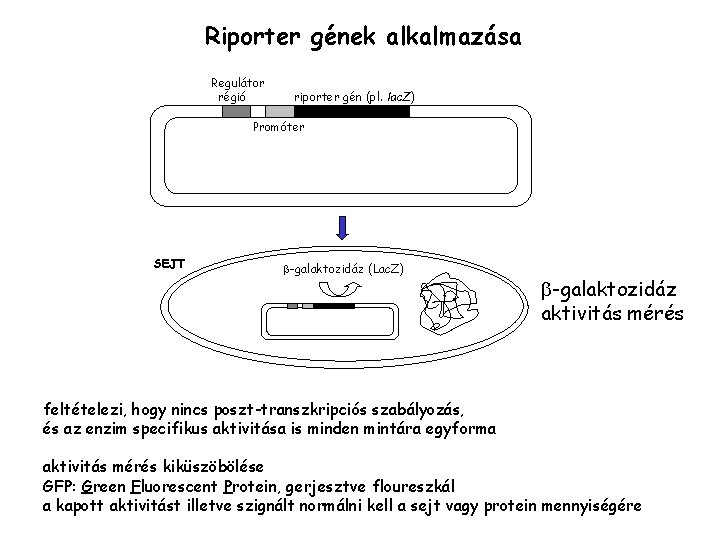
Riporter gének alkalmazása Regulátor régió riporter gén (pl. lac. Z) Promóter SEJT -galaktozidáz (Lac. Z) -galaktozidáz aktivitás mérés feltételezi, hogy nincs poszt-transzkripciós szabályozás, és az enzim specifikus aktivitása is minden mintára egyforma aktivitás mérés kiküszöbölése GFP: Green Fluorescent Protein, gerjesztve floureszkál a kapott aktivitást illetve szignált normálni kell a sejt vagy protein mennyiségére
- Slides: 39