ELEMENTLER ARASINDAK PERYODK LKLER Kaynak Fen ve Mhendislik


![Temsilci (Baş grup) Elementlerinin Anyon ve Katyonlarının Elektronik Konfigurasyonları Na [Ne]3 s 1 Na+ Temsilci (Baş grup) Elementlerinin Anyon ve Katyonlarının Elektronik Konfigurasyonları Na [Ne]3 s 1 Na+](https://slidetodoc.com/presentation_image_h2/65410b56086232795c701ce2f997f6ef/image-5.jpg)




- Slides: 21

ELEMENTLER ARASINDAKİ PERİYODİK İLİŞKİLER Kaynak: Fen ve Mühendislik Bilimleri için KİMYA Raymond Chang

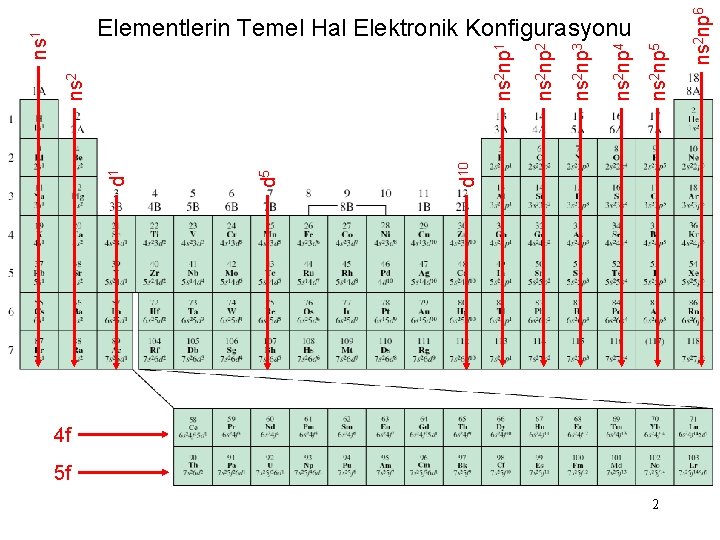
4 f 5 f 2 ns 2 np 6 ns 2 np 5 ns 2 np 4 ns 2 np 3 ns 2 np 2 ns 2 np 1 d 10 d 5 d 1 ns 2 ns 1 Elementlerin Temel Hal Elektronik Konfigurasyonu

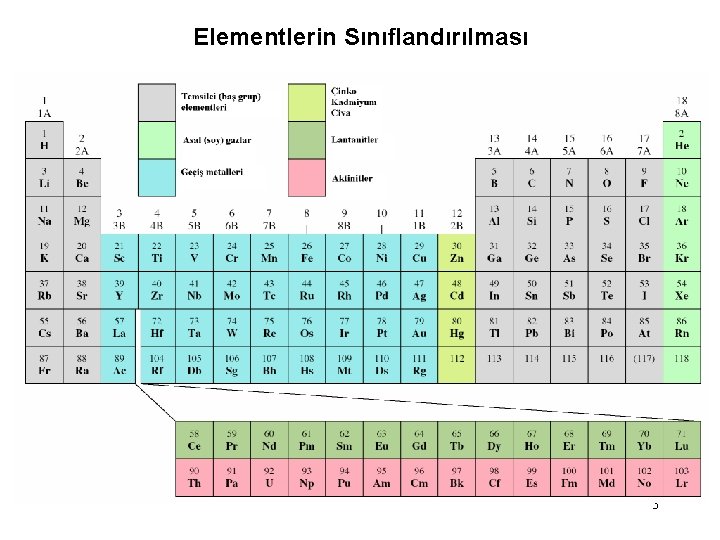
Elementlerin Sınıflandırılması 3

Baş grup elementleri: 1 A dan 7 A ya kadar olan tüm gruplardaki elementlerdir. En yüksek ana grup kuantum sayısının s ve p orbitalleri tam dolu değildir. Soy gazlar (Asal gazlar): He (1 s 2) dışında ns 2 np 6 elektronik konfigurasyonunda olan asal gazların p alt kabukları tamamen doludur. Geçiş metalleri: 3 B – 8 B, 1 B – 2 B grup elementleri olup, tam dolu olmayan d alt kabukları ile karakterize edilirler, kolayca katyon olştururlar. Zn, Cd ve Hg ne temsilci ne de geçiş elementidir. . Lantanitler ve Aktinitler: f alt kabukları tam dolu olmayan elementlerdir.
![Temsilci Baş grup Elementlerinin Anyon ve Katyonlarının Elektronik Konfigurasyonları Na Ne3 s 1 Na Temsilci (Baş grup) Elementlerinin Anyon ve Katyonlarının Elektronik Konfigurasyonları Na [Ne]3 s 1 Na+](https://slidetodoc.com/presentation_image_h2/65410b56086232795c701ce2f997f6ef/image-5.jpg)
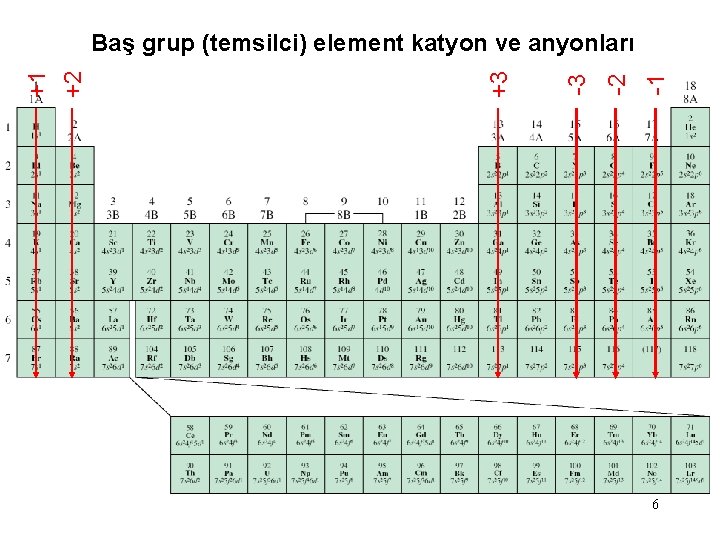
Temsilci (Baş grup) Elementlerinin Anyon ve Katyonlarının Elektronik Konfigurasyonları Na [Ne]3 s 1 Na+ [Ne] Ca [Ar]4 s 2 Ca 2+ [Ar] Al [Ne]3 s 23 p 1 Al 3+ [Ne] Atomlar elektron alarak “anyon” olarak adlandırılırlar e kazandıklarında elektronik konfigurasyonları soy gazların elektronik konfigurasyonuna benzer Atomlar elektron kayberek “katyon” olarak adlandırılırlar e kaybettiklerinde elektronik konfigurasyonları soy gazların elektronik konfigurasyonuna benzer H 1 s 1 H- 1 s 2 veya [He] F 1 s 22 p 5 F- 1 s 22 p 6 veya [Ne] O 1 s 22 p 4 O 2 - 1 s 22 p 6 veya [Ne] N 1 s 22 p 3 N 3 - 1 s 22 p 6 veya [Ne] 5

-1 -2 -3 +3 +1 +2 Baş grup (temsilci) element katyon ve anyonları 6

Izoelektronik: aynı sayıda elektrona sahip olan ve böylece aynı temel hal elektronik konfigurasyonuna sahip olan atomlardır. Na+: [Ne] Al 3+: [Ne] O 2 -: 1 s 22 p 6 or [Ne] F-: 1 s 22 p 6 yada [Ne] N 3 -: 1 s 22 p 6 yada [Ne] Na+, Al 3+, F-, O 2 -, and N 3 - Ne ile izoelektronik tir. H- ile izoelektronik olan nötral atom hangisidir ? H-: 1 s 2 He ile aynı elektronik konfigurasyondadır. 7

Geçiş elementlerine ait katyonların elektronik konfigurasyonları Bir geçiş metalinin katyonu oluşurken elektron önce ns daha sonra (n-1) d orbitalinden verilir. Fe: [Ar]4 s 23 d 6 Fe 2+: [Ar]4 s 03 d 6 or [Ar]3 d 6 Mn: [Ar]4 s 23 d 5 Mn 2+: [Ar]4 s 03 d 5 or [Ar]3 d 5 Fe 3+: [Ar]4 s 03 d 5 or [Ar]3 d 5 8

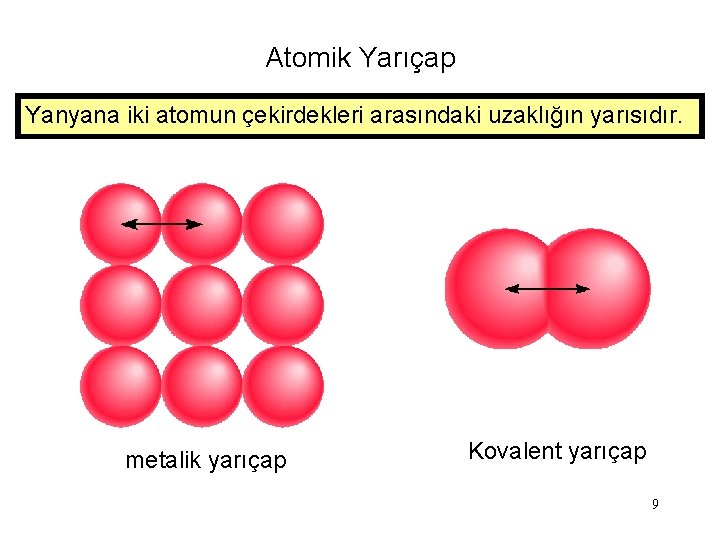
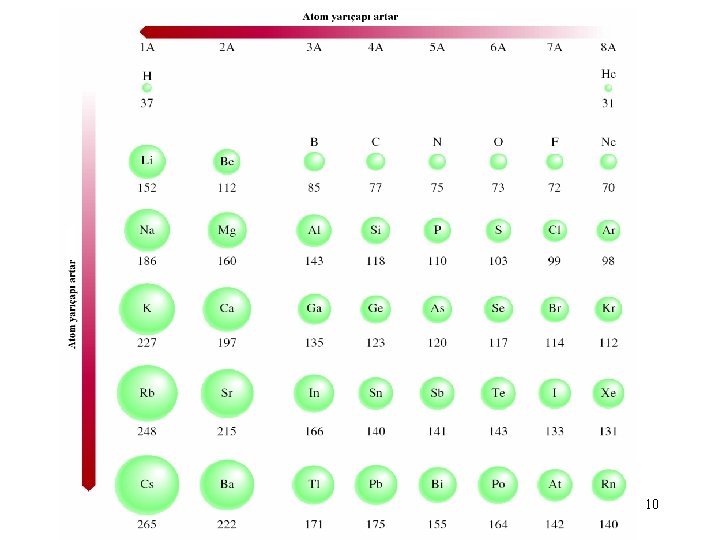
Atomik Yarıçap Yanyana iki atomun çekirdekleri arasındaki uzaklığın yarısıdır. metalik yarıçap Kovalent yarıçap 9

10

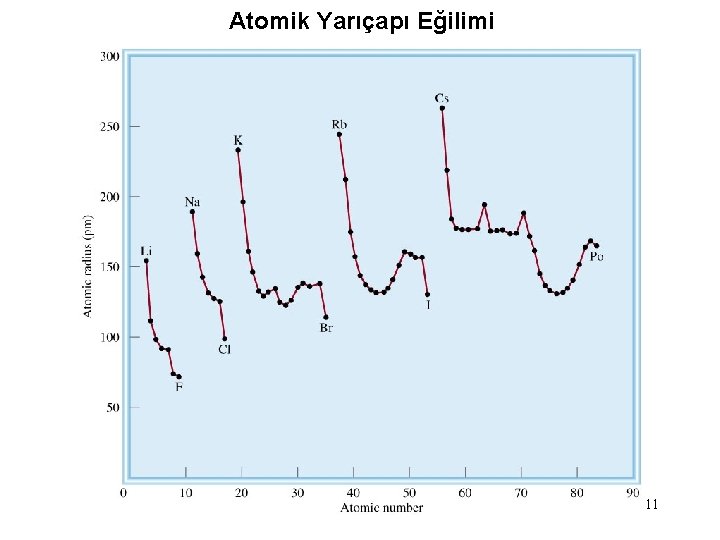
Atomik Yarıçapı Eğilimi 11

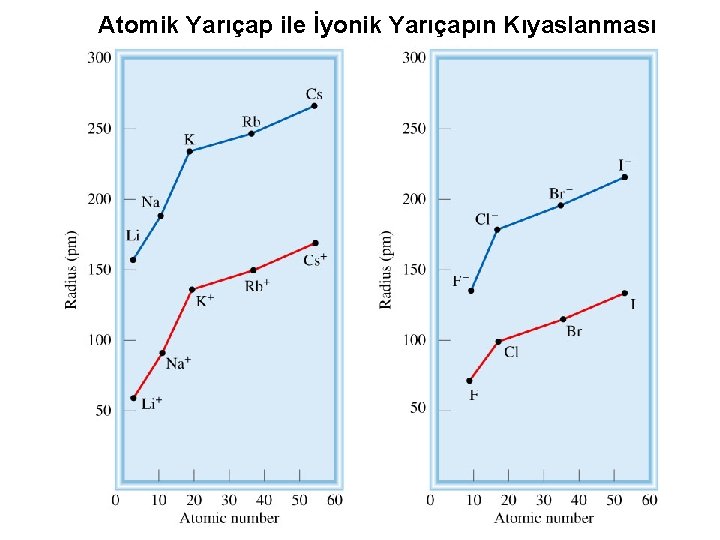
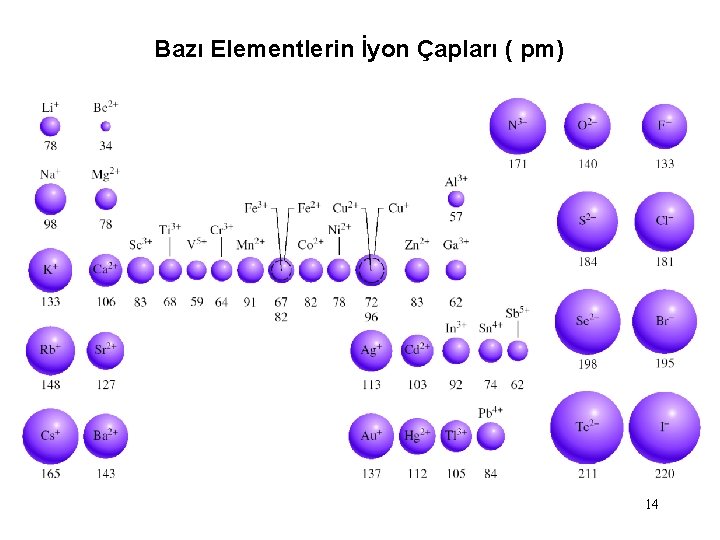
Atomik Yarıçap ile İyonik Yarıçapın Kıyaslanması 12

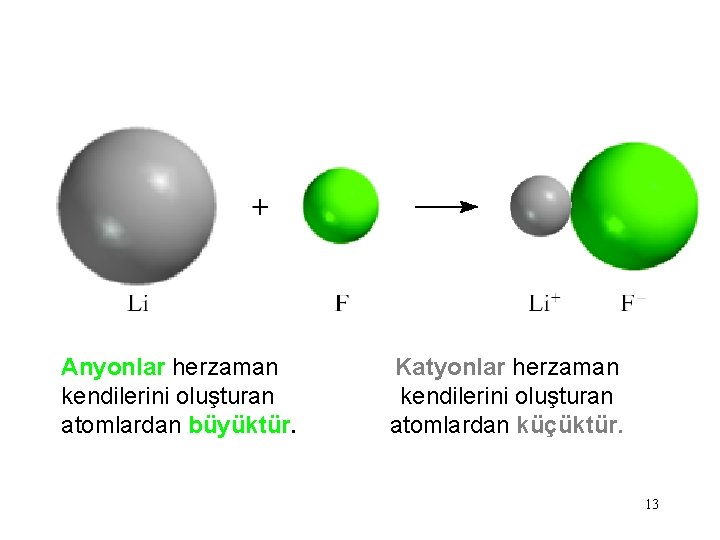
Anyonlar herzaman kendilerini oluşturan atomlardan büyüktür. Katyonlar herzaman kendilerini oluşturan atomlardan küçüktür. 13

Bazı Elementlerin İyon Çapları ( pm) 14

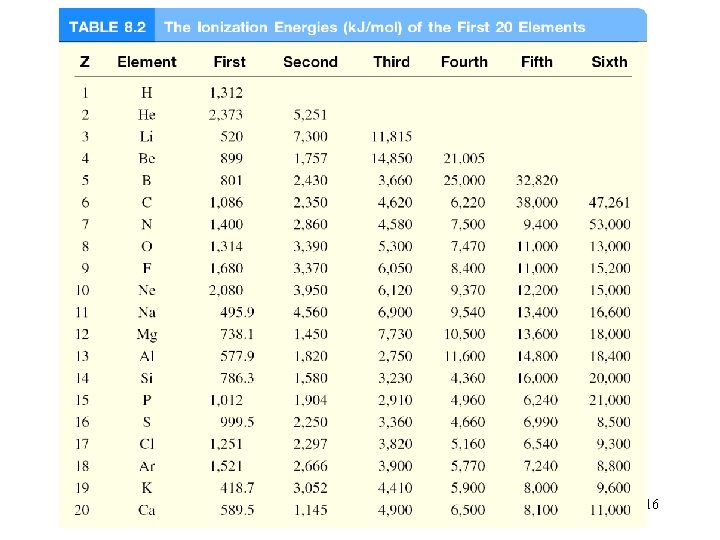
İyonizasyon Enerjisi temel halde bulunan gaz fazındaki bir atomdan bir elektron kopartılması için gereken (kj/mol) cinsinden minimum enerjidir. I 1 + X (g) X+(g) + e- I 1 birinci iyonizasyon enerjisi I 2 + X+(g) X 2+(g) + e- I 2 ikinci iyonizasyon enerjisi I 3 + X 2+(g) X 3+(g) + e- I 3 üçüncü iyonizasyon enerjisi I 1 < I 2 < I 3 15

16

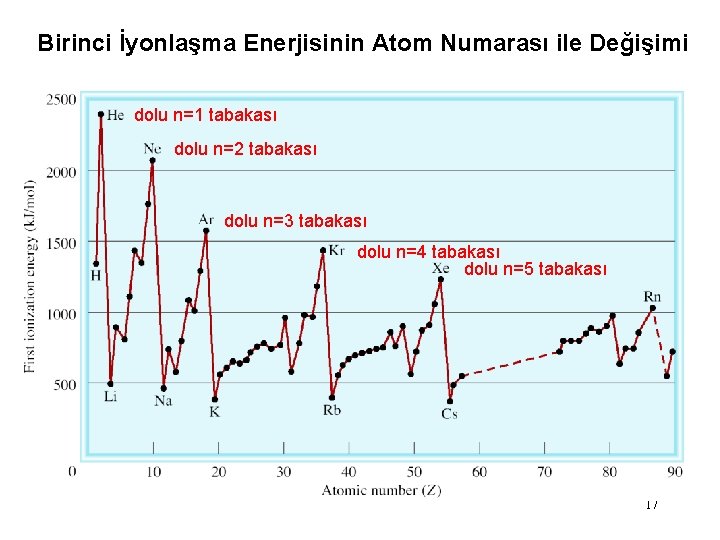
Birinci İyonlaşma Enerjisinin Atom Numarası ile Değişimi dolu n=1 tabakası dolu n=2 tabakası dolu n=3 tabakası dolu n=4 tabakası dolu n=5 tabakası 17

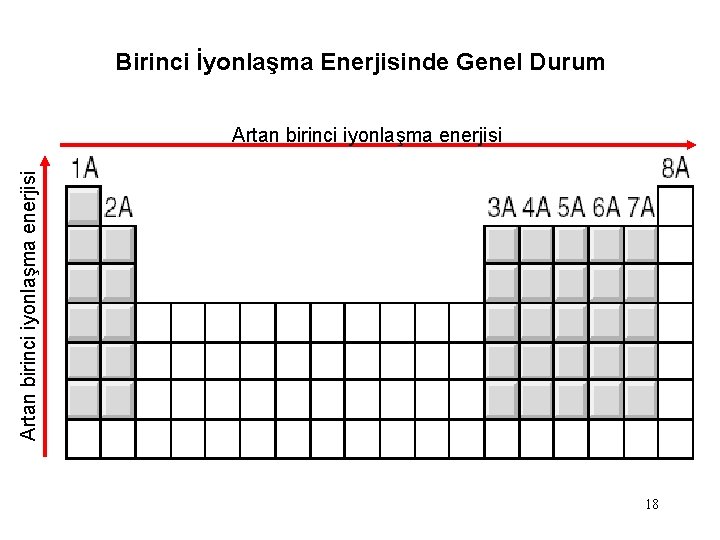
Birinci İyonlaşma Enerjisinde Genel Durum Artan birinci iyonlaşma enerjisi 18

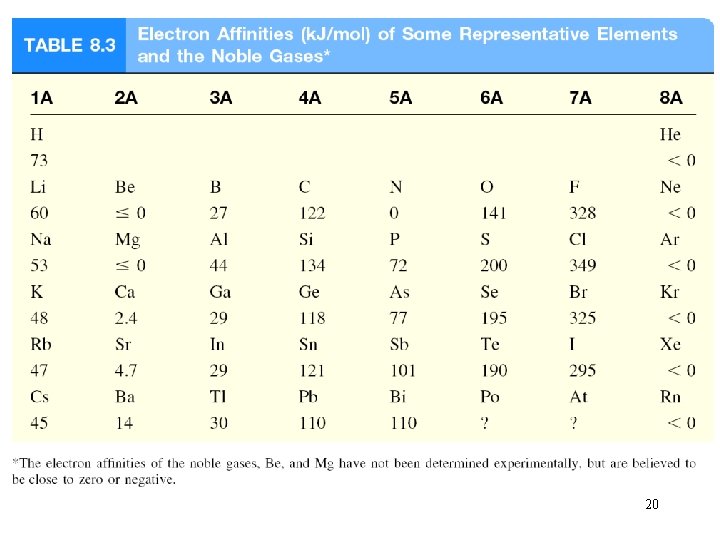
Elektron ilgisi gaz fazındaki bir atomun bir elektron alarak anyona dönüşmesi sırasında açığa çıkan enerjidir. X (g) + e- X-(g) F (g) + e- X-(g) DH = -328 k. J/mol EA = +328 k. J/mol O (g) + e- O-(g) DH = -141 k. J/mol EA = +141 k. J/mol 19

20

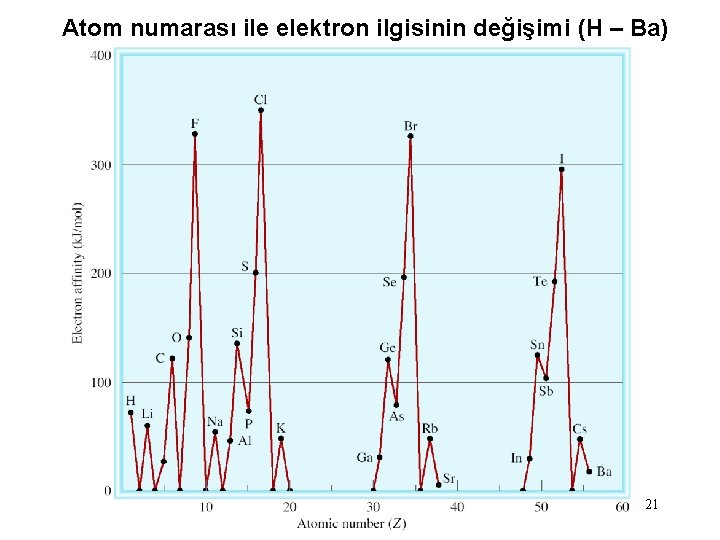
Atom numarası ile elektron ilgisinin değişimi (H – Ba) 21