Autonomn nervov systm Leona Nepejchalov SKVBL znan nezvisl

Autonomní nervový systém Leona Nepejchalová ÚSKVBL

značně nezávislý, jeho činnost nepodléhá přímé volní kontrole. Primárně ovlivňuje základní viscerální funkce: srdeční výdej, průtok krve jednotlivými orgány, trávení, vylučování, … (x somatický nervový systém) Léčiva ovlivňující autonomní nervový systém, příslušné autonomní receptory v cílových buňkách (myokard, hladká svalovina, endoteliální buňky, žlázy).

Anatomické dělení: ústředí v jádrech CNS (nejvyšší regulační úroveň ve středním mozku a prodloužené míše) Sympatický (thorakolumbální) – pregangliová vlákna vycházejí z CNS v hrudní a bederní oblasti míchy (míšní rohy) přes míšní nervy – ganglia jsou lokalizována převážně paravertebrálně, zbývající prevertebrálně v břišní dutině (krátká pregangliová a dlouhá postgangliová vlákna) – dříve označován jako ergotropní (umožňující výdej energie): stimulace srdeční činnosti, vzestup glykémie a kožní vazokonstrikce

Parasympatický (kraniosakrální) – pregangliová vlákna opouštějí CNS přes hlavové nervy (hlavně III. , VII. , IX. a X. ) a třetí a čtvrté sakrální míšní kořeny – motorická ganglia jsou uložena difúzně ve stěně inervovaných orgánů (výjma gangl. ciliare, pterygopalatinum, submandibulare, oticum), (dlouhá preganliová a krátká postgangliová vlákná) – trofotropní (podporující růst): např. zpomalené srdeční frekvence a stimulace trávícího traktu

aferentní vlákna – z periferie do CNS eferentní vlákna – z CNS do efektorových buněk

Neuropřenašeče (uvolňují se z terminálních zakončení a varikozit) Acetylcholin – cholinergní vlákna syntetizují – eferentní pregangliová autonomní vlákna – somatická (neautonomní) motorická vlákna pro kosterní svalovinu (neurosvalová ploténka) – postgangliová vlákna parasympatiku – některý postgangliová vlákna sympatiku u synaptické části buněčné membrány velké množství vezikul s acetylcholinem

– je syntetizován v cytoplazmě z cholinu a acetyl. Co. A, tato syntéza je katalyzována cholinacetyltransferázou, acetyl-Co. A je syntetizován v mitochondriích, které se rovněž hromadí v synaptické části cytoplazmy – po vyplavení z presynaptického zakončení se molekuly ACh vážou na cholinergní (acetylcholinový) receptor a aktivují jej. ACh je štěpen acetylcholinesterázou na cholin a acetát. Ve většině cholinergních synapsí jsou vysoké koncentrace acetylcholinesterázy, proto poločas ACh je velmi krátký. AChe je i v erytrocytech, obdobným typem enzymu s nižší afinitou je butyrylcholinesteráza (v krevní plazmě, játrech, gliových buňkách, …)

Noradrenalin (norepinefrin) – noradrenergní (= adrenergní) vlákna – většina postgangliových (postganglionárních) vláken sympatiku – dřeň nadledvin analogická s postgangliovými neurony sympatiku (embryologicky) uvolňuje směs adrenalinu a noradrenalinu – skladován také v měchýřcích, syntéza katecholaminových neurotransmiterů je mnohem složitější (tyrosin → dopamin→ NA …) – po vyplavení se váže na postsynaptické a presynaptické receptory

– uvolněný noradrenalin je zpět vychytáván do cytoplazmy nervové synapse, varikozity, na jeho degradaci se podílí monoaminooxidáza (v mitochondriích) – metabolická degradace není hlavním mechanismem ukončení účinku: difúze po koncentračním gradientu od receptorů (rozklad v plazmě nebo játrech), zpětné vychytávání (reuptake) do cytoplazmy nervového zakončení (uptake 1) nebo perisynptických gliových buněk nebo hladkosvalových buněk (uptake 2)

purinergní vlákna – jejich aktivací dochází k uvolnění ATP a dalších příbuzných purinů; jsou v autonomních efektorových tkáních zažívacího a močového ústrojí = jedná se o neadrenergní, necholinergní přenašeče…)

Receptory: cholinergní-muskarinové M 1, M 2, M 3 -nikotinové adrenergní-Alfa 1 -Alfa 2 -Beta 1 -Beta 2 -Beta 3 -Dopaminové 1 (D 1, DA 1) -Dopaminové 2 (D 2, DA 2) V srdci jsou přítomny β 1 a β 2 adrenergní receptory, početně převažuje β 1 nad β 2.

Funkční uspořádání Sympatický (thorakolumbální) – dříve označován jako ergotropní (umožňující výdej energie): stimulace srdeční činnosti, vzestup glykémie a kožní vazokonstrikce Parasympatický (kraniosakrální) – trofotropní (podporující růst): např. zpomalené srdeční frekvence a stimulace trávícího traktu

Kardiovaskulární systém – kontrola středního arteriálního tlaku – jakákoliv změna, která ho ovlivňuje, vyvolá kompenzující homeostatickou sekundární odpověď (při i. v. podání noradrenalinu se předpokládají silné vazokonstrikční účinky, zvýšení periferní cévní rezistence a středního arteriálního tlaku a u srdce zvýšení tepové frekvence a kontraktility, ale v organismu se zachovanými reflexy dojde prostřednictvím impulsů z baroreceptorů k negativní zpětné reakci na zvýšení krevního tlaku, sníží se aktivita sympatiku, zvýší se působení parasympatiku → zřetelný pokles tepové frekvence (bradykardie), dojde pouze k mírnému vzestupu středního tepenného tlaku a vzestupu periferního cévního odporu.

Presynaptická regulace Princip negativní zpětné vazby – přes autoreceptory (regulují vyplavování vlastního neurotransmiteru Presynaptické α 2 -adrenergní receptory – po aktivaci NA (a podobnými molekulymi) sníží další vyplavování NA z nervových zakončení Presynaptické β-receptory – usnadňují vyplavování NA Heteroreceptory – na zakončení adrenergních vláken pro ACh (M 1 receptory), prostaglandiny a polypeptidy

Postsynaptická regulace Vliv předchozí aktivity – up nebo down-regulace počtu receptorů Vliv jiných souběžných dějů – rychlý excitační postsynaptický potenciál je následován pomalým inhibičním postsynaptickým potenciálem (hyperpolarizace) a po něm následuje pomalý EPSP (pomalý potenciál, lze ho vyvolat i peptidem P, který uvolňují kolaterály senzorických vláken = pomalé potenciály jsou důležité pro ovlivnění dalších odpovědí postsynaptické buňky na následující primární excitační podněty z presynaptických zakončení).

Farmakologické ovlivnění Léčiva vegetativního nervového systému (autonomic drugs) a) selektivní – zasažení syntézy a skladování neurotransmiteru, obsazování receptorů (aktivace nebo blokování) b) neselektivní – např. lokální anestetika

· sympatotropní látky sympatomimetika, adrenergika, andrenegní agonisté, adrenergní látky, stimulátory sympatiku sympatolytika, adrenolytika, antiadrenergika, adrenergní blokátory, antagonisté adrenergních receptorů, sympatoplegika · parasympatotropní látky parasympatomimetika, cholinergika, cholinergní agonisté, cholinergní látky, stimulátory parasympatiku parasympatolytika, cholinolytika, anticholinergika · látky působící v gangliích gangioplegika, gangliové blokátory
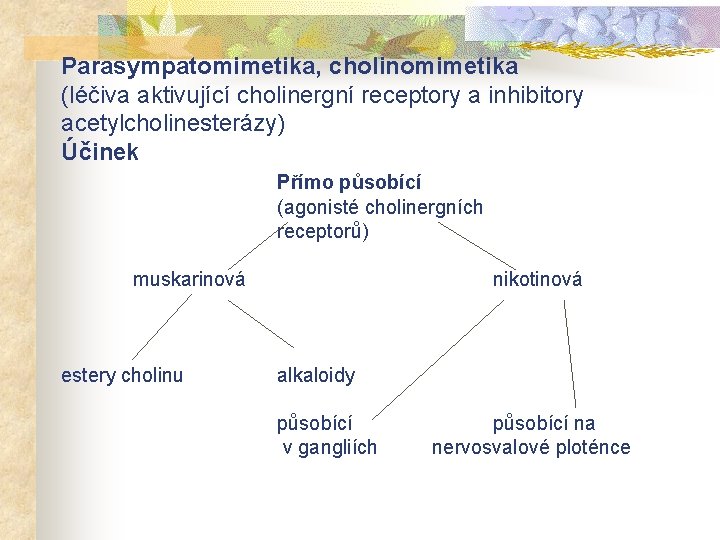
Parasympatomimetika, cholinomimetika (léčiva aktivující cholinergní receptory a inhibitory acetylcholinesterázy) Účinek Přímo působící (agonisté cholinergních receptorů) muskarinová nikotinová estery cholinu alkaloidy působící v gangliích působící na nervosvalové ploténce

estery cholinu – obsahují kvarterní amoniovou skupinu, nesou trvale náboj, a nejsou rozpustné v tucích – špatně se absorbují a špatně pronikají do CNS, v GIT podléhají hydrolýze a mají tedy nízkou účinnost při p. o. podání – rozdíly v rychlosti hydrolýzy acetylcholinesterázou (a jinými) – nejrychleji acetylcholin, odolnější metacholin, zcela odolné estery kyseliny karbamové (karbachol, betanechol) – acetylcholin má afinitu jak k muskarinovým, tak nikotinovým receptorům, u metacholinu převyšuje afinita k muskarinovým, u karbacholu je afinita k nikotinovým nepatrně vyšší, betanechol má afinitu pouze k muskarinovým receptorům, pilokarpin (při i. v. podání krátká hypotenze následovaná hypertenzním účinkem díky stimulaci M 1 receptorů v membránách postgangliových buněk = stimulace ganglií)

cholinomimetické alkaloidy – terciární struktura, dobře rozpustné v tucích (muskarin má terciální strukuru a hůře se vstřebává z GIT), odolné vůči cholinesteráze – pilokarpin, nikotin, lobelin, oxotremorin (dobře proniká do CNS), dimetylfenylpiperazin (málo proniká do CNS) – vylučování převážně ledvinami, clearance terciálních aminů zvýší okyselení moče

Ovlivnění muskarinových receptorů v orgánech – stimulace parasympatiku a ovlivnění rozmístění muskarinových receptorů Vliv nikotinových agonistů – fyziologie vegetativních ganglií a nervosvalové ploténky příčně pruhované svaloviny

Oko – muskarinové receptory – kontrakce hladkého svalstva duhovky (s následnou miózou) a řasnatého tělesa (akomodace do blízka, drenáž přední oční komory)

Kardiovaskulární systém – muskarinoví agonisté – snížení periferního cévního odporu a tepové frekvence – srdce – sinoatriální uzel – snížená frekvence (negativní chronotropie) – síně – pokles kontraktility (negativní ionotropie), zkrácení refrakterní periody – atrioventrikulární uzel – snížená rychlost vedení (negativní dromotropie), prodloužení refrakterní periody – komory – malý pokles kontraktility – cévy – tepny – dilatace (prostřednictvím EDRF – endothelium derived relaxing factor) – konstrikce (přímý účinek vysokých dávek) – žíly – dilatace (prostřednictvím EDRF – endothelium derived relaxing factor) – konstrikce (přímý účinek vysokých dávek) tyto projevy jsou regulovány homeostatickými reflexy

Respirační systém – průduškové svaly – kontrakce (bronchokonstrikce) – žlázy průdušnice a průdušek - stimulace Gastrointestinální trakt – vzestup motility – sfinktery – relaxace – stimulace sekrece slinných a žaludečních žláz, slaběji pankreatu a intestinálních žlázek Urogenitální trakt – m. detrusor – kontrakce – trigonum a sfinkter – relaxace

Žlázy – stimulace sekrece potních, slzných a nazofaryngeálních žláz CNS – mozek více muskarinových receptorů (nikotin má ale výraznější vliv) – mícha více nikotinových receptorů – vliv průchodnosti hematoencefalickou bariérou Periferní nervový systém – ovlivnění ganglií (nikotinové receptory) (nervosvalové spojení – nikotinové receptory – acetylcholin a nikotin vyvolávají ionoforézu a depolarizaci nervosvalové ploténky)
Nepřímo působící (inhibitory cholinesterázy) reverzibilní ireverzibilní edrofonium, karbamáty organofosfáty

Primární účinek nepřímých cholinomimetik – ovlivnění aktivního centra acetylcholinesterázy Jednoduché primární alkoholy s kvarterní amoniovou skupinou – edrofonium – indikace – myasthenia gravis, ileus, arytmie Estery karbamové kyseliny s alkoholy nesoucími terciární amoniovou skupinu (karbamáty) – neostigmin (myasthenia gravis, ileus), pyridostigmin (myasthenia gravis), fysostigmin (glaukom), ambenonium (myasthenia gravis), demecarium (glaukom) Organické sloučeniny kyseliny fosforečné (organofosfáty) – isoflurofát, je nahrazen echothiofátem (glaukom)

Karbamáty – slabá absorbce kvarterních sloučenin přes spojivky, kůži, plíce; relativně málo rozpustné v tucích (téměř neproniká do CNS) – fysostigmin – při obdobných cestách podání se dobře absorbuje a proniká do CNS – v organismu rozkládány nespecifickými esterázami a cholinesterázou, poločas účinku je závislý na stabilitě komplexu inhibitor - enzym

Organofosfáty – se dobře vstřebávají přes kůži, střevo, plíce i spojivky – pro obratlovce většinou nebezpečné – thiofosfáty (parathion, malathion, …) – dobře rozpustné v tucích, v organismu aktivnovány na kyslíkaté sloučeniny; malathion a některé další organofosfáty jsou v organismu savců a ptáků degradovány na neúčinné metabolity, u ryb k této detoxikaci nedochází – parathion obratlovci nedetoxikují

snížením aktivity cholinesterázy dojde k zvýšení koncentrace endogenní acetylcholinu u cholinergních receptorů kvarterní alkoholy – váží se reverzibilně na aktivní centrum a brání přístupu acetylcholinu, komplex přetrvává krátce (2 – 10 min. ) = reverzibilní inhibitory karbamátové estery – dvoustupňová hydrolýza jako u acetylcholinu, s prodlouženým druhým hydratačním krokem karbamylového enzymu (30 min. – 6 hod. ) = reverzibilní inhibitory organofosfáty – vazba na enzym s následnou hydrolýzou a fosforylací aktivního centra; komplex je mimořádně stabilní (stovky hodin) = ireverzibilní inhibitory

Vliv na: CNS – v tucích rozpustné inhibitory difúzní aktivace EEG a subjektivní pocit povzbuzení (nízké koncentrace), vysoké koncentrace vyvolávají generalizované křeče (kóma s respirační zástavou) Oko, respirační trakt, zažívací a močové ústrojí – analogický účinek jako o přímých cholinomimetik Kardiovaskulární systém – zvýší aktivaci parasympatických i sympatických ganglií inervujících srdce a cholinergních receptorů na neuroefektorových buňkách srdeční a cévní svaloviny s cholinergní inervací – převažují účinky na parasympatickou složku, které napodobují vagové dráždění: klesá srdeční frekvence, zpomaluje se atrioventrikulární vedení, snižuje se stažlivost síní a rovněž poněkud kontraktilita komor (díky presynaptické modulaci sympatické aktivity a inhibici postsynaptických účinků sympatiku) – cholinomimetický efekt na hladké svalstvo cév je minimální, protože je málo cévních řečišť inervováno cholinergně

– střední dávky vedou k mírné bradykardii, poklesu srdečního výdeje a krevní tlak je nezměněn nebo mírně pokleslý; vysoké (toxické) dávky vedou k výrazné bradykardii a hypotenzi Nervosvalové spojení – nízké terapeutické koncentrace prodlužují a zesilují účinky fyziologicky uvolňovaného acetylcholinu = zvýšení síly svalových stahů (hlavně relaxovaných kurareformními myorelaxačními látkami nebo při myasthenii gravis – vyšší koncentrace vedou k fibrilacím svalových vláken, fascikulace postihující celou motorickou jednotku (šíření po motorickém nervu), při silné inhibici se vytváří neuromuskulární blok – některé kvarterní karbamáty (neostigmin) mají i druhotný přímý agonistický účinek na nikotinové receptory nervosvalového spojení

Klinické využití cholinomimetik Glaukom – snížení nitroočního tlaku usnadněním odtoku očního moku a snížením rychlosti jeho produkce – metacholin, karbachol, pilokarpin (nejčastěji používán) – fysostigmin, demecarium, echothiofát, isoflurofát snížená činnost hladkého svalstva gastrointestinálního a močového traktu, kde není obstrukce – např. pooperační ileus, retence moči (po operaci, porodu, poškozená mícha – betanechol – neostigmin Léčiva: Hormotonin inj ad. us. vet (karbachol) a Kostigmin inj ad us. vet. inj. (neostigmin)

myasthenia gravis – nepřímá cholinomimetika (neostigmin, pyridostigmin, ambenonin) přerušení neuromuskulární blokády, která je doplňkem chirurgického zákroku – neostigmin, edrofonium supraventrikulární tachykardie – dříve edrofonium (nahrazeno blokátory kalciového kanálu a adenosinem) otravy atropinem, tricyklickými antidepresivy – blokády muskarinových receptorů (kompetetivní) – teoreticky fysostigmin

Nežádoucí účinky Přímo působící muskarinová cholinomimetika – zvýšené muskarinové dráždění – nevolnost, zvracení, průjmy, slinění, pocení, kožní vazodilataci, bronchokonstrikci Inhibitory cholinesterázy – obdobné (mióza, slinění, pocení, bronchokonstrikce, zvracení a průjmy), rychle následuje postižení CNS a periferní nervosvalové blokády Reaktivátor acetylcholinesterázy Trimedoxim

Parasympatolytika, cholinolytika (látky blokující cholinergní receptory) 2 velké skupiny látek – antimuskarinové a antinikotinové látky A) Léčiva blokující muskarinové receptory Typický příklad: atropin (Atropin Biotika inj. ad us. vet. , Atropin Biotika mite inj. ad us. vet. )

- Přírodní látky jsou terciálními estery kyseliny tropové: atropin – rulík zlomocný, velice slabě ovlivňuje nikotinové receptory (nelze klinicky téměř pozorovat) = vysoce selektivní (specifita u syntetických látek je nižší), ale nerozlišuje M 1, M 2 a M 3 skopolamin – blín černý Účinnější l(-)-izomery (jsou přítomné v rostlinách), ale snadno racemizují, a komerční substance jsou racemáty. - semisyntetické terciární amoniové analogy homatropin - syntetické propanthelin, glykopyrolát, pirenzepin, dicyklomin, tropicamid, ipratropium, benzotropin

Farmakokinetika Absorbce – přírodní a většina terciárních se absorbuje dobře ze střeva a přes spojivku, ve vhodném vehikulu i transdermálně – jen 10 – 30 % se absorbuje u p. o. podaných kvarterních sloučenin (mají náboj a jsou málo rozpustné v tucích) Distribuce – po absorbci široce distribuovány, CNS zasáhnou do 0, 5 – 1 hodiny (kvarterní deriváty se do mozku dostávají jen v malém množství) Metabolismus a exkrece – atropin má poločas 2 hodiny, velká část je vyloučena nezměněná močí, zbytek jako hydrolytické zbytky a konjugáty. Účinky odeznívají rychle, výjimka oko (48 – 72 hodin). Některé živočišné druhy (králík) s účinným enzymem atropin esterázou rychle metabolizují atropin (ochrana před intoxikací).

Farmakodynamika Reverzibilní kompetitivní blokáda účinku acetylcholinu na muskarinových receptorech. Účinek záleží na tkáni a na příslušném agonistovi. CNS – atropin mírně stimuluje centra v prodloužené míše (jádra vagu) – bradykardie (ta je pak vystřídána tachykardií vyvolanou antimuskarinovým působením v sinoatriálním uzlu) a má pomalu se rozvíjející a dlouho trvající sedativní účinky – skopolamin má výraznější sedativní účinek – léčba kinetóz Oko – pupilární sfinkter pod převahou sympatické dilatační aktivity = mydriáze – paralýza ciliárního svalu – cykloplegie = ztráta akomodační schopnosti (nezaostří do blízka) – snížení lakrimace (využití v oftalmologii)

Kardiovaskulární systém – srdeční síně s množstvím parasympatických vláken (n. vagus) a sinoatriální uzel vnímavé k účinku látek blokujících muskarinové receptory – blokáda bradykardického účinku vagu = tachykardie (střední a vysoké dávky) x nízké dávky stimulují centrálně vagus; – atrioventrikulární uzel – ovlivňování stavu při zvýšené stimulaci vagu (vliv na EKG) – ovlivnění komor je slabé – omezená parasympatická inervace cévního řečiště, téměř všechny cévy obsahují na endoteliálních buňkách muskarinové receptory, které vyvolávají vazodilataci (stimulace přímými muskarinovými agonisty vede k uvolnění endoteliálního relaxačního faktoru EDRF blokování antimuskarinovými léčivy

Respirační systém – vagus inervuje hladkou svalovinu a žlázy (bronchodilatace a snížená bronchiální sekrece – nejsou tak účinná jako β-mimetika, ale využívají se také k léčbě astmatu Gastrointestinální trakt – ovlivňuje motilitu a některé sekretorické funkce střeva, protože je ovlivněn také lokálními hormony a necholinrgními nervy, ani úplná muskarinová blokáda aktivitu střeva úplně nepotlačí – snížení tvorby slin – sekrece v žaludku je snížena méně výrazně (až vyšší dávky), bazální sekrece ovlivněna více než sekrece stimulovanou (např. potravou)

– využití pirenzepinu vhodnější než atropinu – sekreční činnost střev a slinivky ovlivněna málo – motilita hladké svaloviny ovlivněna výrazně (relaxace, snížení tonu a peristaltické aktivity, zpomaleno vyprazdňování žaludku a prodloužena délka střevní pasáže) – některá syntetické látky mají i spazmolytický vliv Urogenitální trakt – relaxace hladké svaloviny dělohy a močového měchýře (léčba spazmů při mírných zánětech) Potní žlázy – potlačení termoregulačního pocení

Léčebné využití Kinetózy – ovlivnění některých vestibulárních poruch (skopolamin) Oční onemocnění a oftalmologický vyšetření – využití mydriázy (někdy vhodnější krátkodoběji působící stimulátory α-adrenergních receptorů – fenylefrin) – prevence vzniku synechií (srůstů) při uveitidě nebo iritidě (dlouhodoběji působící léčiva – homatropin) Peptické vředy - využívány při léčbě před využíváním antagonistů histaminových (H 2) receptorů (dnes jako doplňková terapie při intoleranci k H 2 antagonistům), u gastrických peptických vředů je mnohdy kontraindikováné jejich využití (zpomalení vyprazdňování)

Vagové dráždění při infarktu myokardu – mohou vést až k depresi sinoatriálního a atrioventrikulárního uzlu Inhalační terapie astmatu – ipratropium v aerosolu (dříve využívány jako premedikace při asnestezii etherem) Otrava cholinomimetiky – houby, insekticidy (organofosfáty), využití látek s terciárním dusíkem ovlivní nejen periferní, ale i centrální nežádoucí účinky – dále se využívají látky regenerující aktivní enzym komplexu organofosforcholinesteráza (tzv. aktivátory cholinesterázy): oximy (pralidoxim = PAM, diacetylmonoxim = DAM, obidoxim, u nás schválen pro použití trimedoxim), účinné hlavně pokud fosforylované komplexy nepodlehly stárnutí

Nežádoucí účinky Mydriáza a cykloplegie – vedlejší účinek, pokud nastoupil během terapeutického snížení motility GIT, … x terapeutický v oftalmologii Intoxikace – sucho v dutině ústní, mydriáza, tachykardie, horká a začervenalá kůže, rozrušení Mláďata mnohem citlivější. Léčba – symptomatická – fyzostigmin – nemusí být vždy prospěšný (méně bezpečný) – kontrola teploty – ochlazující zábaly – terapie křečí - diazepam dále lze využít neostigmin, na hypotenzi sympatomimetická léčiva (fenylefrin, metoxamin)

Kontraindikace Relativní (jasné antimuskarinové dráždění lze vždy léčit atropinem) Glaukom, gastrické vředy (ale lze mírnit současným podáním antacid nebo H 2 antagonistů)

B) Ganglioplegika Blokují účinky acetylcholinu a cholinergních agonistů na nikotinových receptorech parasympatických a sympatických vegetativních ganglií; některé látky blokují iontový kanál ovládaný nikotinovým receptorem. Problémem je nedostatečná selektivita, nežádoucí účinky – současná terapeutická indikace už jen na krátkodobou kontrolu krevního tlaku

Kinetika Syntetické aminy: tetraetylamonium (velice krátkodobý účinek ) hexametonium dekametonium (vyvolává výraznou depolarizaci nervosvalové ploténky) tyto látky s kvarterním dusíkem jsou po p. o. příjmu slabě a nepravidelně vstřebávány mecamylamin (sekundární dusík, lépe se vstřebává z GIT) trimethafan (krátkodobě působící ganglioplegikum, p. o. neúčinné)

Mechanismus účinku (dynamika) Depolarizační blokáda nikotinových receptorů – nikotin, karbamylcholin (i acetylcholin pokud se podá po inhibitoru cholinesterázy) Nedepolarizační blokáda – všechna terapeuticky využívaná ganglioplegika Hexametonium – obsazuje vazebná místa v iontovém kanálu CNS – kvarterní amoniové látky a trimethafan nemají centrální účinek – mecamylamin – proniká hematoencefalickou bariérou – útlum, třes, choreatické pohyby a mentální poruchy Oko – cykloplegie se ztrátou akomodace, mírná mydriáza (sympaticka i parasympatická inervace duhovky)

Kardiovaskulární systém – blokáda ganglií vyvolá významný pokles arteriolárního a venomotorického tonu pokles krevního tlaku (snížení periferního cévního odporu a venózního návratu) = ortostatická hypotenze – snížení kontraktility a mírná tachykardie (ganglioplegika blokují vliv parasympatiku na sinoatriální uzel) GIT – snížení sekrece (ale není dostatečné), výrazný pokles motility Dále – ztížení mikce (u pacientů s problémy s prostatou), zamezení erekce a ejakulace – potlačení termoregulačního pocení, ale k termoregulaci postačuje vazodilatace Nejsou ovlivněny muskarinové, α- a β-adrenergní receptory, spíše homeostatické reflexy.

Léčebné použití a nežádoucí účinky Výhodnější využití mnohem selektivnějších léčiv Spíše pouze na snižování krevního tlaku, akutní plicní edém (trimethafan)

Sympatomimetika, adrenomimetika (látky aktivující adrenergní receptory) α-receptory – α 1 A – α 1 B – α 2 A – α 2 B atd. β-receptory – β 1 – β 2 – β 3 dopaminové receptory – důležité v mozku, splanchnickém a renálním krevním řečišti – D 1 – D 2 – D 3 (limbický systém mozku) Selektivita receptorů – léčiva preferenčně aktivují jednu skupiny receptorů v koncentracích, které u další skupiny nejsou dostačující pro aktivaci – nejde o přirozeně absolutní vlastnost, při vyšších koncentracích mohou být aktivovány i jiné, příbuzné receptory

α–agonisté fenylefrin, metoxamin – α 1 -selektivní adrenalin, noradrenalin – α 1 ~ α 2 klonidin, α-metylnoradrenalin – α 2 -selektivní β–agonisté noradrenalin, dobutamin, prenalterol – β 1 -selektivní isoprenalin, adrenalin – β 1 ~ β 2 fenoterol, albuterol, terbutalin, metaproterenol – β 2 selektivní

Farmakokinetika Účinek katecholaminů je zprostředkován receptory, které jsou funkčně spojeny s G-proteinem s různými efektorovými bílkovinami G proteiny typu Gs – stimulují adenylylcyklázu typu Gi – inhibiční vliv na aktivitu adenylylcyklázy GDP GTP Příklady dalších efektorů funkčně spojených s aktivací α -podjednotek G proteinu: adenylylcykláza, c. GMP fosfodiesteráza, fosfolipáza C, iontové kanály (kalciové)

Receptorová regulace – odpovědi nejsou fixní – katecholaminy, léčiva, hormony, věk … mohou způsobit změny v reaktivitě tkání (změny počtu a funkčních vlastností) = desenzitizace – po vystavení tkáně (buňky) působení agonisty je méně citlivá na další stimulaci tímto podnětem (tolerance, refrakterita, tachyfylaxe). Mechanismus desenzitizace – sekvestrace receptorů (reverzibilní proces, receptory dočasně nedostupné) – down-regulace (snížení počtu díky enzymatickému ovlivnění nebo sníženou syntézou – fosforylace receptoru na jeho plazmatické části – stížení interakce s G proteinem afinita k α- nebo β-adrenergním receptorům, účinnost, odolnost vůči enzymům je ovlivněna chemickou strukturou sympatomimeticky působících katecholaminů.
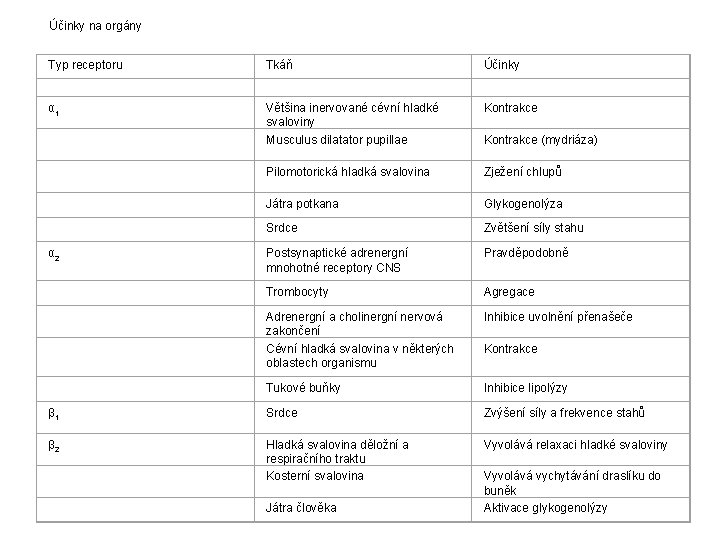
Účinky na orgány Typ receptoru Tkáň Účinky α 1 Kontrakce Většina inervované cévní hladké svaloviny Musculus dilatator pupillae Pilomotorická hladká svalovina Zježení chlupů Játra potkana Glykogenolýza Srdce Zvětšení síly stahu α 2 Postsynaptické adrenergní mnohotné receptory CNS Pravděpodobně Trombocyty Agregace Adrenergní a cholinergní nervová zakončení Cévní hladká svalovina v některých oblastech organismu Inhibice uvolnění přenašeče Tukové buňky Inhibice lipolýzy β 1 Srdce Zvýšení síly a frekvence stahů β 2 Vyvolává relaxaci hladké svaloviny Hladká svalovina děložní a respiračního traktu Kosterní svalovina Játra člověka Kontrakce (mydriáza) Kontrakce Vyvolává vychytávání draslíku do buněk Aktivace glykogenolýzy

Kardiovaskulární systém Cévy Významné ovlivnění periferní cévní resistence a kapacity žilního řečiště. α-receptory zvyšují arteriální rezistenci, ale β 2 -receptory způsobují relaxaci hladké svaloviny cév. Rozdíly v zastoupení receptorů: kožní cévy, splanchnická oblast – převážně α vazokonstrikce kosterní svalovina - podle aktivace α- nebo β- receptorů kontrakce nebo dilatace renální, splanchnické, koronární a mozkové arterie – D 1 -receptory vazodilatace

Srdce β-receptory – zvýšený přísun vápníku do buněk myokardu, zvýšená aktivita fyziologických (sinoatriální uzel) i abnormálních (Purkyňova vlákna) pacemakerů, pozitivně chronotropní účinek, zvýšená rychlost vedení v atrioventrikulárním uzlu, zkrácení refrakterní periody, zvýšení kontraktility (pozitivně ionotropní účinek), zrychluje se relaxace. Svalové vlákno se silněji stahuje, stah trvá krátce. Rychleji stoupá a klesá nitrokomorový tlak a je zkrácena vypuzovací doba.

Krevní tlak α-selektivní účinek – zvýšení periferní arteriální rezistence (prudké zvýšení krevního tlaku), snížení žilní kapacitance (u zdravích jedinců po zvýšení tlaku dojde ke stimulaci vagu a zpomalení tepové frekvence, zvýšení žilního návratu vede ke zvýšení tepového objemu) β-selektivní účinek – zvýšení srdečního výdeje, nezměněný nebo mírně zvýšený systolický tlak a pokles diastolického tlaku; snižuje periferní odpor v některých cévních řečištích (dilatace)

Oko α-adrenergní receptory v musculus dilatator pupillae – mydriáza α-agonisté zvyšují odtok nitroočního moku, β-agonisté zřejmě zvyšují jeho tvorbu Respirační trakt β 2 -receptory – hladká svalovina bronchů (relaxace = bronchodilatace) α 1 -receptory – cévy v horních partiích dýchacího ústrojí (dekongestivní účinky) GIT α-agonisté i β-agosnisté – relaxace hladké svaloviny α 2 -receptory – snižují také pronikání vody a solí do střevního lumen

Urogenitální trakt β-receptory – relaxace dělohy α-receptory – spodina močového měchýře, uretrální sfinkter – kontrakce β 2 -receptory – stěna močového měchýře – relaxace α-receptory – ejakulace Exokrinní žlázy Slinné žlázy – regulace sekrece amylázy a vody Apokrinní potní žlázy – α-stimulace zvýšení produkce potu (psychogenní) x termoregulační žlázy ovládány sympatickými cholinergními postgangliovými vlákny (muskarinové cholinergní receptory)

Metabolismus β-adrenergní receptory v tukových buňkách – zvýšení lipolýzy (typ β 3) α 2 -receptory – inhibice lipolýzy Zvýšení glykogenolýzy a uvolnění glukózy do krevního oběhu (ve vysokých koncentracích mohou katecholaminy vyvolat metabolickou acidózu) Stimulace β 2 -adrenergních receptorů vede k zvýšenému průniku draslíku do buněk a tím snížení extracelulárního draslíku. Endokrinní žlázy Inzulin – β-adrenergní receptory – stimulace sekrece – α 2 -receptory – inhibice sekrece renin – β-adrenergní receptory – stimulace sekrece – α 2 -receptory – inhibice sekrece Dále je ovlivněna sekrece parathormonu, kalcitoninu, thyroxinu a gastrinu

Léčiva Katecholaminy Adrenalin (epinefrin) –vazokonstrikční látka (α 2), pozitivní ionotropní a chronotropní účinek na srdce (vzestup systolického tlaku, β 1), vazodilatace některých cév (β 2) Noradrenalin – podobné účinky na β 1 v srdci a srovnatelné na αreceptorech jako adrenalin, méně působí β 2 Isoprenalin – β-agonista (na α působí jen málo), pozitivně ionotropní a chronotropní, účinný vazodilatátor, vyvolává vzestup srdečního výdeje provázený poklesem diastolického a středního arteriálního tlaku Dopamin – metabolický prekurzor noradrenalinu, aktivací D 1 receptorů způsobuje vazodilataci, v srdci aktivuje β 1, ve vysokých koncentracích napodobuje účinky adrenalinu. Ibopamin – ester, který je v krvi štěpen a vzniká účinný epinin (účinek podobný dopaminu) Dobutamin – relativní β 1 -selektivní agonista, aktivuje také α 1

Další Fenylefrin – α-agonista, nemá katecholovou strukturu (není inaktivován COMT, působí déle), účinné mydriatikum, dekongesční látka, zvyšuje krevní tlak Metoxamin – α-agonista, zvýšení krevního tlaku v důsledku vazokonstrikce, vagovým reflexem vyvolá bradykardii

Efedrin – primárně působí mechanismem uvolnění endogenních katecholaminů, neselektivní (připomíná adrenalin), dekongesce nosní sliznice a presorický účinek Xylometazolin a oxymetazolin – α-agonisté, vazokonstrikce na nosní sliznici (místní dekongesce) Amfetamin – proniká snadno co CNS (ještě snadněji než efedrin), vyvolává primárně uvolnění katecholaminů Metamfetamin – podobná účinek jako předchozí a ještě výraznější Fenmetrazin – podobný jako předchozí, využíván jako anorektikum Metylfenidat a pemolin – analogy amfetaminu, větší farmakologický účinky a potenciál k zneužití Fenylpropanolamin – další příbuzná sloučenina se slabými účinky na psychiku Hydroxyamfetamin – do CNS proniká omezeně, uvolňuje periferní katecholaminy (periferní účinek) NÁVYKOVÉ LÁTKY

α 2 – selektivní agonisté – terapie hypertenze: klonidin a metyldopa, podobný mechanismus účinku guanfacin a guanabenz β 1 – selektivní agonisté – dobutamin a parciální agonista prenalterol (v menší míře aktivují i β 2 -receptory a tak mohou zvyšovat srdeční výkon ) β 2 – selektivní agonisté – důležití při léčbě bronchiálního astmatu, relaxace dělohy u nástupu předčasného porodu

Atypická sympatomimetika Kokain – lokální anestetikum se sympatomimetickou složkou účinku (inhibice zpětného vychytávání neurotransmiterů na adrenergních synapsích), proniká do CNS Tyramin – fyziologicky v organismu (produkt metabolismu tyrosinu), po parenterálním podání způsobí vyplavení katecholaminů (účinky podobné podání noradrenalinu).

U kardivaskulárních onemocnění Terapeutické zvýšení krevního tlaku Hypotenze – zvýšení tlaku, když není pacient bezprostředně ohrožen (zachovaná perfúze mozku, srdce a ledvin), může mít svá rizika – vhodné při akutních hypotenzních stavech v důsledku masivního krvácení, úrazů páteřní míchy, předávkování antihypertenzivy, látkami způsobujícími depresi aktivity CNS: krátkodobá léčba pro udržení dostatečného průtoku mozkem a koronárními cévami. – pokud je nutná vazokonstrikce – αagonisté (noradrenalin, fenylefrin, metoxamin)

šok – hypovolémie, srdeční nedostatečnost, změna cévní rezistence; podle příčin je třeba určit možné využití vazokonstrikčních nebo vazodilatačních látek kardiogenní šok – bývá vyvolán rozsáhlým infarktem myokardu, má špatnou prognózu, v nízkých až středně vysokých dávkách může dopamin a dobutamin zvýšit srdeční výkon, tyto látky vyvolávají ve srovnání s noradrenalinem nízkou periferní vazokonstrikci. Isoprenalin zvýší tepovou frekvenci a srdeční práci ve vyšší míře. – využití vazokonstrikčních sympatomimetik k udržení krevního tlaku po chirurgickém zákroku (cílem terapie by nemělo být pouze udržení krevního tlaku, ale i optimální tkáňová perfuze).

Situace vyžadující snížené prokrvení tkání – dosažení hemostázy v chirurgii (adrenalin, kokain), zpomalení difúze lokálních anestetik z místa aplikace – prodloužení účinku a vhodné snížení dávky (adrenalin), které sníží i možný výskyt toxických reakcí, snížení překrvení a édému sliznic – dekongesce (fenylefrin, fenylpropanolamin, efedrin, pseudoefedrin, xylometazolin, oxymetazolin) – aktivace α – adrenergních receptorů.

Kardiologické využití – paroxysmální síňové tachykardie (fenylefrin, metoxamin) – kompletní blokáda a zástava srdce (katecholaminy – adrenalin a isoprenalin – městnavé srdeční selhání (příznivé působení pozitivně ionotropních látek dobutaminu, prenalterolu, a β 2 -selektivních látek, které snižují zatížení poklesem periferního krevního odporu. U respiratorních onemocnění Léčba bronchiálního astmatu Anafylaktická reakce Adrenalin – ústup bronchospazmu, překrvení sliznic, angioedému a kardiovaskularního kolapsu (sekundární terapii – glukokortikoidy a antihistaminika)

Oftalmologie Mydriatika – fenylefrin – usnadnění vyšetření sítnice Glaukom – adrenalin – snižuje nitrooční tlak, protože primárně usnadňuje odtok nitroočního moku Urogenitální trakt Ritodrin, terbutalin – relaxace svaloviny gravidní dělohy, potlačení děložních stahů u předčasných porodů; potlačení stresové inkontinence moče CNS Sympatomimetika amfetaminové skupiny mají euforizující účinky, navozují stav čilosti a potlačují spánek, zlepšení pozornosti – léčba narkolepsie

Nežádoucí účinky Adrenergní agonisté – vystupňování jejich působení na receptory kardivaskulárního a centrálního nervového systému (značné zvýšení krevního tlaku, který může způsobit krvácení do mozku nebo plicní edém; nárůst srdeční práce může vést až k infarktu myokardu, βstimulancia často způsobují tachykardie a mohou vyvolat až komorové arytmie. Poškození myokardu při dlouhodobém infuzním podávání. Fenylisopropylaminy vyvolávají neklid, třes, nespavost a pocity úzkosti)

Sympatolytika, adrenolytika (látky, které blokují adrenergní receptory) Podstata jejich účinku spočívá v obsazení α- nebo β-adrenergních receptorů a tím zabrání jejich aktivaci katecholaminy nebo příbuznými agonisty. α adrenolytika mají omezené klinické využití, narozdíl od βblokátorů, které mají širokou oblast indikací. α-adrenergní antagonisté: 1) reverzibilní – fentolamin, tolazolin, prazosin a labetalol (tyto dva jsou primárně využívány jako antihypertenziva) 2) ireverzibilní – fenoxybenzamin – kovalentně se váží na vazebné centrum αadrenergního receptoru a vyvolají tak jeho blokádu, účinky přetrvávají dlouho po tom, co bylo léčivo odstraněno z plazmy.

Účinek na kardiovaskulární aparát Tonus arteriol – pokles periferního cévního odporu a krevního tlaku (v hladké svalovině cév je převaha αadrenergních receptorů). Mohou zabránit účinku normálních dávek α-agonistů, při podání se smíšeným agonistou (α a β 2, např. adrenalin, změní presorickou odpověď na depresorickou ) = zvrat adrenalinového účinku. Reflexní tachykardie – výraznější u α 2 -blokátorů Snížený tonus musculus dilatator pupillae, …

Fentolamin – snižuje periferní cévní odpor, kardiostimulační účinek je částečně reflexní (baroreceptory) a částečně blokáda α 2 receptorů. P. o. podání může vyvolat stimulační účinek na GIT (průjmy, zvýšení sekrece žaludeční kyseliny). Tolazolin – méně účinný než předchozí, ale lépe se vstřebává z GIT Námelové alkaloidy – ergotamin, dihydroergotamin Fenoxybenzamin – dlouhodobá ireverzibilní blokáda, blokuje i receptory pro histamin, acetylcholin, serotonin. Proniká do CNS. Prazosin – vysoká selektivita k α 1, dochází k relaxaci arteriální a venózní hladkoé svaloviny, vyvolává tedy méně výraznou tachykardii. Yohimbin – zvyšuje uvolňování neurotransmiterů
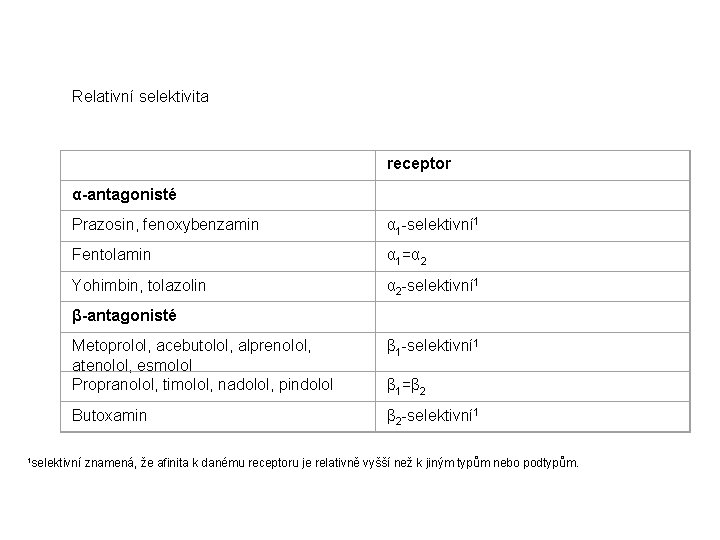
Relativní selektivita receptor α-antagonisté Prazosin, fenoxybenzamin α 1 -selektivní 1 Fentolamin α 1=α 2 Yohimbin, tolazolin α 2 -selektivní 1 β-antagonisté Metoprolol, acebutolol, alprenolol, atenolol, esmolol Propranolol, timolol, nadolol, pindolol β 1 -selektivní 1 Butoxamin β 2 -selektivní 1 β 1=β 2 1 selektivní znamená, že afinita k danému receptoru je relativně vyšší než k jiným typům nebo podtypům.

β-adrenergní antagonisté neselektivní, bez vnitřní aktivity – propranolol, metipranolol, timolol, nadolol, penbutolol s vnitřní aktivitou – pindolol, oxprenolol, alprenolol, bopindolol kardioselektivní – metoprolol, atenolol, bisoprolol, betaxolol, acebutolol s vasodilatačními účinky: celiprolol, nebivolol, dilevalol většina látek této skupiny se po p. o. příjmu dobře vstřebává, podléhá výraznému metabolismu po prvním průchodu játry, rychle se distribuují a mají velké distribuční objemy.

Účinek na kardiovaskulární systém: dlouhodobé snížení krevního tlaku – působí na srdce (negativní ionotropní a chronotropní účinek), cévy, renin -angiotensinový a zřejmě i na centrální nervový systém. U zdravých osob v běžných dávkách nezpůsobují hypotenzi. Účinek na dýchací systém: blokátory vyvolávají bronchokonstrikci, kontraindikace u pacientů s astmatem Účinek na oko: některé snižují oční tlak u pacientů s glaukomem (snížení produkce komorové tekutiny)

Účinky metabolické a endokrinní: inhibice lipolýzy glykogenolýzy mohou potencovat hypoglykémii zvýšení koncentrace triacylglycerolů (VLDL) v plazmě a k poklesu koncentrace cholesterolu v lipoproteinech o vysoké denzitě (HDL) – riziko ischemické choroby srdeční Ostatní účinky lokální anestetický účinek (membránově stabilizační efekt – vzniká u některých β-blokátorů jako následek blokády sodíkového kanálu na neuronech, v srdečním svalu a na membránách kosterní svaloviny.

Propranolol – β-adrenolytikum Metoprolol – selektivní β 1 -blokátory Atenolol Esmolol Betaxolol Acebutolol Nadolol – velmi dlouhodobý účinek Timolol – vynikající účinek při snižování nitroočního tlaku Pindolol – látky s vnitřní aktivitou Aceburolol Carteolol Pentabutolol Labetalol – hypotenze vyvolaná touto látkou je provázena nižším výskytem tachykardie Esmolol – ultrakrátce působící selektivní β 1 -blokátor

Klinické využití: léčba hypertenze v kombinaci s diuretikem nebo vazodilatátorem ischemická choroba srdeční – snižování frekvence anginózních záchvatů a zlepšení tolerance námahy srdeční arytmie – supraventrikulární i ventrikulární glaukom – snížení nitroočního tlaku hyperthyreoidismus – brání působení katecholaminů zvláště na srdeční činnost a inhibice konverze thyroxinu na trijodthyronin

Nežádoucí účinky na CNS: útlum, poruchy spánku, deprese

Myorelaxancia Účinek acetylcholinu na zakončení motorických nervů, blokáda tohoto účinku způsobuje ochabnutí příčně pruhovaných svalů. 2 skupiny: 1) nervosvalové blokátory – způsobují svalovou paralýzu, vyuřití v chirurgii, = kurarimimetika 2) spazmolytika – snižují spasticitu svalů při poruchách nervového původu (centrální myorelaxancia)

Neuromuskulární blokátory Mohou působit dvojím mechanismem: antagonisti – účinek podobný kurare (nedepolarizující blokáda účinků acetylcholinu) D-tubokurarin (popsáno použití u prasat a skotu) Metokurin (dimetyltubokurarin) Gallamin (koně, psi, kočky) Pankuronium Pipekuronium Vekuronium Atrakurium Působí přednostně v nízkých klinických dávkách na nikotinových receptorech, ve vyšších dávkách některé látky vstupují do iontových kanálů ploténky a způsobují jejich blokádu – tak zeslabují nervový přenos a snižují schopnost inhibitorů acetylcholinesterázy antagonizovat účinky nedepolarizujících svalových relaxancií Inhalační anstetika zvyšují účinek myorelaxancií, lokální anestetika stupňují nervosvalový blok

agonisti – nadbytek látky s depolarizujícím účinkem suxametonium (sukcinylcholin) – reaguje s nikotinovými receptory a otvírá sodíkové kanály a tím depolarizuje ploténku, užívá se v klinické praxi jako jediný ovlivňuje srdce – klinické využití u psů, koní a koček všechny jsou strukturálně podobné acetylcholinu ovlivňují krevní hladiny kalcia kontraindikovány u pacientů s glaukomem (zvyšují nitrooční tlak)

Centrální myorelaxancia Guaifenasin – Myolaxin inj. ad us. vet. – položení koně 60 – 80 ml/100 kg ž. hm. Diazepam – primární centrum tlumení je pravděpodobně ve spinální míše, působí na všech GABA synapsích Baklofen – agonista na GABAB receptorech
- Slides: 87