10 11 elads A sznek s a fny











- Slides: 18

10 -11. előadás A színek és a fény. Dalton atommodellje. A katódsugárzás, az elektron felfedezése, Thomson és Rutherford modellje. A fénykibocsátás és elnyelés elmélete. Színképek értelmezése atomfizikai ismeretek alapján. A fényelektromos hatás. A szilárdtestek felépítése, félvezetők.

A színek • A prizmán átvezetett fényt ernyőn felfogva a különböző frekvenciájú fénysugarak egy kicsit más helyen hagynak foltot, színes vonalat. A kapott úgynevezett színkép tehát elárulja, hogy a kevert fény milyen frekvenciájú összetevőkből áll. • A színképben minden frekvenciának egy keskeny tartomány felel meg. Ahol sötét a kép, oda nem érkezik fénysugár, olyan frekvenciájú összetevője nincs a vizsgált fénynek. • A Nap fényében minden frekvencia megtalálható. A színkép nagyjából folytonos a vöröstől az ibolyáig. A látható spektrum (http: //architectureideas. info/ 2008/10/vastu-shastra-factors -the-sun-and-its-effects/, 2011)

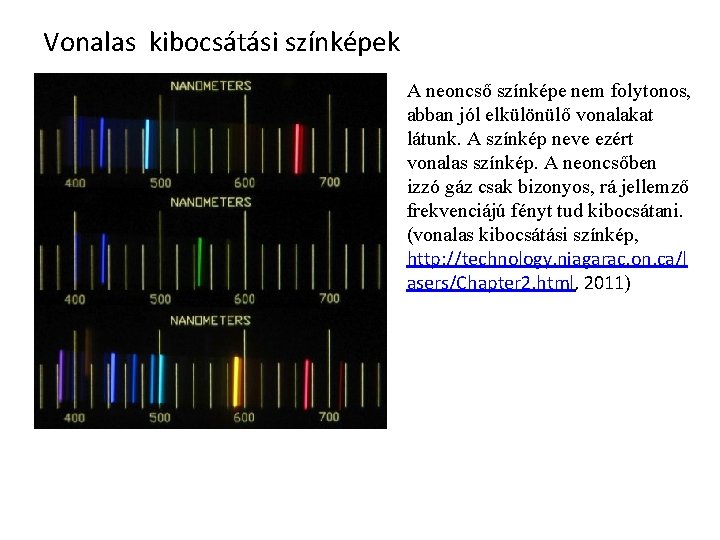
Vonalas kibocsátási színképek A neoncső színképe nem folytonos, abban jól elkülönülő vonalakat látunk. A színkép neve ezért vonalas színkép. A neoncsőben izzó gáz csak bizonyos, rá jellemző frekvenciájú fényt tud kibocsátani. (vonalas kibocsátási színkép, http: //technology. niagarac. on. ca/l asers/Chapter 2. html, 2011)

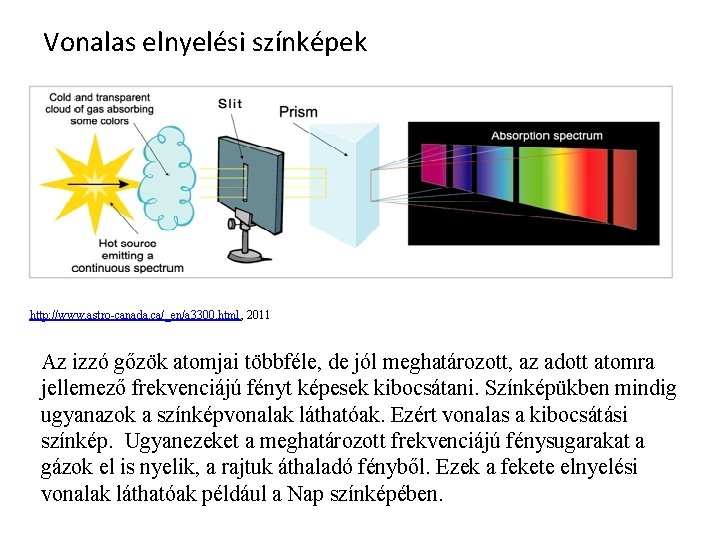
Vonalas elnyelési színképek http: //www. astro-canada. ca/_en/a 3300. html, 2011 Az izzó gőzök atomjai többféle, de jól meghatározott, az adott atomra jellemező frekvenciájú fényt képesek kibocsátani. Színképükben mindig ugyanazok a színképvonalak láthatóak. Ezért vonalas a kibocsátási színkép. Ugyanezeket a meghatározott frekvenciájú fénysugarakat a gázok el is nyelik, a rajtuk áthaladó fényből. Ezek a fekete elnyelési vonalak láthatóak például a Nap színképében.

A fényelektromos hatás • A fizikusok az 1800 -as évek végén vizsgálták az anyag és a fény kölcsönhatását. • Ha negatív elektromos állapotú, tehát elektrontöbblettel rendelkező fémlemezt megvilágítanak, az elveszíti töltését, többletelektronjait. • A jelenség további részletei azonban igen különösek voltak. • Az elektronok kilépése csak akkor volt megfigyelhető, ha a megvilágító fény frekvenciája meghaladott egy, az adott fémre jellemző értéket. A fény erősségét hiába növelték, ha a frekvencia kisebb volt a küszöbnél. • Másrészt a kilépő elektronok maximális energiája is kizárólag a megvilágítás frekvenciájától függött, nem pedig a fény erősségétől, intenzitásától.

A kvantumhipotézis • A rejtélyt Albert Einstein oldotta meg, különös feltételezéssel: • E_foton=h*f • Feltételezte, hogy a fény az energiát adagokban szállítja, egy ilyen részecskét fotonnak nevezett el. A foton energiája a fény frekvenciájával arányos. Az arányossági tényezőnek a Planck állandó adódott. h=6. 62*10 e-31 J*s • A Planck állandót először Max Planck, német fizikus használta. • A fényelektromos hatás során a fém elnyeli a fotont, annak teljes energiája a fém egy elektronjának adódik át. Ha ez az energia elegendően nagy, akkor az elektron elhagyja a fémet, de mozgási energiája nem lehet több, mint a foton energiájának és az un. kilépési munkának a különbsége.

Az atomok Az anyag oszthatatlan építőköveinek elképzelése sok esetben sikeresnek bizonyul. Az ütköző golyókkal jól meg lehetett magyarázni a gázok viselkedését, az elektromos áramot. Az 1800 -as évek végén atomokra és az anyag felépítésére vonatkozó tapasztalatok gyorsan gyarapodtak.

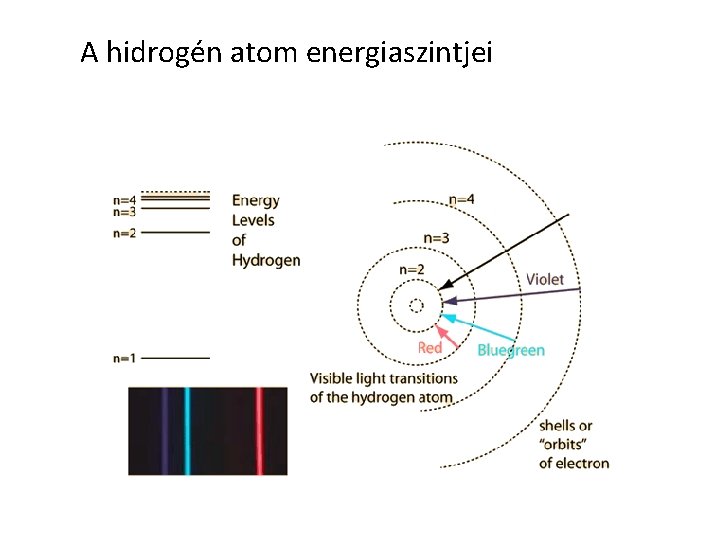
A hidrogén atom energiaszintjei

Az atom körüli elektronok energiája kvantált • Az atommag körül elhelyezkedő elektronok többféle, jól meghatározott energiájú állapotokban lehetnek. • Egy ilyen állapot energiája a mag és az elektron közötti elektromos kölcsönhatáshoz tartozó helyzeti és az elektron mozgási energiájának az összege. A legkisebb energiájú állapot neve alapállapot, az ennél nagyobb energiájú további állapotok a gerjesztett állapotok. • A hidrogén atom esetében az alapállapot energiája -13. 6 e. V. A negatív előjel arra utal, hogy ebben az állapotban az elektron kötött, nem hagyhatja el az atommag környezetét. Ilyen nagyságú energiát kell közölni az elektronnal ahhoz, hogy eltávolítsuk az atomból. • Az e. V, azaz elektronvolt az atomfizikában használatos energia mértékegység, nagyon kis energiát jelent. 1 e. V = 1. 6*10 -19 J.

Fénykibocsátás és elnyelés elmélete Ha az érkező foton energiája éppen elegendő ahhoz, hogy azt felvéve egy elektron nagyobb energiájú állapotba kerüljön, az atom elnyeli a fotont, azt mondjuk, az atom gerjesztődik. KÉP: A fény elnyelésének (abszorbció) és kibocsátásának (emisszió) ábrázolása. (Az energiánál a h*f alakot kell felírni!) Ha az atom egy elektronja nagyobb energiájú állapotból alacsonyabb energiájú állapotba kerül, az energiakülönbséggel megegyező energiájú foton távozik az atomból, azt mondjuk, az atom legerjesztődik. Számoljuk ki a hidrogénatom által elnyelt fotonok energiáját! Az alapállapotú elektron energiája - 13. 6 e. V. az első gerjesztett állapoté -3. 4 e. V,

Kvantumfizika: az állapotfüggvény • Gyanúsan sokszor: e=h*f, ennek mélyebb értelme kell legyen. • A részecskéket nem a lendületükkel és sebességükkel jellemzik, hanem az úgynevezett állapotfüggvénnyel. • Az állapotfüggvényből a részecskék helyét és lendületét csak bizonyos körülmények között és bizonyos valószínűséggel lehet meghatározni. • Pl. a szabad részecske helyét nem tudni, lendülete pontosan számolható: • De Broglie: • Ahol „h” planck állandó, p a lendület • Az állapotfüggvény négyzete a tér egy pontjában megadja azt, hogy milyen valószínűséggel található az elektron az adott pont kis környezetében.

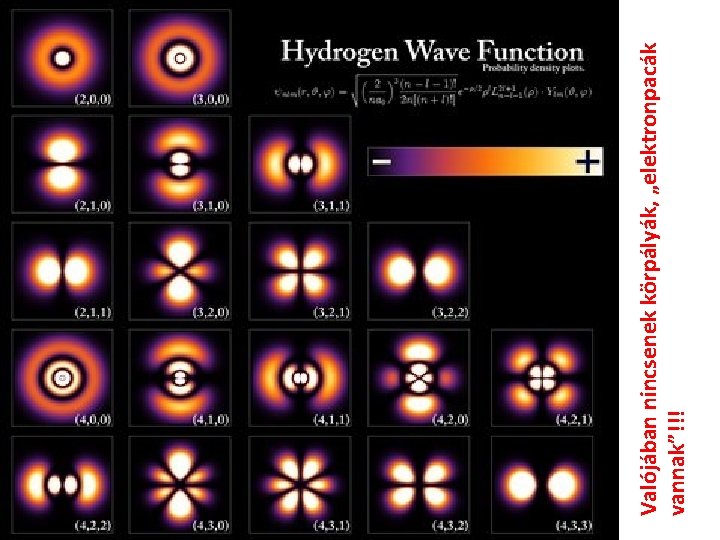
Valójában nincsenek körpályák, „elektronpacák vannak”!!!

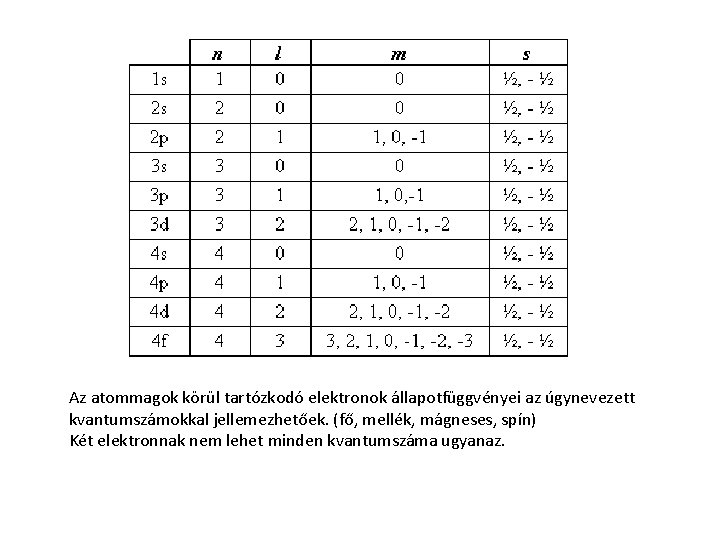
Az atommagok körül tartózkodó elektronok állapotfüggvényei az úgynevezett kvantumszámokkal jellemezhetőek. (fő, mellék, mágneses, spín) Két elektronnak nem lehet minden kvantumszáma ugyanaz.

Amikor az elektron energiát vesz fel akkor egy kisebb energiájú állapotból (gombóc) egy nagyobb energiájú állapotba (piskóta) kerül. Klasszikus értelemben nem beszélhetünk mozgásról, hiszen helye sincs!

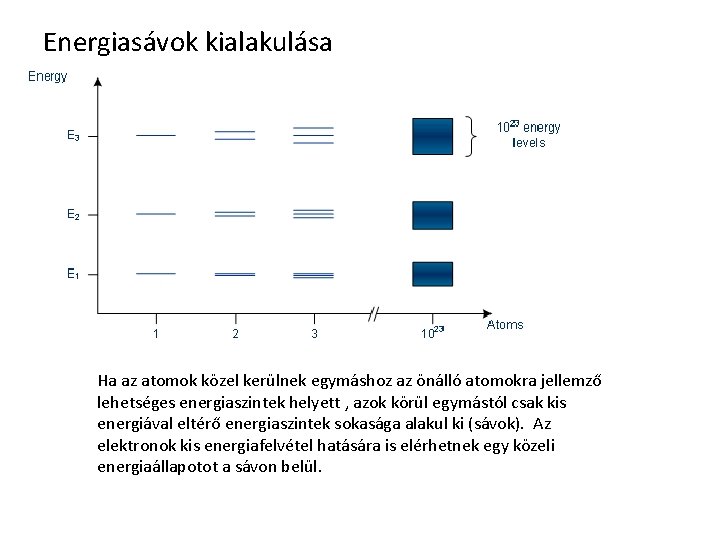
Energiasávok kialakulása Ha az atomok közel kerülnek egymáshoz az önálló atomokra jellemző lehetséges energiaszintek helyett , azok körül egymástól csak kis energiával eltérő energiaszintek sokasága alakul ki (sávok). Az elektronok kis energiafelvétel hatására is elérhetnek egy közeli energiaállapotot a sávon belül.

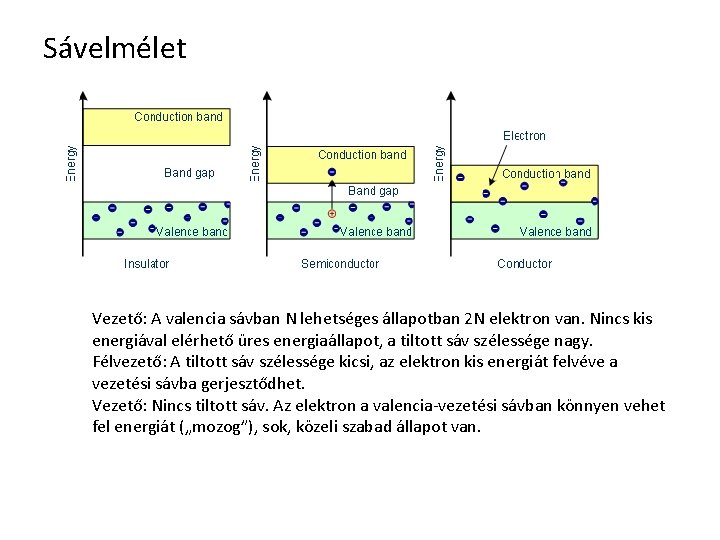
Sávelmélet Vezető: A valencia sávban N lehetséges állapotban 2 N elektron van. Nincs kis energiával elérhető üres energiaállapot, a tiltott sáv szélessége nagy. Félvezető: A tiltott sáv szélessége kicsi, az elektron kis energiát felvéve a vezetési sávba gerjesztődhet. Vezető: Nincs tiltott sáv. Az elektron a valencia-vezetési sávban könnyen vehet fel energiát („mozog”), sok, közeli szabad állapot van.

A Standard modell • A proton, elektron, neutron felfedezése csak a kezdet volt a sorban. Egyre több, egyre különlegesebb részecskéket fedeztek fel a szóráskísérletek és az atomok ütközéseinek megfigyelése során. Ilyen részecske a nagyon kis tömegű semleges részecske, a neutrínó, az elektronnal egyforma tömegű de pozitív töltésű pozitron, az elektron töltésével megegyező töltésű de jóval nagyobb tömegű müon. A szaporodó kísérleti eredmények alapján alkották meg a részecskéket és a köztük levő kölcsönhatásokat leíró Standard Modellt. • • A standard modell elképzelése szerint a protonok és a neutronok is kvarkokból épülnek fel. A hat féle kvark elektromos töltése az elektron töltésénél is kisebb, egy protont és egy neutront három- három kvark alkot. Az elektron töltésének nagyságát e-vel jelölve a proton két +(2/3)*e elektromos töltésű „up” kvarkot és egy -(1/3)*e töltésű „down” kvarkot tartalmaz, amelyek szoros kölcsönhatásban vannak egymással. A neutron két „down” és egy „up” kvarkból áll. (http: //static. astronomija. co. rs/nauke/fizika/atom/kvark/kva rk. htm)

A négy alapvető kölcsönhatás • A standard modellben a természetben fellelhető alapvető kölcsönhatásokat is részecskék közvetítik. • A világegyetemben négy alapvető kölcsönhatás van, ezek az erős, a gyenge, az elektromágneses és a gravitációs kölcsönhatás. Közülük a gravitációs kölcsönhatás a leggyengébb, de ennek a hatótávolsága a legnagyobb, gyakorlatilag végtelen. Az elektromágneses kölcsönhatás is hasonlóan nagy hatótávolságú, de sokszor erősebb mint a gravitációs. A gyenge és erős (vagy nukleáris) kölcsönhatások nagyon rövid hatótávolságúak, gyakorlatilag az atomokon belül lépnek csak fel. Az elmélet szerint az alapvető kölcsönhatások a megfelelő, a kölcsönhatást közvetítő részecskék kicserélésével értelmezhetőek. Az elektromágneses kölcsönhatás közvetítő részecskéi a fotonok, az erős kölcsönhatásé a gluonok, a gravitációs kölcsönhatásé a gravitonok.