Wykad 6 Rozpranie swobodne gazu doskonaego Rozpranie swobodne

Wykład 6 Rozprężanie swobodne gazu doskonałego Rozprężanie swobodne jako przemiana nieodwracalna Definicja entropii dla przemiany odwracalnej Entropia w przemianie nieodwracalnej Entropia jako funkcja stanu Czy entropia może maleć? Entropia w układzie zamkniętym II zasada termodynamiki Entropia w ujęciu statystycznym 1
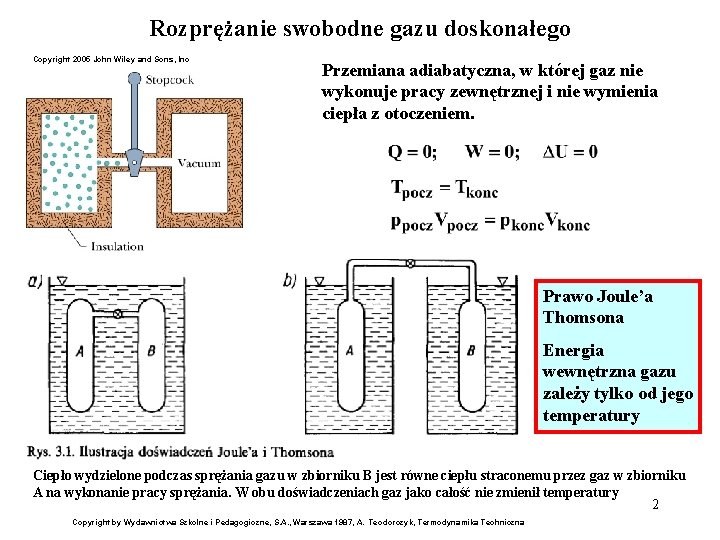
Rozprężanie swobodne gazu doskonałego Copyright 2005 John Wiley and Sons, Inc Przemiana adiabatyczna, w której gaz nie wykonuje pracy zewnętrznej i nie wymienia ciepła z otoczeniem. Prawo Joule’a Thomsona Energia wewnętrzna gazu zależy tylko od jego temperatury Ciepło wydzielone podczas sprężania gazu w zbiorniku B jest równe ciepłu straconemu przez gaz w zbiorniku A na wykonanie pracy sprężania. W obu doświadczeniach gaz jako całość nie zmienił temperatury 2 Copyright by Wydawnictwa Szkolne i Pedagogiczne, S. A. , Warszawa 1987, A. Teodorczyk, Termodynamika Techniczna
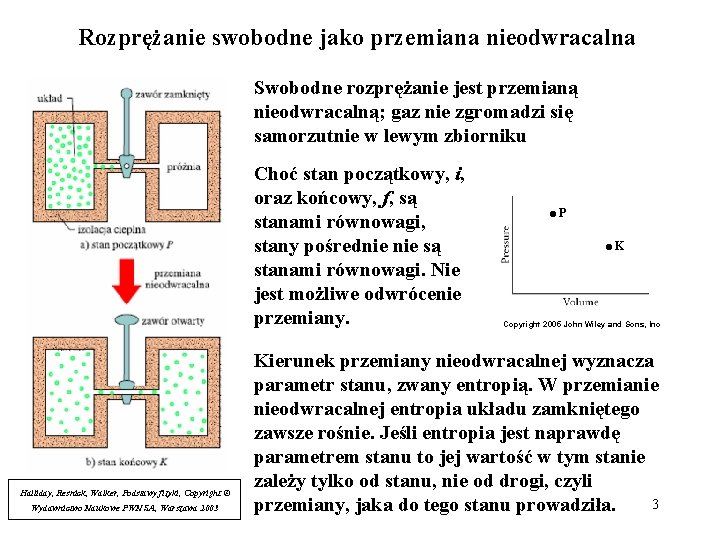
Rozprężanie swobodne jako przemiana nieodwracalna Swobodne rozprężanie jest przemianą nieodwracalną; gaz nie zgromadzi się samorzutnie w lewym zbiorniku Choć stan początkowy, i, oraz końcowy, f, są stanami równowagi, stany pośrednie są stanami równowagi. Nie jest możliwe odwrócenie przemiany. Halliday, Resnick, Walker, Podstawy fizyki, Copyright © Wydawnictwo Naukowe PWN SA, Warszawa 2003 . P . K Copyright 2005 John Wiley and Sons, Inc Kierunek przemiany nieodwracalnej wyznacza parametr stanu, zwany entropią. W przemianie nieodwracalnej entropia układu zamkniętego zawsze rośnie. Jeśli entropia jest naprawdę parametrem stanu to jej wartość w tym stanie zależy tylko od stanu, nie od drogi, czyli 3 przemiany, jaka do tego stanu prowadziła.
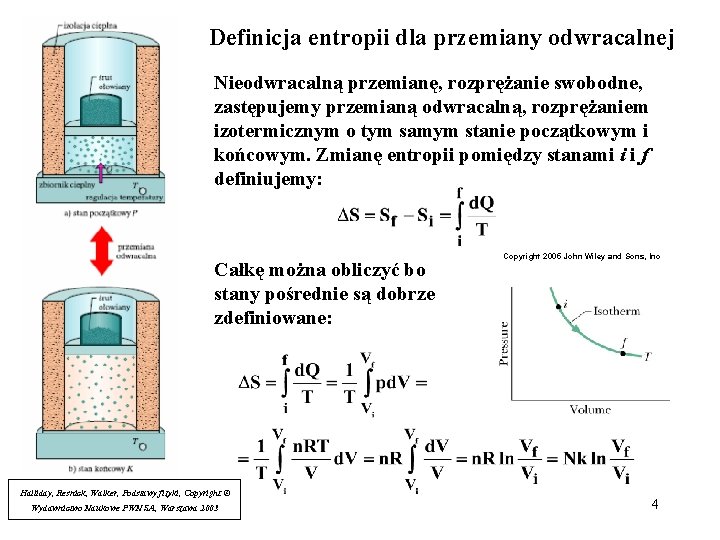
Definicja entropii dla przemiany odwracalnej Nieodwracalną przemianę, rozprężanie swobodne, zastępujemy przemianą odwracalną, rozprężaniem izotermicznym o tym samym stanie początkowym i końcowym. Zmianę entropii pomiędzy stanami i i f definiujemy: Całkę można obliczyć bo stany pośrednie są dobrze zdefiniowane: Halliday, Resnick, Walker, Podstawy fizyki, Copyright © Wydawnictwo Naukowe PWN SA, Warszawa 2003 Copyright 2005 John Wiley and Sons, Inc 4

Entropia w przemianie nieodwracalnej Aby obliczyć zmianę entropii w przemianie nieodwracalnej w układzie zamkniętym zastępujemy przemianę nieodwracalną przemianą odwracalną o takich samych stanach początkowym i i końcowym f. Zmianę entropii pomiędzy tymi stanami dla przemiany odwracalnej obliczamy korzystając z definicji: Jeśli zmiana temperatury jest nieduża, można skorzystać z przybliżenia: Entropia układu do którego dostarczamy ciepło, rośnie, a entropia układu, który oddaje ciepło, maleje. 5

Sprawdzian Woda jest ogrzewana za pomocą kuchenki. Uszereguj od największej do najmniejszej zmiany entropii wody w następujących przedziałach temperatury: a) od 20°C do 30°C, b) od 30°C do 35°C i c) od 80°C do 85°C. Copyright 2005 John Wiley and Sons, Inc Zadanie 1 W lewym zbiorniku znajduje się jeden mol gazowego azotu. Po otwarciu zaworu objętość zajmowana przez gaz podwaja się. Ile wynosi zmiana entropii w opisanej przemianie nieodwracalnej? Przyjmij, że azot jest gazem doskonałym. Rozprężanie swobodne bez zmiany temperatury zastępujemy przemianą izotermiczną. 6

Sprawdzian Gaz doskonały w stanie początkowym i ma temperaturę T 1. W stanach końcowych a i b, które gaz może osiągnąć w wyniku przemian zaznaczonych na wykresie, jego temperatura T 2 jest większa niż w stanie początkowym. Copyright 2005 John Wiley and Sons, Inc Czy zmiana entropii w przemianie prowadzącej do stanu a jest większa, taka sama, czy mniejsza niż w przemianie prowadzącej do stanu b? 7
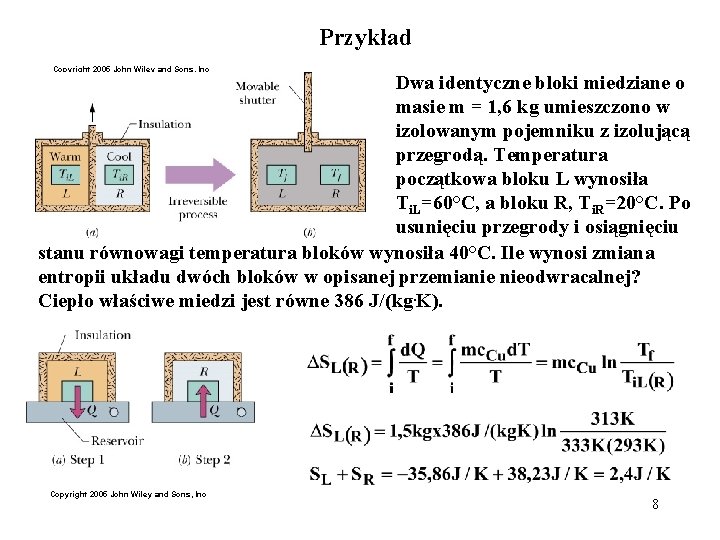
Przykład Copyright 2005 John Wiley and Sons, Inc Dwa identyczne bloki miedziane o masie m = 1, 6 kg umieszczono w izolowanym pojemniku z izolującą przegrodą. Temperatura początkowa bloku L wynosiła Ti. L=60°C, a bloku R, Ti. R=20°C. Po usunięciu przegrody i osiągnięciu stanu równowagi temperatura bloków wynosiła 40°C. Ile wynosi zmiana entropii układu dwóch bloków w opisanej przemianie nieodwracalnej? Ciepło właściwe miedzi jest równe 386 J/(kg. K). Copyright 2005 John Wiley and Sons, Inc 8

Entropia jako funkcja stanu Pokażemy, że dla gazu doskonałego entropia jest funkcją stanu, tzn. jej wartość zależy od stanu, a nie od drogi, po której dany stan został osiągnięty. Z pierwszej zasady termodynamiki: Dla gazu doskonałego: co daje: a po podzieleniu przez T otrzymujemy: W końcu, po scałkowaniu od stanu początkowego i do stanu końcowego f mamy: niezależnie od przemiany prowadzącej z i do f. 9
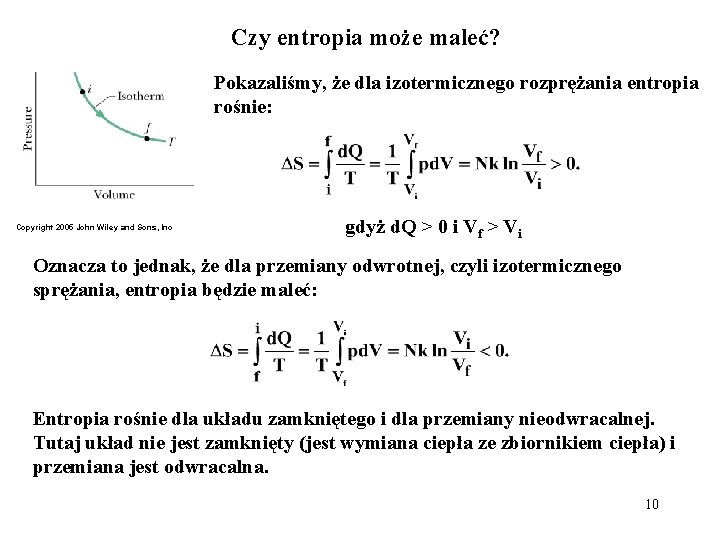
Czy entropia może maleć? Pokazaliśmy, że dla izotermicznego rozprężania entropia rośnie: Copyright 2005 John Wiley and Sons, Inc gdyż d. Q > 0 i Vf > Vi Oznacza to jednak, że dla przemiany odwrotnej, czyli izotermicznego sprężania, entropia będzie maleć: Entropia rośnie dla układu zamkniętego i dla przemiany nieodwracalnej. Tutaj układ nie jest zamknięty (jest wymiana ciepła ze zbiornikiem ciepła) i przemiana jest odwracalna. 10

Jeśli potraktujemy gaz i zbiornik ciepła jako dwie części większego układu zamkniętego, to entropia całego układu będzie równa zeru dla odwracalnego rozprężania izotermicznego. Dla rozprężania: Copyright 2005 John Wiley and Sons, Inc a dla odwracalnego sprężania izotermicznego: gdyż: Entropia układu zamkniętego nie zmienia się w przemianie odwracalnej. Ponieważ tarcie zamienia na ciepło część wykonywanej pracy, a więc powoduje niezbilansowany wzrost ciepła przekazanego układowi. Zatem zmiana entropii układu zamkniętego w wyniku zachodzącej w nim przemiany nieodwracalnej (ze stratami) nie bilansuje się do zera, lecz będzie dodatnia (entropia układu zamkniętego rośnie w wyniku przemiany nieodwracalnej). Entropia układu zamkniętego nigdy nie maleje. 11

Druga zasada termodynamiki Jest to jedno ze sformułowań II zasady termodynamiki, wynikające z obserwacji i badań przemian termodynamicznych. Inne sformułowanie, bardzo bliskie, wynika z rozważań nad silnikami cieplnymi (niedługo do niego dojdziemy), a jeszcze inne z rozważań statystycznych. Wszystkie te sformułowania są równoważne. 12
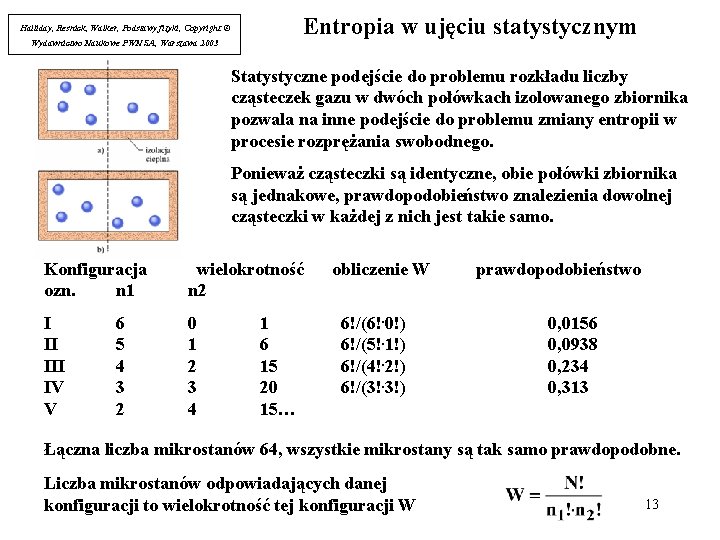
Entropia w ujęciu statystycznym Halliday, Resnick, Walker, Podstawy fizyki, Copyright © Wydawnictwo Naukowe PWN SA, Warszawa 2003 Statystyczne podejście do problemu rozkładu liczby cząsteczek gazu w dwóch połówkach izolowanego zbiornika pozwala na inne podejście do problemu zmiany entropii w procesie rozprężania swobodnego. Ponieważ cząsteczki są identyczne, obie połówki zbiornika są jednakowe, prawdopodobieństwo znalezienia dowolnej cząsteczki w każdej z nich jest takie samo. Konfiguracja ozn. n 1 wielokrotność n 2 I II IV V 0 1 2 3 4 6 5 4 3 2 1 6 15 20 15… obliczenie W 6!/(6!. 0!) 6!/(5!. 1!) 6!/(4!. 2!) 6!/(3!. 3!) prawdopodobieństwo 0, 0156 0, 0938 0, 234 0, 313 Łączna liczba mikrostanów 64, wszystkie mikrostany są tak samo prawdopodobne. Liczba mikrostanów odpowiadających danej konfiguracji to wielokrotność tej konfiguracji W 13

Copyright 2005 John Wiley and Sons, Inc Wykres liczby mikrostanów w zależności od procentowej zawartości cząsteczek w lewej połowie zbiornika w przypadku wielkiej liczby cząsteczek w zbiorniku. Niemal wszystkie mikrostany odpowiadają w przybliżeniu równemu rozkładowi liczby cząsteczek gazu pomiędzy dwoma połówkami zbiornika. Wzór Boltzmanna na entropię Wzór Stirlinga: 14
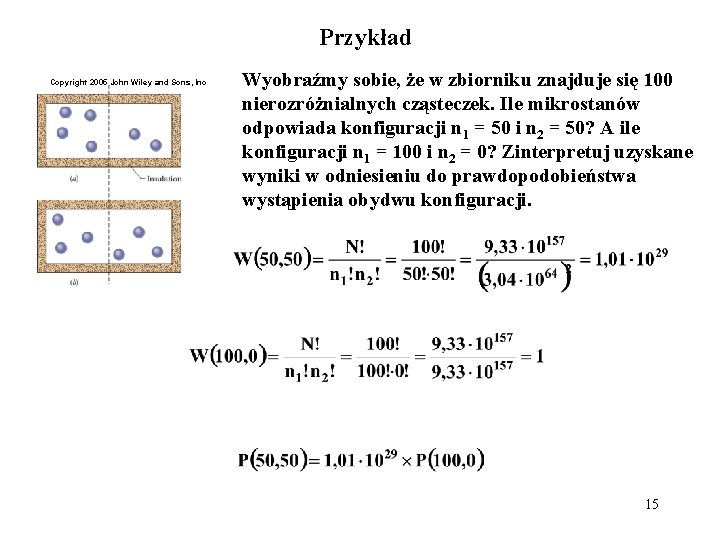
Przykład Copyright 2005 John Wiley and Sons, Inc Wyobraźmy sobie, że w zbiorniku znajduje się 100 nierozróżnialnych cząsteczek. Ile mikrostanów odpowiada konfiguracji n 1 = 50 i n 2 = 50? A ile konfiguracji n 1 = 100 i n 2 = 0? Zinterpretuj uzyskane wyniki w odniesieniu do prawdopodobieństwa wystąpienia obydwu konfiguracji. 15

Przykład Pokazaliśmy wcześniej, że kiedy n moli gazu doskonałego zwiększa dwukrotnie swoją objętość na drodze rozprężania swobodnego, to wzrost entropii od stanu początkowego i do stanu końcowego f jest równy: Wyprowadź to równanie, korzystając z mechaniki statystycznej. Stosując wzór Stirlinga otrzymujemy: 16
- Slides: 16