Tepeln jevy Vnitn energie Vechny atomy a molekuly












- Slides: 14

Tepelné jevy

Vnitřní energie § Všechny atomy a molekuly jsou v neustálém pohybu. § Součet pohybových i potencionálních energií všech molekul v tělese se nazývá vnitřní energie tělesa. § Vnitřní energie tělesa závisí na vzájemné poloze molekul v tělese, vzrůstá s počtem molekul a s teplotou tělesa.

Jak můžeme zvýšit vnitřní energii? § Vnitřní energii tělesa lze zvýšit dvěma způsoby: 1. Prvním způsobem je dotyk tělesa s jiným tělesem, které má vyšší teplotu. 2. Druhým způsobem je působení síly, která koná práci.

Teplo § je fyzikální veličina udávající energii, kterou si vyměňují tělesa různé teploty. § Teplo označujeme písmenem Q. § Stejně jako energii měříme i teplo v joulech [J].

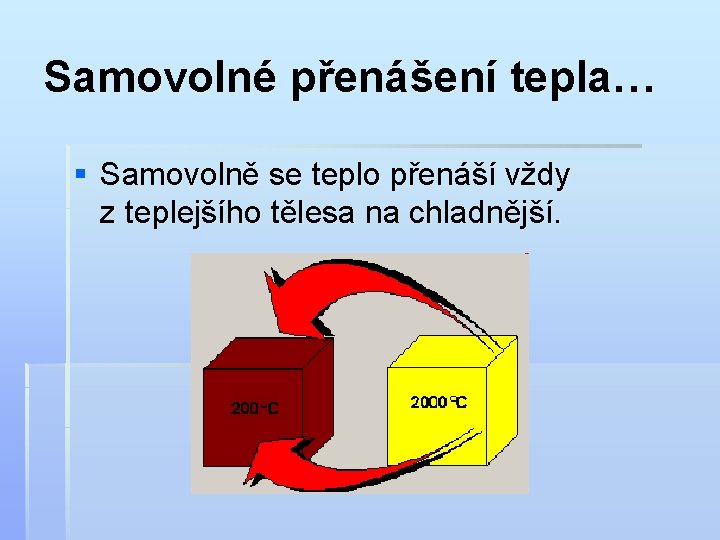
Samovolné přenášení tepla… § Samovolně se teplo přenáší vždy z teplejšího tělesa na chladnější.

Měrná tepelná kapacita § je fyzikální veličina, která určuje, kolik tepla musíme dodat 1 kg látky, aby se její teplota zvýšila o 1 °C. § Značíme: c § Jednotkou měrné tepelné kapacity je

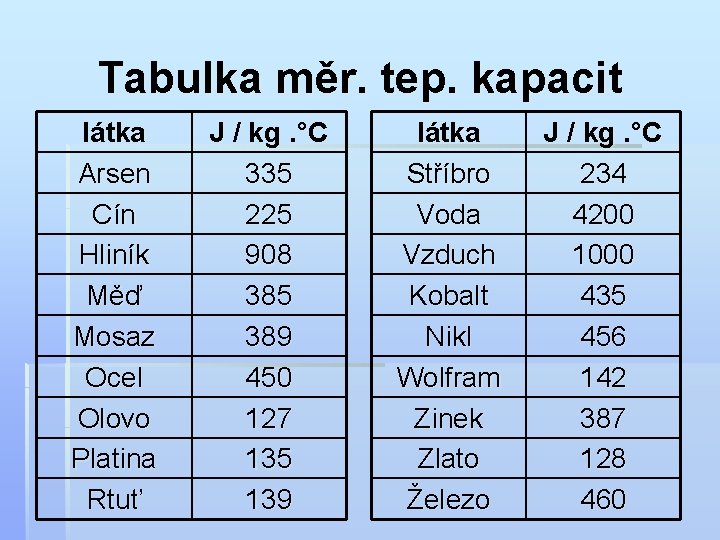
Tabulka měr. tep. kapacit látka Arsen Cín Hliník Měď Mosaz Ocel Olovo Platina Rtuť J / kg. °C 335 225 908 385 389 450 127 135 139 látka Stříbro Voda Vzduch Kobalt Nikl Wolfram Zinek Zlato Železo J / kg. °C 234 4200 1000 435 456 142 387 128 460

Výpočet tepla § Teplo Q, které musíme dodat tělesu, aby se jeho teplota zvýšila z teploty t 1 na teplotu t 2, určíme ze vzorce Q = c. m. (t 2 - t 1) c – měrná tepelná kapacita m – hmotnost t 2 - t 1 – rozdíl teplot

Příklad: Jaké teplo přijme voda o hmotnosti 5 kg, když zvýší svou teplotu z 20 °C na 90 °C? m = 5 kg c = 4. 200 J/kg. °C t 2 = 90 °C t 1 = 20 °C Q = c. m. (t 2 - t 1) Q = ? J Q = 1. 470. 000 J = = 1, 47 MJ Q = c. m. (t 2 - t 1) Q = 4200. 5. 70

Příklady § Během noci klesla teplota vzduchu v pokoji horské chaty na 17°C. Objem místnosti je 35 m 3. Kolik tepla musí vzduchu předat topné těleso, aby se teplota v uzavřené místnosti vzrostla o 3 °C. § Do bazénu, ve kterém je voda s objemem 1 m 3, spal kámen s hmotností 10 kg z výšky 10 m nad dnem bazénku. O kolik stupňů se voda v bazénku ohřála?

Kalorimetrická rovnice § Při tepelné výměně mezi dvěma tělesy platí kalorimetrická rovnice: c 1. m 1. (t 1 – t) = c 2. m 2. (t – t 2) hmotnosti těles jsou označeny m, měrné tepelné kapacity c, teploty: § t 1 je přiřazen teplejšímu § t 2 chladnějšímu tělesu § t je výsledná teplota

Příklady § Do ocelové vany o hmotnosti 25 kg a teplotě 20 °C napustíme 50 l litrů vody o teplotě 60 °C. Na jaké teplotě se vana s vodou ustálí, považujeme-li vanu s vodou za izolovanou soustavu? § Do skleněné termoláhve o hmotnosti 1 kg a teplotě 20 °C byl nalit vroucí vody o teplotě 100 °C. Na jaké hodnotě se ustálí teplota termoláhve s vodou.

Šíření tepla § Látky, které dobře vedou teplo, nazýváme tepelné vodiče (kovy). § Látky, které špatně vedou teplo, nazýváme tepelné izolanty (kapaliny, plyny, dřevo, sklo plasty).

Šíření tepla § 1. 2. 3. Aplet – šíření tepla Teplo se může šířit Vedením – vedením se teplo může šířit ve všech látkách Prouděním – prouděním se teplo šíří jen v kapalinách a v plynech Zářením – zářením se teplo šíří průhlednými látkami a vakuem.