SIAPIAU MOLECIWLAU SIAPIAU MOLECIWLAU CYNNWYS Gwybodaeth flaenorol Damcaniaeth

SIAPIAU MOLECIWLAU

SIAPIAU MOLECIWLAU CYNNWYS • Gwybodaeth flaenorol • Damcaniaeth gwrthyriad parau electron • Siapiau moleciwlaidd rheolaidd • Siapiau moleciwlau â pharau unig • Siapiau ïonau • Moleciwlau â bondiau dwbl • Enghreifftiau eraill • Cwestiynau prawf • Rhestr wirio

SIAPIAU MOLECIWLAU Cyn dechrau, byddai’n ddefnyddiol i chi wybod… • y diffiniad o fond cofalent • beth yw pâr unig • bod gwefrau tebyg yn gwrthyrru

DAMCANIAETH GWRTHYRIAD PARAU ELECTRON Y PLISGYN FALENS (VSEPR) “MAE SI P MOLECIWL NEU ÏON YN DIBYNNU AR NIFER Y PARAU ELECTRON (WEDI BONDIO NEU HEB EU BONDIO) YM MHLISGYN FALENS YR ATOM CANOLOG OHERWYDD MAENT YN AROS CYN BELLED I FFWRDD O’I GILYDD PHOSIBL ER MWYN LLEIHAU GWRTHYRIAD. ” Mae gan foleciwlau fondiau cofalent. Gan fod bondiau cofalent yn cynnwys pâr o electronau, bydd pob bond yn gwrthyrru bondiau eraill. Felly, bydd bondiau yn gwthio ei gilydd cyn belled â phosibl i leihau’r grymoedd gwrthyrrol. Oherwydd bod y gwrthyriadau yn hafal, bydd y bondiau hefyd yn gytbell. Al Mae bondiau yn agosach at ei gilydd felly mae grymoedd gwrthyrrol yn fwy Mae bondiau ymhellach o’i gilydd felly mae grymoedd gwrthyrrol yn llai Al Mae pob bond mor gytbell â phosibl

DAMCANIAETH GWRTHYRIAD PARAU ELECTRON “MAE SI P MOLECIWL NEU ÏON YN DIBYNNU AR NIFER Y PARAU ELECTRON (WEDI BONDIO NEU HEB EU BONDIO) YM MHLISGYN FALENS YR ATOM CANOLOG OHERWYDD MAENT YN AROS CYN BELLED I FFWRDD O’I GILYDD PHOSIBL ER MWYN LLEIHAU GWRTHYRIAD. ” O Mae pob bond mor gytbell â phosibl fel bod y grymoedd gwrthyrrol yn llai Oherwydd y grymoedd gwrthyrrol hafal rhwng parau bond, mae gan y rhan fwyaf o foleciwlau syml (rhai ag atom canolog ac eraill wedi bondio ato), siapiau safonol ac onglau bond hafal. Er hynny, mae presenoldeb parau unig ar yr atom canolog yn effeithio’r ongl rhwng y bondiau, ac felly’n effeithio ar y siâp. MOLECIWLAU HEB BARAU UNIG MOLECIWLAU PHARAU UNIG

SIAPIAU RHEOLAIDD Mae moleciwlau, neu ïonau, sydd â PHARAU BOND YN UNIG o electronau yn perthyn i set o siapiau safonol. Mae’r holl wrthyriadau pâr bond - pâr bond yn hafal. Y cwbl sydd angen i chi wneud yw cyfrif y nifer o barau bond a dewis un o’r enghreifftiau canlynol… PARAU BOND SI P ONGL(AU) BOND C Bydd bond cofalent yn gwrthyrru bond cofalent arall ENGHRAIFFT 2 LLINOL 180º Be. Cl 2 3 TRIGONOL PLANAR 120º Al. Cl 3 4 TETRAHEDROL 109. 5º CH 4 5 DEUBYRAMID TRIGONOL 90º & 120º PCl 5 6 OCTAHEDROL 90º SF 6
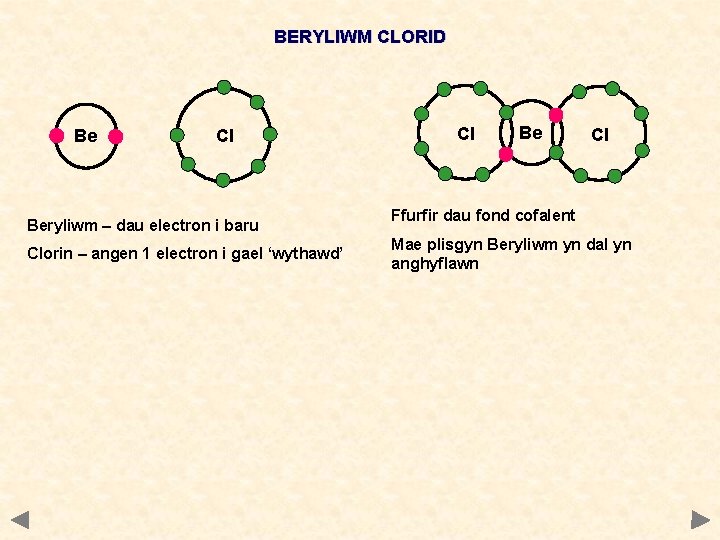
BERYLIWM CLORID Be Cl Beryliwm – dau electron i baru Clorin – angen 1 electron i gael ‘wythawd’ Cl Be Cl Ffurfir dau fond cofalent Mae plisgyn Beryliwm yn dal yn anghyflawn
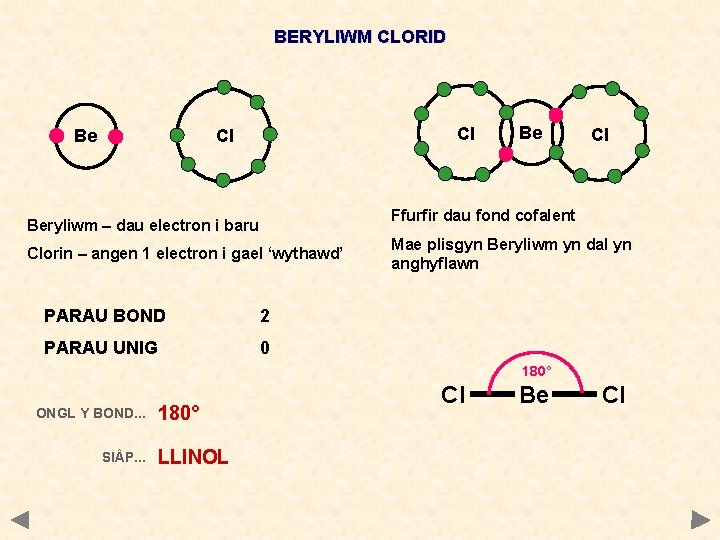
BERYLIWM CLORID Be Cl Cl Be Cl Ffurfir dau fond cofalent Beryliwm – dau electron i baru Clorin – angen 1 electron i gael ‘wythawd’ PARAU BOND 2 PARAU UNIG 0 Mae plisgyn Beryliwm yn dal yn anghyflawn 180° ONGL Y BOND. . . SI P. . . 180° LLINOL Cl Be Cl

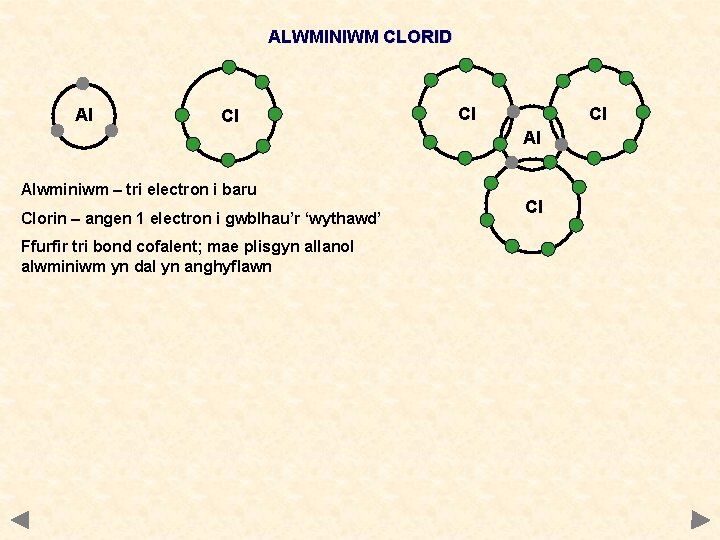
ALWMINIWM CLORID Al Cl Cl Cl Al Alwminiwm – tri electron i baru Clorin – angen 1 electron i gwblhau’r ‘wythawd’ Ffurfir tri bond cofalent; mae plisgyn allanol alwminiwm yn dal yn anghyflawn Cl

ALWMINIWM CLORID Al Cl Cl Cl Al Alwminiwm – tri electron i baru Cl Clorin – angen 1 electron i gwblhau’r ‘wythawd’ Ffurfir tri bond cofalent; mae plisgyn allanol alwminiwm yn dal yn anghyflawn PARAU BOND 3 PARAU UNIG 0 120° Cl ONGL Y BOND. . . SI P. . . 120 TRIGONOL PLANAR Cl Al Cl
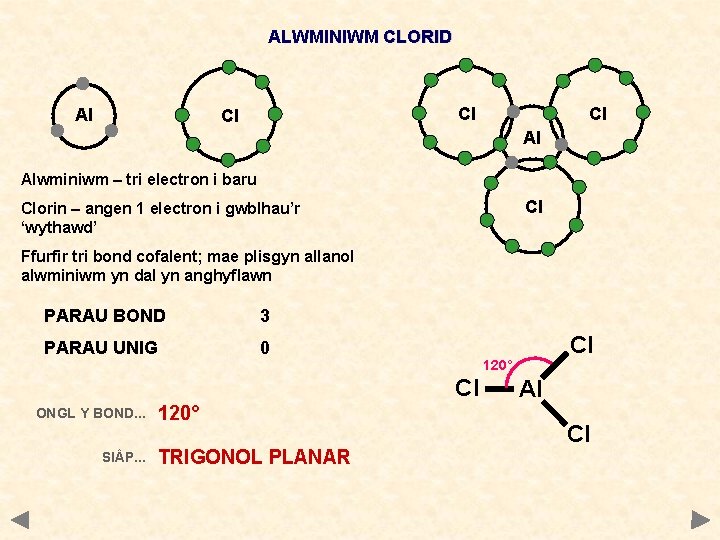
ALWMINIWM CLORID Al Cl Cl Cl Al Alwminiwm – tri electron i baru Cl Clorin – angen 1 electron i gwblhau’r ‘wythawd’ Ffurfir tri bond cofalent; mae plisgyn allanol alwminiwm yn dal yn anghyflawn PARAU BOND 3 PARAU UNIG 0 120° Cl ONGL Y BOND. . . SI P. . . 120° TRIGONOL PLANAR Cl Al Cl


METHAN H C H H Carbon – pedwar electron i baru Ffurfir pedwar bond cofalent Hydrogen - 1 electron i gwblhau’r plisgyn Mae gan C a H bellach blisg cyflawn
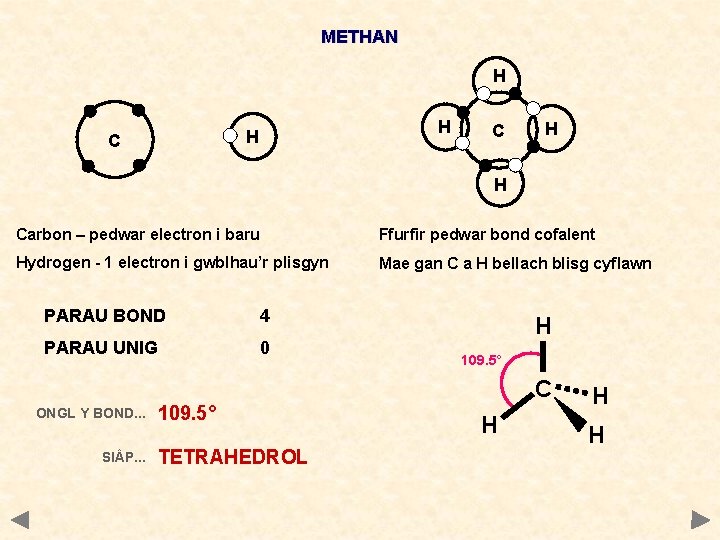
METHAN H H H C C H H Carbon – pedwar electron i baru Ffurfir pedwar bond cofalent Hydrogen - 1 electron i gwblhau’r plisgyn Mae gan C a H bellach blisg cyflawn PARAU BOND 4 PARAU UNIG 0 H 109. 5° C ONGL Y BOND. . . SI P. . . 109. 5° TETRAHEDROL H H H
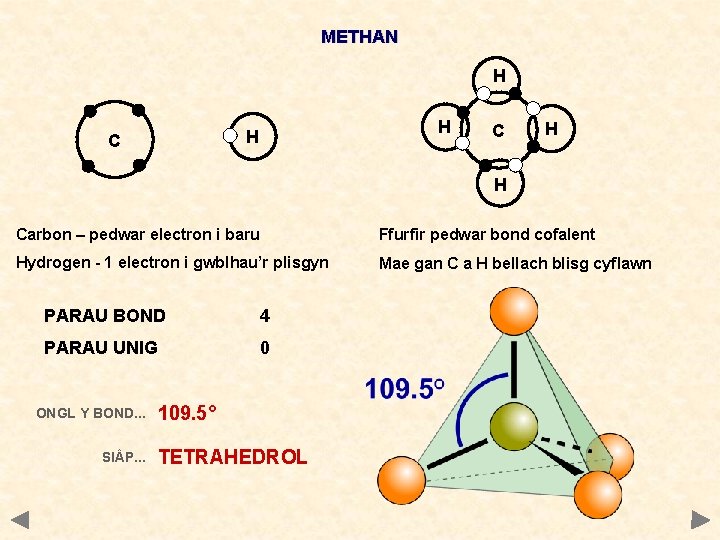
METHAN H H H C C H H Carbon – pedwar electron i baru Ffurfir pedwar bond cofalent Hydrogen - 1 electron i gwblhau’r plisgyn Mae gan C a H bellach blisg cyflawn PARAU BOND 4 PARAU UNIG 0 ONGL Y BOND. . . SI P. . . 109. 5° TETRAHEDROL

FFOSFFORWS(V) FFLWORID P F F P Ffosfforws – pump electron i baru Fflworin – angen un electron i gwblhau’r ‘wythawd’ Ffurfir pump bond cofalent; gall ffosfforws ddefnyddio orbitalau d i ymestyn ei ‘wythawd’ F F

FFOSFFORWS(V) FFLWORID F F P Ffosfforws – pump electron i baru F Fflworin – angen un electron i gwblhau’r ‘wythawd’ F Ffurfir pump bond cofalent; gall ffosfforws ddefnyddio orbitalau d i ymestyn ei ‘wythawd’ PARAU BOND 5 PARAU UNIG 0 F F 120° ONGL Y BOND. . . SI P. . . 120° & 90° DEUBYRAMID TRIGONOL F 90° P F F
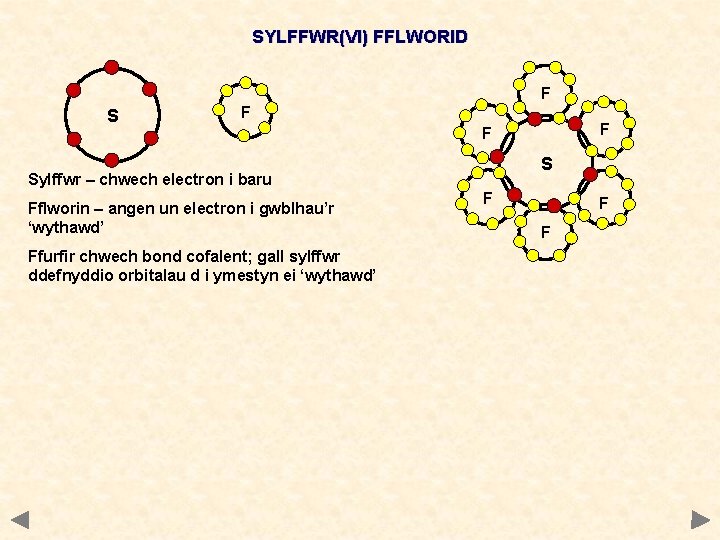
SYLFFWR(VI) FFLWORID F S Sylffwr – chwech electron i baru Fflworin – angen un electron i gwblhau’r ‘wythawd’ Ffurfir chwech bond cofalent; gall sylffwr ddefnyddio orbitalau d i ymestyn ei ‘wythawd’ F F F

SYLFFWR(VI) FFLWORID F F S Sylffwr – chwech electron i baru F Fflworin – angen un electron i gwblhau’r ‘wythawd’ F F Ffurfir chwech bond cofalent; gall sylffwr ddefnyddio orbitalau d i ymestyn ei ‘wythawd’ PARAU BOND 6 PARAU UNIG 0 F 90° F F S ONGL Y BOND. . . SI P. . . 90° OCTAHEDROL F F F

SYLFFWR(VI) FFLWORID F F S S Sylffwr – chwech electron i baru Fflworin – angen un electron i gwblhau’r ‘wythawd’ Ffurfir chwech bond cofalent; gall sylffwr ddefnyddio orbitalau d i ymestyn ei ‘wythawd’ PARAU BOND 6 PARAU UNIG 0 ONGL Y BOND. . . SI P. . . F F 90° OCTAHEDROL F F F
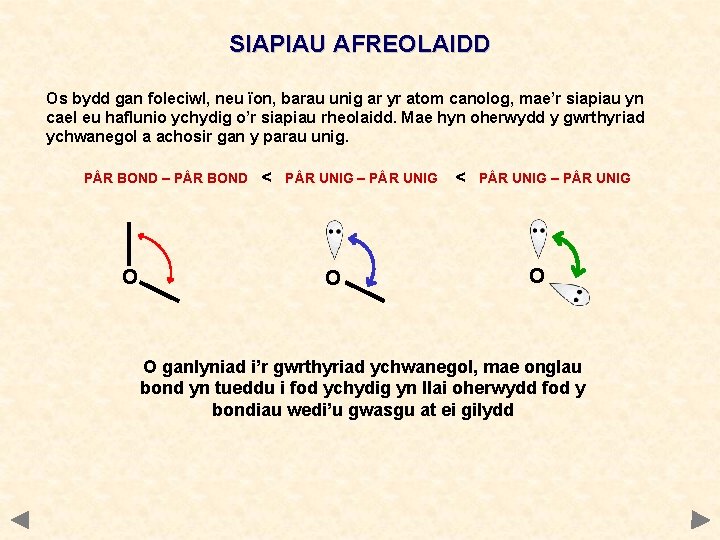
SIAPIAU AFREOLAIDD Os bydd gan foleciwl, neu ïon, barau unig ar yr atom canolog, mae’r siapiau yn cael eu haflunio ychydig o’r siapiau rheolaidd. Mae hyn oherwydd y gwrthyriad ychwanegol a achosir gan y parau unig. P R BOND – P R BOND O < P R UNIG – P R UNIG O O ganlyniad i’r gwrthyriad ychwanegol, mae onglau bond yn tueddu i fod ychydig yn llai oherwydd fod y bondiau wedi’u gwasgu at ei gilydd
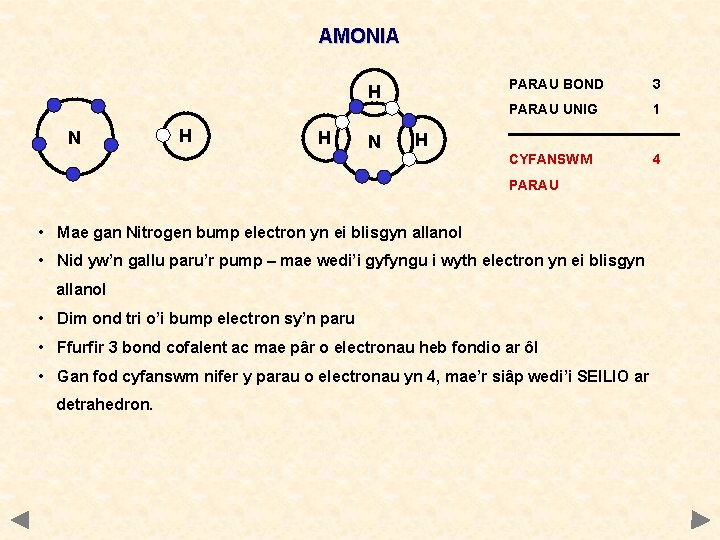
AMONIA H N H H N PARAU BOND 3 PARAU UNIG 1 CYFANSWM 4 H PARAU • Mae gan Nitrogen bump electron yn ei blisgyn allanol • Nid yw’n gallu paru’r pump – mae wedi’i gyfyngu i wyth electron yn ei blisgyn allanol • Dim ond tri o’i bump electron sy’n paru • Ffurfir 3 bond cofalent ac mae pâr o electronau heb fondio ar ôl • Gan fod cyfanswm nifer y parau o electronau yn 4, mae’r siâp wedi’i SEILIO ar detrahedron.
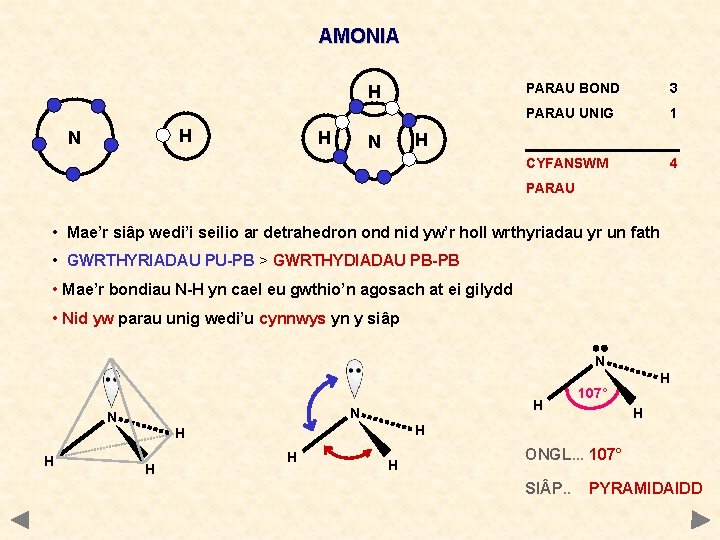
AMONIA H H N H PARAU BOND 3 PARAU UNIG 1 CYFANSWM 4 H N PARAU • Mae’r siâp wedi’i seilio ar detrahedron ond nid yw’r holl wrthyriadau yr un fath • GWRTHYRIADAU PU-PB > GWRTHYDIADAU PB-PB • Mae’r bondiau N-H yn cael eu gwthio’n agosach at ei gilydd • Nid yw parau unig wedi’u cynnwys yn y siâp N H N N H 107° H H H H ONGL. . . 107° SI P. . PYRAMIDAIDD

AMONIA H N H

DŴR H O H H O PARAU BOND 2 PARAU UNIG 2 CYFANSWM PARAU 4 • Mae gan ocsigen chwech electron yn ei blisgyn allanol • Nid yw’n gallu paru’r chwech i gyd – mae wedi’i gyfyngu i wyth electron yn ei blisgyn allanol • Dim ond dau o’i chwech electron sy’n paru • Ffurfir 2 fond cofalent ac mae 2 bâr o electronau heb fondio ar ôl • Gan fod cyfanswm nifer y parau o electronau yn 4, mae’r siâp wedi’i SEILIO ar detrahedron.

DŴR H H O PARAU BOND 2 PARAU UNIG 2 CYFANSWM PARAU 4 • Mae’r siâp wedi’i seilio ar detrahedron ond nid yw’r holl wrthyriadau yr un fath • GWRTHYRIADAU PU-PU > GWRTHYRIADAU PU-PB > GWRTHYRIADAU PB-PB • Mae’r bondiau O-H yn cael eu gwthio’n agosach byth at ei gilydd • Nid yw parau unig wedi’u cynnwys yn y siâp O H O O H H 104. 5° H ONGL. . . 104. 5° SI P. . . CAM neu siâp V

XENON TETRAFFLWORID F F Xe Xe F PARAU BOND 4 PARAU UNIG 2 CYFANSWM PARAU 6 F F • Mae gan Xenon wyth electron yn ei blisgyn allanol • Mae’n paru pedwar o’i wyth electron • Ffurfir 4 bond cofalent ac mae 2 bâr o electronau heb fondio ar ôl • Gan fod cyfanswm nifer y parau o electronau yn 6, mae’r siâp wedi’i SEILIO ar octahedron
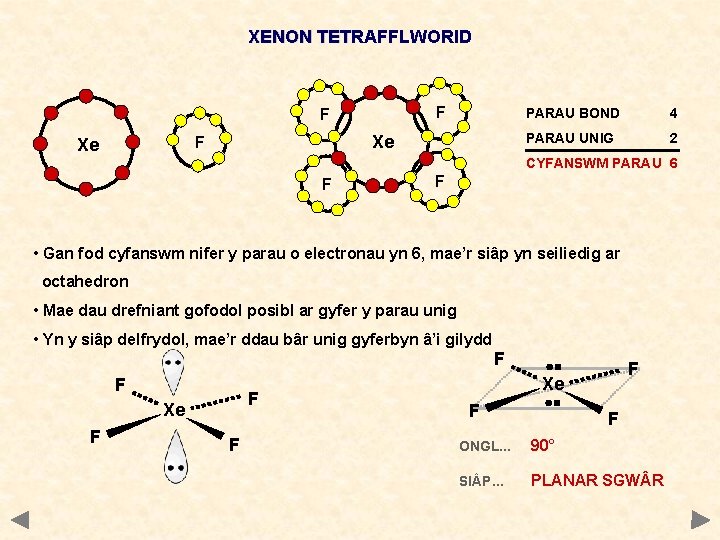
XENON TETRAFFLWORID F F Xe PARAU BOND 4 PARAU UNIG 2 CYFANSWM PARAU 6 F F • Gan fod cyfanswm nifer y parau o electronau yn 6, mae’r siâp yn seiliedig ar octahedron • Mae dau drefniant gofodol posibl ar gyfer y parau unig • Yn y siâp delfrydol, mae’r ddau bâr unig gyferbyn â’i gilydd F F F Xe F F ONGL. . . 90° SI P. . . PLANAR SGW R

CYFRIFO SIAPIAU ÏONAU Cyfrifir siâp ïon cymhleth yn yr un ffordd â moleciwl wrth… • gyfrifo nifer yr electronau ym mhlisgyn allanol y rhywogaeth ganolog* • paru electronau, gan ofalu nad oes mwy na’r uchafswm yn y plisgyn allanol • cyfrifo nifer y parau bond a pharau unig • defnyddio DAMCANIAETH GWRTHYRIAD PARAU ELECTRON i gyfrifo siâp ac ongl(au) bond * mae nifer yr electronau yn y plisgyn allanol yn dibynnu ar yr wefr ar yr ïon * os yw’r ïon yn bositif, rydych yn tynnu cymaint o electronau â sydd o wefrau positif * os yw’r ïon yn negatif, rydych yn ychwanegu cymaint o electronau â sydd o wefrau negatif e. e. ar gyfer PF 6 - ychwanegu un electron at blisgyn allanol P ar gyfer PCl 4+ tynnu un electron o blisgyn allanol P

ENGHRAIFFT SIAPIAU ÏONAU Lluniwch electronau plisgyn allanol atom canolog N
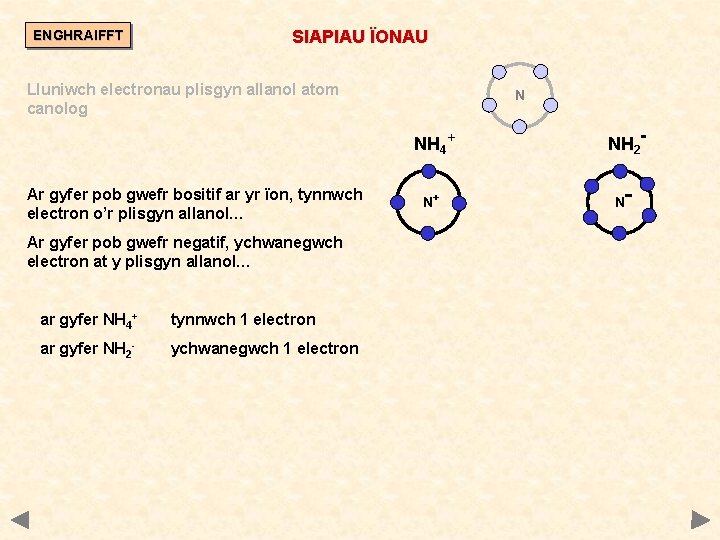
ENGHRAIFFT SIAPIAU ÏONAU Lluniwch electronau plisgyn allanol atom canolog N NH 4+ Ar gyfer pob gwefr bositif ar yr ïon, tynnwch electron o’r plisgyn allanol… Ar gyfer pob gwefr negatif, ychwanegwch electron at y plisgyn allanol… ar gyfer NH 4+ tynnwch 1 electron ar gyfer NH 2 - ychwanegwch 1 electron N+ NH 2 N

ENGHRAIFFT SIAPIAU ÏONAU Lluniwch electronau plisgyn allanol atom canolog N NH 2 - NH 4+ Ar gyfer pob gwefr bositif ar yr ïon, tynnwch electron o’r plisgyn allanol… N+ N H H Ar gyfer pob gwefr negatif, ychwanegwch electron at y plisgyn allanol… ar gyfer NH 4+ tynnwch 1 electron ar gyfer NH 2 - ychwanegwch 1 electron Parwch yr electronau yn y ffordd arferol H N+ H H H N
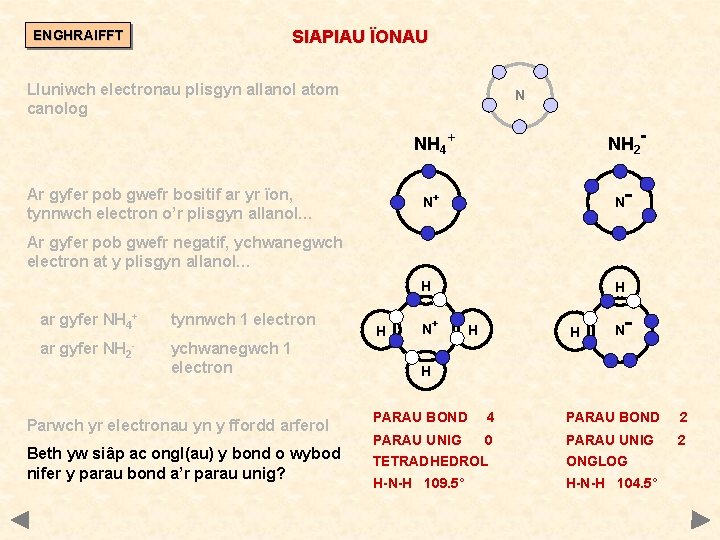
ENGHRAIFFT SIAPIAU ÏONAU Lluniwch electronau plisgyn allanol atom canolog N NH 2 - NH 4+ Ar gyfer pob gwefr bositif ar yr ïon, tynnwch electron o’r plisgyn allanol… N+ N H H Ar gyfer pob gwefr negatif, ychwanegwch electron at y plisgyn allanol… ar gyfer NH 4+ tynnwch 1 electron ar gyfer NH 2 - ychwanegwch 1 electron Parwch yr electronau yn y ffordd arferol Beth yw siâp ac ongl(au) y bond o wybod nifer y parau bond a’r parau unig? H N+ H H N H PARAU BOND 4 PARAU BOND 2 PARAU UNIG 0 PARAU UNIG 2 TETRADHEDROL ONGLOG H-N-H 109. 5° H-N-H 104. 5°
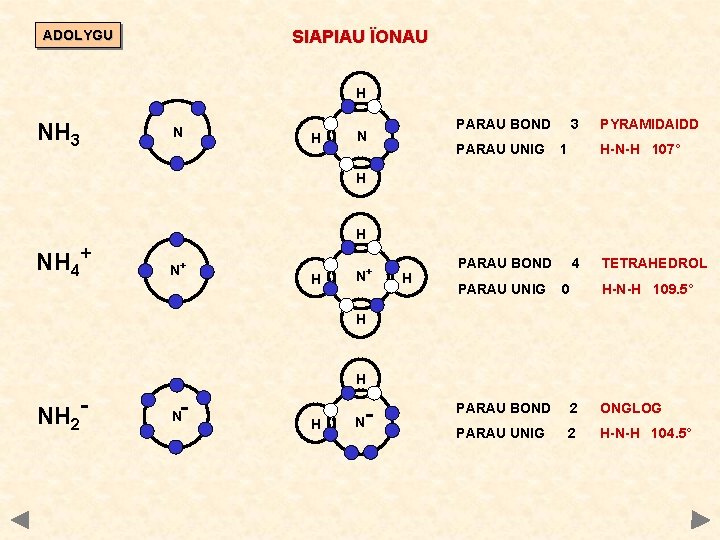
SIAPIAU ÏONAU ADOLYGU H NH 3 N H PARAU BOND N PARAU UNIG 3 1 PYRAMIDAIDD H-N-H 107° H NH 4+ H N+ H PARAU BOND PARAU UNIG 4 0 TETRAHEDROL H-N-H 109. 5° H H NH 2 - N H N PARAU BOND 2 ONGLOG PARAU UNIG 2 H-N-H 104. 5°
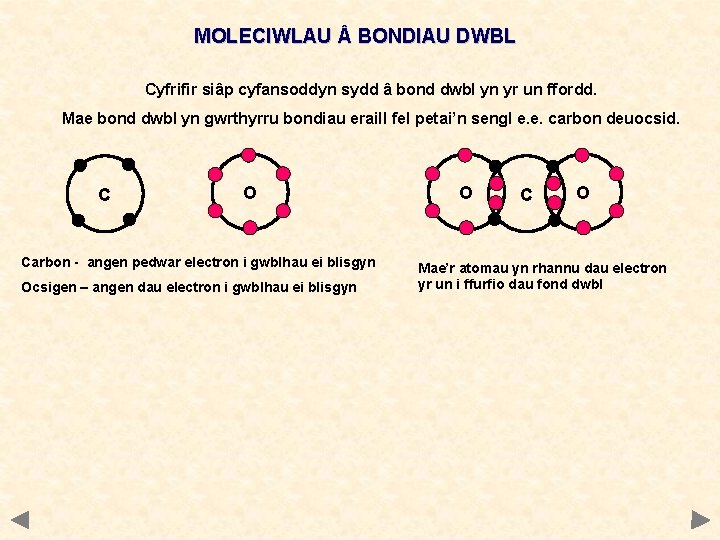
MOLECIWLAU BONDIAU DWBL Cyfrifir siâp cyfansoddyn sydd â bond dwbl yn yr un ffordd. Mae bond dwbl yn gwrthyrru bondiau eraill fel petai’n sengl e. e. carbon deuocsid. C O Carbon - angen pedwar electron i gwblhau ei blisgyn Ocsigen – angen dau electron i gwblhau ei blisgyn O C O Mae’r atomau yn rhannu dau electron yr un i ffurfio dau fond dwbl
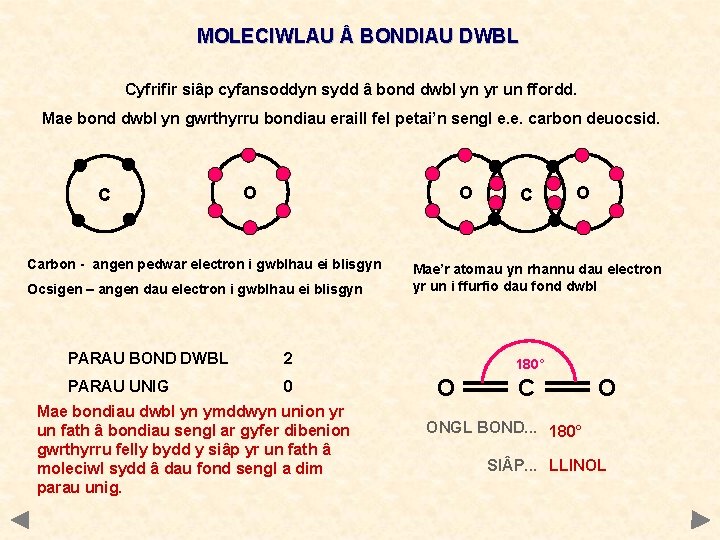
MOLECIWLAU BONDIAU DWBL Cyfrifir siâp cyfansoddyn sydd â bond dwbl yn yr un ffordd. Mae bond dwbl yn gwrthyrru bondiau eraill fel petai’n sengl e. e. carbon deuocsid. C O O Carbon - angen pedwar electron i gwblhau ei blisgyn Ocsigen – angen dau electron i gwblhau ei blisgyn PARAU BOND DWBL 2 PARAU UNIG 0 Mae bondiau dwbl yn ymddwyn union yr un fath â bondiau sengl ar gyfer dibenion gwrthyrru felly bydd y siâp yr un fath â moleciwl sydd â dau fond sengl a dim parau unig. C O Mae’r atomau yn rhannu dau electron yr un i ffurfio dau fond dwbl 180° O C O ONGL BOND. . . 180° SI P. . . LLINOL
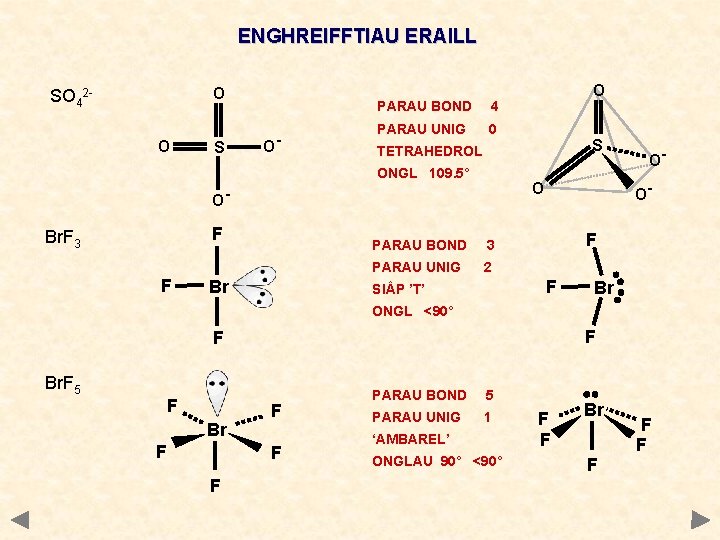
ENGHREIFFTIAU ERAILL O SO 42 O S O- PARAU BOND 4 PARAU UNIG 0 F Br PARAU BOND 3 PARAU UNIG 2 F F SI P ’T’ OO- O O- F S TETRAHEDROL ONGL 109. 5° Br. F 3 O Br ONGL <90° F F Br. F 5 F Br F F PARAU BOND 5 PARAU UNIG 1 ‘AMBAREL’ ONGLAU 90° <90° F F Br F F F

CWESTIYNAU PRAWF Ar gyfer pob un o’r ïonau/moleciwlau canlynol, nodwch nifer y parau bond nodwch nifer y parau unig nodwch yr ongl(au) bond nodwch, neu luniwch, y siâp BF 3 Si. Cl 4 PCl 4+ PCl 6 Si. Cl 62 H 2 S ATEBION DROSODD

CWESTIYNAU PRAWF ATEB Ar gyfer pob un o’r ïonau/moleciwlau canlynol, nodwch nifer y parau bond nodwch nifer y parau unig nodwch yr ongl(au) bond nodwch, neu luniwch, y siâp BF 3 3 pb 0 pu 120º trigonol planar mae boron yn paru ei 3 electron yn y plisgyn allanol Si. Cl 4 4 pb 0 pu 109. 5º tetrahedrol mae silicon yn paru ei 4 electron yn y plisgyn allanol PCl 4+ 4 pb 0 pu 109. 5º tetrahedrol gan fod yr ïon yn +, tynnu electron yn y plisgyn allanol wedyn paru 6 pb 0 pu 90º octahedrol gan fod yr ïon yn -, ychwanegu un electron at y 5 yn y plisgyn allanol wedyn paru 6 pb 0 pu 90º octahedrol gan fod yr ïon yn 2 -, ychwanegu dau electron at y plisgyn allanol wedyn paru 2 pb 2 pu 92º cam neu siâp V mae sylffwr yn paru 2 o’i 6 electron yn ei blisgyn allanol – mae 2 bâr unig ar ôl PCl 6 Si. Cl 62 H 2 S

GWIRIO Beth sydd angen i chi allu gwneud? Dwyn i gof Damcaniaeth Gwrthyriad Parau Electron Deall pam fod gwrthyriad rhwng parau electron yn effeithio ar y siâp Dwyn i gof ac egluro siapiau ac onglau bond moleciwlau â 2, 3, 4, 5 a 6 parau bond Dwyn i gof cryfderau cymharol gwrthyriadau pâr bond a phâr unig Dwyn i gof ac egluro siapiau ac onglau bond dŵr ac amonia Cymhwyso’r cysyniadau uchod i foleciwlau ac ïonau eraill, gan gynnwys y rheiny â bondiau dwbl YDYCH CHI’N GALLU GWNEUD POB UN? YDW NAC YDW

Mae angen i chi fynd dros y testun(au) perthnasol eto Cliciwch ar y botwm i ddychwelyd i’r ddewislen

DA IAWN! Rhowch gynnig ar gwestiynau papurau blaenorol

SIAPIAU MOLECIWLAU Y Diwedd
- Slides: 44