Radiklov adice AR Jedn se o adice kter










- Slides: 18

Radikálové adice (AR) Jedná se o adice, které jsou zahájeny interakcí nepárového elektronu volných radikálů s p vazbou nenasyceného systému. Radikálová činidla a jejich vznik 1) Tvorba radikálů homolytickým štěpením kovalentní vazby (bývá označována jako iniciace) Energii potřebnou k uvedenému homolytickému štěpení je možno dodat buď ve formě tepla termolýza (ve schematech označována často jako T), nebo ve formě záření, nejčastěji ultrafialového - fotolýza (ve schematech často označováno světelnými kvanty hn). Reaktivita vzniklých radikálů závisí jak na elektronegativitě atomů Y a Z, tak na možné konjugaci a sterických faktorech.

2) Tvorba radikálů redoxními reakcemi Jednoelektronové redoxní procesy vedou rovněž k volným radikálům, které jsou schopné zahájit AR : Donorem nebo akceptorem elektronu mohou být jak oxidační nebo redukční činidla, tak i anoda nebo katoda při elektrochemických procesech: a) Jednoelektronová oxidace Např. : b) Jednoelektronová redukce Např. :

Faktory ovlivňující průběh AR 1) AR málo reaktivních radikálů U málo reaktivních radikálů nedochází k řetězové reakci, ale pouze ke koligaci: a) S dalším výchozím radikálem b) S dalším vzniklým radikálem, což znamená jeho dimerizaci 2) AR reaktivních radikálů Je-li naopak vzniklý radikálový adukt dostatečně reaktivní, ke koligaci nedochází, poněvadž by při ní došlo k uvolnění tak velké energie, která by vzniklou vazbu opět rozštěpila. Vchází proto do interakcí s kovalentními vazbami výchozích molekul, což vede k tvorbě dalších reaktivních radikálů, které dále reagují stejným způsobem. Tím je zahájen řetězový průběh těchto reakcí.

Co se týče uvedených interakcí vzniklého reaktivního radikálového aduktu, jsou zde v zásadě dvě možnosti: a) Interakce s kovalentní vazbou adující se molekuly, což je počátek AR s řetězovým mechanismem b) Interakce s p-vazbou nenasyceného systému, což je počátek polymeračních reakcí Která z těchto interakcí převažuje, závisí na vzájemném poměru reakčních komponent. Při poměru 1: 1 převažuje AR. Při nedostatku adující se komponenty dochází i k interakcím typu b. Tento typ interakcí pak zcela převažuje, je-li množství adující se komponenty jen zanedbatelné.

Schematicky můžeme tyto řetězové AR a polymerace znázornit následujícím schematem:

AR na vazbu C=C AR halogenů

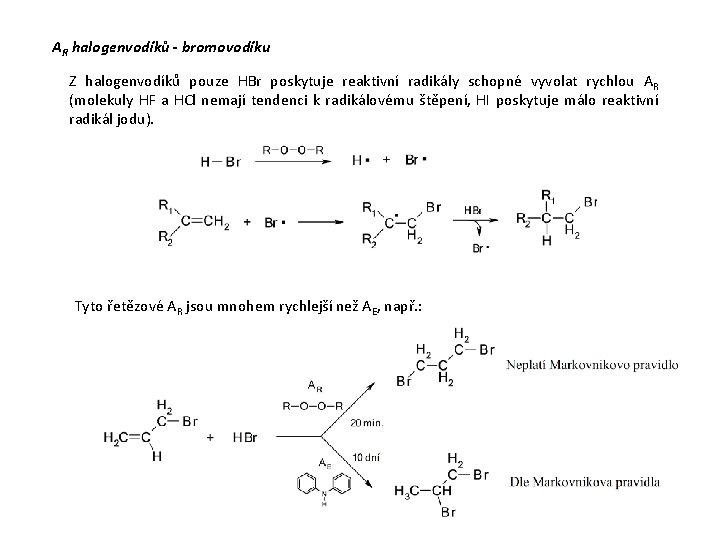
AR halogenvodíků - bromovodíku Z halogenvodíků pouze HBr poskytuje reaktivní radikály schopné vyvolat rychlou AR (molekuly HF a HCl nemají tendenci k radikálovému štěpení, HI poskytuje málo reaktivní radikál jodu). Tyto řetězové AR jsou mnohem rychlejší než AE, např. :

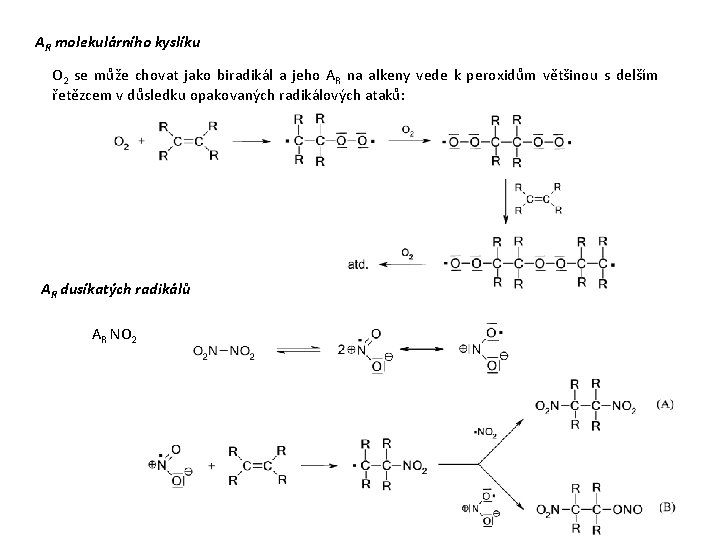
AR molekulárního kyslíku O 2 se může chovat jako biradikál a jeho AR na alkeny vede k peroxidům většinou s delším řetězcem v důsledku opakovaných radikálových ataků: AR dusíkatých radikálů AR NO 2

AR uhlíkatých radikálů a) AR halogenovaných methanů Iniciací peroxidy nebo UV zářením dochází k adici na p vazbu za vzniku halogenderivátů s řetězcem o 1 atom delším: Např. : Kde X = F, Cl, Br, I a Y = H, Cl, Br, I v různých kombinacích.

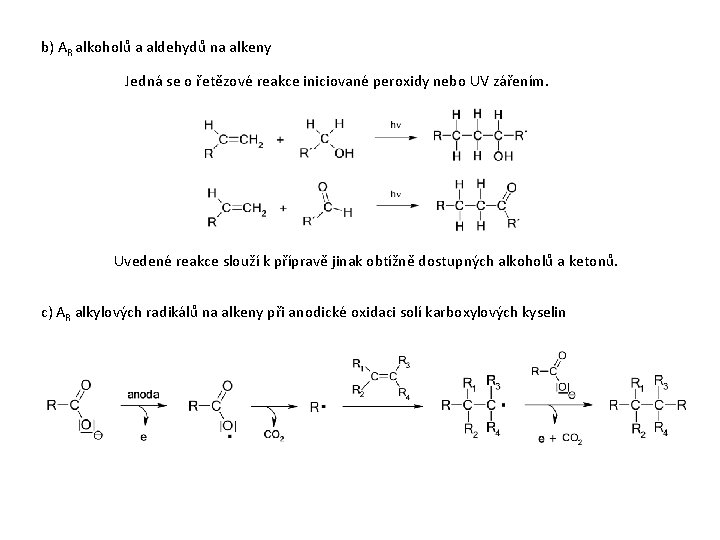
b) AR alkoholů a aldehydů na alkeny Jedná se o řetězové reakce iniciované peroxidy nebo UV zářením. Uvedené reakce slouží k přípravě jinak obtížně dostupných alkoholů a ketonů. c) AR alkylových radikálů na alkeny při anodické oxidaci solí karboxylových kyselin

d) Radikálová polymerace alkenů Jedná se rovněž o řetězovou AR, kde se na molekulu alkenu aduje vždy alkylový radikál vzniklý předchozí AR. Je-li n malé číslo (1 -5), hovoříme o telomeraci a substituenty Y mají vliv na vlastnosti telomeru. Jeli n číslo vysoké (100 -100 000), pak skupiny Y hrají zanedbatelnou roli a neovlivňují tak vlastnosti polymeru. Pro vznik vysokých polymerů je důležité, aby množství iniciátoru bylo co nejmenší. Typickými iniciátory radikálové řetězové polymerace jsou peroxidy a azosloučeniny:

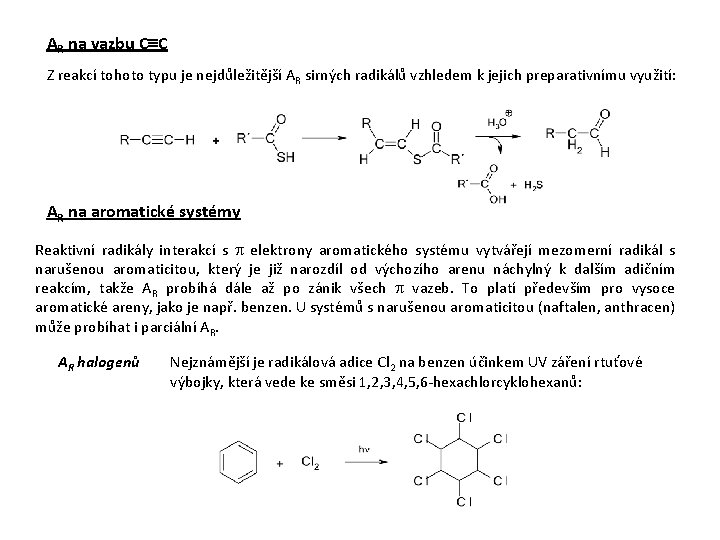
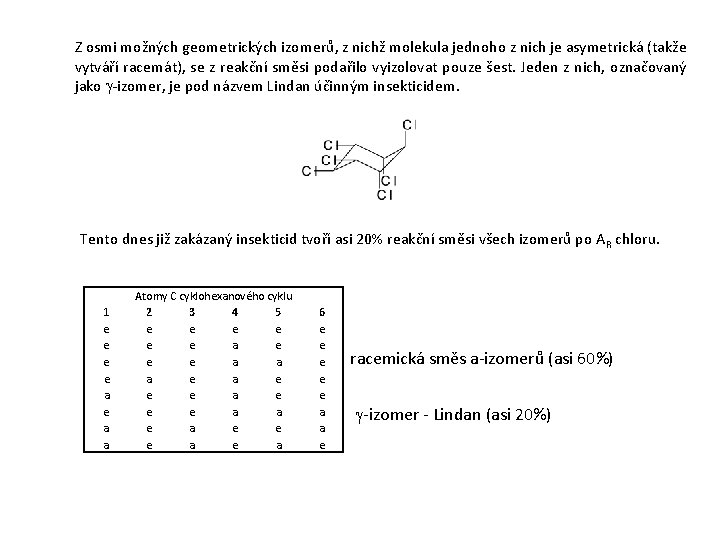
AR na vazbu C C Z reakcí tohoto typu je nejdůležitější AR sirných radikálů vzhledem k jejich preparativnímu využití: AR na aromatické systémy Reaktivní radikály interakcí s p elektrony aromatického systému vytvářejí mezomerní radikál s narušenou aromaticitou, který je již narozdíl od výchozího arenu náchylný k dalším adičním reakcím, takže AR probíhá dále až po zánik všech p vazeb. To platí především pro vysoce aromatické areny, jako je např. benzen. U systémů s narušenou aromaticitou (naftalen, anthracen) může probíhat i parciální AR. AR halogenů Nejznámější je radikálová adice Cl 2 na benzen účinkem UV záření rtuťové výbojky, která vede ke směsi 1, 2, 3, 4, 5, 6 -hexachlorcyklohexanů:

Z osmi možných geometrických izomerů, z nichž molekula jednoho z nich je asymetrická (takže vytváří racemát), se z reakční směsi podařilo vyizolovat pouze šest. Jeden z nich, označovaný jako g-izomer, je pod názvem Lindan účinným insekticidem. Tento dnes již zakázaný insekticid tvoří asi 20% reakční směsi všech izomerů po A R chloru. 1 e e a e a a Atomy C cyklohexanového cyklu 2 3 4 5 e e e a a a e e e a a e e e a 6 e e e a a e racemická směs a-izomerů (asi 60%) g-izomer - Lindan (asi 20%)

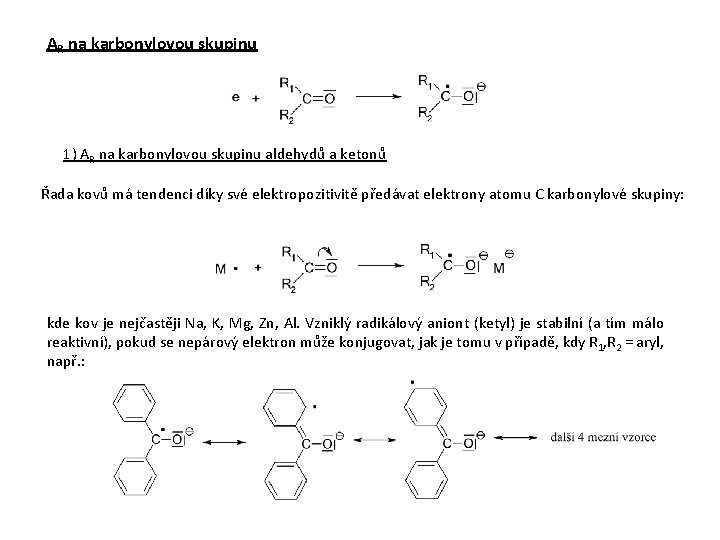
AR na karbonylovou skupinu 1) AR na karbonylovou skupinu aldehydů a ketonů Řada kovů má tendenci díky své elektropozitivitě předávat elektrony atomu C karbonylové skupiny: kde kov je nejčastěji Na, K, Mg, Zn, Al. Vzniklý radikálový aniont (ketyl) je stabilní (a tím málo reaktivní), pokud se nepárový elektron může konjugovat, jak je tomu v případě, kdy R 1, R 2 = aryl, např. :

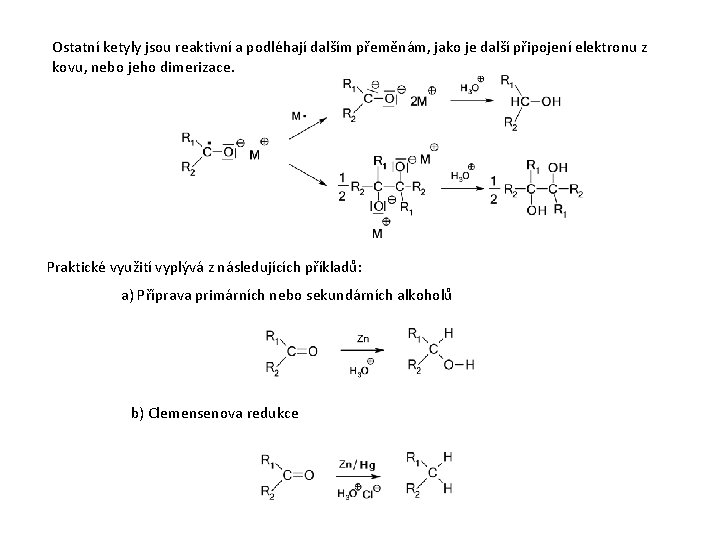
Ostatní ketyly jsou reaktivní a podléhají dalším přeměnám, jako je další připojení elektronu z kovu, nebo jeho dimerizace. Praktické využití vyplývá z následujících příkladů: a) Příprava primárních nebo sekundárních alkoholů b) Clemensenova redukce

c) Syntéza vicinálních glykolů dimerizací ketylů 2. AR na karbonylovou skupinu esterů karboxylových kyselin Z reakcí tohoto typu jsou nejdůležitější reakce zahájené AR sodíku vedoucí k radikálovému aniontu (A), který podléhá dalším přeměnám. V aprotickém prostředí přechází na dimer (B), který je v rovnováze s a-diketonem (C). Konečným produktem je však sůl endiolu (D), který vzniká 1, 4 -adicí sodíku. Po okyselení přechází sůl na endiol, který se tautomerizuje na a-hydroxyketon (acyloin). V protickém prostředí (nejčastěji alkoholickém) dochází k dalším AR sodíku a k protonizacím vznikajících aniontů, takže konečným produktem je alkoholát, resp. primární alkohol (F). Příprava primárních alkoholů z esterů touto metodou se nazývá Bouveaultova. Blancova redukce.

Syntéza acyloinů Bouveaultova-Blancova redukce

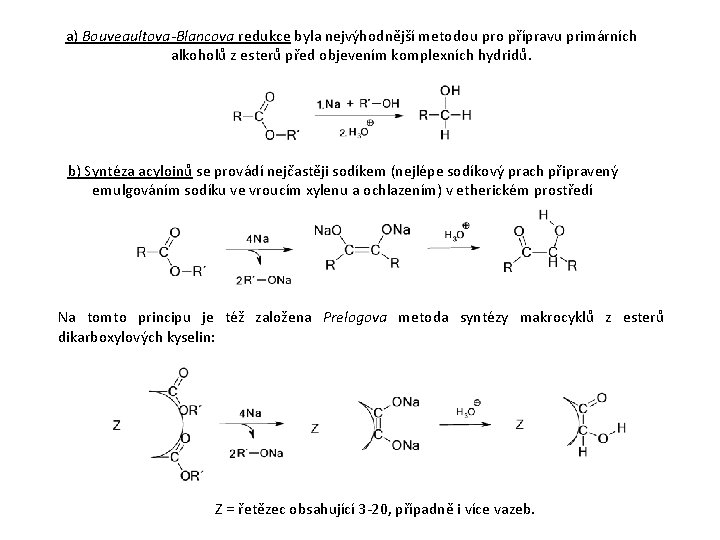
a) Bouveaultova-Blancova redukce byla nejvýhodnější metodou pro přípravu primárních alkoholů z esterů před objevením komplexních hydridů. b) Syntéza acyloinů se provádí nejčastěji sodíkem (nejlépe sodíkový prach připravený emulgováním sodíku ve vroucím xylenu a ochlazením) v etherickém prostředí Na tomto principu je též založena Prelogova metoda syntézy makrocyklů z esterů dikarboxylových kyselin: Z = řetězec obsahující 3 -20, případně i více vazeb.