Reakce alkyn CH 4 Chemick reakce a dje



- Slides: 15


Reakce alkynů CH- 4 Chemické reakce a děje , DUM č. 12 septima osmiletého studia Mgr. Radovan Sloup Gymnázium Sušice Tento materiál byl vytvořen v rámci projektu Gymnázium Sušice – Brána vzdělávání II

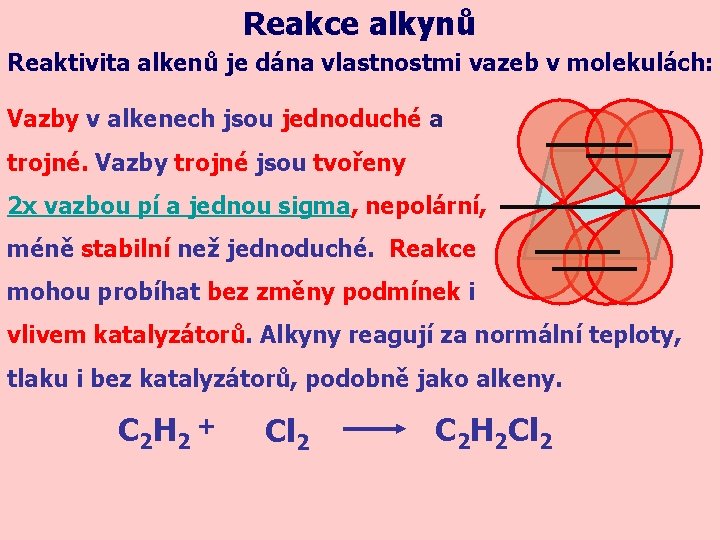
Reakce alkynů Reaktivita alkenů je dána vlastnostmi vazeb v molekulách: Vazby v alkenech jsou jednoduché a trojné. Vazby trojné jsou tvořeny 2 x vazbou pí a jednou sigma, nepolární, méně stabilní než jednoduché. Reakce mohou probíhat bez změny podmínek i vlivem katalyzátorů. Alkyny reagují za normální teploty, tlaku i bez katalyzátorů, podobně jako alkeny. C 2 H 2 + Cl 2 C 2 H 2 Cl 2

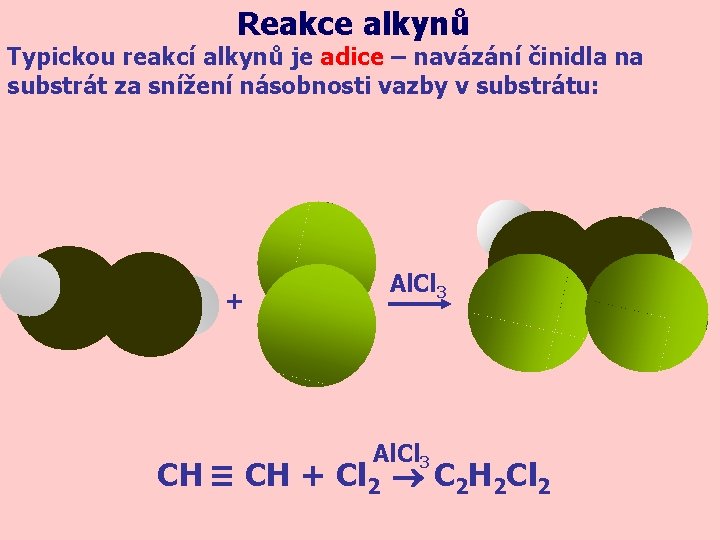
Reakce alkynů Typickou reakcí alkynů je adice – navázání činidla na substrát za snížení násobnosti vazby v substrátu: + Al. Cl 3 CH ≡ CH + Cl 2 C 2 H 2 Cl 2

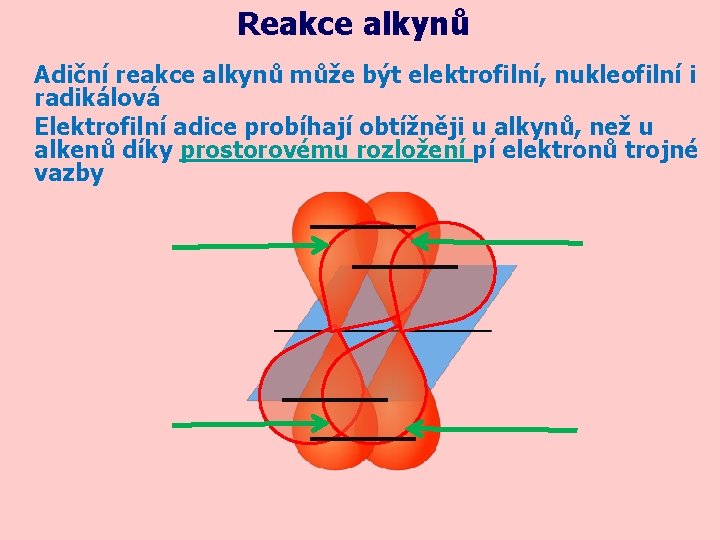
Reakce alkynů Adiční reakce alkynů může být elektrofilní, nukleofilní i radikálová Elektrofilní adice probíhají obtížněji u alkynů, než u alkenů díky prostorovému rozložení pí elektronů trojné vazby

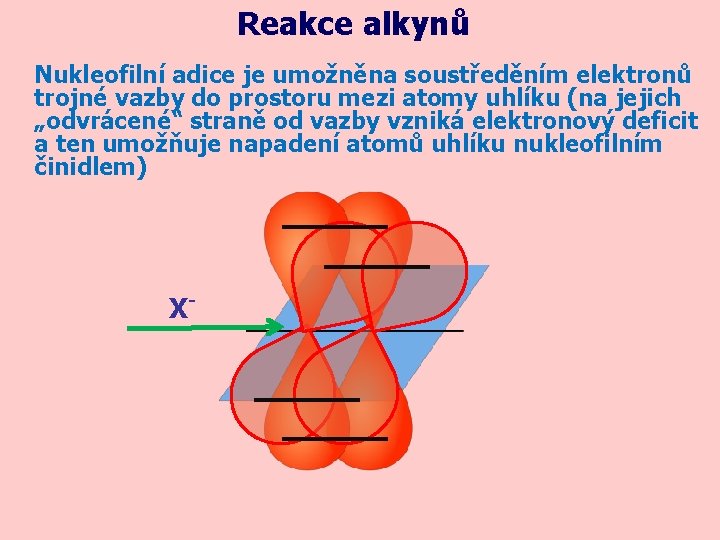
Reakce alkynů Nukleofilní adice je umožněna soustředěním elektronů trojné vazby do prostoru mezi atomy uhlíku (na jejich „odvrácené“ straně od vazby vzniká elektronový deficit a ten umožňuje napadení atomů uhlíku nukleofilním činidlem) X-

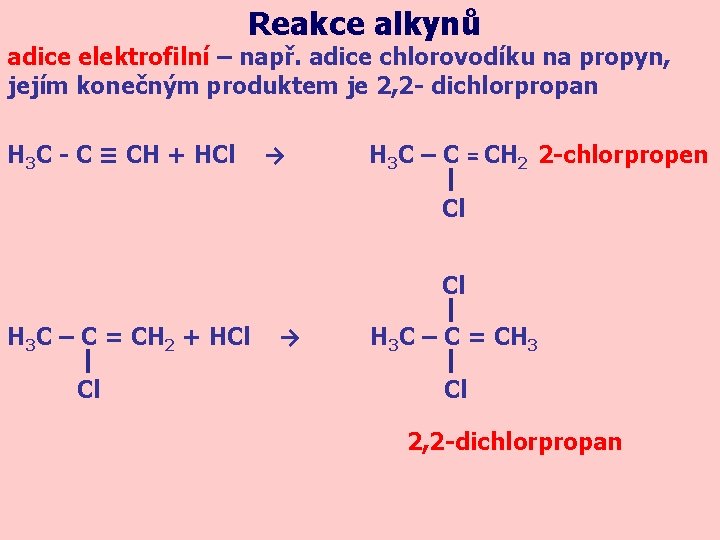
Reakce alkynů adice elektrofilní – např. adice chlorovodíku na propyn, jejím konečným produktem je 2, 2 - dichlorpropan H 3 C - C ≡ CH + HCl → H 3 C – C = CH 2 2 -chlorpropen Cl Cl H 3 C – C = CH 2 + HCl Cl → H 3 C – C = CH 3 Cl 2, 2 -dichlorpropan

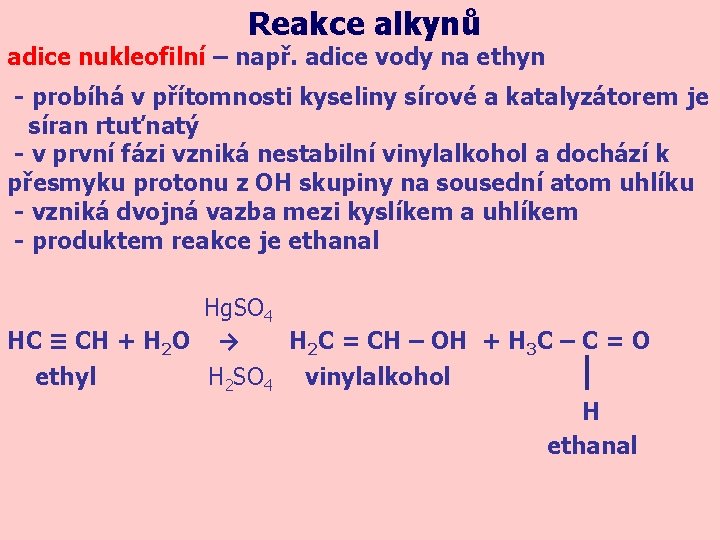
Reakce alkynů adice nukleofilní – např. adice vody na ethyn - probíhá v přítomnosti kyseliny sírové a katalyzátorem je síran rtuťnatý - v první fázi vzniká nestabilní vinylalkohol a dochází k přesmyku protonu z OH skupiny na sousední atom uhlíku - vzniká dvojná vazba mezi kyslíkem a uhlíkem - produktem reakce je ethanal Hg. SO 4 HC ≡ CH + H 2 O → H 2 C = CH – OH + H 3 C – C = O ethyl H 2 SO 4 vinylalkohol H ethanal

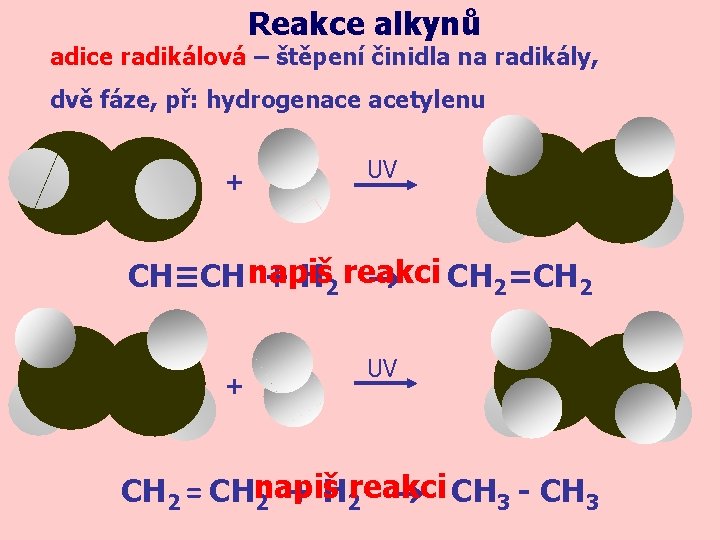
Reakce alkynů adice radikálová – štěpení činidla na radikály, dvě fáze, př: hydrogenace acetylenu + UV CH≡CH napiš + H 2 reakci CH 2=CH 2 + UV reakci CH 2 = CHnapiš 2 + H 2 CH 3 - CH 3

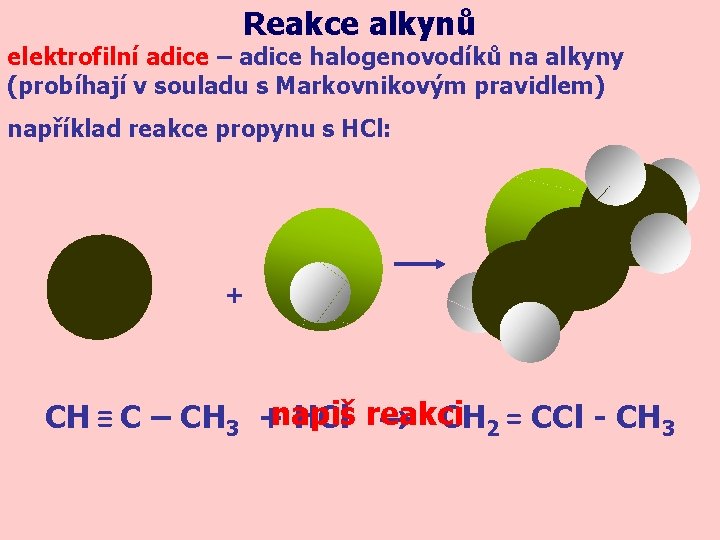
Reakce alkynů elektrofilní adice – adice halogenovodíků na alkyny (probíhají v souladu s Markovnikovým pravidlem) například reakce propynu s HCl: + CH ≡ C – CH 3 +napiš HCl reakci CH 2 = CCl - CH 3

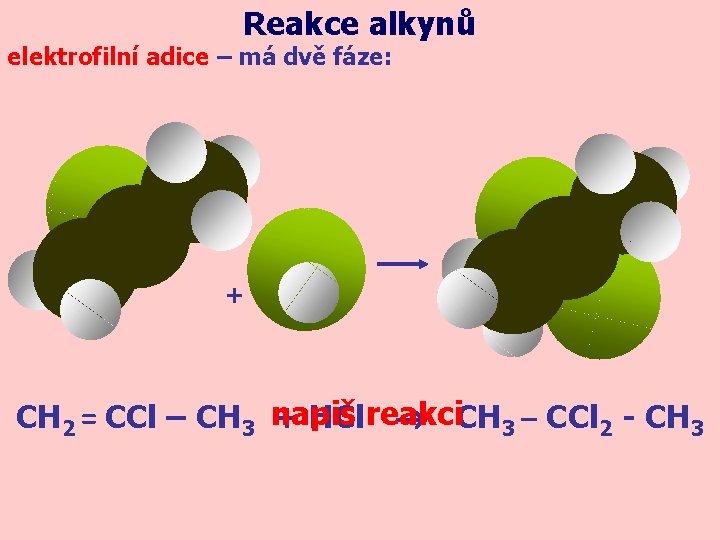
Reakce alkynů elektrofilní adice – má dvě fáze: + CH 2 = CCl – CH 3 napiš + HCl reakci CH 3 – CCl 2 - CH 3

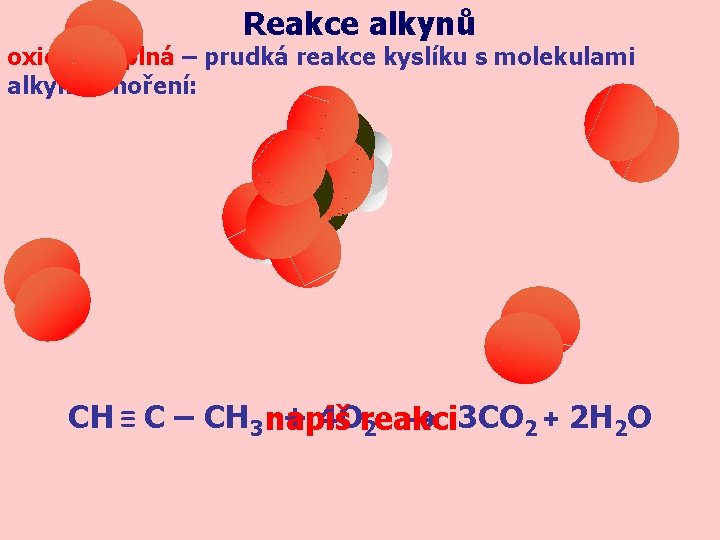
Reakce alkynů oxidace úplná – prudká reakce kyslíku s molekulami alkynů - hoření: CH ≡ C – CH 3 napiš + 4 Oreakci 2 3 CO 2 + 2 H 2 O

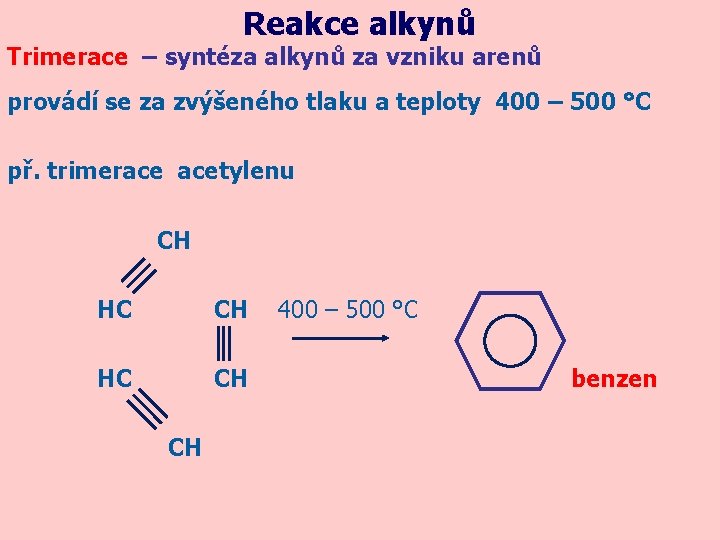
Reakce alkynů Trimerace – syntéza alkynů za vzniku arenů provádí se za zvýšeného tlaku a teploty 400 – 500 °C př. trimerace acetylenu CH HC CH CH 400 – 500 °C benzen

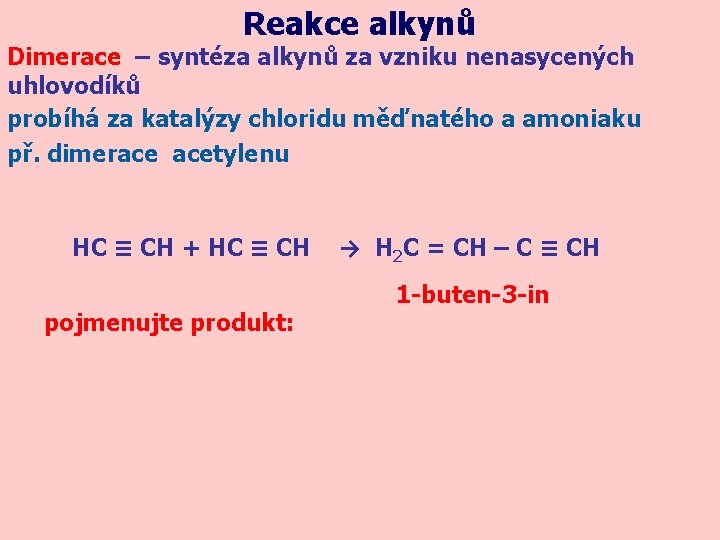
Reakce alkynů Dimerace – syntéza alkynů za vzniku nenasycených uhlovodíků probíhá za katalýzy chloridu měďnatého a amoniaku př. dimerace acetylenu HC ≡ CH + HC ≡ CH pojmenujte produkt: → H 2 C = CH – C ≡ CH 1 -buten-3 -in

REAKCE ALKYNŮ Vytvořeno v rámci projektu Gymnázium Sušice - Brána vzdělávání II Autor: Mgr. Radovan Sloup, Gymnázium Sušice Předmět: Chemie (Chemické reakce a děje) Třída: septima osmiletého studia Označení: VY_32_INOVACE_Ch-4_12 Datum vytvoření: září 2013 Anotace a metodické poznámky Reakce alkynů vychází z tématu organických reakcí a jejich průběhu. Navazují na reakce alkanů a alkenů. Mezi základní reakce alkynů patří radikálová, nukleofilní a elektrofilní adice, oxidace a dimerace, případně trimerace. Tato prezentace poskytuje přehled základních reakcí alkynů s jejich konkrétními příklady. Během prezentace je několik jednoduchých animací a cvičení k orientaci v reakcích. Prezentaci je možné doplnit dalšími reakcemi. Použité materiály: Honza, J. ; Mareček, A. ; Chemie pro čtyřletá gymnázia (2. díl). Brno: Da. Ta. Print, 1996; ISBN 80 -902200 -4 -5 Pacák, J. ; Chemie pro 2. ročník gymnázií. Praha: SPN, 1986 Obrázky, animace a schémata jsou dílem autora prezentace. Vše je vytvořeno pomocí nástrojů Power. Point 2003, Chem. Sketch 11. 01, Gimp 2 Materiály jsou určeny pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízení. Jakékoliv další využití podléhá autorskému zákonu.