ALKYNY RNDr Marta Najbertov Gymnzium a Jazykov kola

ALKYNY RNDr. Marta Najbertová

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Název školy Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Adresa školy IČO Operační program Registrační číslo Označení vzdělávacího materiálu Vzdělávací oblast Vzdělávací obor Tematický okruh Sokolovská 1638 620 330 26 Operační program Vzdělávání pro konkurenceschopnost CZ. 1. 07/1. 1. 28/01. 0050 K_INOVACE_1. CH. 17 Člověk a příroda Chemie Uhlovodíky - alkyny Zhotoveno Ročník Vyšší stupeň osmiletého gymnázia a čtyřleté gymnázium (RVP – G) Anotace Materiál je určen jako studijní materiál v předmětu chemie. Je zaměřen na obecnou charakteristiku, rozdělení, vlastnosti a popis zástupců alkynů. Předpokládá zvládnutí teorie atomového obalu, chemické vazby a obecné chemie. Materiál je určen pro seminář chemie, lze jej využít i v hodinách chemie.
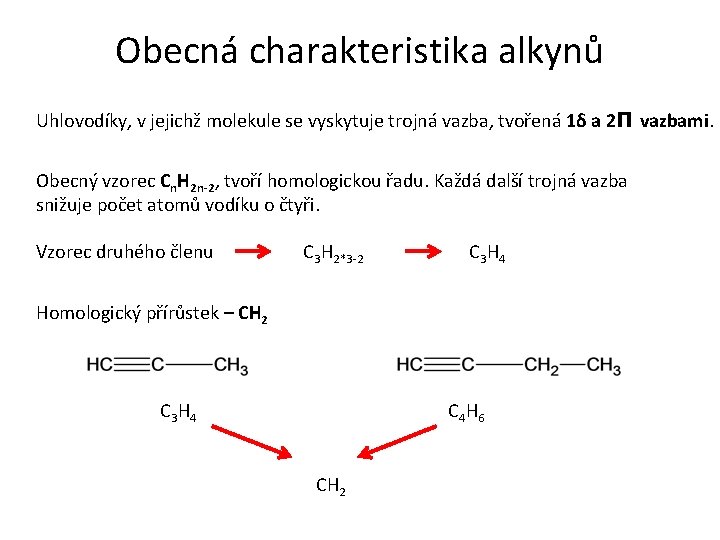
Obecná charakteristika alkynů Uhlovodíky, v jejichž molekule se vyskytuje trojná vazba, tvořená 1δ a 2Π vazbami. Obecný vzorec Cn. H 2 n-2, tvoří homologickou řadu. Každá další trojná vazba snižuje počet atomů vodíku o čtyři. Vzorec druhého členu C 3 H 2*3 -2 C 3 H 4 Homologický přírůstek – CH 2 C 3 H 4 C 4 H 6 CH 2
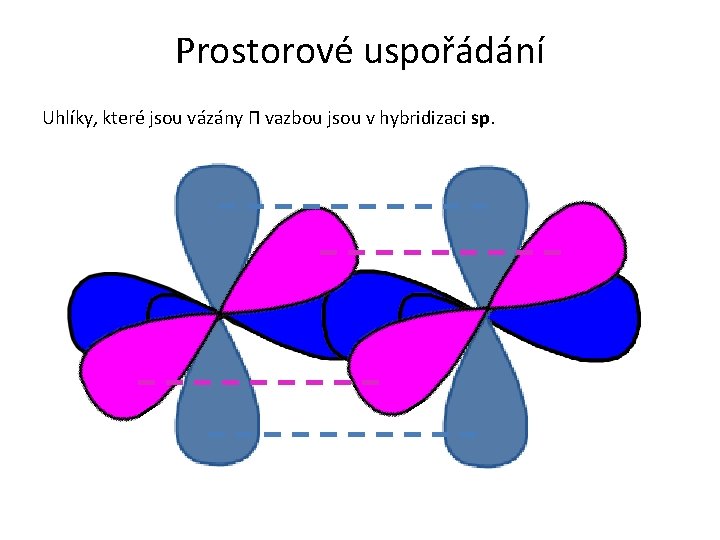
Prostorové uspořádání Uhlíky, které jsou vázány Π vazbou jsou v hybridizaci sp.
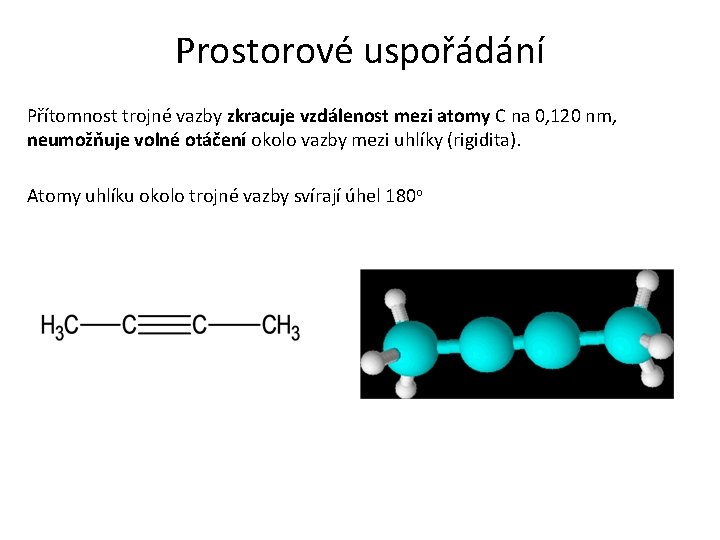
Prostorové uspořádání Přítomnost trojné vazby zkracuje vzdálenost mezi atomy C na 0, 120 nm, neumožňuje volné otáčení okolo vazby mezi uhlíky (rigidita). Atomy uhlíku okolo trojné vazby svírají úhel 180 o
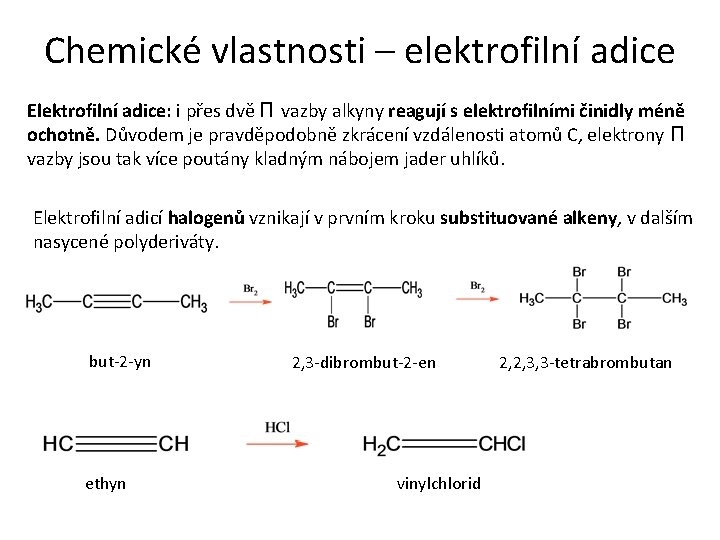
Chemické vlastnosti – elektrofilní adice Elektrofilní adice: i přes dvě Π vazby alkyny reagují s elektrofilními činidly méně ochotně. Důvodem je pravděpodobně zkrácení vzdálenosti atomů C, elektrony Π vazby jsou tak více poutány kladným nábojem jader uhlíků. Elektrofilní adicí halogenů vznikají v prvním kroku substituované alkeny, v dalším nasycené polyderiváty. but-2 -yn ethyn 2, 3 -dibrombut-2 -en vinylchlorid 2, 2, 3, 3 -tetrabrombutan
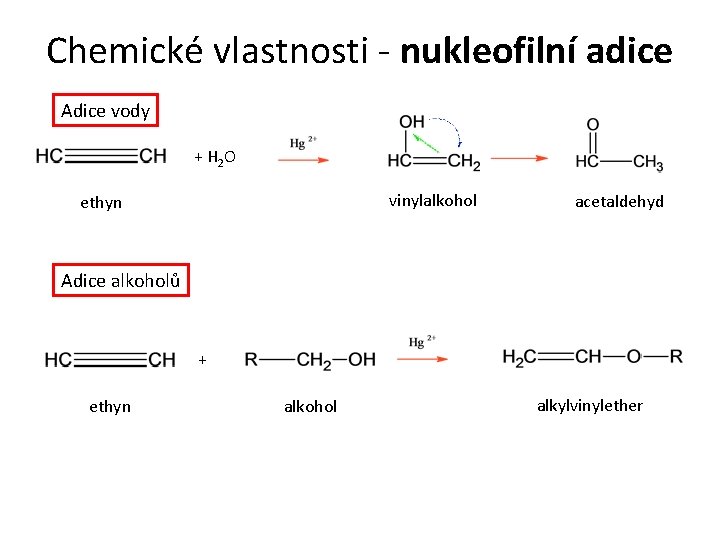
Chemické vlastnosti - nukleofilní adice Adice vody + H 2 O vinylalkohol ethyn acetaldehyd Adice alkoholů + ethyn alkohol alkylvinylether
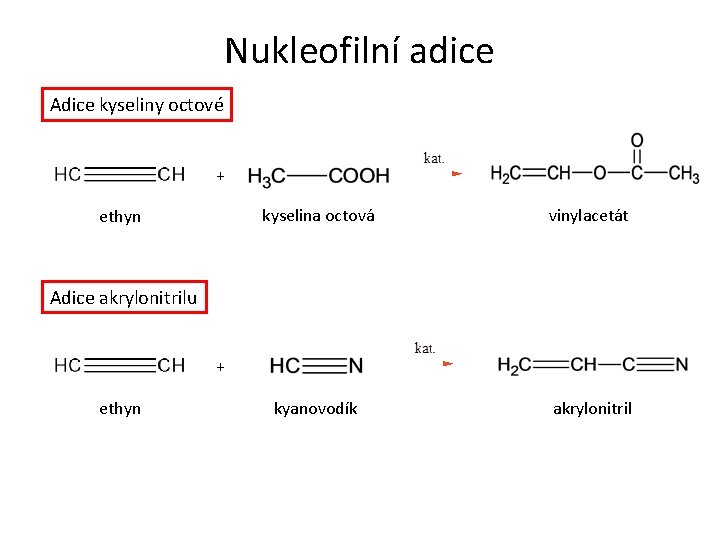
Nukleofilní adice Adice kyseliny octové + ethyn kyselina octová vinylacetát kyanovodík akrylonitril Adice akrylonitrilu + ethyn
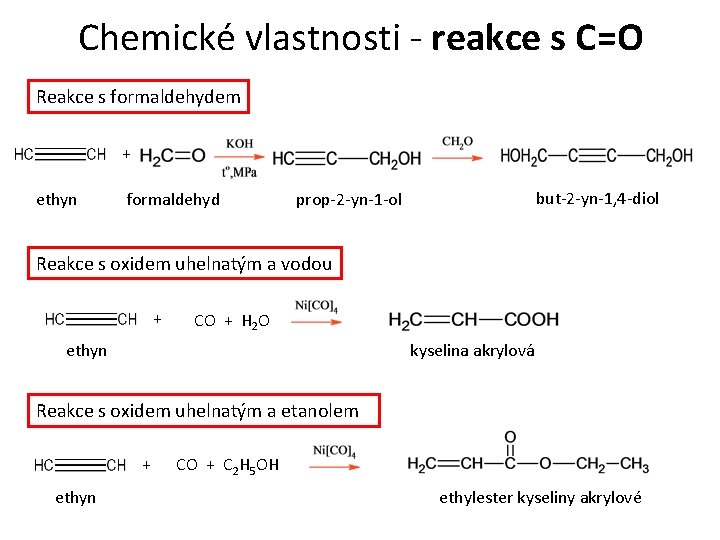
Chemické vlastnosti - reakce s C=O Reakce s formaldehydem + ethyn formaldehyd but-2 -yn-1, 4 -diol prop-2 -yn-1 -ol Reakce s oxidem uhelnatým a vodou + CO + H 2 O ethyn kyselina akrylová Reakce s oxidem uhelnatým a etanolem + ethyn CO + C 2 H 5 OH ethylester kyseliny akrylové

Chemické vlastnosti - acetylidy Vodík na atomu uhlíku trojné vazby je kyselý, lze jej nahradit kovem. Vznikají tak sloučeniny acetylidy (karbidy). Podle postavení v elektrochemické řadě napětí kovů jsou vzniklé acetylidy kovalentní (ušlechtilé kovy) - nestálé, výbušné nebo iontové (alkalické kovy, kovy alkalických zemin). Aniont HCC- má silné nukleofilní účinky. Acetylidy alkalických kovů alkalických zemin se vodou rozkládají za vzniku acetylenu.

Ethyn=acetylen Bezbarvý plyn, čistý bez zápachu, technický se vzduchem (3 -70%) výbušná směs. Výroba – tavením koksu s oxidem vápenatým s následnou hydrolýzou karbidu vápenatého. Ca. O + 3 C Ca. C 2 + CO + Ca(OH)2 Ca. C 2 V současnosti převažuje výroba pyrolýzou methanu. 2 CH 4 + 2 H 2 Vzhledem k teplotě je výroba energeticky náročná, proto je snaha některé produkty reakcí ethynu nahrazovat výrobou z ethenu.
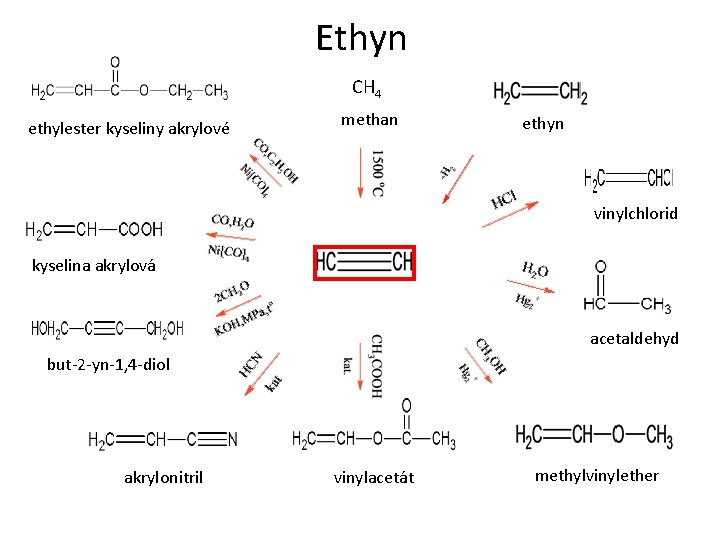
Ethyn CH 4 ethylester kyseliny akrylové methan ethyn vinylchlorid kyselina akrylová acetaldehyd but-2 -yn-1, 4 -diol akrylonitril vinylacetát methylvinylether
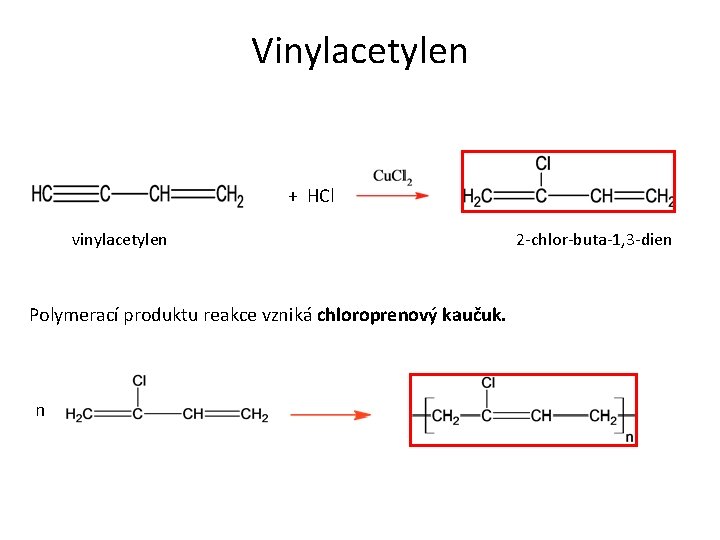
Vinylacetylen + HCl vinylacetylen Polymerací produktu reakce vzniká chloroprenový kaučuk. n 2 -chlor-buta-1, 3 -dien
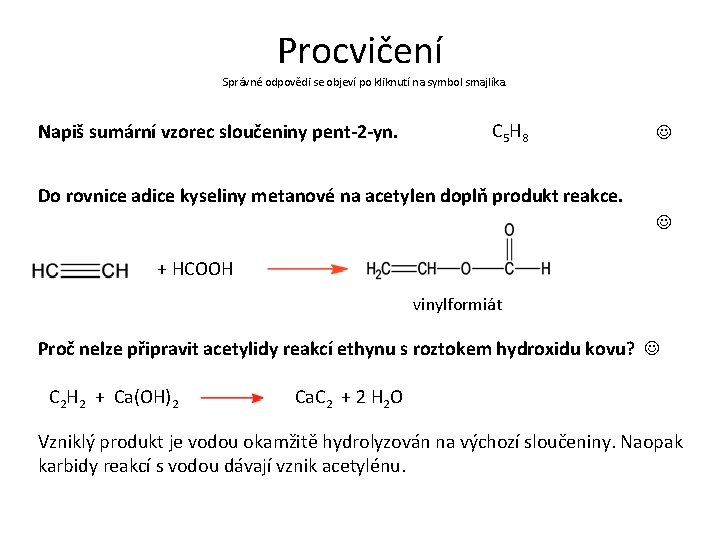
Procvičení Správné odpovědi se objeví po kliknutí na symbol smajlíka. Napiš sumární vzorec sloučeniny pent-2 -yn. C 5 H 8 Do rovnice adice kyseliny metanové na acetylen doplň produkt reakce. + HCOOH vinylformiát Proč nelze připravit acetylidy reakcí ethynu s roztokem hydroxidu kovu? C 2 H 2 + Ca(OH)2 Ca. C 2 + 2 H 2 O Vzniklý produkt je vodou okamžitě hydrolyzován na výchozí sloučeniny. Naopak karbidy reakcí s vodou dávají vznik acetylénu.
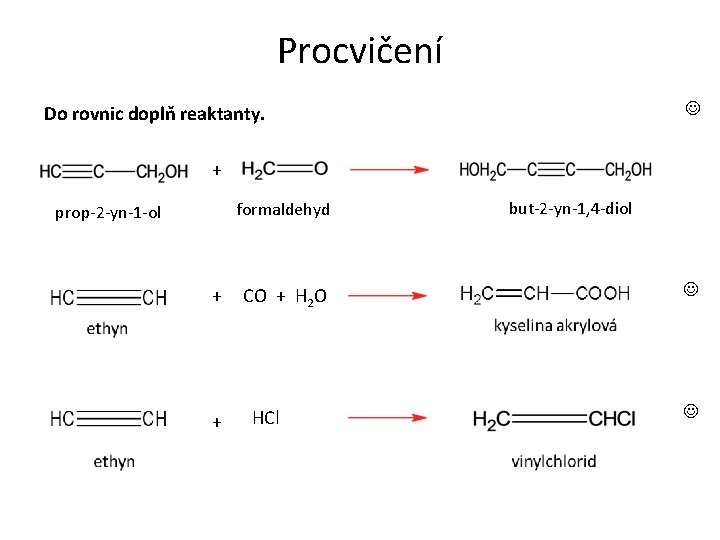
Procvičení Do rovnic doplň reaktanty. + formaldehyd prop-2 -yn-1 -ol + + CO + H 2 O HCl but-2 -yn-1, 4 -diol

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura 1. ČERVINKA, Otakar a kol. Mechanismy organických reakcí: učebnice pro vys. školy chemickotechnologické. 1. vyd. Praha: SNTL, 1976. 483, [1] s. Řada chemické literatury. 2. HALBYCH, Josef a KLÍMOVÁ, Helena. Didaktika organické chemie: příklady vyučovacích postupů. 1. vyd. Praha: Univerzita Karlova, 1988. 158 s. 3. MCMURRY, John. Organická chemie. Vyd. 1. V Brně: VUTIUM, 2007. xxv, 1176, 61, 31 s. Překlady vysokoškolských učebnic; sv. 2. ISBN 978 -80 -214 -3291 -8. 4. PACÁK, Josef. Stručné základy organické chemie. 1. vydání. Praha: SNTLNakladatelství technické literatury, 1975. Řada chem. literatury. 5. Fotografie a vzorce z vlastní databáze autora. Vytvořeny programy ACD FREE 12, Snagit Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura 1. Petroleum. cz/ropa/. Petroleum. cz [online]. [cit. 2013 -11 -27]. Dostupné z: http: //www. petroleum. cz/ 2. Studiumchemie. cz: Portál PřF UK na podporu výuky chemie na ZŠ a SŠ [online]. [cit. 2013 -11 -27]. Dostupné z: http: //www. studiumchemie. cz/ 3. Ethyn. In: Wikipedia: the free encyclopedia [online]. San Francisco (CA): Wikimedia Foundation, 2001 - [cit. 2013 -11 -27]. Dostupné z: http: //cs. wikipedia. org/wiki/Ethyn Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.
- Slides: 17