ALKYNY Cn H 2 n2 nenasycen acyklick uhlovodky










- Slides: 11

ALKYNY -Cn H 2 n-2 -nenasycené acyklické uhlovodíky s trojnou vazbou -odvozeny od alkanů + koncovka –YN - jejich zbytky mají příponu – ynyl (vznik - odtržením H+)

NÁZVOSLOVÍ ALKYNŮ S NEROZVĚTVENÝM ŘETĚZCEM: uhlíkový řetězec číslujeme tak, aby uhlíky s trojnou vazbou měli co nejmenší číslo.

NÁZVOSLOVÍ ALKYNŮ S ROZVĚTVENÝM ŘETĚZCEM: určení hlavního řetězce – ten který má největší počet trojných vazeb číslování hlavního řetězce tak, aby uhlíky s trojnými vazbami měli co nejmenší číslo ale pokud jsou v řetězci dvojné i trojné vazby, pak má číslování vazeb s dvojnými vazbami přednost

CHARAKTERISTIKA VAZBY - dvě vazby π a jedna σ, vazby π spolu splývají a vytvářejí kolem vazby σ souvislý obal - reakce většinou probíhají na vazbách π

VLASTNOSTI: -mají vyšší teploty tání a varu než u příslušných alkanů a alkenů -hořlavé - nerozpustné ve vodě - převážně plynné - jsou méně stabilní a reaktivnější než alkany a alkeny

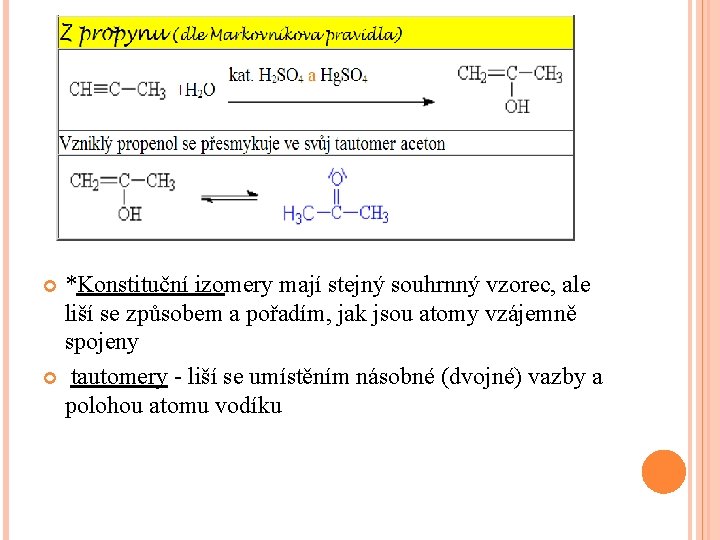
REAKCE 1) adice (nukleofilní) - vody na ethyn- výroba acetaldehydu (ethanal) - Kučerovova reakce, tautomerie

*Konstituční izomery mají stejný souhrnný vzorec, ale liší se způsobem a pořadím, jak jsou atomy vzájemně spojeny tautomery - liší se umístěním násobné (dvojné) vazby a polohou atomu vodíku

2)ADICE ELEKTROFILNÍ chlorovodíku na ethyn (je katalyzována rtuťnatými kationty, které naruší trojnou vazbu) + HCl kat. Hg 2+ 3)Adice radikálová (pomocí Br/ H) Cl. C

ZÁSTUPCI - ETHYN - bezbarvý plyn, bez zápachu, ve směsi se vzduchem vybuchuje - používá se při svařování autogennním (s kyslíkem vytváří speciální plamen), řezání kovů - ocelové láhve -využití: karbidové lampy (/Maďarsko, Anglie –pouliční osvětlení) -průmyslová surovina pro výrobu mnoha organických sloučenin, např. acetaldehydu, vinyl chloridu (chlorethen)

PŘÍPRAVA A VÝROBA ETHYNU hydrolýza acetylidů alkalických kovů alkalických zemin: Ca. C 2 + 2 H 2 O → CH≡CH + Ca(OH)2 Nedokonalé spalování methanu: 4 CH 4 + O 2 → 2 CO + 7 H 2 + CH≡CH

VZNIK ACETYLIDŮ - z alkynů, přesněji z ethynu (acetylenu) – jeho reakcí s kovy - záměnou vodíkových atomů (u trojné vazby) za atomy kovu -pevné látky rozpustné ve vodě, stálé vůči teplotě Ca. C 2 - acetylid vápenatý, také nazývaný karbid vápníku, reakcí s vodou vzniká acetylen: Ca. C 2 + 2 H 2 O → CH≡CH + Ca(OH)2 -avšak acetylidy těžkých kovů, jsou ve vodě nerozpustné, pokud je zahříváme, explodují – Ag 2 C 2 -výroba karbidu vápníku - reakce oxidu vápenatého s koksem v elektrické peci: 2 Ca. O + 3 C 2 → 2 Ca. C 2 + 2 CO