UNIDAD CURRICULAR TERMODINMICA TEMA 2 SUSTANCIAS PURAS Prof





- Slides: 15

UNIDAD CURRICULAR: TERMODINÁMICA TEMA 2: SUSTANCIAS PURAS Prof. : Ing. Johanna M, Krijnen Romero PUNTO FIJO, JUNIO DE 2008 AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 1 UNEFM

PROPIEDADES DE LAS SUSTANCIAS PURAS SUSTANCIA PURA: Aquellas que conservan una composición fija e invariable y cuyas propiedades físicas y químicas son siempre las mismas. Ejemplo: Agua, Nitrógeno, helio y Dióxido de carbono NO tiene que ser de un solo elemento químico o compuesto. Ejemplo el AIRE Una mezcla de dos o más fases de una misma sustancia pura sigue siendo sustancia pura siempre que la composición química de las fases sea la misma. AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 2

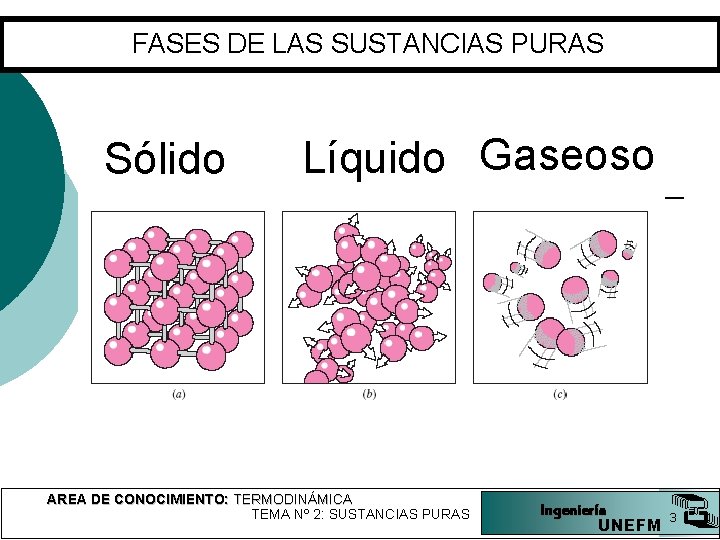
FASES DE LAS SUSTANCIAS PURAS Sólido Líquido Gaseoso AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 3

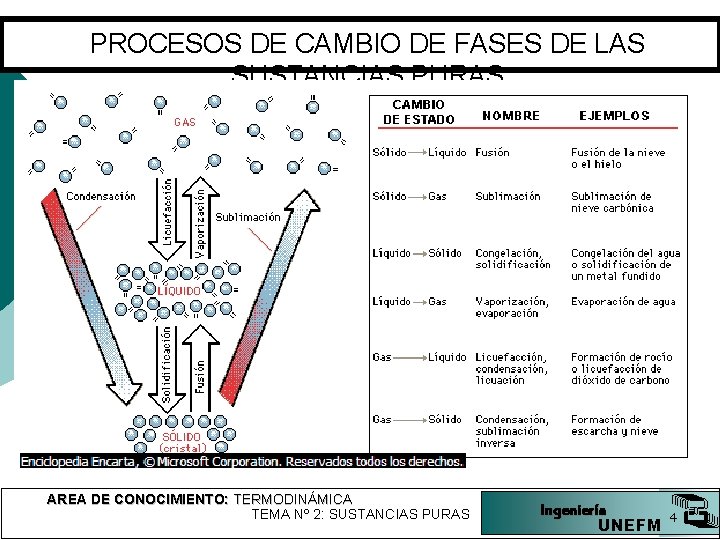
PROCESOS DE CAMBIO DE FASES DE LAS SUSTANCIAS PURAS AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 4

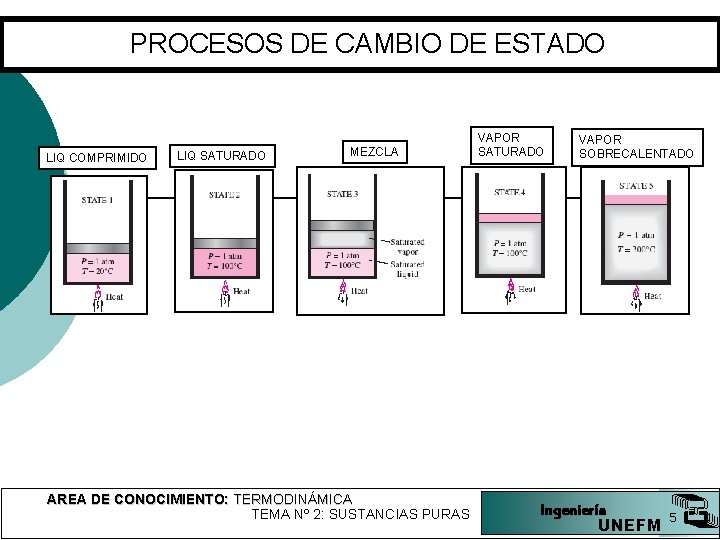
PROCESOS DE CAMBIO DE ESTADO LIQ COMPRIMIDO LIQ SATURADO MEZCLA AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS VAPOR SATURADO VAPOR SOBRECALENTADO Ingeniería UNEFM 5

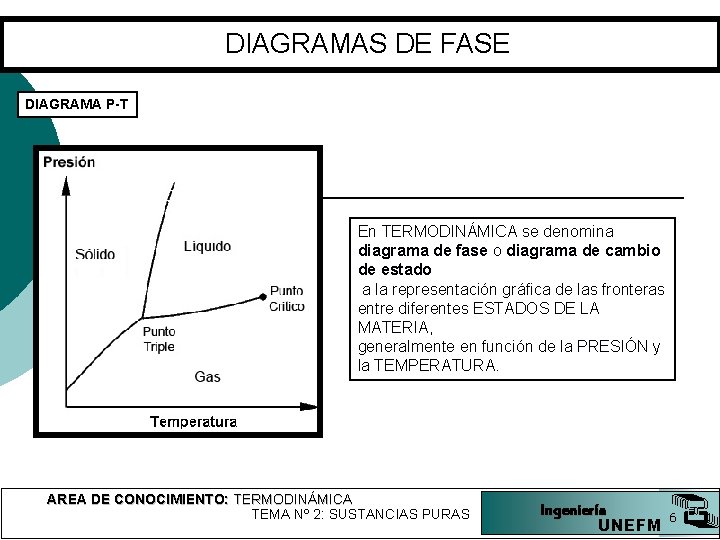
DIAGRAMAS DE FASE DIAGRAMA P-T En TERMODINÁMICA se denomina diagrama de fase o diagrama de cambio de estado a la representación gráfica de las fronteras entre diferentes ESTADOS DE LA MATERIA, generalmente en función de la PRESIÓN y la TEMPERATURA. AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 6

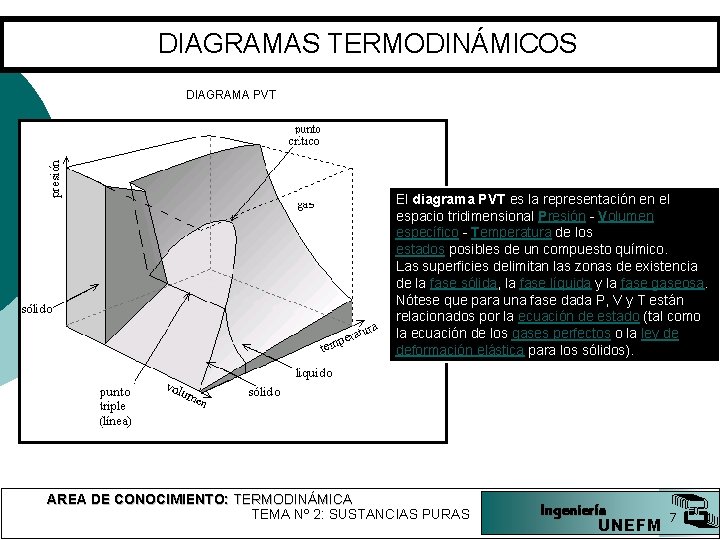
DIAGRAMAS TERMODINÁMICOS DIAGRAMA PVT El diagrama PVT es la representación en el espacio tridimensional Presión - Volumen específico - Temperatura de los estados posibles de un compuesto químico. Las superficies delimitan las zonas de existencia de la fase sólida, la fase líquida y la fase gaseosa. Nótese que para una fase dada P, V y T están relacionados por la ecuación de estado (tal como la ecuación de los gases perfectos o la ley de deformación elástica para los sólidos). AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 7

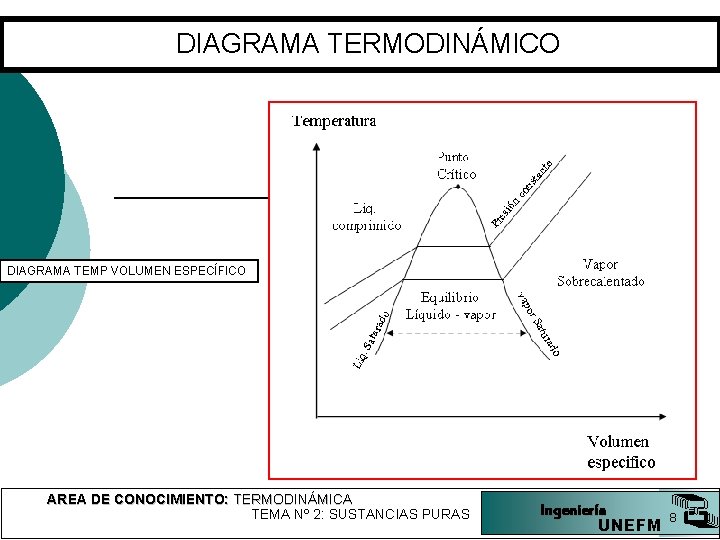
DIAGRAMA TERMODINÁMICO DIAGRAMA TEMP VOLUMEN ESPECÍFICO AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 8

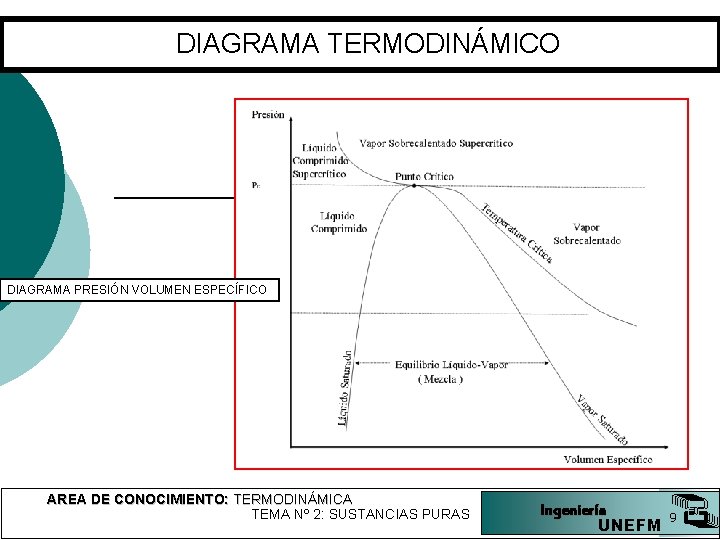
DIAGRAMA TERMODINÁMICO DIAGRAMA PRESIÓN VOLUMEN ESPECÍFICO AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería UNEFM 9

MEZCLA SATURADA LIQUIDO VAPOR Humedad Calculo de propiedades en mezcla. AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería 10 UNEFM

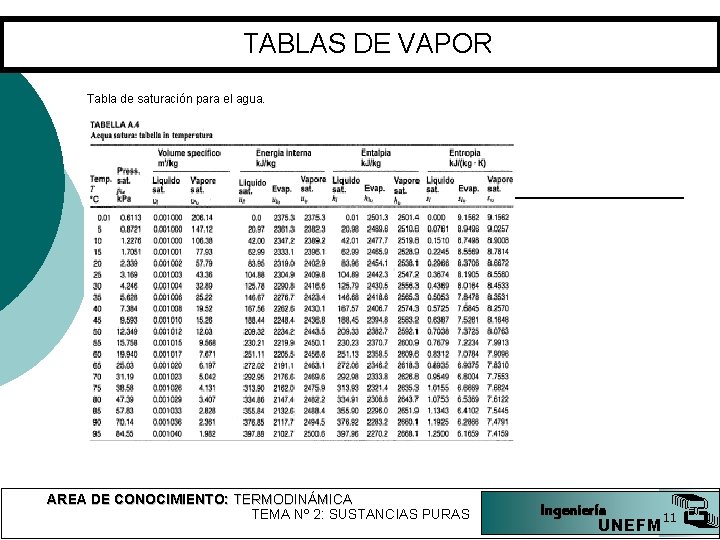
TABLAS DE VAPOR Tabla de saturación para el agua. AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería 11 UNEFM

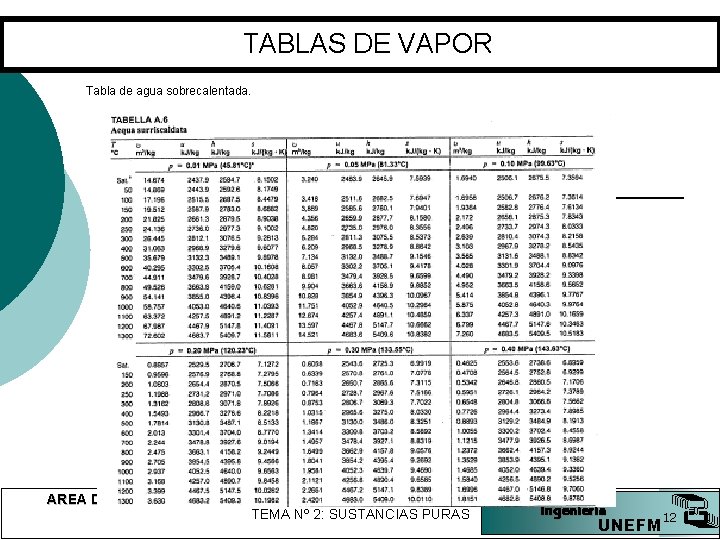
TABLAS DE VAPOR Tabla de agua sobrecalentada. AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería 12 UNEFM

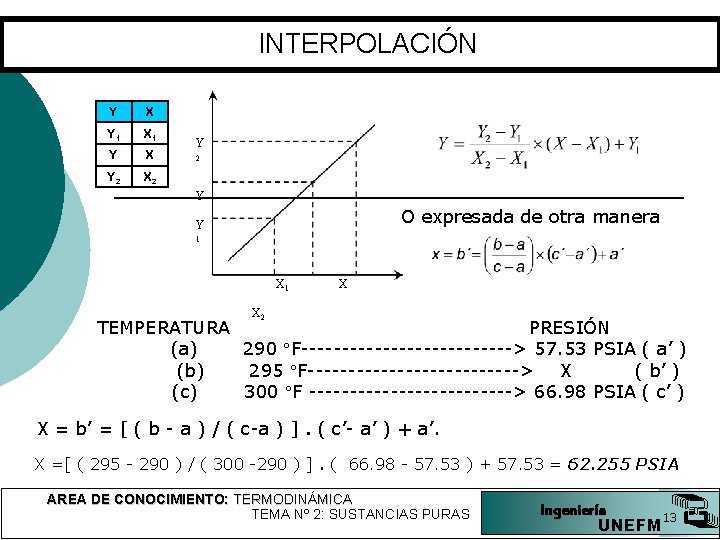
INTERPOLACIÓN Y X Y 1 X 1 Y X Y 2 X 2 Y O expresada de otra manera Y 1 X X 2 TEMPERATURA PRESIÓN (a) 290 F-------------> 57. 53 PSIA ( a’ ) (b) 295 F-------------> X ( b’ ) (c) 300 F -------------> 66. 98 PSIA ( c’ ) X = b’ = [ ( b - a ) / ( c-a ) ]. ( c’- a’ ) + a’. X =[ ( 295 - 290 ) / ( 300 -290 ) ]. ( 66. 98 - 57. 53 ) + 57. 53 = 62. 255 PSIA AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería 13 UNEFM

DETERMINACIÓN DE ESTADO Liquido Comprimido 1) Tsist < Tsat 2) Psist > Psat 3) sist < f 4) hsist< hf 5) usist < uf 6) Ssist < Sf Estados de Saturación 1) sist > f y sist < g f < sist < g (mezcla) 2) hsis > hf y hsist < hg hf < hsist < hg (mezcla) 3) usis > ut y usist < ug uf < usist < ug (mezcla) 4) ssist > sf y ssist < sg sf < ssist < sg (mezcla) 5) Psist = Psat y Tsist=Tsat (Estado de saturación indefinido) 6) Psist = Psat y sist= g (Vapor saturado) 7) Tsist = Tsat y sist = g (Vapor saturado) 8) Psist = Psat y sist = f (Líquido saturado) 9) Tsist = Tsat y sist = f (Líquido saturado) Vapor Sobrecalentado 1) Tsist > Tsat 2) Psist < Psat 3) sist > g 4) hsist > hg 5) usist > ug 6) Ssist > sg AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería 14 UNEFM

DETERMINACIÓN DE ESTADO Determine los datos requeridos del agua para las siguientes condiciones: • La presión y el volumen específico de líquido saturado a 150ºF. • La temperatura y la entalpía del vapor saturado a 80ºF • El volumen específico y la energía interna a 140 psia y 500 ºF • La temperatura y el volumen específico a 100 psia y una calidad de 80 %. • El volumen específico y la entalpía a 100 ºF y 1500 psia. • La presión y la entalpía específica a 300ºF y 70% de calidad. • La temperatura y la energía interna específica a 200 psia y una entalpía de 1268, 8 Btu/lbm • La calidad de un volumen específico a 370 ºF y una entalpía de 770 Btu/Lbm • Energía interna y el volumen específico a 240 ºF y una entalpía de 1160, 7 Btu/Lbm • La presión y la entalpía a 500ºF y una energía interna de 1171, 7 Btu/Lbm • La temperatura y el volumen específico a 2000 psia y una entalpía de 73, 3 Btu/Lbm AREA DE CONOCIMIENTO: TERMODINÁMICA TEMA Nº 2: SUSTANCIAS PURAS Ingeniería 15 UNEFM