Neurosarcoidosi del Sistema Nervoso Centrale Esperienza del Centro






- Slides: 10

Neurosarcoidosi del Sistema Nervoso Centrale Esperienza del Centro di Riferimento Regionale per la Sarcoidosi e altre Interstiziopatie Polmonari Dott. ssa Silvia Bocci Dipartimento di Scienze Mediche, Chirurgiche e Neuroscienze Università degli Studi di Siena

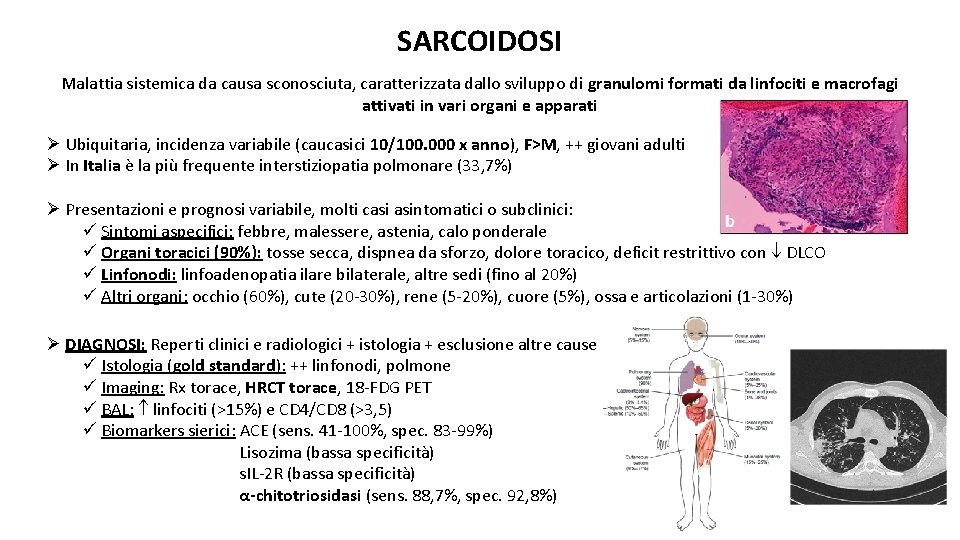
SARCOIDOSI Malattia sistemica da causa sconosciuta, caratterizzata dallo sviluppo di granulomi formati da linfociti e macrofagi attivati in vari organi e apparati Ø Ubiquitaria, incidenza variabile (caucasici 10/100. 000 x anno), F>M, ++ giovani adulti Ø In Italia è la più frequente interstiziopatia polmonare (33, 7%) Ø Presentazioni e prognosi variabile, molti casi asintomatici o subclinici: ü Sintomi aspecifici: febbre, malessere, astenia, calo ponderale ü Organi toracici (90%): tosse secca, dispnea da sforzo, dolore toracico, deficit restrittivo con DLCO ü Linfonodi: linfoadenopatia ilare bilaterale, altre sedi (fino al 20%) ü Altri organi: occhio (60%), cute (20 -30%), rene (5 -20%), cuore (5%), ossa e articolazioni (1 -30%) Ø DIAGNOSI: Reperti clinici e radiologici + istologia + esclusione altre cause ü Istologia (gold standard): ++ linfonodi, polmone ü Imaging: Rx torace, HRCT torace, 18 -FDG PET ü BAL: linfociti (>15%) e CD 4/CD 8 (>3, 5) ü Biomarkers sierici: ACE (sens. 41 -100%, spec. 83 -99%) Lisozima (bassa specificità) s. IL-2 R (bassa specificità) α-chitotriosidasi (sens. 88, 7%, spec. 92, 8%)

NEUROSARCOIDOSI Ø Incidenza: casi sintomatici 3 -16% sarcoidosi studi autoptici 25 -27% sarcoidosi (50% non diagnosticati) Ø Quadro neurologico = esordio patologia in >50% Ø Neurosarcoidosi isolata: 10% neurosarcoidosi, 1% sarcoidosi Ø Non noti fattori predisponenti o scatenanti CLINICA – marcata eterogeneità Ø Ø Ø Ø Nervi cranici: isolati o multipli, VII (1/3 bilat. ), II (>50% bilat. ), VIII, V Meningi: sia pachimeningi che leptomeningi, ++ base cranica, talora idrocefalo Parenchima encefalico: clinica variabile in base a sede Midollo spinale: parenchima ++ cervico-toracico, radici ++ lombosacrali, imaging >> clinica Patologia neuroendocrinologica: ipotalamo/ipofisi (+ leptomeningi), disfunzioni ormonali persistenti Patologia cerebrovascolare: ischemie, emorragie, coinvolgimento seni venosi, meccanismo vasculitico Nervo periferico: poli-multineuropatie assonali > demielinizzanti, SFN (paraneurosarcoidosi) Muscolo: spesso asintomatico, miosite acuta, miopatia cronica, miopatia nodulare

NEUROSARCOIDOSI - DIAGNOSI Zajicek, 1999 (e succ. modifiche) WASOG, 2014 NCCG, 2018 Quadro clinico/radiologico suggestivo + granulomi sarcoidei in SNC + esclusione diagnosi alternative Invasività biopsia sistema nervoso Fino al 40% di falsi negativi 2 obiettivi iter diagnostico: Conferma meccanismo infiammatorio alla base della Ricerca manifestazioni sarcoidee definite a livello patologia neurologica sistemico NEUROIMAGING REPERTI NON SEMPRE SPECIFICI Ø RM encefalo e midollo: reperti vari Comunicazione orale Dott. Chiarotti, Dom. 7 aprile 10. 30 -11. 30, Sala Regina ANALISI DEL LIQUOR REPERTI NON SEMPRE SPECIFICI Ø Pattern infiammatorio: prot. , cell. (L), talora gluc. , BO (19 -40%), Link (40%); possibile negatività Ø Biomarkers liquorali: tipizzazione linfocitaria (CD 4+/CD 8+>5), ACE, s. IL-R 2; attendibilità?

LA CASISTICA DI SIENA U. O. C. Neurologia e Neurofisiologia Clinica U. O. C. Clinica Neurologica e Malattie Neurometaboliche U. O. C. Malattie Respiratorie e Trapianto Polmonare U. O. C. Neuroimmagini e Neurointerventistica Centro di Riferimento Regionale per la Sarcoidosi e altre Interstiziopatie Polmonari Neuroradiologia Diagnostica Avanzata FONTE DEI CASI (studio retrospettivo, 15 anni) Ø Pazienti con diagnosi di sarcoidosi inviati in consulenza neurologica Ø Pazienti primariamente afferenti alle U. O. neurologiche e successivamente diagnosticati con sarcoidosi Ø Pazienti affetti da sarcoidosi con complicanze neuroendocrinologiche, sottoposti a esami neuroradiologici diagnostici e di follow-up INCLUSIONE Ø Grado di certezza diagnostica possibile o superiore in almeno uno dei set di criteri (Zajicek, 1999 e succ. modifiche; WASOG, 2014; NCCG, 2018) ESCLUSIONE Ø Pazienti con sarcoidosi neuromuscolare non inclusi in questo studio

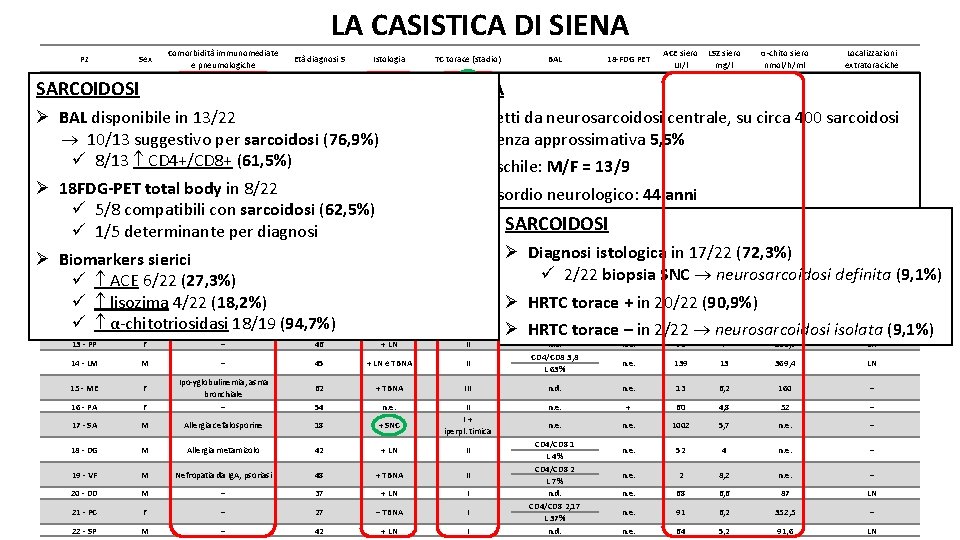
LA CASISTICA DI SIENA Pz Sex Comorbidità immunomediate e pneumologiche Età diagnosi S 1 - DA M Allergia ASA e β-lattamici 62 SARCOIDOSI 2 - GP M – 37 Istologia TC torace (stadio) + SNC 0 EPIDEMIOLOGIA + LN II BAL 18 -FDG PET ACE siero UI/l LSZ siero mg/l α-chito siero nmol/h/ml Localizzazioni extratoraciche n. e. 33 3, 9 109 – n. e. 67 4, 1 275, 3 – n. e. 91 7 268, 9 LN n. e. 139 13 369, 4 LN CD 4/CD 8 6, 2 L 23% CD 4/CD 8 1, 95 L 30% CD 4/CD 8 3, 58 L 34% CD 4/CD 8 3, 98 L 46, 5% n. e. CD 4/CD 8 2, 35 L 5% CD 4/CD 8 3, 55 L 2% CD 4/CD 8 8, 6 L 53% CD 4/CD 8 2, 53 L 40% n. d. CD 4/CD 8 3, 04 L 15% n. e. CD 4/CD 8 3, 8 L 63% Ø BAL disponibile in 13/22 Øn. e. 22 pazienti III + affetti da neurosarcoidosi centrale, su circa 400 sarcoidosi 3 - TG M Pregressa GBS, asbestosi 53 – 64 4, 8 133 – asbestosi 10/13 suggestivo per sarcoidosi (76, 9%) incidenza approssimativa 5, 5% 4 - SD M – 31 n. e. 0 – 59 3, 8 60 – ü 8/13 CD 4+/CD 8+ (61, 5%) Ø+ TBNA Prevalenza. III maschile: M/F = 13/9 n. e. 5 - MV F – 16 63 4, 4 64 – Ø 18 FDG-PET 6 - GM Ftotal body–in 8/22 45 + 44 anni 48 11 98 LN, ossa Ø+ LNEtà media IIall’esordio neurologico: ü con sarcoidosi 46(62, 5%)+ orb e rene 7 - SM 5/8 compatibili F – II + 72 3, 3 260 Rene, orbita Ø Comorbidità immunologiche in 9/22 (40, 9%) SARCOIDOSI SM, allergia cefalosporine, ü 1/5 determinante per diagnosi 56 8 - CL F + LN II + 4 7 43, 3 LN asma bronchiale ü Allergiche (farmaci, asma, oculorinite) Ø Diagnosi istologica in 17/22 (72, 3%) Ø Biomarkers 9 - VC F sierici Sindrome di Sjögren 51 n. e. ü Immunomediate II n. e. 107 6, 3 303, 2 – (GBS) ü 2/22 biopsia SNC neurosarcoidosi definita (9, 1%) ü ACE M 6/22 (27, 3%) 10 - SP Oculorinite allergica 43 + TBNAü Autoimmuni II + 68 11 96, 5 – (SM, Sjögren, Berger, psoriasi) Ø HRTC torace +– in 20/22 (90, 9%) ü lisozima 4/22 (18, 2%) 11 - MG M – 30 + TBNA II 43 6 99 – 12 M – 18/19 (94, 7%) 53 + pleura II 99 7, 3 155 Cute ü- AM α-chitotriosidasi Ø HRTC torace n. e. – in 2/22 neurosarcoidosi isolata (9, 1%) 13 - PP F – 46 + LN II 14 - LM M – 45 + LN e TBNA II 15 - ME F 62 + TBNA III n. d. n. e. 13 6, 2 160 – 16 - PA F Ipo-γglobulinemia, asma bronchiale – 54 n. e. + 60 4, 8 52 – 17 - SA M Allergia cefalosporine 18 + SNC II I+ iperpl. timica n. e. 1002 5, 7 n. e. – 18 - DG M Allergia metamizolo 42 + LN II n. e. 52 4 n. e. – 19 - VF M Nefropatia da Ig. A, psoriasi 48 + TBNA II n. e. 2 8, 2 n. e. – 20 - DD M – 37 + LN I n. e. 68 6, 6 87 LN 21 - PC F – 27 – TBNA I n. e. 91 6, 2 352, 5 – 22 - SP M – 42 + LN I n. e. 64 5, 2 91, 6 LN CD 4/CD 8 1 L 4% CD 4/CD 8 2 L 7% n. d. CD 4/CD 8 2, 17 L 37% n. d.

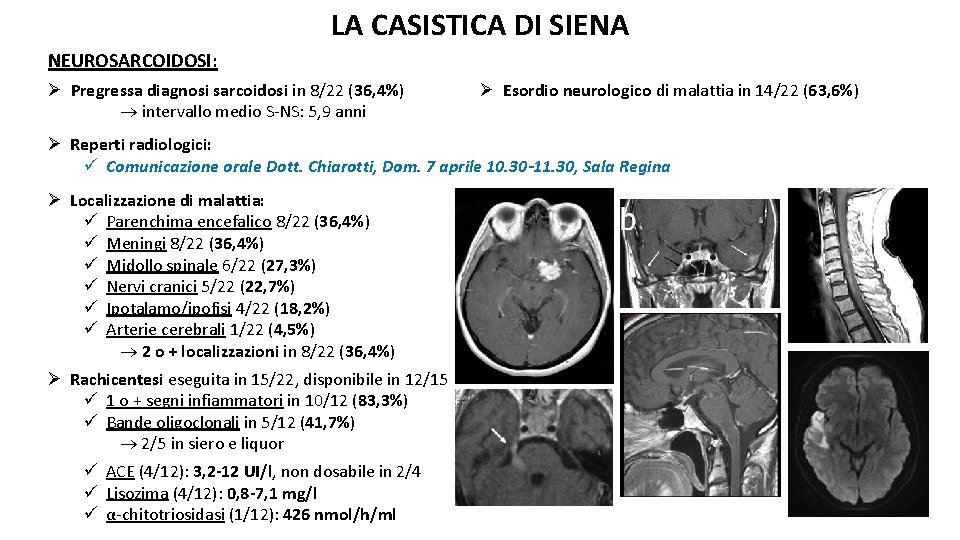
LA CASISTICA DI SIENA NEUROSARCOIDOSI: Ø Pregressa diagnosi sarcoidosi in 8/22 (36, 4%) intervallo medio S-NS: 5, 9 anni Ø Esordio neurologico di malattia in 14/22 (63, 6%) Ø Reperti radiologici: ü Comunicazione orale Dott. Chiarotti, Dom. 7 aprile 10. 30 -11. 30, Sala Regina Ø Localizzazione di malattia: ü Parenchima encefalico 8/22 (36, 4%) ü Meningi 8/22 (36, 4%) ü Midollo spinale 6/22 (27, 3%) ü Nervi cranici 5/22 (22, 7%) ü Ipotalamo/ipofisi 4/22 (18, 2%) ü Arterie cerebrali 1/22 (4, 5%) 2 o + localizzazioni in 8/22 (36, 4%) Ø Rachicentesi eseguita in 15/22, disponibile in 12/15 ü 1 o + segni infiammatori in 10/12 (83, 3%) ü Bande oligoclonali in 5/12 (41, 7%) 2/5 in siero e liquor ü ACE (4/12): 3, 2 -12 UI/l, non dosabile in 2/4 ü Lisozima (4/12): 0, 8 -7, 1 mg/l ü α-chitotriosidasi (1/12): 426 nmol/h/ml

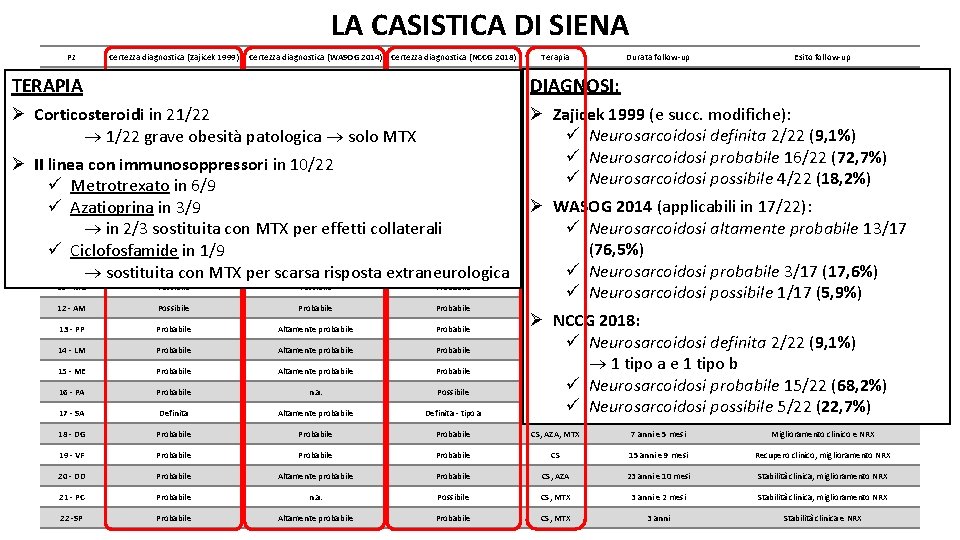
LA CASISTICA DI SIENA Pz Certezza diagnostica (Zajicek 1999) Terapia Durata follow-up Esito follow-up 1 - DA Definita Altamente probabile Definita - tipo b CS, MTX 3 anni e 1 mese Miglioramento clinico e NRX, complicanze CS Probabile Altamente probabile Probabile CS, MTX 2 anni e 1 mese Recupero clinico, miglioramento NRX 11 - MG Possibile Probabile 12 - AM Possibile Probabile 13 - PP Probabile Altamente probabile Probabile 14 - LM Probabile Altamente probabile Probabile 15 - ME Probabile Altamente probabile Probabile 16 - PA Probabile n. a. Possibile 17 - SA Definita Altamente probabile Definita - tipo a 18 - DG Probabile CS, AZA, MTX 7 anni e 5 mesi Miglioramento clinico e NRX 19 - VF Probabile CS 15 anni e 9 mesi Recupero clinico, miglioramento NRX 20 - DD Probabile Altamente probabile Probabile CS, AZA 23 anni e 10 mesi Stabilità clinica, miglioramento NRX 21 - PC Probabile n. a. Possibile CS, MTX 3 anni e 2 mesi Stabilità clinica, miglioramento NRX 22 -SP Probabile Altamente probabile Probabile CS, MTX 3 anni Stabilità clinica e NRX TERAPIA 2 - GP Certezza diagnostica (WASOG 2014) Certezza diagnostica (NCCG 2018) Ø Corticosteroidi in. Possibile 21/22 3 - TG n. a. Possibile 4 - SD 1/22 grave Possibileobesità patologica n. a. solo MTX Possibile 5 - MV Probabile probabile Probabile Ø II linea con immunosoppressori in. Altamente 10/22 GM Probabile Altamente probabile Probabile ü 6 - Metrotrexato in 6/9 SM Probabile Altamente probabile Probabile ü 7 - Azatioprina in 3/9 8 - CL Probabile Altamente probabile in 2/3 sostituita con MTX per effetti collaterali. Probabile VC Probabile n. a. Possibile ü 9 -Ciclofosfamide in 1/9 10 - SP Probabile sostituita con MTX per scarsa risposta extraneurologica DIAGNOSI: Ø CSZajicek 1999 modifiche): 2 anni(e e 8 succ. mesi Recupero clinico, miglioramento NRX definita 2/22 (9, 1%) CS ü Neurosarcoidosi 8 mesi Recupero clinico, miglioramento NRX probabile Recupero 16/22 (72, 7%) CS ü Neurosarcoidosi 7 anni clinico e NRX possibile 4/22 CS ü Neurosarcoidosi 1 anno e 2 mesi Recupero clinico, (18, 2%) miglioramento NRX Miglioramento clinico e NRX, complicanze CS Ø CSWASOG 20141 anno (applicabili in 17/22): CS 1 anno e 4 mesi Miglioramento clinico e NRX, complicanze CS ü Neurosarcoidosi altamente probabile 13/17 CS, CYC, MTX 4 anni e 10 mesi Stabilità clinica e NRX (76, 5%) MTX 1 anno e 3 mesi Miglioramento clinico, stabilità NRX ü Neurosarcoidosi probabile 3/17 (17, 6%) CS 8 mesi Recupero clinico e NRX ü Neurosarcoidosi possibile 1/17 (5, 9%) CS, MTX 1 anno Recupero clinico, stabilità NRX Ø CSNCCG 2018: 5 anni e 2 mesi Miglioramento clinico, recupero NRX ü Neurosarcoidosi definita 2/22 (9, 1%) CS, MTX 7 anni e 1 mese Stabilità clinica, recupero NRX, complicanze CS 1 tipo a e 1 tipo b CS 8 anni e 5 mesi Miglioramento clinico e NRX ü Neurosarcoidosi probabile CS, AZA, MTX 3 anni e 10 mesi Stabilità 15/22 clinica e NRX, (68, 2%) complicanze CS possibile 5/22 (22, 7%) CS ü Neurosarcoidosi n. d.

CONCLUSIONI CRITERI DIAGNOSTICI PRO: ü No limiti a possibili presentazioni cliniche ü Focus su obiettivi iter diagnostico: conferma meccanismo infiammatorio della patologia neurologica ricerca manifestazioni sarcoidee a livello sistemico CONTRO: ü Stretta dipendenza dalla conferma istologica invasività biopsia SNC per diagnosi definita biopsia altri organi non sempre eseguita nella pratica clinica ü Reperti NRX e liquorali spesso non specifici rachicentesi non sempre eseguita (presentazioni lievi, quadri neuroendocrinologici) ü Assenza di alcuni biomarkes sierici s. IL-R 2, α-chitotriosidasi ü Neurosarcoidosi isolata se assenti manifestazioni extraneurologiche criteri non applicabili (se biopsia SNC non praticabile) ü Diagnosi differenziali Nessuna indicazione in criteri: «esclusione possibili cause alternative» Localizzazioni linfomatose, SM

CONCLUSIONI NEUROSARCOIDOSI ISOLATA O DI ESORDIO (>50%) sfida diagnostica per neurologo (+++ se biopsia SNC impraticabile) Ø RUOLO BIOMARKERS LIQUORALI ü Necessari ulteriori studi: α-chitotriosidasi cut-off normalità sensibilità/specificità vs soggetti sani e patologie in DD Ø RUOLO RISPOSTA TERAPEUTICA ü Pattern tipico risposta clinica e radiologica criterio ex-juvantibus TERAPIA E FOLLOW-UP Ø Classi farmaceutiche = sarcoidosi sistemica Ø Dosaggi e durate > sarcoidosi sistemica gestione del paziente condivisa tra specialisti neurologo e pneumologo di riferimento