ENZIMAS CATALIZADORES BIOLGICOS QUE Velocidades de reaccin 106

ENZIMAS CATALIZADORES BIOLÓGICOS QUE: Velocidades de reacción 106 -1012 > que las reacciones no catalizadas y varios órdenes de magnitud más que la catálsis química. Requieren condiciones de reacción “suaves”: <100°C, P atm, p. H neutro ESPECIFICIDAD: no hay productos “secundarios” Mecanismos de regulación: Alosterismo, modificación covalente, cantidad de enzima
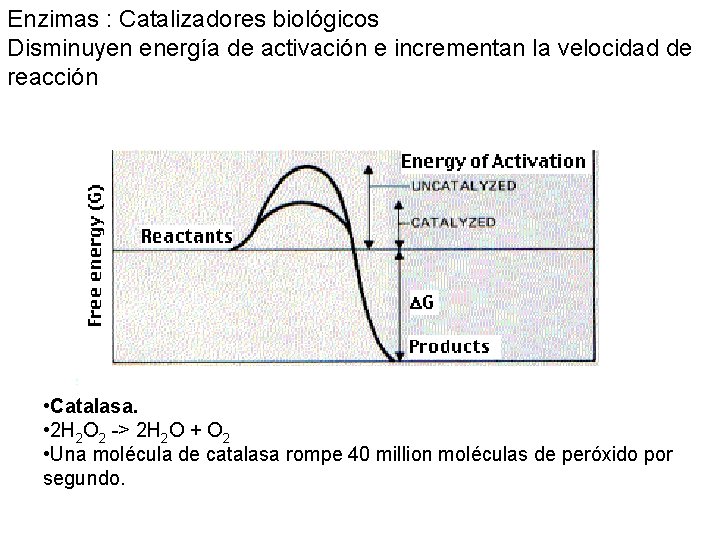
Enzimas : Catalizadores biológicos Disminuyen energía de activación e incrementan la velocidad de reacción • Catalasa. • 2 H 2 O 2 -> 2 H 2 O + O 2 • Una molécula de catalasa rompe 40 million moléculas de peróxido por segundo.
![Factores que influyen en la actividad enzimática • Concentración de sustrato [S] • Temperatura Factores que influyen en la actividad enzimática • Concentración de sustrato [S] • Temperatura](http://slidetodoc.com/presentation_image_h/2eb47801edf23cd8a10e9d1306848bd7/image-3.jpg)
Factores que influyen en la actividad enzimática • Concentración de sustrato [S] • Temperatura • Inhibidores • Competitivos: unen mismo sitio de l sustrato • No competitivos: unen sitio diferente pero disminuyen capacidad catalítica • p. H. Afecta conformación
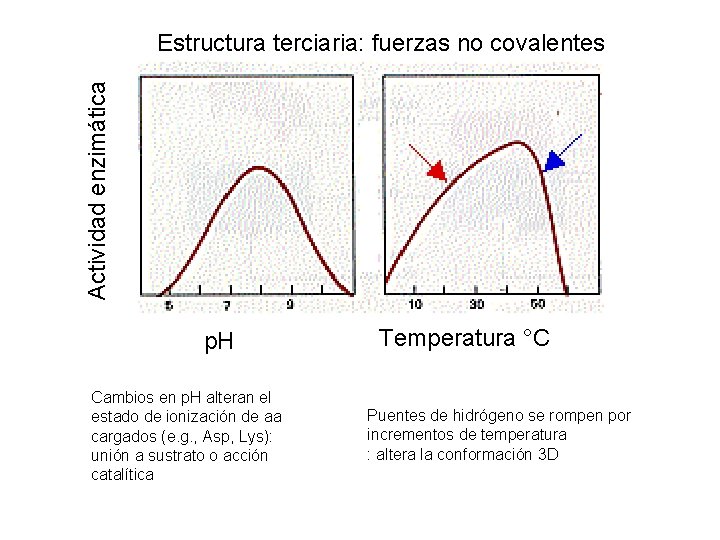
Actividad enzimática Estructura terciaria: fuerzas no covalentes p. H Cambios en p. H alteran el estado de ionización de aa cargados (e. g. , Asp, Lys): unión a sustrato o acción catalítica Temperatura °C Puentes de hidrógeno se rompen por incrementos de temperatura : altera la conformación 3 D
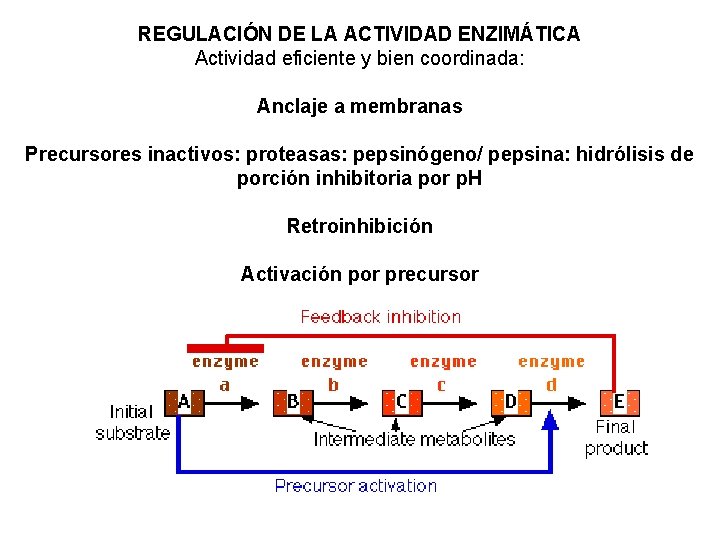
REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Actividad eficiente y bien coordinada: Anclaje a membranas Precursores inactivos: proteasas: pepsinógeno/ pepsina: hidrólisis de porción inhibitoria por p. H Retroinhibición Activación por precursor
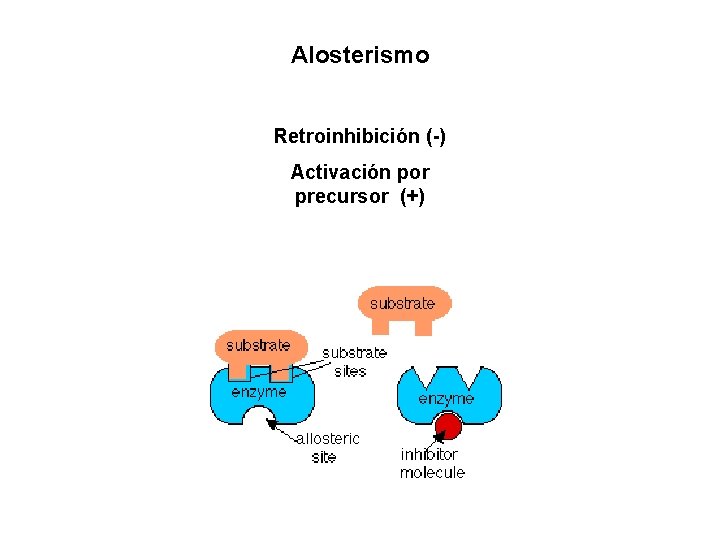
Alosterismo Retroinhibición (-) Activación por precursor (+)

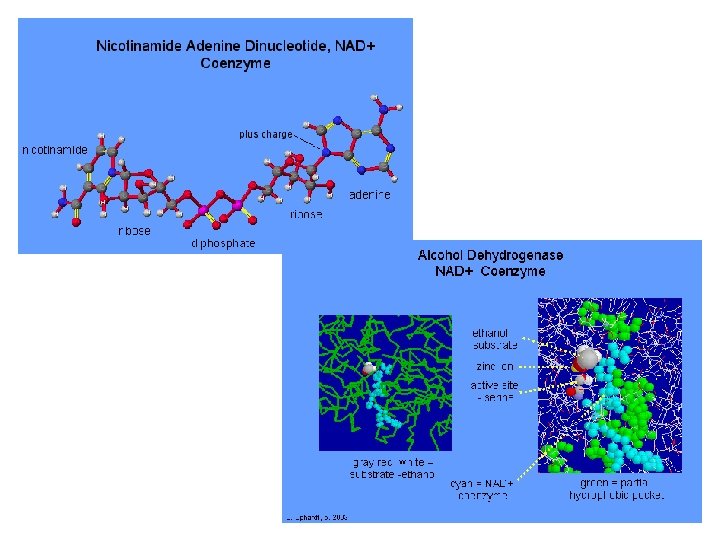
COFACTORES ENZIMÁTICOS NO PROTÉICOS Pueden ser: • Iones metálicos : Zn 2+, Cu 2+, Mn 2+, K+, Na+ , Ca+2 • Moléculas orgánicas pequeñas: coenzimas. • tiamina (B 1) Tiaminpirofosfato (transf. Aldehído) • riboflavina (B 2) FAD (transf. H+) Nicotinamida NAD (transf. H+) • Co. A Acarrea acilo Coenzimas se unen covalentemente a la apoenzima: Grupo prostético Otras sólo transitoriamente durante la catálisis

- Slides: 9