ENZIMAS CATALIZADORES BIOLGICOS QUE Velocidades de reaccin 106

ENZIMAS CATALIZADORES BIOLÓGICOS QUE: Velocidades de reacción 106 -1012 > que las reacciones no catalizadas y varios órdenes de magnitud más que la catálsis química. Requieren condiciones de reacción “suaves”: <100°C, P atm, p. H (+/-) neutro ESPECIFICIDAD: no hay productos “secundarios” Mecanismos de regulación: Alosterismo, modificación covalente, cantidad de enzima
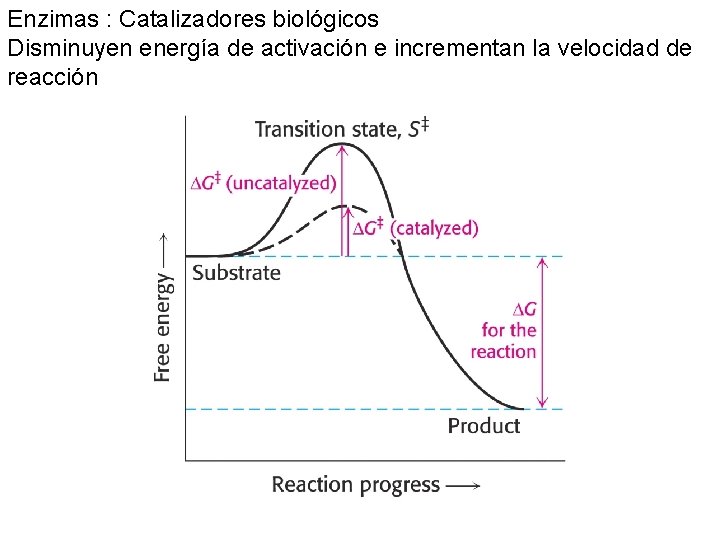
Enzimas : Catalizadores biológicos Disminuyen energía de activación e incrementan la velocidad de reacción

• Catalasa. • 2 H 2 O 2 -> 2 H 2 O + O 2 • Una molécula de catalasa rompe 40 millones moléculas de peróxido por segundo.
![Factores que influyen en la actividad enzimática • Concentración de sustrato [S] • Temperatura Factores que influyen en la actividad enzimática • Concentración de sustrato [S] • Temperatura](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-4.jpg)
Factores que influyen en la actividad enzimática • Concentración de sustrato [S] • Temperatura • Inhibidores • Competitivos: unen mismo sitio de l sustrato • No competitivos: unen sitio diferente pero disminuyen capacidad catalítica • p. H. Afecta conformación
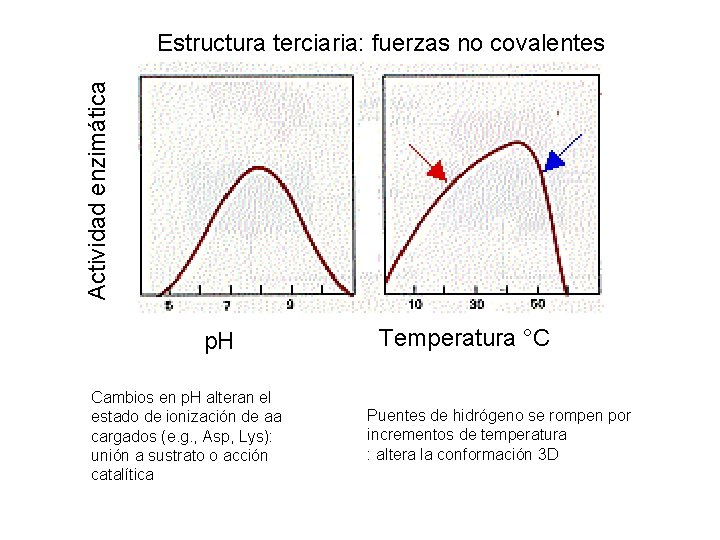
Actividad enzimática Estructura terciaria: fuerzas no covalentes p. H Cambios en p. H alteran el estado de ionización de aa cargados (e. g. , Asp, Lys): unión a sustrato o acción catalítica Temperatura °C Puentes de hidrógeno se rompen por incrementos de temperatura : altera la conformación 3 D
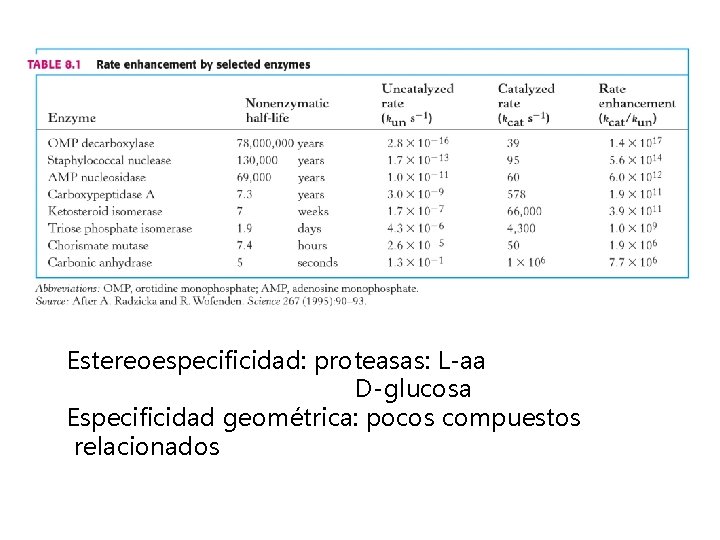
Estereoespecificidad: proteasas: L-aa D-glucosa Especificidad geométrica: pocos compuestos relacionados

PRINCIPALES REACCIONES DE LAS ENZIMAS

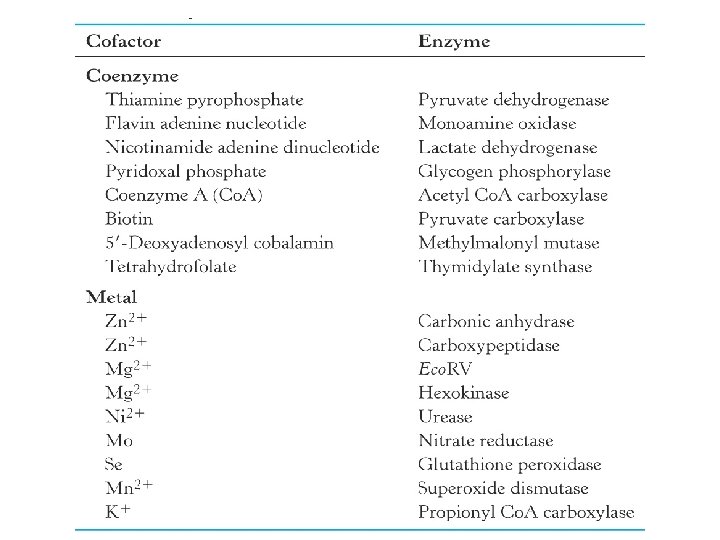
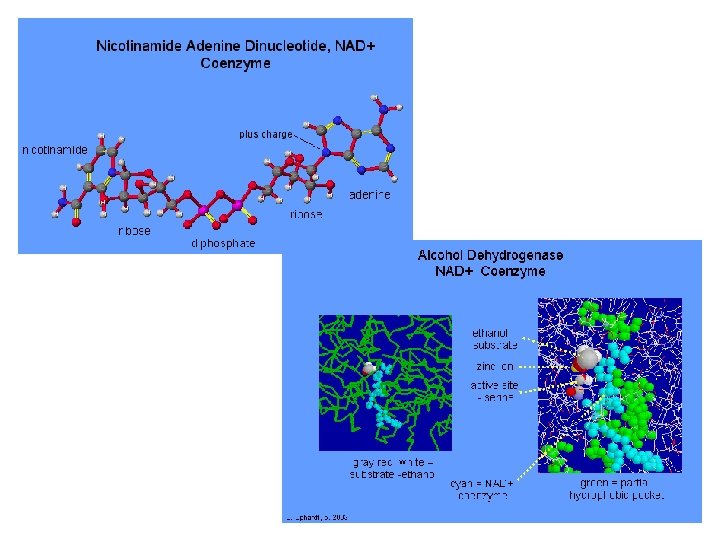

CINÉTICA ENZIMÁTICA Estudio de las velocidades a las que ocurren las reacciones Permite dilucidar Mecanismos de reacción Se pueden conocer: Afinidades de unión a sustratos e inhibidores Máxima velocidad catalítica Mecanismo catalítico Papel de una enzima en la vía Velocidad a cantidad de enzima: condiciones de Medición de las enzimas para BQ y Análisis clínicos
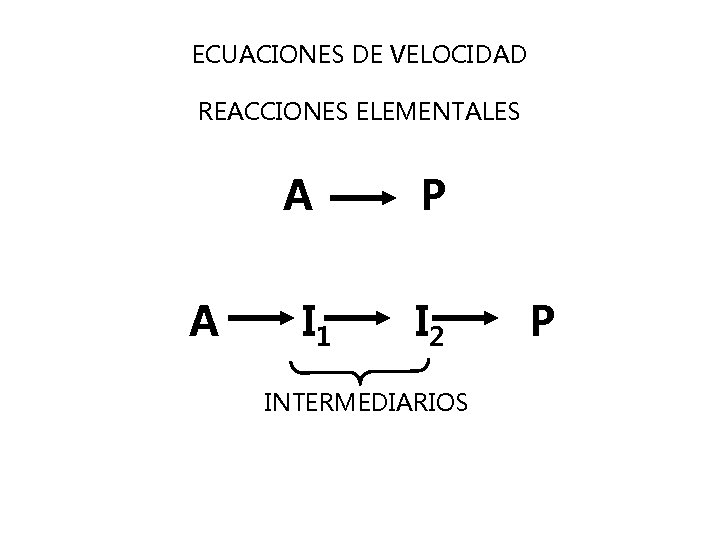
ECUACIONES DE VELOCIDAD REACCIONES ELEMENTALES A A I 1 P I 2 INTERMEDIARIOS P

A TEMPERATURA CONSTANTE: LA VELOCIDAD DE REACCIÓN VARÍA CON LA CONCENTRACIÓN DE LOS REACTIVOS a. A + b. B + c. C +. . . + n. N P La velocidad es proporcional a la frecuencia de Choques simultáneos entre los reactivos Velocidad = K[A]a [B]b [C]c. . . [N]n Cte. Proporcionalidad Cte. De velocidad
![ORDEN DE LA REACCIÓN S EXPONENTES DE LA EC. DE VELOCIDAD Velocidad = K[A]a ORDEN DE LA REACCIÓN S EXPONENTES DE LA EC. DE VELOCIDAD Velocidad = K[A]a](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-14.jpg)
ORDEN DE LA REACCIÓN S EXPONENTES DE LA EC. DE VELOCIDAD Velocidad = K[A]a [B]b [C]c. . . [N]n (a+b+c. . . +n) Para A P Orden = molecularidad= #moléculas que deben chocar simultáneamente Reacción de primer orden Unimolecular
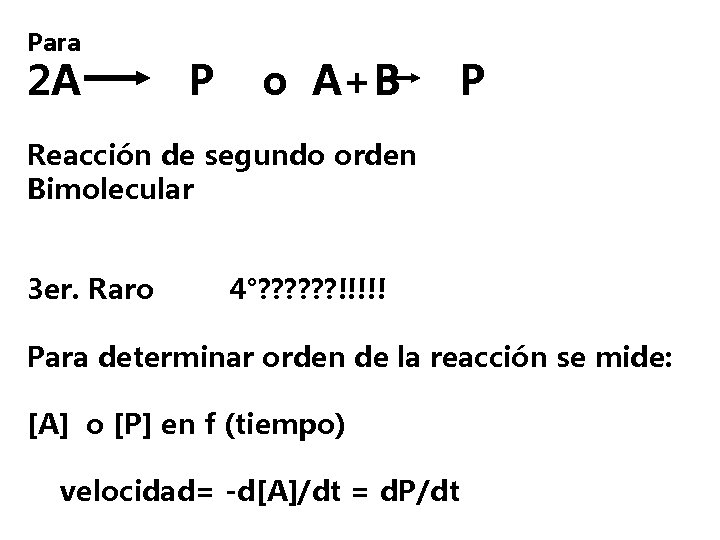
Para 2 A P o A+B P Reacción de segundo orden Bimolecular 3 er. Raro 4°? ? ? !!!!! Para determinar orden de la reacción se mide: [A] o [P] en f (tiempo) velocidad= -d[A]/dt = d. P/dt

ECUACIÓN DE MICHAELIS- MENTEN 1902: ADRIAN BROWN : SACAROSA + H 2 O GLUCOSA+ FRUCTOSA INVERTASA CUANDO SACAROSA>>>ENZIMA REACCIÓN INDEPENDIENTE DE SACAROSA: ORDEN CERO E + S k 1 k-1 ES k 2 P COMPLEJO ENZIMA-SUSTRATO + E
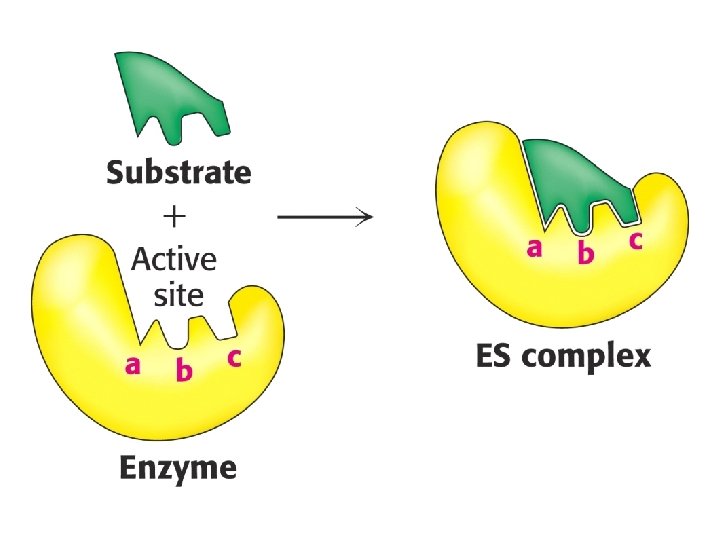
![E + S k 1 k-1 ES Cuando [S] es suficientemente alta para que E + S k 1 k-1 ES Cuando [S] es suficientemente alta para que](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-18.jpg)
E + S k 1 k-1 ES Cuando [S] es suficientemente alta para que toda E k 2 P + Se vuelve el paso limitante Insensible a más adición de [S] V= d[P]/ dt= k 2[ES] d[ES]/dt= k 1[E][S]-k-1[ES]-k 2[ES] No es integrable!!!!! E
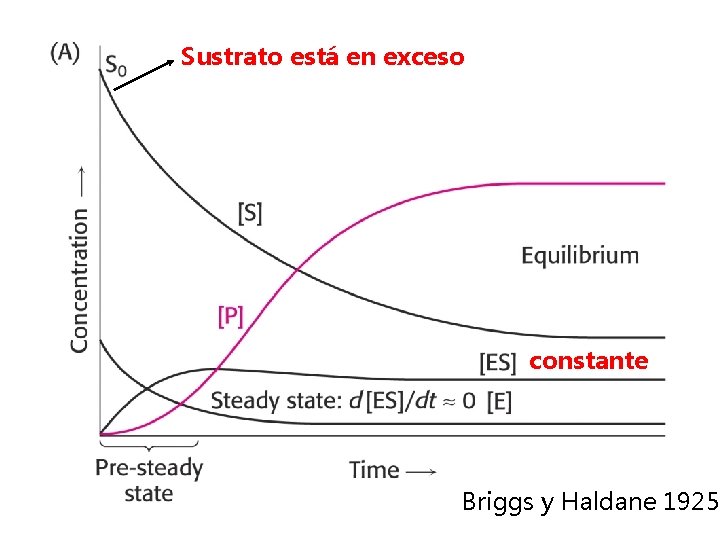
Sustrato está en exceso constante Briggs y Haldane 1925
![V= d[P]/ dt= k 2[ES] d[ES]/dt= k 1[E][S]-k-1[ES]-k 2[ES] d[ES]/dt=0 edo estacionario y [E] V= d[P]/ dt= k 2[ES] d[ES]/dt= k 1[E][S]-k-1[ES]-k 2[ES] d[ES]/dt=0 edo estacionario y [E]](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-20.jpg)
V= d[P]/ dt= k 2[ES] d[ES]/dt= k 1[E][S]-k-1[ES]-k 2[ES] d[ES]/dt=0 edo estacionario y [E] T= [E] +[ES] No medibles [ES]= [E]T[S] / KM + [S] Donde KM = (k-1 + k 2)/ k 1= cte. de Michaelis Entonces: Vo= (d[P]/dt)t=0 = k 2[ES]= k 2 [E]T [S] / KM + [S] medibles

¿Porqué considerar únicamente tiempos iniciales? Vo: minimiza efectos de reversibilidad inhibición por producto inactivación enzimática Vmax: ocurre a alta [S]: enzima está saturada: [ES] 0 [E]T=[E]+[ES] Vo=k 2[ES] Vmax= k 2[E]T
![Si Vo= k 2 [E]T [S] / KM + [S] y Vmax= k 2[E]T Si Vo= k 2 [E]T [S] / KM + [S] y Vmax= k 2[E]T](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-22.jpg)
Si Vo= k 2 [E]T [S] / KM + [S] y Vmax= k 2[E]T Vo= Vmax [S] / KM + [S] ECUACIÓN DE MICHAELIS-MENTEN
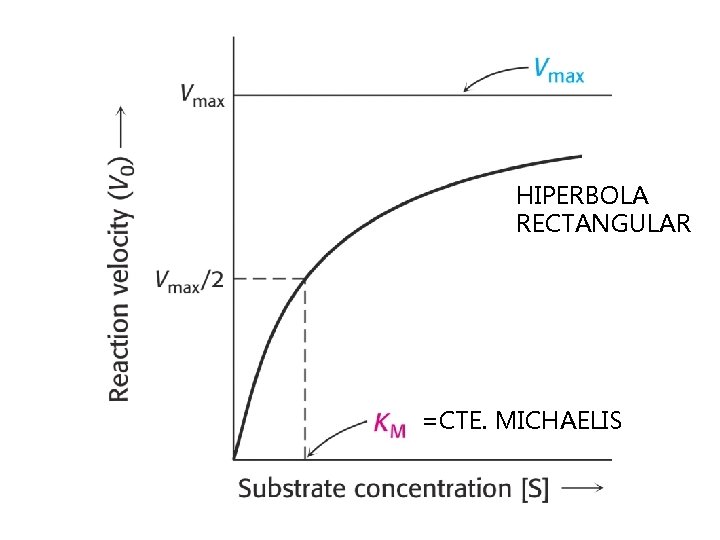
HIPERBOLA RECTANGULAR =CTE. MICHAELIS
![Cuando [S]=KM Vo= Vmax / 2 KM = [S] a la que la velocidad Cuando [S]=KM Vo= Vmax / 2 KM = [S] a la que la velocidad](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-24.jpg)
Cuando [S]=KM Vo= Vmax / 2 KM = [S] a la que la velocidad de reacción Es la mitad de la velocidad máxima
![KM = [S] a la que la velocidad de reacción Es la mitad de KM = [S] a la que la velocidad de reacción Es la mitad de](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-25.jpg)
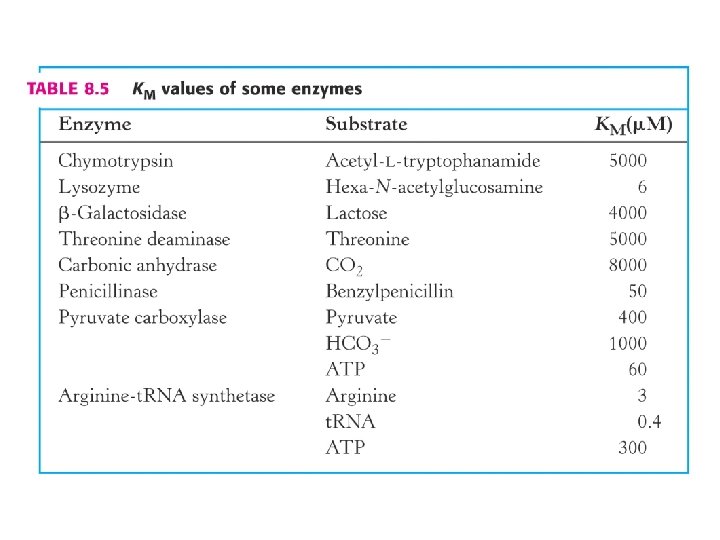
KM = [S] a la que la velocidad de reacción Es la mitad de la velocidad máxima Si KM es pequeña: requiero poco sustrato para alcanzar la mitad de Vmax: Se logra máxima eficiencia catalítica a baja [S] KM depende de cada enzima sustrato temperatura y p. H
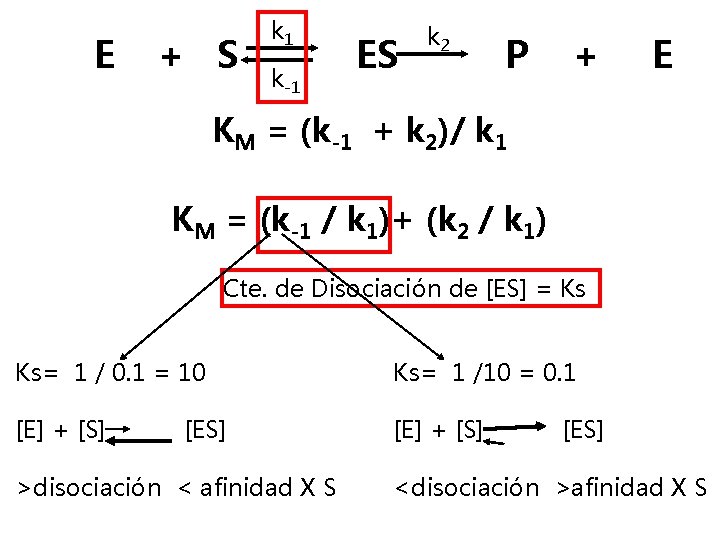
E + S k 1 k-1 ES k 2 P + E KM = (k-1 + k 2)/ k 1 KM = (k-1 / k 1)+ (k 2 / k 1) Cte. de Disociación de [ES] = Ks Ks= 1 / 0. 1 = 10 Ks= 1 /10 = 0. 1 [E] + [S] [ES] >disociación < afinidad X S [ES] <disociación >afinidad X S

KM = (k-1 + k 2)/ k 1 KM = Ks +(k 2 / k 1) Si es pequeño predomina Ks KM es una medida de afinidad
![Cálculo de parámetros Poco preciso Lineweaver-Burk Ec. Doble recíprocos Vo= Vmax [S] / KM Cálculo de parámetros Poco preciso Lineweaver-Burk Ec. Doble recíprocos Vo= Vmax [S] / KM](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-29.jpg)
Cálculo de parámetros Poco preciso Lineweaver-Burk Ec. Doble recíprocos Vo= Vmax [S] / KM + [S] 1 KM 1 1 Vo= Vmax [S] + Vmax ECUACIÓN DE MICHAELIS- ECUACIÓN DE Lineweaver. MENTEN Burk
![1 KM 1 1 Vo= Vmax [S] + Vmax Y= m x + b 1 KM 1 1 Vo= Vmax [S] + Vmax Y= m x + b](http://slidetodoc.com/presentation_image_h/e0997ab48d62ce71a1ec1da3af45ab76/image-30.jpg)
1 KM 1 1 Vo= Vmax [S] + Vmax Y= m x + b =m =b
- Slides: 30