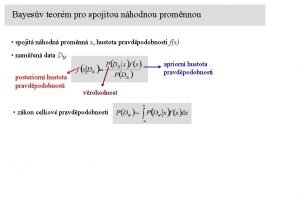
Molekulov fyzika Vnitn energie plynu ekvipartin teorm Kinetick











- Slides: 16

Molekulová fyzika Vnitřní energie plynu, ekvipartiční teorém

Kinetická energie částic v jednom molu ideálního plynu 1 molekula 1 stupeň volnosti Na každý stupeň volnosti neuspořádaného postupného pohybu molekul plynu, který je ve stavu termodynamické rovnováhy, připadá stejně velká, na druhu plynu nezávislá, střední kinetická energie rovná k. BT/2. → EKVIPARTIČNÍ TEORÉM PRO JEDNOATOMOVÝ PLYN

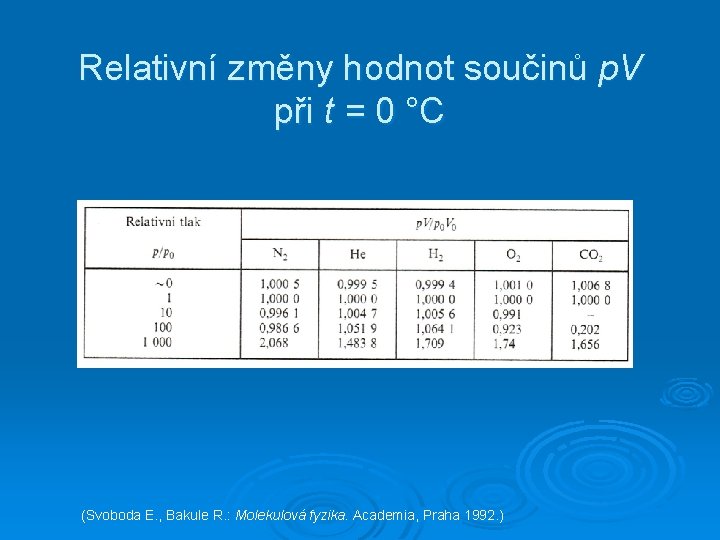
Relativní změny hodnot součinů p. V při t = 0 °C (Svoboda E. , Bakule R. : Molekulová fyzika. Academia, Praha 1992. )

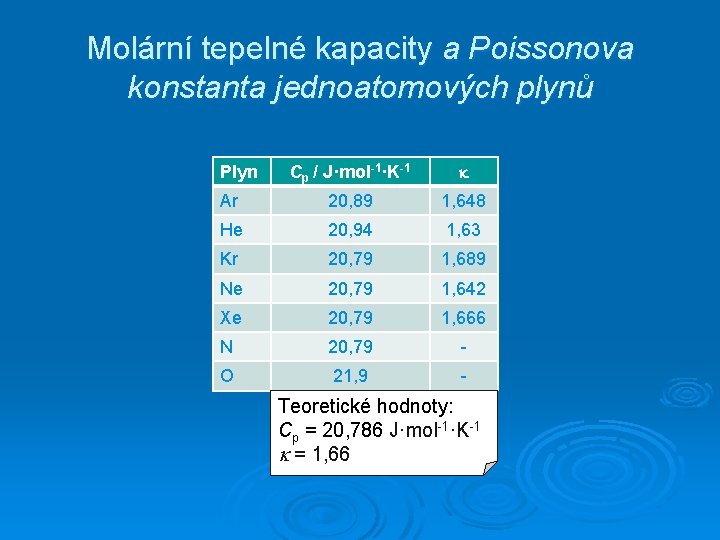
Molární tepelné kapacity a Poissonova konstanta jednoatomových plynů Cp / J·mol-1·K-1 Ar 20, 89 1, 648 He 20, 94 1, 63 Kr 20, 79 1, 689 Ne 20, 79 1, 642 Xe 20, 79 1, 666 N 20, 79 - O 21, 9 - Plyn Teoretické hodnoty: Cp = 20, 786 J·mol-1·K-1 = 1, 66

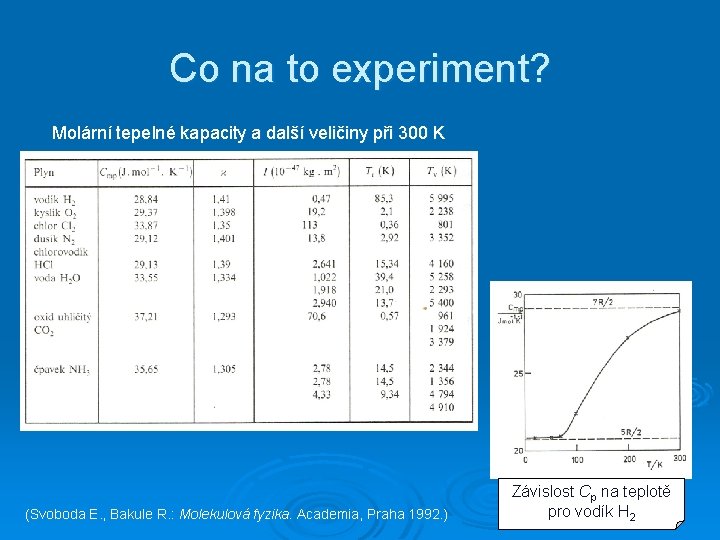
Co na to experiment? Molární tepelné kapacity a další veličiny při 300 K (Svoboda E. , Bakule R. : Molekulová fyzika. Academia, Praha 1992. ) Závislost Cp na teplotě pro vodík H 2

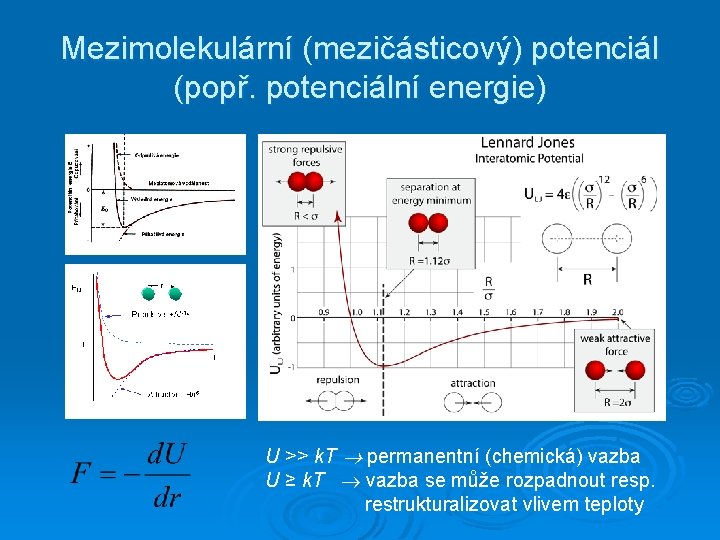
Mezimolekulární (mezičásticový) potenciál (popř. potenciální energie) U >> k. T permanentní (chemická) vazba U ≥ k. T vazba se může rozpadnout resp. restrukturalizovat vlivem teploty

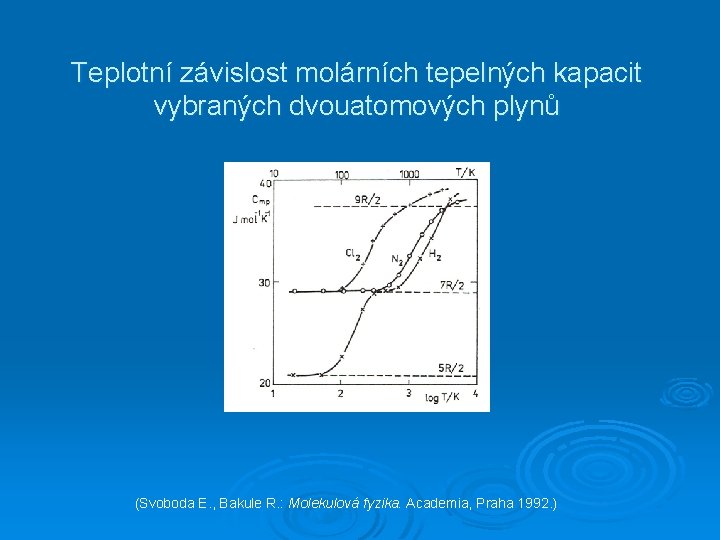
Teplotní závislost molárních tepelných kapacit vybraných dvouatomových plynů (Svoboda E. , Bakule R. : Molekulová fyzika. Academia, Praha 1992. )

Obecná formulace ekvipartičního principu Na každý z kvadratických členů, z nichž se skládá energie molekuly přísluší střední energie rovná k. BT/2. i – počet kvadratických členů

Kde jsme zatím použili statistický přístup střední hodnota kvadrátu rychlosti (statistická veličina)

Některé pojmy z teorie pravděpodobnosti Vlastnosti náhodných jevů Ø jsou vzájemně neslučitelné (nastal-li jeden, nemůže nastat druhý) Ø vždy musí nastat aspoň jeden výsledek Ø výsledek není složen z dílčích výsledků (nerozkládáme jej na dílčí výsledky)

Ø relativní četnost i-tého náhodného jevu počet pozorování výsledku, který nás zajímá celkový počet pozorování Ø pravděpodobnost i-tého náhodného jevu Ø pravděpodobnost určitého výsledku počet příznivých případů počet možných výsledků

Spojitá změna sledované veličiny Ø hustota pravděpodobnosti Ø pravděpodobnost, že výsledek bude z intervalu (x, x+ x) nebo normovací podmínka

Nezávislé náhodné pokusy a – pokus s možnými výsledky a 1, a 2, . . . an pravděpodobnosti výsledků: p(a 1), p(a 2), . . . p(an) b – pokus s možnými výsledky b 1, b 2, . . . bm pravděpodobnosti výsledků: q(b 1), q(b 2), . . . q(bm) pravděpodobnost současného výskytu výsledků ai, bj:

Neslučitelné výsledky a 1, a 2 Ø N opakování pokusu Ø N 1 krát výsledek a 1 Ø N 2 krát výsledek a 2 Ø počet příznivých výsledků: N 1+N 2 Ø Pravděpodobnost výskytu aspoň jednoho z výsledků a 1, a 2: věta o součtech pravděpodobností

Číselné charakteristiky Ni – četnost výskytu xi při N pozorováních → spojité rozložení (náhodné) veličiny: - střední hodnota funkční závislosti f(x) náhodné veličiny x, definované v intervalu a, b

Rozptyl (kvadratická fluktuace) Rozptyl je mírou variability náhodné veličiny x a může charakterizovat odchylku veličiny x od její střední hodnoty x. Je-li rozptyl malý, potom hodnota veličiny x je při každém pozorování blízká x a touto hodnotou můžeme dobře charakterizovat naměřené výsledky.
 Teorm
Teorm Kinetische energie in elektrische energie
Kinetische energie in elektrische energie Hydrostatický tlak vzorec
Hydrostatický tlak vzorec Mechanické vlastnosti kapalin test
Mechanické vlastnosti kapalin test Stavová rovnice ideálního plynu
Stavová rovnice ideálního plynu Pretlak a podtlak
Pretlak a podtlak Světové zásoby plynu
Světové zásoby plynu Analyzátorů krevních plynů poc
Analyzátorů krevních plynů poc Periodicky
Periodicky Mechanika plynů
Mechanika plynů Analyzátor krevních plynů
Analyzátor krevních plynů Společná vlastnost kapalín a plynu
Společná vlastnost kapalín a plynu Vlastnosti plynů
Vlastnosti plynů Vlastnosti plynů prezentace
Vlastnosti plynů prezentace Stavová rovnica ideálneho plynu
Stavová rovnica ideálneho plynu Benjamin franklin bleskozvod
Benjamin franklin bleskozvod Fyzikálna veličina objem
Fyzikálna veličina objem