Metallbindung zwischen Metallatomen Elektropositive Elemente Atombindung zwischen Nichtmetallatomen

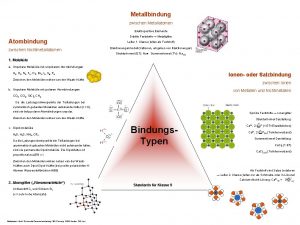
Metallbindung zwischen Metallatomen Elektropositive Elemente Atombindung zwischen Nichtmetallatomen Duktile Feststoffe → Metallgitter Leiter 1. Klasse (leiten als Feststoff) Elektronengasmodell (Kationen, umgeben von Elektronengas) Strukturformel (ET): Na● Summenformel (TV): Na (s) 1. Moleküle a. Unpolare Moleküle mit unpolaren Atombindungen H 2, O 2, N 2, F 2, Cl 2, Br 2, I 2, S 8, P 4 Ionen- oder Salzbindung Zwischen den Molekülen wirken van-der-Waals-Kräfte zwischen Ionen b. Unpolare Moleküle mit polaren Atombindungen von Metallen und Nichtmetallen CO 2, CCl 4, Si. Cl 4, CH 4 Da die Ladungsschwerpunkte der Teilladungen bei symmetrisch gebauten Molekülen aufeinander fallen (l = 0), sind sie trotz polarer Atombindungen unpolar. Spröde Feststoffe → Ionengitter Zwischen den Molekülen wirken van-der-Waals-Kräfte c. Dipolmoleküle H 20, H 2 S, NH 3, OF 2 Da die Ladungsschwerpunkte der Teilladungen bei asymmetrisch gebauten Molekülen nicht aufeinander fallen, Strukturformel-Darstellung: Bindungs. Typen sind sie permanente Dipolmoleküle. Die Dipolstärke ist Ca 2+, 2 l. Cll 1 - (1 ET=Einzelteilchen) Ca 2+, 2 l. Cll 1 -(s) (Teilchenverband) Summenformel-Darstellung: Ca. Cl 2 (1 ET) Ca. Cl 2 (s) (Teilchenverband) proportional zu ∆EN x l. Zwischen den Molekülen wirken neben van-der Waals. Kräften auch Dipol-Kräfte (bei positiv polarisierten H- Als Feststoff sind Salze Isolatoren Atomen Wasserstoffbrücken HBB) → Leiter 2. Klasse (leiten nur als Schmelze oder in Lösung) 2. Atomgitter („Riesenmoleküle“) Kohlenstoff Cx und Silicium Six (x = sehr hohe Atomzahl) Bildquellen: Klett, Schroedel Zusammenstellung: St. D Colberg, OSt. R Harder, St. D List Calciumchlorid-Lösung: Ca 2+aq + Standards für Klasse 9
- Slides: 1