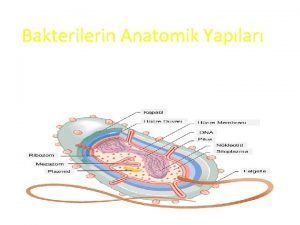
BOTTEKSB Izolace mezofylovch a hypokotylovch protoplast Boena Navrtilov

BOT/TEKSB Izolace mezofylových a hypokotylových protoplastů Božena Navrátilová

Příprava rostlinného materiálu pro izolace mezofylových a hypokotylových protoplastů Rostlinný materiál: okurka setá (Cucumis sativus cv. MARKETER). 1. Příprava semen vybereme nepoškozená semena a vložíme do injekční stříkačky, kterou si označíme 2. Sterilizace semen opláchneme v 70 % etanolu sterilizujeme v 36 % roztoku SAVO s kapkou Tweenu 30 min propláchneme 3 x sterilní destilovanou vodou (již v aseptickém prostředí) 3. Výsev semena pinzetou přeneseme ze střičky na sterilní vodou přelitý filtrační papír v Petriho miskách (90 mm, 8 - 10 semen) a uzavřeme parafilmem nebo na ½ MS medium v Petriho miskách (90 mm, 8 - 10 semen) a uzavřeme parafilmem

4. Kultivace semen a) Petriho misky umístíme v termostatu a kultivujeme ve tmě při 25 o. C po dobu 5 - 7 dnů b) po prorůstání přenesemenáčky na sterilní filtrační papír, odřízneme nadzemní část asi 2 cm pod dělohami a přeneseme na médium OK (MS + 0. 01 IBA + 0. 01 BAP + 20 mg/l kys. askorbové) v kultivačních nádobkách dále bod 6) 5. Výběr semenáčků před izolací protoplastů důkladně kontrolujeme výskyt kontaminací (semenáčky s kontaminací nepoužíváme) etiolované hypokotyly připravujeme cca 7 dnů před izolací a fúzí protoplastů

6. Rostlinky pro izolaci mezofylových protoplastů použijeme plně vyvinuté listy ze 4 - 6 týdenních rostlin pro izolaci mezofylových protoplastů (rostlinky s kontaminací nepoužíváme)

Izolace mezofylových a hypokotylových protoplastů 1. mladé, nepoškozené listy nařežeme na 1 mm proužky a umístíme do enzymatického roztoku v Petriho miskách (60 mm, 5 ml roztoku), které zalepíme parafilmem (500 mg rostlinného materiálu na 5 ml enzymatického roztoku): 1 % cellulasa Onozuka R 10 0, 25 % macerozym R 10 v promývacím roztoku PGLy p. H 5, 8 (sterilizace filtrací) stejně nařežeme a inkubujeme etiolované hypokotyly (1 000 mg rostlinného materiálu na 5 ml enzymatického roztoku) 2. inkubujeme v termostatu 18 hod ve tmě při 25 o. C (přes noc)

Izolace a purifikace mezofylových a hypokotylových protoplastů 3. hrubou protoplastovou suspenzi (mezofyl nebo hypokotyl) filtrujeme přes uhelonové sítko (72 m), které pak promyjeme W 5 roztokem asi 2 ml do Petriho misky (60 mm), přeneseme suspenzi (skleněnou Pasteurovou pipetou) do centrifugační zkumavky a doplníme na objem 10 ml 4. centrifugujeme při 800 rpm po dobu 5 min
5. odstraníme supernatant a sediment resuspendujeme do objemu 4 ml 20% sacharózou a opatrně převrstvíme pomocí skleněné Pasteurovy pipety do objemu 6 ml promývacím roztokem !!! nemíchat 6. centrifugujeme při 800 ot/min po dobu 10 minut 7. odebereme flotující protoplasty = kroužek na rozhraní sacharózy a promývacího roztoku Pasteurovou pipetou do čisté centrifugační zkumavky a resuspendujeme v promývacím roztoku do objemu 4 ml 8. centrifugujeme při 800 ot/min po dobu 10 minut 9. odstraníme supernatant a protoplasty v sedimentu resuspendujeme v médiu LCM 1 na objem 1 ml stanovíme hustotu a životnost pro kultivaci protoplastů
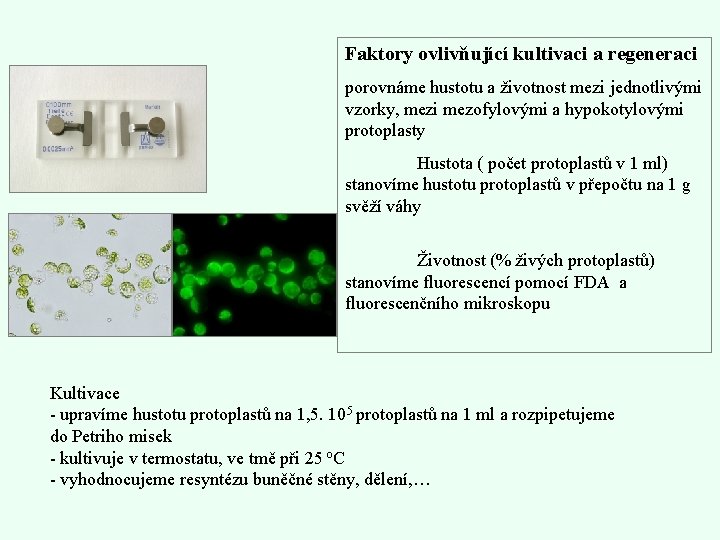
Faktory ovlivňující kultivaci a regeneraci porovnáme hustotu a životnost mezi jednotlivými vzorky, mezi mezofylovými a hypokotylovými protoplasty Hustota ( počet protoplastů v 1 ml) stanovíme hustotu protoplastů v přepočtu na 1 g svěží váhy Životnost (% živých protoplastů) stanovíme fluorescencí pomocí FDA a fluorescenčního mikroskopu Kultivace - upravíme hustotu protoplastů na 1, 5. 105 protoplastů na 1 ml a rozpipetujeme do Petriho misek - kultivuje v termostatu, ve tmě při 25 o. C - vyhodnocujeme resyntézu buněčné stěny, dělení, …
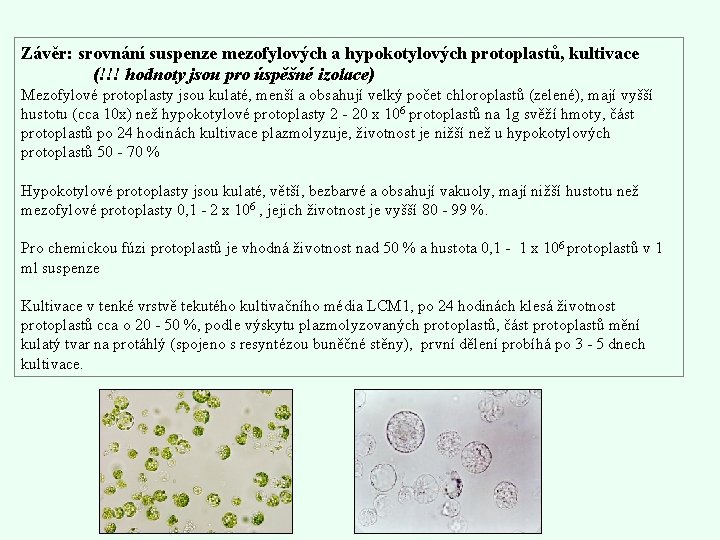
Závěr: srovnání suspenze mezofylových a hypokotylových protoplastů, kultivace (!!! hodnoty jsou pro úspěšné izolace) Mezofylové protoplasty jsou kulaté, menší a obsahují velký počet chloroplastů (zelené), mají vyšší hustotu (cca 10 x) než hypokotylové protoplasty 2 - 20 x 106 protoplastů na 1 g svěží hmoty, část protoplastů po 24 hodinách kultivace plazmolyzuje, životnost je nižší než u hypokotylových protoplastů 50 - 70 % Hypokotylové protoplasty jsou kulaté, větší, bezbarvé a obsahují vakuoly, mají nižší hustotu než mezofylové protoplasty 0, 1 - 2 x 106 , jejich životnost je vyšší 80 - 99 %. Pro chemickou fúzi protoplastů je vhodná životnost nad 50 % a hustota 0, 1 - 1 x 106 protoplastů v 1 ml suspenze Kultivace v tenké vrstvě tekutého kultivačního média LCM 1, po 24 hodinách klesá životnost protoplastů cca o 20 - 50 %, podle výskytu plazmolyzovaných protoplastů, část protoplastů mění kulatý tvar na protáhlý (spojeno s resyntézou buněčné stěny), první dělení probíhá po 3 - 5 dnech kultivace.
- Slides: 9