11 AZ ATOMMAGOK ENERGIALLAPOTAI 11 1 A maghj



















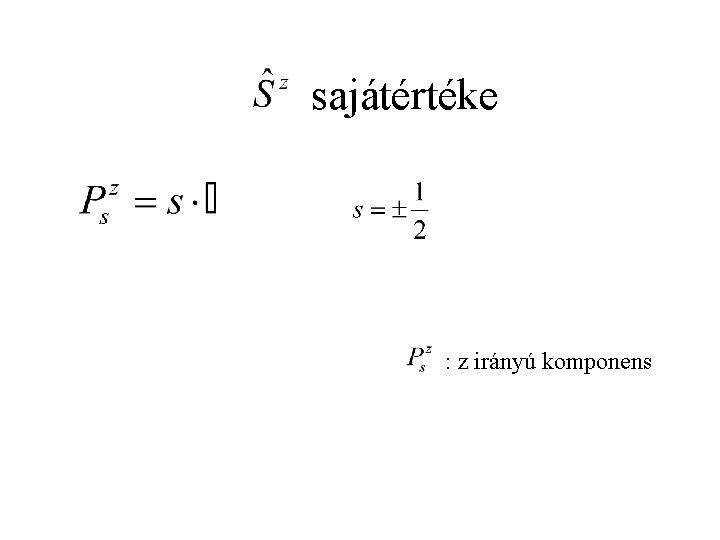














![A csatolási állandó megadása: JCH/h, JHH/h, [Hz] JCC/h, stb. A csatolási állandó megadása: JCH/h, JHH/h, [Hz] JCC/h, stb.](https://slidetodoc.com/presentation_image_h2/d464f4d6a5b7286c1eb74fc0ba322c66/image-48.jpg)











- Slides: 68

11. AZ ATOMMAGOK ENERGIAÁLLAPOTAI

11. 1. A maghéj modell

Maghéj modell

Nukleonok spinből származó impulzusmomentuma (A proton és a neutron 1/2 spinű részecske, mint az elektron. )

Maghéj modell • Az atommag kvantumállapotainak leírására használt modell • Hasonlít a többelektronos atomok szerkezetének tárgyalásánál használt modellre, amelyekből az elektronhéjak adódnak. (Bonyolultabb annál, mivel nukleonból kétféle van. )

Atommagok kvantumállapotának jellemzése (A maghéj modell szerinti tárgyalás eredménye) A magok állapotát két kvantumszám jellemzi: - I : magspin-kvantumszám - MI : mag mágneses kvantumszám

A magkvantumszámok lehetséges értékei I: magspin-kvantumszám attól függ, hogy a mag rendszáma és tömegszáma páros vagy páratlan. rendszám páros páratlan tömegszám páros páratlan I lehetséges értékei csak 0 lehet “félegész” számok (1/2, 3/2, 5/2…) egész számok (1, 2, 3…) “félegész” számok (1/2, 3/2, 5/2…) MI : mag mágneses kvantumszám : MI = I, I-1, …, -I.

Az atommag energiája Mágneses tér távollétében: csak I-től függ, MI szerint degenerált Mágneses térben: a degenerált szintek MI szerint felhasadnak.

Atommagok gerjesztése • Mössbauer effektus: I változik, gerjesztés gamma-fotonnal • Mágneses magrezonancia: MI változik (mágneses térben!), gerjesztés rádióhullámú fotonnal

Rudolf Ludwig Mössbauer 1929"for his researches concerning the resonance absorption of gamma radiation and his discovery in this connection of the effect which bears his name"

"for their development of new methods for nuclear magnetic precision measurements and discoveries in connection therewith" Felix Bloch 1905 - 1983 Edward Mills Purcell 1912 - 1997

11. 2 A Mössbauer-effektus Az I magspin-kvantumszám megváltozásával járó átmenet. - Nagy energiájú, g-sugárzás tartományába esik - Nagyon keskeny sávú

A Mössbauer-effektus technikája Sugárforrás: olyan magot tartalmazó vegyület, amely magot a mintában vizsgálni akarunk Gerjesztett állapot Alapállapot Sugárforrásként szolgáló vegyületben gerjesztett magok radioaktív bomlás során keletkezhetnek.

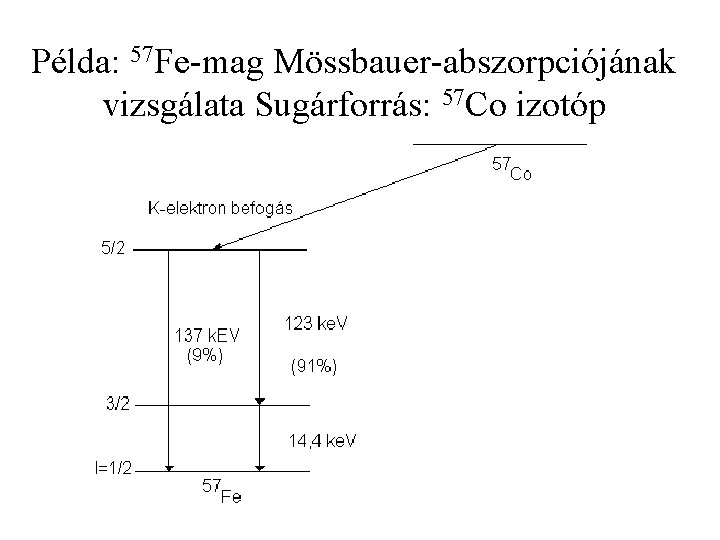
Példa: 57 Fe-mag Mössbauer-abszorpciójának vizsgálata Sugárforrás: 57 Co izotóp

Mössbauer-spektroszkópia • A Mössbauer-effektus felhasználása kémiai szerkezetvizsgálatra. • A periódusos rendszer elemeinek mintegy fele tanulmányozható Mössbauer-spektroszkópiával. • Szükség van eggyel nagyobb rendszámú radioaktív izotópra, amelynek bomlása során a vizsgált atommag keletkezik, mégpedig gerjesztett állapotban. • Néhány gyakran vizsgált mag: 57 Fe, 119 Sn, 121 Sb, 125 Te.

Kísérleti technika g-sugárforrás hangolása Doppler-eltolódással. A fényforrást a mintához képest mozgatják. -t szisztematikusan változtatva mérik az abszorpciót. Detektor: g-sugárzás intenzitását mérő detektor: Na. I kristály. Egy g-foton a Na. I kristályrács számos I--ionjáról elektront szakít le. Az így keletkezett áramot elektronsokszorozóval erősítik.

A spektrum jellemzői • Kémiai eltolódás: az abszorpciós frekvencia jellemző az atommagra, de kis mértékben függ az elektronsűrűségtől a mag környezetében, azaz jellemző a molekula szerkezetére. • Kvadrupólus felhasadás: a kvadrupólus az atommagok töltéseloszlását jellemző mennyiség. Ha a magnak van kvadrupólusa (nem gömbszimmetrikus elektromos tér), az I kvantumszámmal jellemezhető energiaszintek felhasadnak. • Mágneses felhasadás: mágneses térben az I kvantumszámmal jellemzett szintek MI-szerint felhasadnak. Megfigyelhető: – a mintát külső mágneses térbe téve – belső mágneses térrel bíró anyagoknál (pl. ferromágneses anyagok)

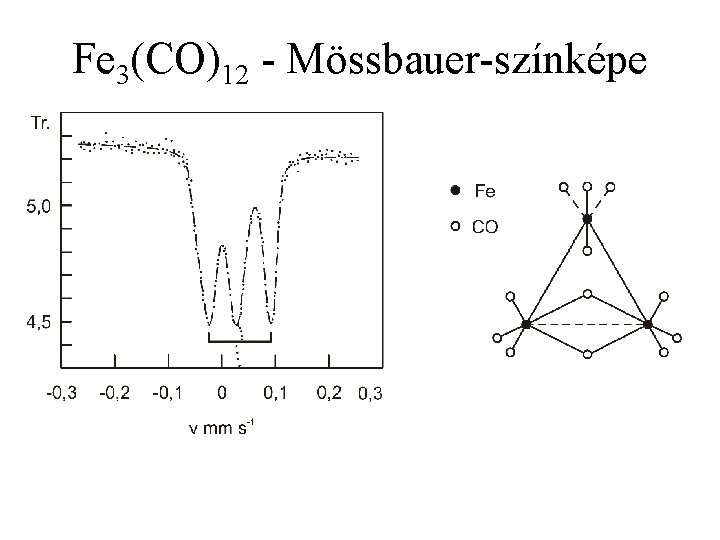
Fe 3(CO)12 - Mössbauer-színképe

12. MÁGNESES MAGREZONANCIA

12. 1. Az atommagok abszorpciója mágneses térben Mössbauer effektus Mágneses tér távollétében: csak I-től függ, MI szerint degenerált Mágneses magrezonancia Mágneses térben: a degenerált szintek MI szerint felhasadnak.

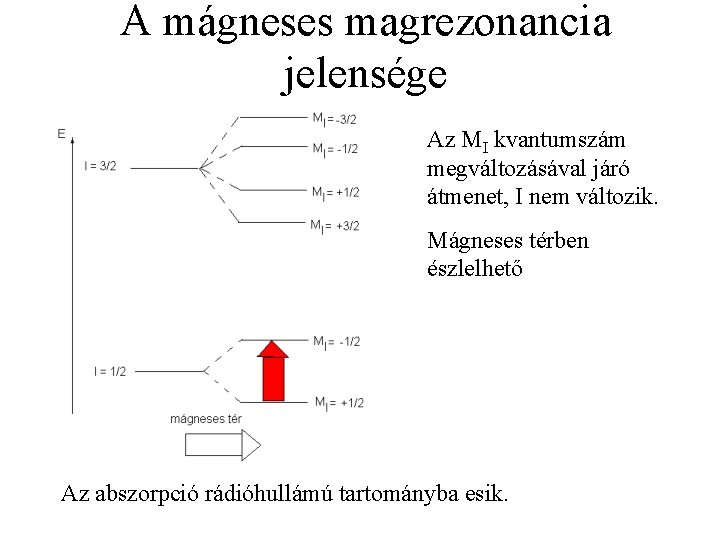
A mágneses magrezonancia jelensége Az MI kvantumszám megváltozásával járó átmenet, I nem változik. Mágneses térben észlelhető Az abszorpció rádióhullámú tartományba esik.

Az energiaszintek a mágneses térben történő felhasadásának oka (Analógia a H-atommal) Ha I nem 0, a magnak mágneses momentuma van, ez a mágneses momentum kölcsönhatásba lép a mágneses térrel.

Spin operátor Jele: Sajátérték egyenletet lehet felírni absz. értékére és z irányú vetületre.

sajátértéke Ps : spinhez tartozó imp. momentum : spinre utaló mellékkvantumszám abszolút érték
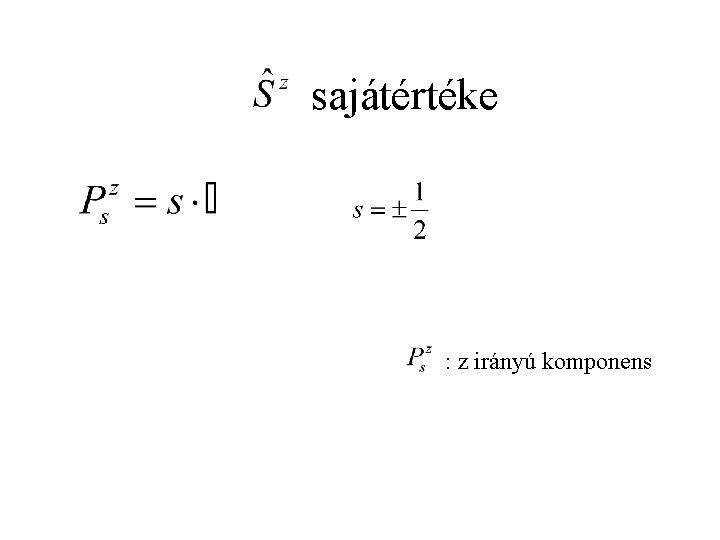
sajátértéke : z irányú komponens

Spinből származó mágneses momentum abszolút érték z irányú komponens ge : Lande-faktor hidrogénatomban ge=2, 0023

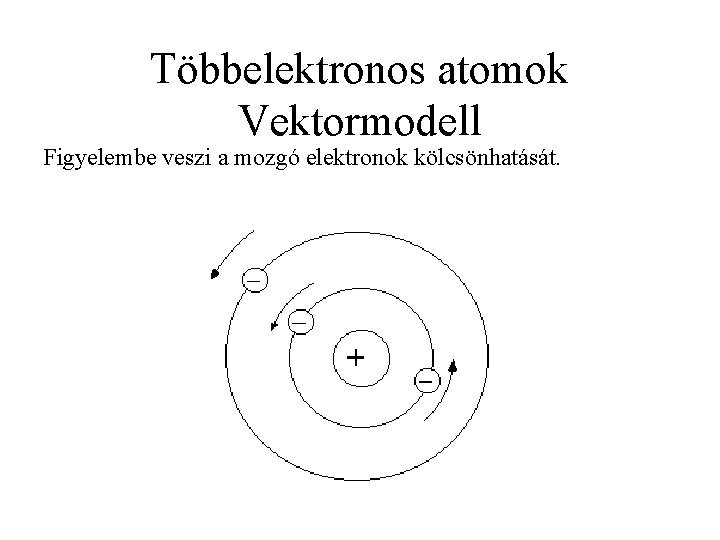
Többelektronos atomok Vektormodell Figyelembe veszi a mozgó elektronok kölcsönhatását.

Impulzusmomentum Elektronok egyedi imp. momentuma nem határozható meg, csak az összes elektron imp. momentumának eredője. Impulzusmomentum sajátértéke H-atom Több elektronos atom Pálya imp. momentum. Spinmomentum Spin-pálya csatolás L, S, J : „csoportkvantumszámok”

Magspinből származó impulzusmomentum és mágneses momentum. (Analógia a többelektronos atomokkal) Impulzusmomentum abszolút értéke: Impulzusmomentum z irányú vetülete: Mágneses momentum abszolút értéke: Mágneses momentum z irányú vetülete: g : „Lande-faktor” mn : atommag Bohrmagnetonja mn : mag tömege

Mágneses momentummal rendelkező részecske potenciális energiája mágneses térben Klasszikus fizika: : mágneses indukció Ha a mágneses tér iránya z, Kvantummechanikában:

Az NMR spektroszkópiában legtöbbet vizsgált magok: 1 H, 13 C

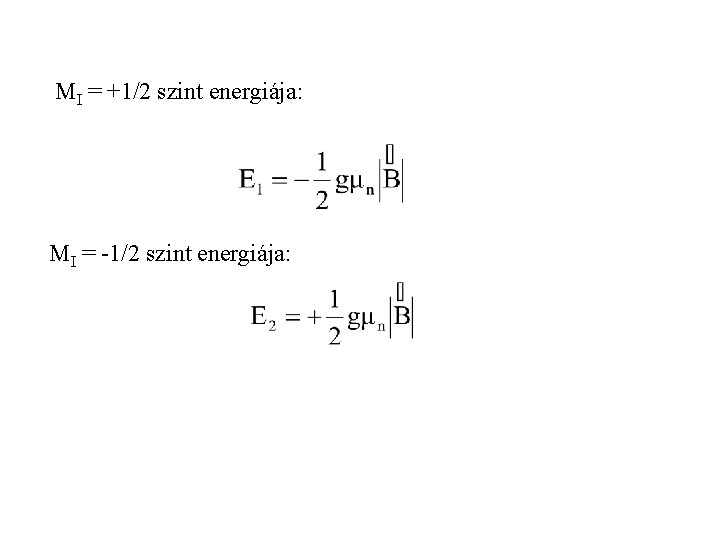
MI = +1/2 szint energiája: MI = -1/2 szint energiája:

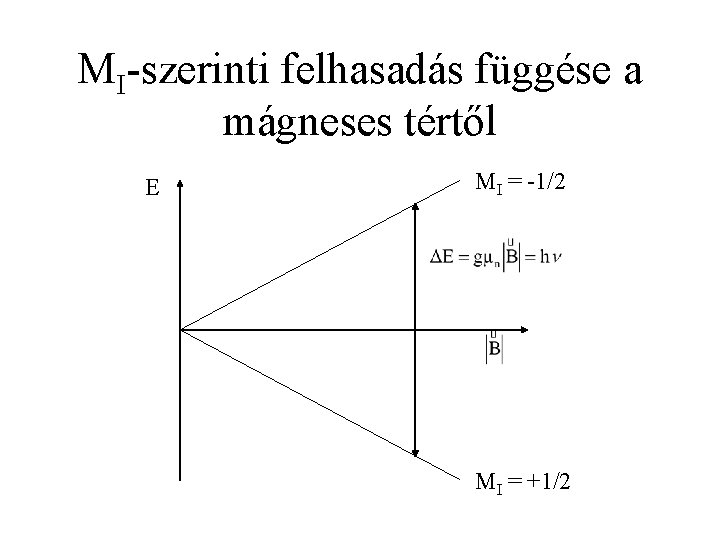
MI-szerinti felhasadás függése a mágneses tértől E MI = -1/2 MI = +1/2

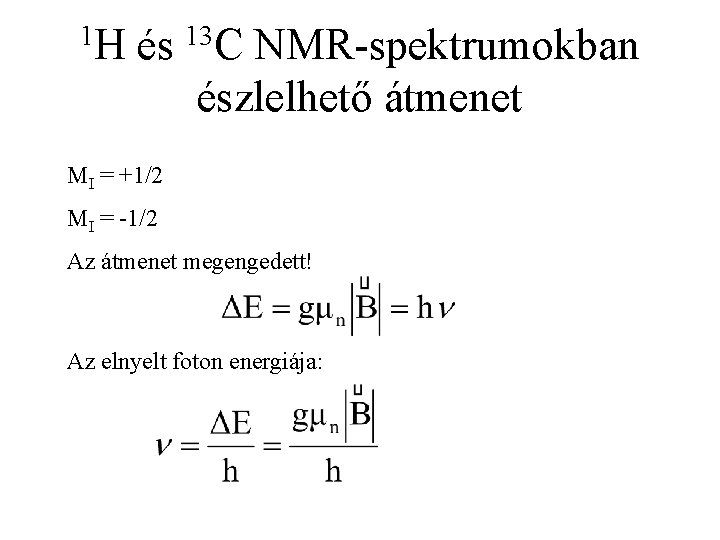
1 H és 13 C NMR-spektrumokban észlelhető átmenet MI = +1/2 MI = -1/2 Az átmenet megengedett! Az elnyelt foton energiája:

Atommagok NMR abszorpciós frekvenciája mágneses térben mag 1 H 11 B 13 C 19 F Természetes gyakoriság (%) I (alapáll. ) (MHz) 99, 98 81, 17 1, 11 100, 0 1/2 3/2 1/2 42, 58 13, 66 10, 70 40, 06

12. 2 Az NMR színképek jellemzői I. A kémiai eltolódás.

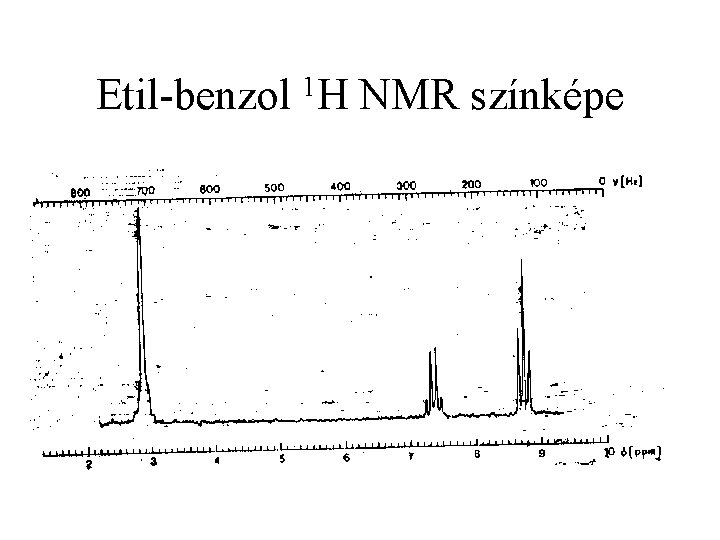
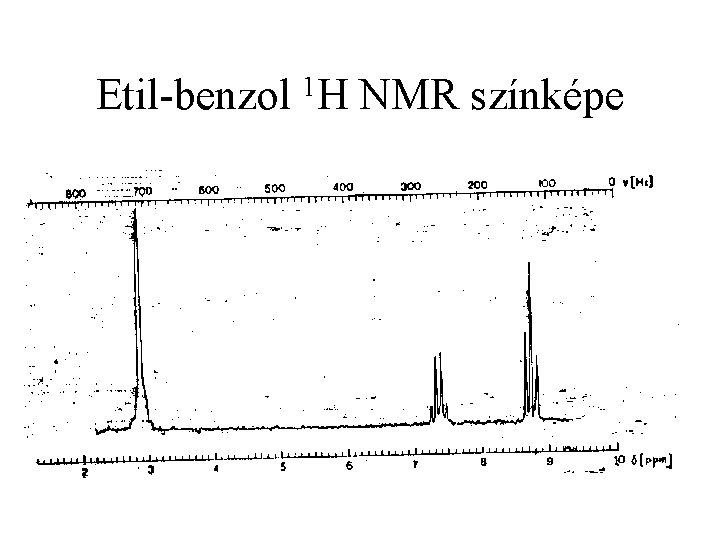
Etil-benzol 1 H NMR színképe

A kémiai eltolódás fogalma: az atomra jellemző abszorpciós (emissziós, ionizációs) frekvencia kismértékben függ az atom környezetétől a molekulában. Megfigyelhető: • XPS (atomtörzsek ionizációs energiáját mérjük) • Mössbauer-effektus (atommag energiájának változása g-foton elnyeléssel) • Mágneses magrezonancia (mágneses térben felhasadt magenergianívók közötti átmenet rádióhullámú sugárzás elnyelésével)

Kémiai eltolódás az NMRspektrumban Mágneses tér hatására rendeződik az elektronok mozgása a magok körül, emiatt megváltozik a lokális mágneses tér. : árnyékolási tényező pozitív: diamágneses árnyékolás negatív : paramágneses árnyékolás A kémiai eltolódás miatt megváltozott abszorpciós frekvencia:

Az NMR-spektrumban a kémiai eltolódással módosult abszorpciós frekvencia megadása: : kémiai eltolódás (a jelenség neve is kémiai eltolódás!) 0 megválasztása: elvi lehetőség: izolált atommag -je konvencionális megoldás: egy kiválasztott vegyület atomjának -je Leggyakoribb referenciavegyület: TMS előnye: az 1 H és 13 C spektrumban is egyetlen abszorpciós sáv van.

d előnye a -vel szemben: független a mágneses térerőtől. Példa: Hány NMR jel van az etanol 1 H spektrumában? Hány NMR jel van az aceton 1 H spektrumában? A funkciós csoportokra jellemző, hogy mekkora a bennük levő 1 H, 13 C, stb. magok kémiai eltolódása.

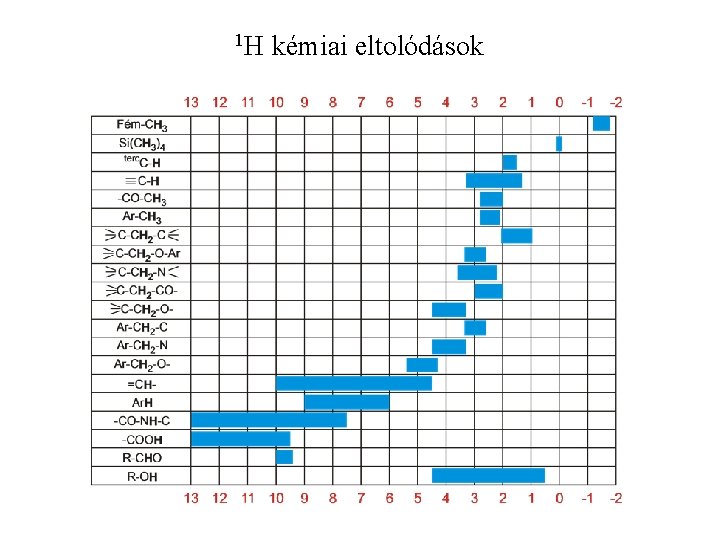
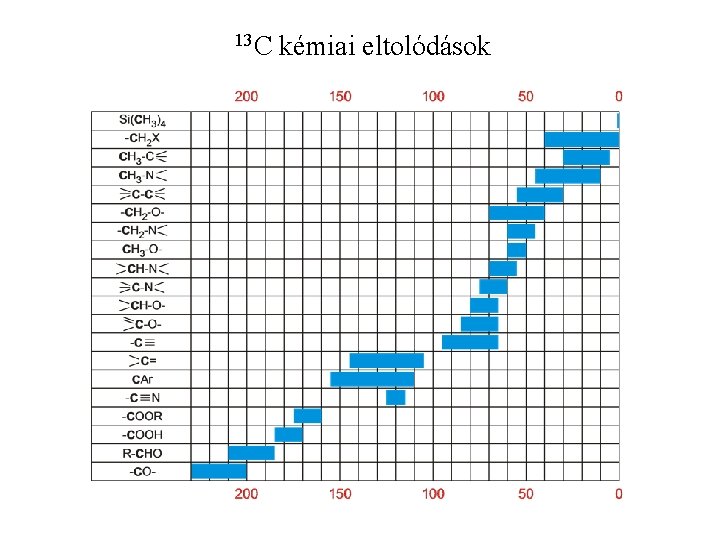
1 H kémiai eltolódások

13 C kémiai eltolódások

12. 3. Az NMR színképek jellemzői II. A spin-spin csatolás. Spin-spin csatolás: egy molekulán belüli NMR-aktív atommagok mágneses momentumai kölcsönhatásba lépnek egymással, emiatt megváltozik az összes egymással kölcsönhatásban lévő mag energiája. A spektrumban ez a sávok felhasadásában nyilvánul meg.

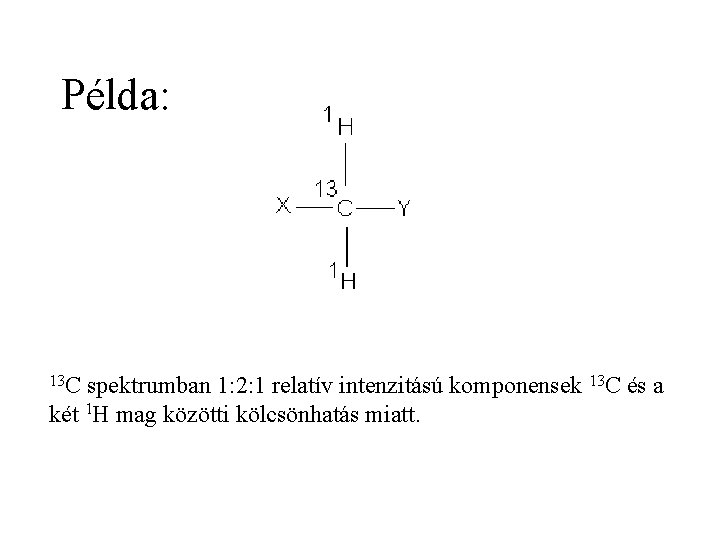
Példa: 13 C spektrumban 1: 2: 1 relatív intenzitású komponensek 13 C és a két 1 H mag közötti kölcsönhatás miatt.

A CH 2 -csoport 13 C-mag energiája a spin-spin kölcsönhatás figyelembevételével. JCH : C-H csatolási állandó Gerjesztés során: MIH 1 +1/2 -1/2 MIH 2 +1/2 -1/2 ECH +1/2 JCH 0 0 -1/2 JCH

A csatolási állandó függ • milyen atomok között alakul ki (pl. 1 H-1 H, 1 H 13 C, 1 H-19 F, 13 C-13 C csatolás) • az atomok közötti távolság • milyen kémiai kötés(ek) van(nak) köztük Nem függ a mágneses térerőtől.
![A csatolási állandó megadása JCHh JHHh Hz JCCh stb A csatolási állandó megadása: JCH/h, JHH/h, [Hz] JCC/h, stb.](https://slidetodoc.com/presentation_image_h2/d464f4d6a5b7286c1eb74fc0ba322c66/image-48.jpg)
A csatolási állandó megadása: JCH/h, JHH/h, [Hz] JCC/h, stb.

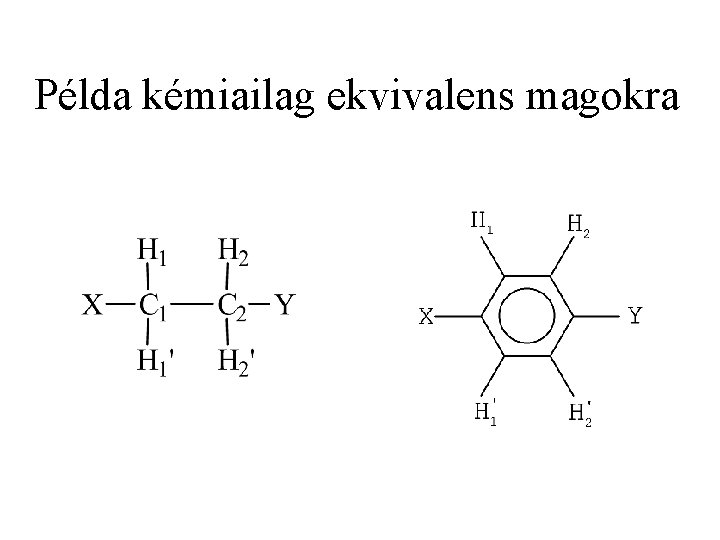
Kémiailag ekvivalens magok: - kémiai eltolódásuk megegyezik Pl. : -CH 3 3 protonja, - CH 2 2 protonja. Mágnesesen ekvivalens magok - olyan kémiailag ekvivalens magok, amelyek egy másik kémiailag ekvivalens csoport egyes tagjaival azonos spin-spin kölcsönhatásban vesznek részt.

Példa kémiailag ekvivalens magokra

NMR-spektrum értékelése Kémiai eltolódások és alapján Spin-spin csatolások I. rendű spektrum: d-k közötti különbségek sokkal nagyobbak, mint a spin-spin csatolás okozta felhasadás. Ezek értékelése viszonylag egyszerű.

Etil-benzol 1 H NMR színképe

A spin-spin csatolás szabályai az 1 H spektrumban • Az azonos szénatomon lévő protonok nem hasítják fel egymás jelét, ha mágnesesen ekvivalensek. • A szomszédos szénatomokon lévő protonok közötti spin -spin csatolás jól látható felhasadást okoz. • A távolabbi szénatomokon lévő protonok közötti spin csatolás az alifás láncok mentén kicsi, csak különösen nagy felbontású spektrumokban észlelhető. Konjugált C-C kötések mentén a távolabbi protonok között is észlelhető spin-spin csatolás alakul ki.

Etil-benzol 1 H NMR-spektruma Felhasadások a CH 3 -csoport jelében (a CH 2 csoport okozza) MIH 1 +1/2 -1/2 MIH 2 +1/2 -1/2 EHH +1/2 JHH 0 0 -1/2 JHH

Etil-benzol 1 H NMR-spektruma Felhasadások a CH 2 -csoport jelében (a CH 3 csoport okozza) MIH 1 +1/2 -1/2 MIH 2 +1/2 -1/2 MIH 3 +1/2 -1/2 +1/2 -1/2 EHH +3/2 JHH +1/2 JHH -1/2 JHH -3/2 JHH

Az NMR-spektrumból tehát meghatározható a vizsgált anyag molekuláinak szerkezeti képlete.

A spin-spin kölcsönhatás a 13 C spektrumban A 13 C atomok jelét a hozzájuk kapcsolódó protonok hasítják fel. CH-csoport 1: 1 dublett CH 2 -csoport 1: 2: 1 triplett CH 3 -csoport 1: 3: 3: 1 kvartett

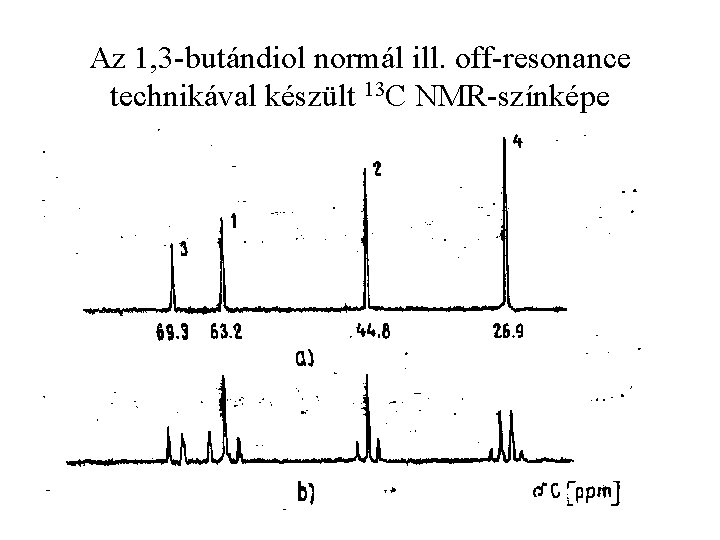
Az 1, 3 -butándiol normál ill. off-resonance technikával készült 13 C NMR-színképe

12. 4. NMR-spektroszkópia Általában oldatmintát vizsgálnak. Oldószerek: CDCl 3, aceton-D 6 (az oldószer 1 H abszorpciója nem zavar) Az oldathoz TMS-t adnak.

Az NMR-spektrumban a jel gyenge 1 H t = 25 o. C Ok: kicsi a DE (különbség az alap és a gerjesztett állapot között). Az abszorpciós és stimulált emisszió valószínűsége csaknem megegyezik. A gerjesztés során tovább közelít az arány az 1 -hez. Relaxációs folyamatok: magok sugárzásmentesen leadják gerjesztési energiájukat.

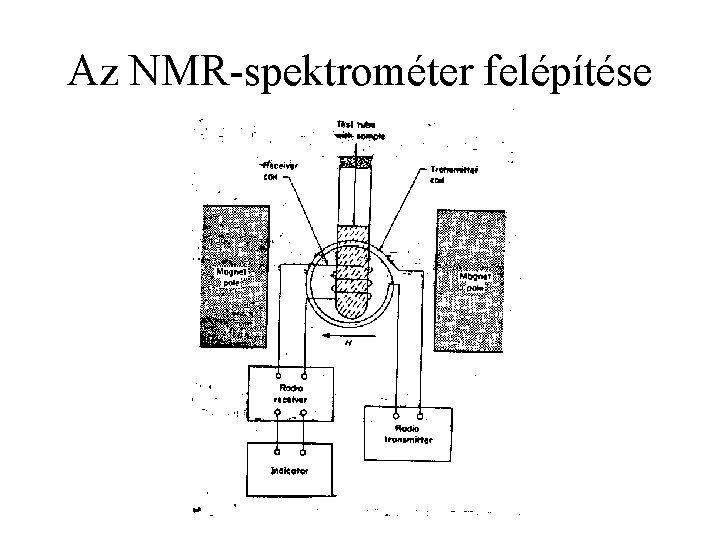
Az NMR-spektrométer felépítése

Korszerű NMR-berendezés • erős mágnes: sok az I. -rendű spektrum részlet • impulzus üzemű készülék (FT-NMR)

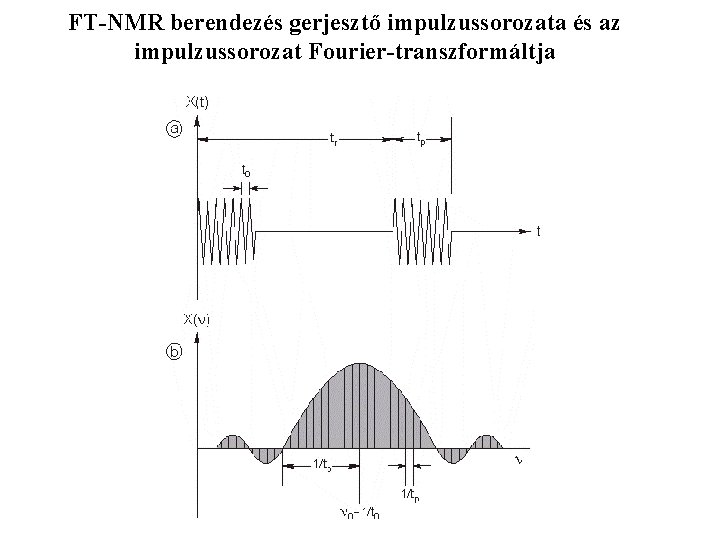
FT-NMR berendezés gerjesztő impulzussorozata és az impulzussorozat Fourier-transzformáltja

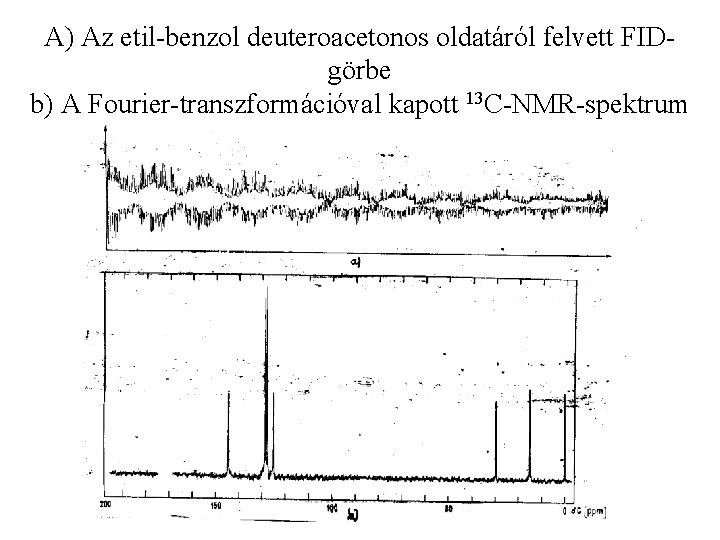
A) Az etil-benzol deuteroacetonos oldatáról felvett FIDgörbe b) A Fourier-transzformációval kapott 13 C-NMR-spektrum

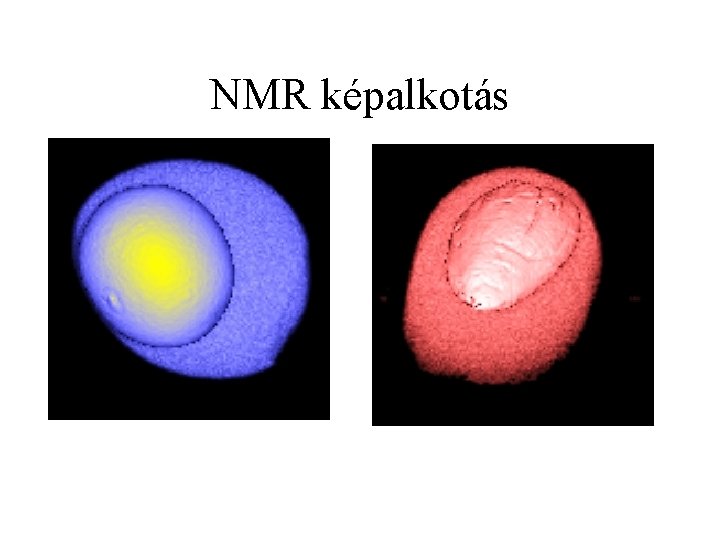
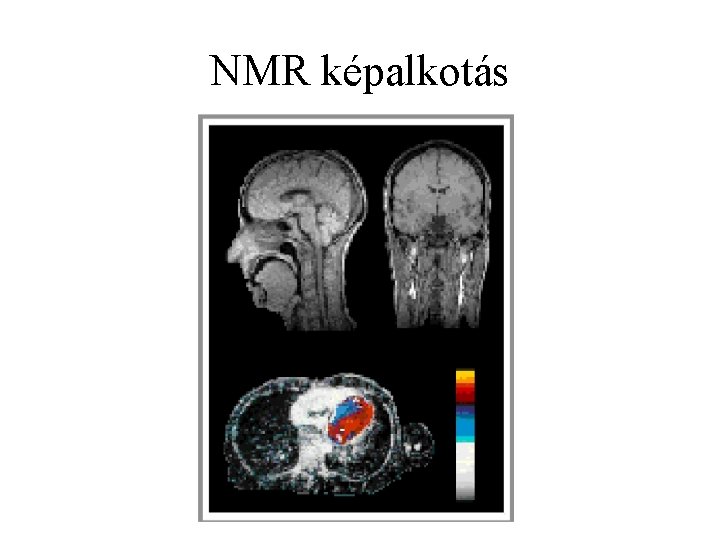
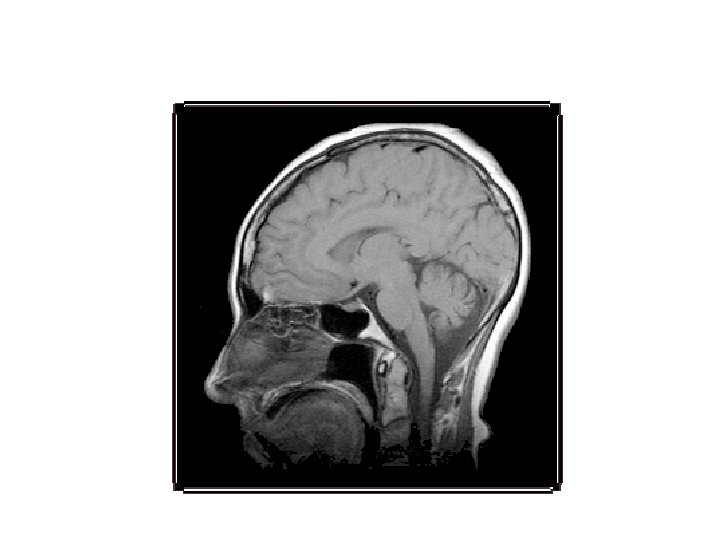
NMR képalkotás

NMR képalkotás

