ZWIZKI CHEMICZNE W YCIU CODZIENNYM Robert Gronowski Szkoa

ZWIĄZKI CHEMICZNE W ŻYCIU CODZIENNYM Robert Gronowski Szkoła Podstawowa Nr 9 Ul. Stoczniowców 6 84 -230 Rumia Zródło: Newsweek. pl Zródło: Placpigal. pl

WSTĘP Chemia to nauka o zjawiskach towarzyszących człowiekowi nieustannie, wszędzie i na każdym kroku. Bez przesady, można by powiedzieć, że gdyby nie postęp jaki dokonał się w naukach chemicznych życie współczesnego człowieka nie byłoby takim jest obecnie. Mądrze wykorzystywane prawidła chemiczne mogą bez wątpienia podnieść poziom cywilizacyjny ludzkości, z drugiej zaś strony brak odpowiedniej wiedzy chemicznej, zła wola, niedbalstwo człowieka doprowadzają do tego, że procesy chemiczne mogą stać się wrogiem naszego zdrowia, środowiska i postępu. Rzeczywiście jest tak, że wszystko co jesteśmy w stanie zaobserwować wokół nas jest skutkiem obecności substancji chemicznych i przebiegających procesów chemicznych. Chemia mądrze wykorzystywana pomaga nam, ale też wielu negatywnym skutkom naszego życia towarzyszy często stwierdzenie, że „wszystkiemu winna jest chemia”. Ale, czy z powodu pożarów wzniecanych, za pomocą zapałek należy potępiać przemysł chemiczne produkujący zapałki? Czy niewłaściwe zastosowanie leków to wina farmaceutów i chemików je produkujących? Te i inne pytania towarzyszą człowiekowi codziennie i odpowiedź jest jedna. Jeśli mądrze będziemy czerpać z tego co nauki chemiczne nam oferują życie współczesnego człowieka może stać się łatwiejsze. Jeśli tak się nie stanie owoce chemicznego postępu pójdą na marne i doprowadzą do zanieczyszczenia, degradacji środowiska naturalnego, chorób z tego wynikających , przedwczesnej śmiertelności ludzi i zwierząt. Poniżej przedstawiam tylko znikomy ułamek tego wielkiego bogactwa jakim obdarzyła nas wiedza chemiczna towarzysząca nam w każdym aspekcie życia codziennego.

CHEMIA W PRZEMIANACH ŻYWNOŚCI • A FERMENTACJA ALKOHOLOWA - to istota powstawania wina. Jest to proces biochemiczny, w wyniku którego dochodzi do przemiany glukozy (cukru zawartego w dojrzałych owocach winogron) pod wpływem enzymów wytwarzanych przez drożdże w odpowiedniej temperaturze. Przez tysiąclecia sądzono, że jest to proces spontaniczny, zachodzący boskim (Dionizosa, Bachusa) zrządzeniem losu. Dopiero francuski chemik Lavoisier wykazał, że polega ona na przekształcaniu cukru w alkohol. Inny francuski uczony Gay. Lussac przedstawił wzór tej reakcji: • C 6 H 1206 -> 2 C 2 H 5 OH + 2 CO 2 • Louis Pasteur udowodnił w 1857 roku, że fermentacja alkoholowa nie zachodzi spontanicznie, lecz pod wpływem drożdży. Rozkładają one cukier na alkohol etylowy, dwutlenek węgla, energię i produkty uboczne. Podczas tej reakcji powstaje kilkaset (dokładnie wiadomo ile, ale na pewno ponad 600) substancji, między innymi gliceryna (nadaje winu oleistość), kwas octowy, kwas bursztynowy, estry, olejki eteryczne. Bez ingerencji człowieka fermentacja alkoholowa w pewnym momencie samoistnie zwalnia, a potem ustaje, gdy moszcz osiąga 14 – 15 proc. alkoholu. W takim stężeniu drożdże obumierają, niezależnie od tego, ile jeszcze pozostało cukru. Zródło: Wino-marekkondrat. pl

Proces fermentacji alkoholowej wykorzystywany jest również do produkcji kefirów, ciast drożdżowych czy alkoholu etylowego. Żródło: Ciasto drożdzowe-portal ANIAGOTUJE. PL Źródło: Kefiry-forummleczrskie. pl

CHEMIA W PRZEMIANACH ŻYWNOŚCI • B FERMENTACJA MLEKOWA -wykorzystywana do otrzymywania kiszonek - jest to dokładnie sposób konserwacji żywności opierający się na tym procesie, przeprowadzanym przez bakterie mlekowe. • W wyniku tego procesu cukry proste zawarte w komórkach roślinnych rozkładają się na kwas mlekowy (1– 1, 8%), hamując m. in. procesy gnicia (przez zahamowanie rozwoju bakterii gnilnych nieodpornych na zakwaszenie środowiska do p. H poniżej 5[1]). Prawidłowy przebieg kiszenia zależy od zawartości w surowcu cukrów (1 – 1, 5%) i wody (ok. 70%), utrzymania w temperaturze 15– 20 °C w początkowych dniach fermentacji, usunięcia powietrza (bakterie przeprowadzające proces są beztlenowe) np. przez ubicie (kapusta) lub zalanie solanką. Na skalę przemysłową kiszenie przeprowadza się w dużych kadziach lub betonowych silosach. • Produkty kiszone stanowią bardzo cenne dietetyczne pożywienie, bogate w witaminy C (w 100 g kiszonej kapusty – 25 do 30 mg wit. C) Źródło: Hajduczeknaturalnie. pl/kiszonkawielowarzywna-samo-zdrowie

CHEMIA W PRZEMIANACH ŻYWNOŚCI • C FERMENTACJA MASŁOWA - to przykład procesu chemicznego działającego na niekorzyść w przemyśle spożywczym. Fermentacja ta przeprowadzana przez bakterie masłowe przyczynia się do psucia mleka pasteryzowanego, konserw warzywnych i owocowych, a także powoduje dekompozycje kiszonych pasz. Bakterie masłowe przeprowadzają procesy życiowe bez użycia tlenu, a ich szczególną zdolnością jest możliwość rozkładu polisacharydów takich jak: skrobia, błonnik, dekstryny - na związki proste. • Równanie reakcji - GLUKOZA C 6 H 12 O 6 + bakterie masłowe -> kwas masłowy + 2 CO 2+ 2 H 2 • Kwas masłowy charakteryzuje się ostrym, nieprzyjemnym zapachem, występ uje np. w zjełczałym maśle. Fermentacja masłowa jest odpowiedzialna za gorzki smak serów żółtych. Źródło: Hajduczeknaturalnie. pl/kiszonka-wielowarzywnasamo-zdrowie/

CHEMIA W PRZEMIANACH ŻYWNOŚCI • D GNICIE - to proces chemiczny niekorzystnie wpływający m. in. na naszą żywność. Polega na rozkładzie żywności zawierającej białko pod wpływem bakterii gnilnych. Zachodzi w nieobecności tlenu, a produktami reakcji są związki chemiczne o nieprzyjemnym zapachu - siarkowodór, amoniak i inne. • Wszelkim procesom chemicznym, które zachodzą w żywności i powodują jej psucie możemy zapobiegać poprzez jej konserwację, również opartą na reakcjach chemicznych. Do podstawowych metod konserwacji żywności należą oprócz omówionej już metody kiszenia, np: wędzenie, liofilizacja, pasteryzacja.

CHEMIA W PRZEMIANACH ŻYWNOŚCI • WĘDZENIE - to jeden z najstarszych sposobów konserwacji żywności, przede wszystkim mięsa oraz ryb. Produkty poddane działaniu ciepła oraz związków zawartych w dymie nabierają niepowtarzalnego smaku i aromatu, ale czasem stają się również źródłem niebezpiecznych dla zdrowia substancji. Wędzenie jest procesem, w trakcie którego przetwory poddawane są działaniu ciepła i związków chemicznych zawartych w dymie wędzarniczym. Dym otrzymywany jest w wyniku spalania odpowiedniego drewna i jego pochodnych (zręby i trociny wędzarnicze). W wyniku wędzenia następuje zmniejszenie zawartości wody w produkcie, a także zmiany chemiczne i fizykochemiczne. • LIOFILIZACJA - Liofilizacja potocznie zwana jest suszeniem mrozem i określenie to dobrze odzwierciedla istotę procesu. Pierwszym jego etapem jest mrożenie, którego dokonuje się bądź w zamrażalniku, bądź w specjalnej mrożącej suszarce. Pożądana temperatura to jednak około -40 stopni C – nie każdy zamrażalnik taką moc posiada. Jest to najbardziej kluczowa część liofilizacji, bowiem musi odbywać się na tyle szybko, aby na żywności nie wytworzyły się duże kryształy lodu, które obniżają jakość końcowego produktu. Następnie zmrożoną porcję poddaje się suszeniu sublimacyjnemu, które łączy obniżanie ciśnienia wokół poprzez warunki próżniowe w połączeniu z falą ciepła. Na tym etapie eliminowane jest 95% ilości wody w pokarmie – trwać on może nawet do dwóch dni. Odseparowana wilgoć nie skrapla się jednak, ale jest kondensowana jest w stanie lotnym – jako para. Ostatnią fazą procesu jest suszenie wtórne, które ma na celu pozbycie się pozostałych zamrożonych cząsteczek wody z produktu. Odbywa się ona we wyższej temperaturze niż pierwotne suszenie, a w końcowym rezultacie w danej żywności pozostaje zalewie 1 -4% oryginalnej wilgoci. Taki produkt najczęściej traktowany jest azotem, a następnie zamykany w folii lub puszkach. Te ostatnie mogą mieć żywotność nawet do 25 lat!

CHEMIA W PRZEMIANACH ŻYWNOŚCI • PASTERYZACJA ŻYWNOŚCI - to proces polegający na ogrzewaniu surowców w temperaturze nie przekraczającej 100ᴼC, najczęściej przeprowadza się ją w zakresie temperatur 65– 85ᴼC. W wyniku przebiegającego mechanizmu zniszczeniu ulegają drobnoustroje chorobotwórcze, a także trwałość produktu zostaje przedłużona, gdyż formy wegetatywne zostają praktycznie w całości unieszkodliwione. W przypadku składników charakteryzujących się kwaśnym p. H o wartości poniżej 4, 5, umożliwia ona całkowicie pełną trwałość mikrobiologiczną. Wyróżniamy różne sposoby pasteryzacji, które różnią się stosowaną temperaturą oraz czasem ogrzewania: pasteryzacja niska (długotrwała) – przebiegająca w temperaturze 63 – 65ᴼC i trwa 20– 30 minut, pasteryzacja momentalna – ogrzewanie do temperatury 85– 90ᴼC, a następnie natychmiastowe schłodzenie, pasteryzacja wysoka – zachodzi w temperaturze od 85ᴼC do prawie 100ᴼC, w ciągu co najmniej 15 sekund do kilku, a niekiedy nawet kilkudziesięciu minut. Procesowi poddaje się zwykle produkty płynne, tj. piwo czy mleko, a także surowce kwaśne (np. ogórki konserwowe). Zachodzi on przed lub po umieszczeniu ich w opakowaniach hermetycznych. Urządzenia, w których jest przeprowadzana nazywają się pasteryzatorami. Co ciekawe mogą pracować w sposób okresowy, jak również ciągły. Źródło: Pasteryzacja-BAKALIE. com. pl

CHEMIA W PRZEMIANACH ŻYWNOŚCI • PEKLOWANIE ŻYWNOŚCI - proces polegający na działaniu mieszanki peklującej na mięso. Efektem tego procesu jest utrwalanie barwy, wytworzenie charakterystycznego smaku i zapachu mięsa oraz przedłużenie trwałości produktu poprzez hamowanie wzrostu bakterii chorobotwórczych i gnilnych. • Do nastrzyku i zalewania mięsa używa się specjalnej solanki peklującej, którą stanowi wodny roztwór zawierający: : • sól kuchenna (Na. Cl); • azotyn potasu (KNO 2) lub azotyn sodu (Na. NO 2); • cukier; • fosforany; • kwas askorbinowy lub askorbinian sodu; • cytryniany; peklowanie Źródło : MOJEGOTOWANIE. PL • Głównym celem PEKLOWANIA jest wytworzenie barwy peklowniczej stabilnej po obróbce termicznej wyrobów. Mechanizm tworzenia się pożądanej barwy jest rezultatem powstawania pochodnych mioglobiny (Mb) i hemoglobiny (Hb), które są naturalnymi białkowymi barwnikami hemowymi mięsa (Mb) i krwi (Hb). W związku z faktem, że mioglobina stanowi dominujący składnik barwników mięsa w ogólnej ich ilości (7590%) przyjmuje się, że to ona decyduje w największym stopniu o jego barwie. • W utrwaleniu barwy mięsa peklowanego bierze bezpośredni udział azotyn, z którego w końcowej fazie przekształceń fizykochemicznych powstaje tlenek azotu. Związek ten zastępując cząsteczkę wody lub tlen w mioglobinie, tworzy z nią nitrozylokompleks barwny zwany nitrozylomioglobiną, która decyduje o nadaniu typowej różowoczerwonej barwy peklowanym wyrobom mięsnym. Pod wpływem obróbki termicznej powstająca nitrozylomioglobina ulega dalszej przemianie do nitrozylomiochromogenu (Ch Mb· NO). Tworzący się związek jest względnie stabilny, jednak pod wpływem światła i tlenu może ulegać degradacji, co powoduje pogarszanie pożądanej barwy produktu peklowanego w miarę upływu czasu od jego obróbki termicznej. Analogicznym przemianom w trakcie peklowania i obróbki termicznej ulega hemoglobina.

WYTWARZANIE LEKÓW I ICH DZIAŁANIE • Nie wyobrażamy sobie współczesnej medycyny bez istnienia nowoczesnych leków, potrafiących efektywnie i często bezpiecznie walczyć z chorobami nękającymi współczesnego człowieka. Opracowywanie , pomysły , procesy technologiczne ale i same działania leku w naszym organizmie nie mogą obejść się zupełnie bez chemii. Zanim powstanie nowa molekuła chemiczna mogąca w przyszłości stać się lekiem , najpierw na drodze syntez chemicznych powstają tysiące związków chemicznych o obiecującym potencjale leczniczym. Po wielu latach , próbach klinicznych , testach, do użytku kosztem wielu miliardów dolarów wchodzi lek- cząsteczka chemiczna mogąca i odmieniająca życie wielu pacjentów. Często u podłoża działania leku lezą podstawowe prawa chemiczne jak np. REAKCJE ZOBOJĘTNIANIA-wykorzystywane np. w lekach zobojętniających kwas solny w żołądku. Leki te znajdują bardzo szerokie zastosowanie w takich chorobach i dolegliwościach jak zgaga, refluks żołądkowo-przełykowy, dyspepsja, choroba wrzodowa żołądka i dwunastnicy , zespół jelita nadwrażliwego , uszkodzenia błony śluzowej żołądka czy dwunastnicy i inne. Leki te mogą w swoim składzie zawierać między innymi wodorotlenki glinu czy magnezu. Wodorotlenek glinu i magnezu w reakcji z żołądkowym kwasem solnym tworzą sole (chlorki). Reakcja ta zwiększa p. H soku żołądkowego i zmniejsza uszkadzające działanie kwasu solnego na błonę śluzową żołądka. Innymi substancjami chemicznymi mogą być węglan wapnia i węglan magnezu , które również neutralizując w reakcji chemicznej kwas żołądkowy skutecznie likwidują objawy np. zgagi. Do leków zawierających mieszaniny soli zobojętniających kwaśny sok żołądkowy należą między innymi Alugastrin (tabletki do rozgryzania) - 340 mg węglanu dihydroksyglinowo-sodowego.

WYTWARZANIE LEKÓW I ICH DZIAŁANIE • Manti (tabletki do rozgryzania i gumy) – 200 mg wodorotlenku glinu, 200 mg wodorotlenku magnezu, 25 mg simetykonu, • Gealcid (tabletki do rozgryzania – 350 mg kwasu alginowego, 120 mg wodorowęglanu sodu, 100 mg wodorotlenku glinu, • Rennie (tabletki do ssania) – 680 mg węglanu wapnia, 80 mg węglanu magnezu, • Gaviscon o smaku mięty (zaw. doustna w saszetkach) – 10 ml zawiera: 500 mg alginianu sodu, 160 mg węglanu wapnia, 267 mg wodorowęglanu sodu, • Gaviscon o smaku mięty TAB (tabletki do rozgryzania) – 250 mg alginianu sodu, 80 mg węglanu wapnia, 133, 5 mg wodorowęglanu sodu, • Maalox (zawiesina doustna w saszetkach) – 460 mg tlenku glinu, 400 mg wodorotlenku magnezu, • Maalox (zawiesina doustna w butelce) – 100 ml zawiera: 3, 5 g wodorotlenku glinu, 4 g wodorotlenku magnezu, • Maalox (tabletki) – 400 mg wodorotlenku glinu, 400 mg wodorotlenku magnezu, • Gelatum Aluminii Phosphorici – 100 g zawiera: 4, 5 g fosforanu glinu, 10 mg olejku miętowego, • Gastrotuss, Refluxin-M, Esoxx One (saszetki). Źródło: LEK –Alugastrin, Manti, Rennie -portal medyczny MEDONET

WYTWARZANIE LEKÓW I ICH DZIAŁANIE • Innym przykładem leku szeroko wykorzystywanego i to już od dawna w medycynie jest WĘGIEL LECZNICZY. Również i ten bardzo popularny i bardzo bezpieczny lek wykorzystuje w swoim działaniu podstawowe prawidła chemiczne. Węgiel aktywny (węgiel aktywowany, węgiel leczniczy) występuje w postaci czarnych tabletek. Wytwarzany jest najczęściej z miazgi drzewnej (wytwarza się go także z torfu, węgla kopalnego lub skorup orzechów) przy temperaturze blisko 900 stopni Celsjusza, a w dalszej fazie produkcji - aktywowany działaniem pary wodnej lub mocnych kwasów. Wszystko to powoduje uzyskanie maksymalnej powierzchni adsorpcyjnej. Już Hipokrates i jego uczniowie polecali użycie sproszkowanego węgla drzewnego do aplikowania na rany, przez co goiły się one znacznie szybciej i nie wydzielały niemiłego zapachu. Warto także wspomnieć, że węgiel aktywny do dziś jest wykorzystywany przez Aborygenów i niektóre plemiona afrykańskie. Ludność ta stosuje węgiel do "wyciągania" trucizny z ran powstałych po ukąszeniu pająków, skorpionów, czy jadowitych węży. Indianie z kolei leczą węglem aktywnym reakcje alergiczne, powstałe w wyniku zatrucia bluszczem. • Węgiel aktywny jest też dostępny w aptekach w postaci przeciwbakteryjnych opatrunków. Warstwa węgla znajdująca się na opatrunkach pochłania wysięk z rany oraz nieprzyjemny zapach, a także wiąże endotoksyny. Takie zastosowanie węgla aktywnego jest szczególnie zalecane w przypadku bardzo trudno gojących się ran, odleżyn czy owrzodzeń. • Potwierdzają to liczne badania np. w jednym czterotygodniowym badaniu obejmującym dwa randomizowane badania z grupą kontrolną, w których uczestniczyło 60 osób, wykazano, że węgiel aktywny i srebro stosowane w opatrunkach na rany pomagają usuwać szkodliwe płyny i toksyny z przewlekłych żylnych owrzodzeń nóg, pomagając je leczyć. W nowszym artykule, który dotyczył czterech opisów przypadków, uzyskano podobny wynik. Badania opublikowane w czerwcu 2016 roku w British Journal of Nursing wykazały, że kiedy osoby z tego typu ranami były leczone opatrunkami z węglem aktywnym, ich rany goiły się lepiej niż wtedy, gdy były leczone innymi opatrunkami przeciwbakteryjnymi. Źrodło: LEK- Węgiel aktywny -portal medyczny MEDONET

WYTWARZANIE LEKÓW I ICH DZIAŁANIE • Węgiel aktywny znajduje zastosowanie przede wszystkim jako specyfik na biegunkę – posiada zdolności wiązania z innymi substancjami. Produkt więc absorbuje m. in. bakterie i toksyny wywołujące biegunkę, a następnie pozbywa się ich z organizmu (węgiel aktywny po doustnym podaniu nie wchłania się z przewodu pokarmowego, ale jest wydalany wraz z kałem, co z kolei wiąże się z czarnym zabarwieniem stolca). Oprócz tego - węgiel aktywny pokrywa błonę śluzową przewodu pokarmowego, chroniąc go tym samym przed działaniem nieprzyjaznych substancji. Trzeba tylko pamiętać, że węgiel może być przyjmowany przez krótki czas ze względu na wchłanianie enzymów trawiennych wraz z witaminami. Dobroczynne działanie węgla aktywnego skupia się także na eliminowaniu niebezpiecznych zatruć – tak substancjami chemicznymi, jak i lekami. Ze względu na zdolność wiązania toksyn, bakterii oraz niektórych leków znajduje on zastosowanie jako pomocniczy lek na zatrucia. Największą skuteczność wykazuje zażycie węgla aktywnego zaraz po przyjęciu trucizny, najlepiej do 1 godziny (badania pokazują, że kiedy pojedyncza dawka 50 -100 gramów węgla aktywnego zostanie przyjęta w ciągu pięciu minut od przyjęcia leku, może to zmniejszyć jego wchłanianie u dorosłych nawet o 74%, a efekt ten zmniejsza się do około 50%, gdy węgiel zostanie przyjęty 30 minut po spożyciu leku i do 20%, jeśli zostanie przyjęty trzy godziny po przedawkowaniu leku). • Warto wiedzieć, że węgla aktywnego nie można stosować we wszystkich typach zatruć. Takie rozwiązanie jest wskazane m. in. przy zatruciach paracetamolem, solami metali ciężkich, salicylanami, fenolami, czy pochodnymi benzodiazepiny i nikotyną. • Warto wspomnieć, że węgiel aktywowany jest również stosowany pomocniczo w niwelowaniu wzdęć. Niewielkie badanie opublikowane w International Medical Journal wykazało, że węgiel aktywny skutecznie zmniejszał gazy i wzdęcia u mężczyzn • z nadmierną ilością gazów i u tych bez tego problemu. Węgiel leczniczy dzięki swojej porowatej strukturze działa oczyszczająco i przeciwzapalnie na skórę. Znajduje zastosowanie w pielęgnacji skóry trądzikowej , łojotokowej , tłustej , z zaskórnikami. Oprócz gotowych kosmetyków z węglem możemy kupić w aptece tabletki lub kapsułki z węglowym proszkiem i przygotować sobie domowy peeling. Węgiel leczniczy świetnie działa również na włosy. Głęboko oczyszcza skórę głowy zapobiegając nadmiernemu przetłuszczeniu.

WYTWARZANIE LEKÓW I ICH DZIAŁANIE PODSUMOWANIE • Generalnie rzecz ujmując mechanizm działania większości leków polega na tym, że większość leków wiąże się chemicznie ze swoistymi strukturami chemicznymi znajdującymi się w błonie lub we wnętrzu komórek, nazywanymi receptorami. Receptory te są związkami chemicznymi zbudowanymi z cukrów i białek. Źródło: Zdrowiewformie. pl

CHEMIA W BUDOWNICTWIE - WAPNO PALONE I GASZONE • Chemia życia codziennego to również tlenek wapnia Ca. O czyli WAPNO PALONE, czyli nieorganiczny związek chemiczny z grupy tlenków zasadowych. W temperaturze pokojowej związek ten jest białym ciałem drobnokrystalicznym. Tlenek wapnia posiada własności higroskopijne. Łączy się gwałtownie z wodą tworząc wodorotlenek wapnia, przy czym wydziela się ciepło. • Tlenek wapnia jest otrzymywany techniczne na wielką skalę przez prażenie (tzw. kalcynowanie) kamienia wapiennego w temperaturze 900– 1000 °C w piecach zwanych wapiennikami. • Ca. CO 3 → Ca. O + CO 2 • Wapno palone występuje w dwóch formach: - wapno palone w bryłach, o barwie zależnej od domieszek; - wapno palone w postaci zmielonego proszku. Źródło: Wapno palone-budujesz. pl • W zależności od rodzaju użytego surowca wyróżnia się następujące rodzaje wapna palonego: - wapno wapniowe – otrzymywane z wapieni, - wapno dolomitowe – otrzymywane z wapieni dolomitycznych (lub mieszaniny dolomitów z wapieniami), - wapno hydrauliczne – otrzymywane z wapieni ilastych.
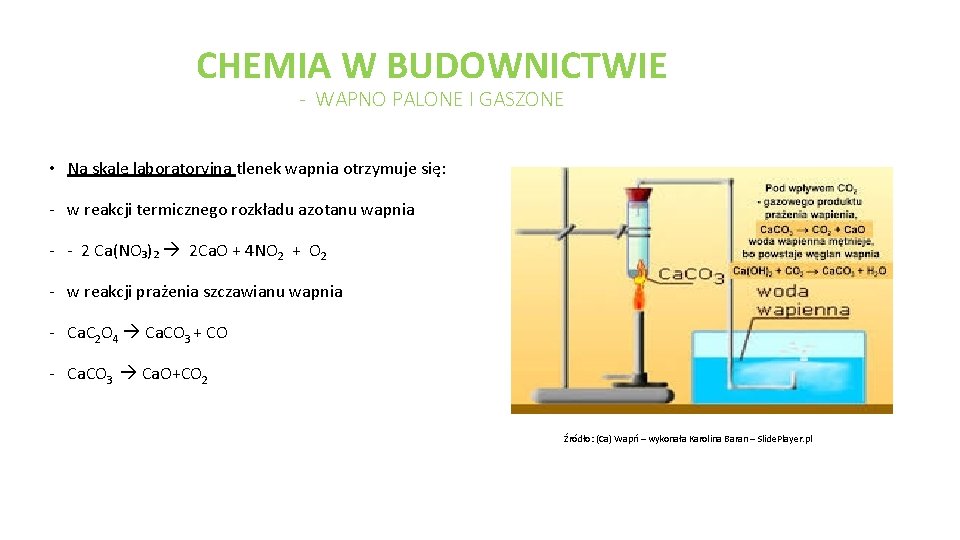
CHEMIA W BUDOWNICTWIE - WAPNO PALONE I GASZONE • Na skalę laboratoryjną tlenek wapnia otrzymuje się: - w reakcji termicznego rozkładu azotanu wapnia - - 2 Ca(NO₃)₂ 2 Ca. O + 4 NO 2 + O 2 - w reakcji prażenia szczawianu wapnia - Ca. C 2 O 4 Ca. CO 3 + CO - Ca. CO 3 Ca. O+CO 2 Źródło: (Ca) Wapń – wykonała Karolina Baran – Slide. Player. pl

CHEMIA W BUDOWNICTWIE A - WAPNO PALONE I GASZONE WAPNO PALONE wykorzystywane jest: • w budownictwie do wyrobu zaprawy murarskiej (mieszaniny wapna gaszonego Ca(OH)₂, piasku – głównie krzemionki Si. O₂, oraz wody); wapno gaszone otrzymywane jest z wapnia palonego w reakcji gaszenia wapna; • do otrzymywania mleka wapiennego (zawiesiny powstającej w wyniku reakcji tlenku wapnia z dużą ilością wody); mleko wapienne wykorzystywane jest jako środek dezynfekcyjny do bielenia ścian oraz do zwalczania szkodników drzew owocowych; • do otrzymywania karbidu (węgliku wapnia Ca. C₂) wykorzystywanego jako środek odstraszający krety i gryzonie oraz jako substancja redukująca w hutnictwie; karbid otrzymywany jest w wyniku ogrzewania mieszaniny wapienia z koksem w piecach łukowych; • do otrzymywania innych związków wapnia, sody, wodorotlenku sodowego, wodorotlenku potasowego oraz amoniaku; • w hutnictwie w procesie redukcji rudy żelaza w wielkim piecu zawierającym mieszaninę rudy, koksu i kamienia wapiennego; tlenek wapnia neutralizuje kwaśne tlenki krzemu Si. O₂, glinu Al₂O₃ i żelaza Fe₂O₃, co prowadzi do powstania żużlu (ciekłej mieszaniny produktów odpadowych) pływającego na powierzchni cięższego ciekłego żelaza; żużel wykorzystywany jest do produkcji materiałów dla przemysłu budowlanego; • jako laboratoryjny środek odwadniający; • w metalurgii jako topnik w procesie lutowania; wapno palone oczyszcza lutowane metale, a ponadto zwiększa ich odporność na zanieczyszczenia; • w przemyśle szklarskim, ceramicznym; • jest składnikiem wielu ceramicznych nadprzewodników wysokotemperaturowych; • w przemyśle petrochemicznym do produkcji past wodoczułych – past do wykrywania obecności wody w zbiornikach zawierających paliwa lub inne pochodne ropy naftowej; składają się z one z mieszaniny tlenku wapnia i fenoloftaleiny; powstały w wyniku reakcji tlenku wapnia z wodą wodorotlenek wapnia zabarwia fenoloftaleinę na kolor różowy, co świadczy o obecności wody w badanym zbiorniku; • w rolnictwie jako środek owadobójczy i składnik nawozów mineralnych; używane do odkwaszania gleby (wapniowania);

CHEMIA W BUDOWNICTWIE - WAPNO PALONE I GASZONE • w budownictwie drogowym do zwiększania nośności gruntów gliniastych poprzez reakcje z krzemionką i tlenkiem glinu, w wyniku czego powstają krzemiany i gliniany wapnia o właściwościach cementujących; • w budownictwie do produkcji bloczków betonu komórkowego, cegły wapienno-piaskowej oraz do wypełniania drewnianych konstrukcji szkieletowych (mieszanina zmielonego wapna palonego z trocinami); • w oczyszczalniach ścieków (wapniowanie – neutralizacja osadów ściekowych); • w procesach uzdatniania wody pitnej; Źródło: CEGŁY z zaprawą murarską strona firmy CEKOBUD • w zmiękczaniu wody kotłowej; • w energetyce w procesie odsiarczania spalin (stałe aerozole lub zawiesiny tlenku wapnia używane są do usuwania dwutlenku siarki SO₂ ze spalin); • w górnictwie do rozsadzania skał (metody wykorzystujące gwałtowną reakcję wapna palonego z wodą); • w ochronie środowiska (stabilizacja i neutralizacja odpadów polegająca na redukcji obecności bakterii i wirusów); • w produkcji przenośnych podgrzewaczy wykorzystujących reakcję gaszenia wapnia, w trakcie której wydziela się znaczna ilość ciepła. Źródło: BLOKI Z BETONU KOMÓRKOWEGO-strona firmy SOLBET

CHEMIA W BUDOWNICTWIE - WAPNO PALONE I GASZONE • B WAPNO GASZONE • Nie wyobrażamy sobie dzisiaj budownictwa, technologii produkcji nawozów sztucznych, czy sadownictwa bez bielenia drzew w celu ochronnym przed uszkodzeniem kory, itd. bez wodorotlenku wapnia Ca(OH)2 zwanego też wapnem gaszonym. Wodorotlenek wapnia otrzymuje się na skalę przemysłową w reakcji gaszenia wapna palonego, czyli reakcji tlenku wapnia z wodą: Ca. O + H 2 O → Ca(OH)2 Źródło: BIELENIE DRZEW – homebook. pl

CHEMIA W BUDOWNICTWIE - WAPNO PALONE I GASZONE Zastosowanie wapna gaszonego • w budownictwie jako spoiwo zapraw murarskiej i tynkarskiej (wapiennej i cementowo-wapiennej), • jako baza i lepiszcze farb malarskich (farba wapienna) o właściwościach dezynfekcyjnych stosowana do malowania (bielenia) wnętrz mieszkalnych, budynków gospodarczych oraz pni drzew owocowych, • w cukrownictwie do oczyszczania soku buraczanego, • jako substancja zmiękczająca wodę, • do produkcji nawozów sztucznych (nawozy wapniowe), • w energetyce do odsiarczania spalin, • w stomatologii jako podkład pod wypełnienie ubytku przy pokryciu miazgi pośrednim i bezpośrednim oraz opatrunek w kanale między wizytami szczególnie przy długich przerwach i zapaleniu tkanek okołowierzchołkowych Źródło: WAPNO GASZONE-budujesz. pl

DESTYLACJA FRAKCJYJNA ROPY NAFTOWEJ • Nie ma dzisiejszej światowej gospodarki bez czarnego złota, bez najcenniejszego chyba dzisiaj przykładu zastosowania w tym przypadku chemii organicznej- ropy naftowej. Destylacja ropy naftowej to proces, który pozwala na oddzielenie od siebie poszczególnych frakcji ropy, różniących się między sobą temperaturą wrzenia. Jest to podstawowy proces technologiczny prowadzony w rafineriach. Podczas destylacji, „surowa” ropa podgrzewana jest do wysokiej temperatury w piecu, a następnie – wprowadzana jest do kolumny frakcjonującej, w której następuje rozdział składników ropy zależnie od temperatury wrzenia. Związki o wysokiej temperaturze wrzenia skraplają się już w najniższej części kolumny (w której panuje najwyższa temperatura), natomiast związki o niższej temperaturze wrzenia (bardziej lotne) przechodzą do wyższych – chłodniejszych przedziałów kolumny frakcjonującej, gdzie stopniowo ulegają skraplaniu. U szczytu kolumny, gdzie panuje najniższa temperatura (zbliżona do temperatury otoczenia), odbierane są gazowe składniki ropy - propan i butan (wchodzące w skład LPG). Schemat destylacji frakcyjnej ropy naftowej przedstawiono na rysunku. Źródło: Destylacja frakcyjna ropy naftowej-skrypt TECHNOLOGIA PRZEROBU ROPY NAFTOWEJ W GRUPIE LOTOS

DESTYLACJA FRAKCJYJNA ROPY NAFTOWEJ • Produkty destylacji ropy naftowej, według rosnącej temperatury wrzenia to: propan i butan (LPG), benzyna, nafta/paliwo lotnicze, olej napędowy („ropa” do silników Diesla), oleje opałowe, ciężkie oleje i smary, mazut, asfalt. We współczesnych rafineriach, zarówno benzyna jak i olej napędowy uzyskane bezpośrednio w destylacji ropy naftowej, poddawane są dalszej obróbce – odsiarczaniu oraz procesom izomeryzacji i reformingu, które zwiększają liczbę oktanową uzyskiwanego paliwa. • Wyżej wrzące frakcje – nafta, czy olej opałowy i ciężkie oleje, są zwykle poddawane procesowi krakingu katalitycznego, w którym długie łańcuchy węglowodorowe są rozbijane na mniejsze części. Wskutek tego procesu powstaje benzyna, która jest mieszana z tą uzyskiwaną bezpośrednio z destylacji ropy. Dzięki temu możliwe jest uzyskanie z ropy większej ilości benzyny niż można to przewidzieć na podstawie jej składu węglowodorowego i powstaje mniejsza ilość ciężkich olejów, które nie są tak użyteczne w dużych ilościach. Ciekawym produktem destylacji ropy naftowej jest mazut. Jest to gęsta, oleista pozostałość po destylacji ropy o barwie od ciemnobrunatnej do czarnej. Część mazutu wykorzystuje się bezpośrednio jako olej opałowy, a z części po uprzedniej destylacji otrzymujemy między innymi- oleje smarowe, wazelinę / farmacja, kosmetologia, parafinę /medycyna, produkcja świec, asfalty – budowa dróg i wyrób papy.

GAZ KOKSOWNICZY, WODA POGAZOWA, SMOŁA WĘGLOWA • Sucha destylacja węgla, koksowanie węgla, odgazowanie węgla – proces polegający na ogrzewaniu węgla w temperaturze 900 – 1200 °C, bez dostępu powietrza. Proces przeprowadza się w koksowniach na drobno zmielonych mieszankach węgli koksowniczych (posiadających zdolność spiekania). W czasie ogrzewania (sucha destylacja) następuje zrywanie wiązań C-C, C-H, C-O. Proces przeprowadza się w ceramicznych komorach koksowniczych o wysokości 4 – 4, 5 metra, długości 12 – 14 metrów i szerokości 0, 35 – 0, 5 metra. Szereg komór poprzedzielanych ścianami grzewczymi tworzy piece koksownicze. Do ogrzewania przeponowego stosuje się gazy spalinowe.

GAZ KOKSOWNICZY, WODA POGAZOWA, SMOŁA WĘGLOWA • Produkty i wydajność suchej destylacji węgla. • koks – 70 -80% • smoła węglowa – 2, 5 -4, 5% • woda pogazowa – 3 -5% • amoniak – 0, 2 -0, 4% • benzol – 0, 8 -1, 4% • gaz koksowniczy – 12 -18% Źródło: KOKS – jswkoks. pl

GAZ KOKSOWNICZY, WODA POGAZOWA, SMOŁA WĘGLOWA • Gaz koksowniczy- produkt koksowania węgla w temperaturze 950 -1100°C zawierający jako domieszki: benzol surowy (benzen, toluen, ksyleny, tiofen, pirydynę, fenol) oraz amoniak, siarkowodór, związki cyjankowe, pył. Po oczyszczeniu, głównymi składnikami gazu koksowniczego są: wodór (45 -60%), metan (20 -30%) i azot (4 -8%). Wartość opałowa 16750 -18850 k. J/m 3. Gaz koksowniczy służy do opalania baterii koksowniczych i pieców martenowskich oraz do syntez chemicznych. • Woda pogazowa- produkt uboczny otrzymywany podczas odgazowywania stałych paliw naturalnych, głównie węgli kopalnych (sucha destylacja węgla). Stanowi mieszaninę zawierającą amoniak (NH 3), sole amonowe ((NH 4)2 CO 3, NH 4 Cl, (NH 4)2 SO 4, (NH 4)2 S 2 O 3, NH 4 SCN), pirydynę, fenole i inne związki. Jest surowcem do otrzymywania amoniaku i siarczanu(VI) amonu. • Smoła węglowa- smoła pogazowa, produkt przeróbki węgla kamiennego (np. uboczny produkt koksowania węgla oraz otrzymywania gazu miejskiego). Wyróżnić można smołę węglową nisko- oraz wysokotemperaturową. Ciecz barwy czarnej o mazistej konsystencji. W skład smoły węglowej wchodzą głównie węglowodory aromatyczne, fenole, zasady pirydynowe i chinolinowe. Surowiec do otrzymywania paku, lepiku, oraz wielu związków organicznych (np. benzenu, toluenu, fenolu, antracenu, naftalenu, aniliny). Źródło: Sucha_destylacja_wegla - GRZEGORZ LEWANDOWSKI EUGENIUSZ MILCHERT - WSPÓŁCZESNA TECHNOLOGIA SUCHEJ DESTYLACJI WĘGLA

REAKCJE POLIMERYZACJI • Są to reakcje łączenia się ze sobą pojedynczych cząsteczek związku organicznego nienasyconegomonomerów. Produktem tej reakcji jest wielkocząsteczkowy związek chemiczny – polimer. I tak na przykład reakcja polimeryzacji etenu prowadzi do powstania jego polimeru, a więc polietylenu, który wykorzystujemy do wytwarzania np. folii, różnych opakowań, obudowy urządzeń elektrycznych i innych. Źródło: Reakcja polimeryzacji etenu – G. P. Chomczenko „Chemia dla Kandydatów na wyższe uczelnie. ”

ZAKOŃCZENIE Tak już wspomniałem na wstępie zaprezentowałem tutaj tylko niewielki zestaw przykładów obecności chemii w życiu codziennym dzisiejszych ludzi. W mojej opinii ale i to wystarczy, by niewątpliwie stwierdzić, że obok takich nauk jak fizyka, biologia, medycyna i parę innych chemia i jej nowoczesne zastosowania są jednym z filarów postępu ludzkości. Źródło: vichemic. pl Źródło: Laboratorium Kryminalistyczne policji w poznaniu – wielkopolska. Policja. gov. pl

BIBLIOGRAFIA 1. K. M. Pazdro; “Podstawy chemii dla kandydatów na wyższe uczelnie”; Wydawnictwo Edukacyjne, Warszawa 1991; 2. Loretta Jones, Peter Atkins; “Chemia ogólna – cząsteczki, materia, reakcje”; Wydawnictwo Naukowe PWN, Warszawa 2009; 3. Adam Bielański; “Podstawy chemii nieorganicznej – część 3”; Wydawnictwo Naukowe PWN, Warszawa 1994; 4. Opracowanie zbiorowe Wydawnictwa Uniwersytetu Jagiellońskiego; “Farmakologia po prostu”, Warszawa 1998; 5. Jan Kulawik, Teresa Kulawik, Maria Litwin ”Chemia Nowej Ery - Podręcznik do chemii dla klasy ósmej szkoły podstawowej”, Wydawnictwo Nowa Era, Warszawa 2018; 6. G. P. Honczarenko; “Chemia dla kandydatów na wyższe uczelnie”, Wydawnictwo Edukacyjne, Warszawa 2019 7. Wikipedia

DZIĘKUJĘ ZA UWAGĘ Robert Gronowski Źródło: studia. studemtsnews. pl
- Slides: 30