Zuurbase titraties H 1 Titraties algemeen 2 Wat

Zuur-base titraties

H 1: Titraties - algemeen 2 Wat zijn titraties? Bij titraties wordt m. b. v. een buret nauwkeurig oplossing (=de titrant) toegevoegd aan het te bepalen analiet. Het analiet is een exacte hoeveelheid materiaal wat is afgewogen met een analytische balans of gepipetteerd met een volumepipet. Waarom titraties? Titreren is een kwantitatieve techniek ook wel titrimetrie of volumetrie genoemd. De analysefout is gemiddeld < 1 %. Een beperking van de techniek: een mengsel kan worden geanalyseerd op een totaal parameter (bijv. zuur), echter vaak niet op zijn individuele componenten (bijv. fosforzuur en azijnzuur). (NC State University Chemistry Department, 2017)
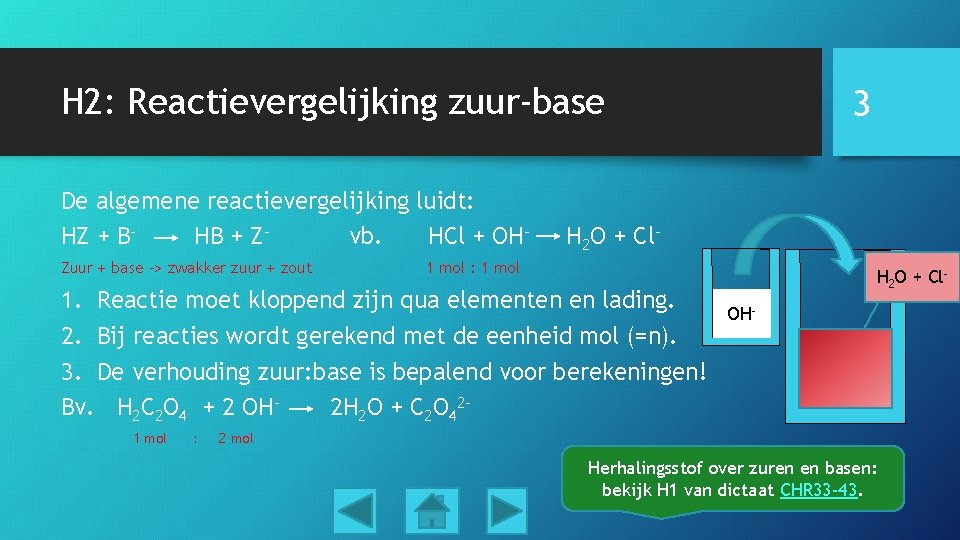
H 2: Reactievergelijking zuur-base De algemene reactievergelijking luidt: HZ + BHB + Zvb. HCl + OHZuur + base -> zwakker zuur + zout H 2 O + Cl- 1 mol : 1 mol 1. Reactie moet kloppend zijn qua elementen en lading. 2. Bij reacties wordt gerekend met de eenheid mol (=n). 3. De verhouding zuur: base is bepalend voor berekeningen! Bv. H 2 C 2 O 4 + 2 OH 2 H 2 O + C 2 O 421 mol : 3 H 2 O + Cl. OHHCl 2 mol Herhalingsstof over zuren en basen: bekijk H 1 van dictaat CHR 33 -43.

H 3: Rekenen met reacties 4 • Maak gebruik van het rekenschema!

H 4: Reacties - Oertiterstoffen Bij een titratie begint men altijd eerst met het bepalen van de concentratie van de titrant (= titerstelling). Dit doet men m. b. v. oertiterstoffen, ook wel primaire standaarden genoemd. Een oertiterstof is een chemische verbinding die: - Zeer zuiver te verkrijgen is (zuiverheid > 99, 99 %) - Zeer stabiel is; dus niet hygroscopisch (water opnemen) of verweren (water afstaan) - Hoog molair gewicht heeft (i. v. m. de inweeg) - Een aflopende reactie (alles wordt omgezet) 5

H 4: Reacties - Oertiterstoffen 6 Oertiterstoffen voor het stellen van een zuur: a. Natriumcarbonaat (Na 2 CO 3) b. Natriumtetraboraat ook borax genoemd (Na 2 B 4 O 7. 10 H 2 O) Oertiterstoffen voor het stellen van een base: a. Kaliumwaterstofftalaat (KH 5 C 8 O 4) b. Benzoëzuur (H 6 C 7 O 2) c. Oxaalzuurdihydraat ook ethaandizuur genoemd (H 2 C 2 O 4. 2 H 2 O) d. Kaliumwaterstofjodaat (KH(IO 3)2) Benzoëzuur

H 5: Het begrip p. H 7 p. H is een maat voor de zuurgraad van een waterige oplossing. p. H komt overeen met de concentratie van H+ ionen in een oplossing Als c[H+] groter wordt, dan wordt de p. H lager. De p. H schaal is logaritmisch en loopt van 0 tot 14. Er geldt: p. H = - log [H+] en dus ook [H+] = 10 -p. H (Sanibel Seaschool, 2017)

H 5: Het begrip p. H (en p. OH) Naast de p. H bestaat ook de gerelateerde term p. OH is eveneens een logaritmische maat, maar dan voor de basegraad (OH- concentratie) van een waterige oplossing Er geldt: p. OH = - log [OH-] en dus ook [OH-] = 10 -p. OH Er geldt: p. H + p. OH = 14 Dus als c[OH-] groter wordt, dan wordt de p. OH lager en dus de p. H hoger! 8

H 6: Acidimetrie - titratiecurve Als men een zuur met een base titreert, verkrijgt men een titratiecurve zoals de afbeelding hiernaast. Klik op deze link en bekijk de diverse curves die mogelijk zijn. (Sint-Martinusscholen Herk-de-Stad, 2017) Klik rechtsonder op het blauwe pijltje om de cursor (van volume) te bewegen en de bijbehorende p. H af te lezen. Verander ook eens de indicator! Vragen die jezelf kan stellen: Wat gebeurt er met de p. H in de curves? En waarom? En waar is het equivalentiepunt of eindpunt van de titratie? En wat is een geschikte indicator? 9 (Syntax Media, 2017)

H 6: Acidimetrie – Visueel (met indicator) 10 Bepaling van het eindpunt met indicator is de authentieke manier van eindpuntbepaling. In een bepaald p. H gebied verandert de indicator van kleur; het equivalentiepunt dient uiteraard in dat gebied te vallen! Dus als het eq-punt bij p. H 4, 0 ligt, dan is methyloranje veel geschikter dan lakmoes of fenolftaleïne. Bij een omslagpunt van p. H 9 of 10 is fenolftaleïne veel geschikter dan methylrood of methyloranje. (Syntax Media, 2017) Meer indicatoren inclusief structuurformules staan hier (Engineeringtoolbox, 2017)

H 6: Acidimetrie – Visueel (met indicator) Daarnaast zijn er ook mengsel van indicatoren mogelijk: mengindicator. Deze hebben een zeer klein p. H-gebied en dus een scherpe kleuromslag. Voorbeelden: - methylrood/broomkresolgroen; p. H omslag is 5, 1 - Thymolblauw/Fenolftaleïne; p. H omslag is 9, 0 De 1. 2. 3. 4. algemene eisen voor een indicator zijn: Verschil in kleur tussen de “zure” en “basische” vorm Hoge kleurintensiteit (inweeg is laag; bijv. 100 mg/100 ml = 0, 1 %) Het kleurevenwicht is snel instelbaar De indicator verbruikt geen titrant 11

H 6: Acidimetrie - indicatoren Het gebruik van indicatoren kan ook problemen geven! Onderstaand een aantal mogelijke foutenbronnen: 1. indicatorfout; het omslagpunt ≠ het equivalentiepunt 2. Verbruik van titreervloeistof door de indicator (eis < 0, 1 %) 3. Ondoorzichtige oplossingen 4. Titratiesnelheid is te hoog (je schiet voorbij equivalentiepunt) 5. Ongevoeligheid van het oog voor de kleuromslag 6. Temperatuurverschil; evenwichten zijn temperatuurafhankelijk 12

H 6: Oefening Indicatoren 13 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! A. Titratie van een sterk zuur (Syntax Media, 2017)

H 6: Oefening Indicatoren 14 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! B. Titratie van een zwak zuur (Syntax Media, 2017)

H 6: Oefening Indicatoren 15 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! C. Titratie van een tweewaardig zwak zuur (Syntax Media, 2017)

H 6: Oefening Indicatoren 16 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! D. Titratie van een sterke base (Syntax Media, 2017)

H 6: Oefening Indicatoren 17 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! E. Titratie van een zwakke base (Syntax Media, 2017)

H 6: Oefening Indicatoren 18 Bekijk de volgende titratiecurves en bepaal welke indicatoren (van bijgaande afbeelding) geschikt zijn voor de titraties. Het equivalentiepunt is met een stippellijn aangegeven. Per titratie zijn meerdere indicatoren te gebruiken! F. Titratie van een tweewaardig zwakke base (Syntax Media, 2017)
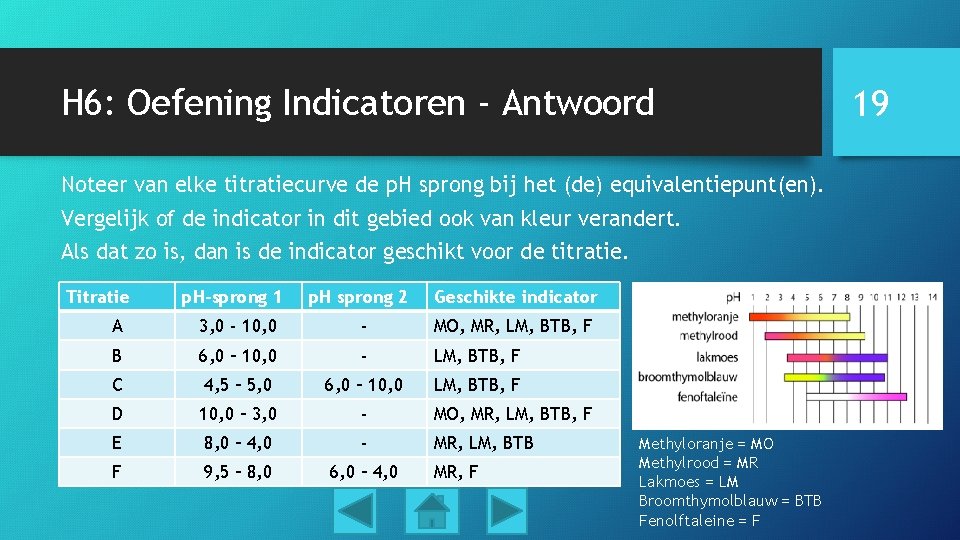
H 6: Oefening Indicatoren - Antwoord Noteer van elke titratiecurve de p. H sprong bij het (de) equivalentiepunt(en). Vergelijk of de indicator in dit gebied ook van kleur verandert. Als dat zo is, dan is de indicator geschikt voor de titratie. Titratie p. H-sprong 1 p. H sprong 2 Geschikte indicator A 3, 0 - 10, 0 - MO, MR, LM, BTB, F B 6, 0 – 10, 0 - LM, BTB, F C 4, 5 – 5, 0 6, 0 – 10, 0 LM, BTB, F D 10, 0 – 3, 0 - MO, MR, LM, BTB, F E 8, 0 – 4, 0 - MR, LM, BTB F 9, 5 – 8, 0 6, 0 – 4, 0 MR, F Methyloranje = MO Methylrood = MR Lakmoes = LM Broomthymolblauw = BTB Fenolftaleine = F 19
- Slides: 19